I期(滤过泡炎)

滤过泡相关感染
一目了然的要点
Section titled “一目了然的要点”1. 什么是滤过泡相关感染?
Section titled “1. 什么是滤过泡相关感染?”滤过泡相关感染(BRI)是青光眼滤过手术(如小梁切除术)后,细菌通过滤过泡侵入引起的感染性并发症。感染局限于滤过泡内称为滤过泡炎,感染波及眼内称为滤过泡相关眼内炎(BAE),临床上将这两种情况分开处理。
- 滤过泡炎(blebitis):感染局限于滤过泡内或周围。可伴有轻度至中度前房反应。
- 滤过泡相关眼内炎(BAE):感染波及玻璃体。视力预后极差。
临床分期如下 1)。
- I期:滤过泡局部炎症(滤过泡炎)
- II期:前房内细胞、闪辉、前房积脓
- IIIa期:玻璃体受累。眼底可见
- IIIb期:玻璃体严重混浊,眼底不可见
与其他内眼手术不同,滤过手术不仅在术后早期,而且在长期内都存在滤过泡感染的风险。一项关于丝裂霉素C联合小梁切除术的多中心前瞻性研究(Collaborative Bleb-Related Infection Incidence and Treatment Study)报告,术后5年滤过泡感染的累积发生率为2.2%,其中滤过泡相关性眼内炎(BAE)为1.1% 5)。该研究由日本青光眼学会实施,是一项全国性的前瞻性调查,数据可靠性高。术后1个月后滤过泡相关性感染的发生率据报道为0.97%~5% 4),高于其他内眼手术的迟发性感染发生率。青光眼术后滤过泡感染常在术后数年发生,发生率高于白内障术后。
根据发病时间,滤过泡相关性感染大致分为早发型(术后1个月内)和迟发型(术后1个月后)1)。早发型多由低毒力菌(凝固酶阴性葡萄球菌)引起,迟发型多由高毒力菌(链球菌属、流感嗜血杆菌)引起,预后往往不良1)。术后早期滤过泡感染的发生率为0.1%~0.2%,低于迟发型4)。对于接受滤过手术的患者,应充分告知迟发性感染的风险,并指示一旦出现充血、流泪、视物模糊、眼痛等提示感染的症状,应立即就医4)。
滤过泡炎是指感染局限于滤过泡内的情况,通过适当的局部治疗有望获得良好的视力预后。而滤过泡相关性眼内炎(BAE)是指感染已波及玻璃体的情况,即使积极治疗,视力预后也往往不良。如果存在前房积脓和明显的滤过泡感染,除非能证明其他原因,否则应作为眼内炎处理1)。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”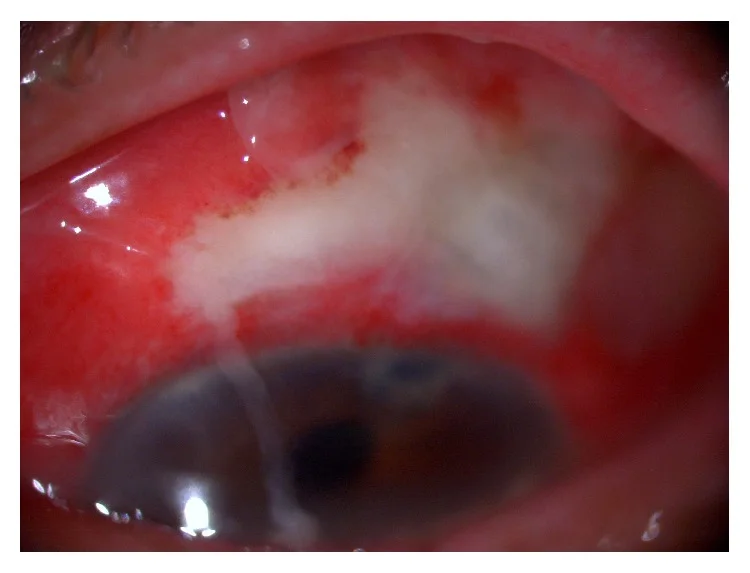
- 眼痛:急性发作。BAE时更剧烈
- 充血:从滤过泡周围扩展到整个结膜
- 视力下降:滤过泡炎时轻度,BAE时显著
- 畏光(刺眼):与前房炎症相关
- 眼分泌物和流泪:可能伴有脓性分泌物
- 前驱症状:35%的患者在发病前数天至数周出现眼睑炎、眉部疼痛、头痛和外眼炎症1)
II-III期(BAE)
当前房积脓和明显的滤过泡感染同时存在时,除非有其他原因证明,否则应作为眼内炎处理1)。常可观察到滤过泡渗漏,但炎性碎片可能暂时堵塞渗漏部位。
滤过泡外观评估(5项)
Section titled “滤过泡外观评估(5项)”为了预测滤过手术后的滤过功能以及早期发现并发症,每次就诊时都需要仔细检查滤过泡。使用裂隙灯显微镜检查以下5个项目。
- 范围(扩散):弥漫性滤过泡比局限性滤过泡降眼压效果更好。向角膜侧下垂的overhanging bleb可能妨碍视力。
- 高度:低平滤过泡提示滤过功能下降。
- 壁厚:使用抗代谢药物时,滤过泡壁变薄的频率较高。薄壁滤过泡通常降眼压效果良好,但容易发生房水渗漏。滤过泡内腔被厚膜包裹的包裹性滤过泡(encapsulated bleb)通常降眼压效果不佳。
- 血管分布:无血管的缺血性滤过泡房水渗漏风险高。
- Seidel试验:用荧光素试纸染色滤过泡表面,检查有无房水渗漏。详见“诊断和检查方法”一节。
3. 原因和风险因素
Section titled “3. 原因和风险因素”主要风险因素
Section titled “主要风险因素”- 滤过泡渗漏(最大风险因素):使感染风险增加26倍1)。滤过泡房水渗漏是主要风险因素4)7),晚期渗漏比早期渗漏风险更高1)。如果是渗出的oozing,可在注意感染的同时观察,但明确的渗漏原则上需要处理。
- 使用抗代谢药物(MMC、5-FU):导致杯状细胞减少,黏蛋白产生下降,结膜防御屏障减弱。促进滤过泡壁整体变薄和无血管化,使用丝裂霉素C后5年渗漏风险达15%11)。
- 滤过泡壁变薄、无血管化:在联合抗代谢药物的小梁切除术中常见。壁变薄的滤过泡容易发生房水渗漏,渗漏是滤过泡感染的风险因素。
- 下方滤过泡:由于暴露于泪液积聚和缺乏上眼睑保护,感染率升高。上方为1.3%/患者·年,而下方为7.8%/患者·年1)。
- 以角膜缘为基底的结膜切口(limbus-based):比以穹窿为基底的切口感染率高(8% vs 0%)1)。无血管滤过泡更容易发生在以角膜缘为基底的切口技术中。
- 其他:结膜炎、眼睑炎、上呼吸道感染、年轻、轴性近视、慢性使用抗菌药物。
致病菌因发病时间而异。文献中已报道超过100种致病微生物1)。
| 发病时间 | 主要致病菌 | 特点 |
|---|---|---|
| 早期发病 | 凝固酶阴性葡萄球菌 | 低毒性,预后相对较好 |
| 晚期发病 | 链球菌、流感嗜血杆菌 | 高毒性,预后不良 |
革兰阳性球菌最常见,其中链球菌属(约385株)和葡萄球菌属(约296株)是主要菌种。革兰阴性菌中,莫拉菌属(约79例)和嗜血杆菌属(约63例)较多1)。罕见情况下,也有报道人畜共患感染如犬咬二氧化碳嗜纤维菌2)。瑞典的一项回顾性研究报道,小梁切除术后眼内炎和严重滤过泡炎的发生率为每1000例手术7.2例12)。
滤过泡的房水渗漏是最大风险因素,使感染风险增加26倍1)。使用抗代谢药物导致滤过泡壁变薄、无血管化,增加了渗漏风险。尤其是壁薄、血管分布少的缺血性滤过泡更容易发生渗漏。每次检查时通过Seidel试验确认有无渗漏非常重要。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”裂隙灯显微镜检查
Section titled “裂隙灯显微镜检查”观察滤过泡外观是基础,需确认上述5个项目(范围、高度、壁厚、血管分布、Seidel试验)。
Seidel试验
Section titled “Seidel试验”这是确认滤过泡房水渗漏的基本检查。
- 将浸有表面麻醉药的荧光素试纸轻轻涂抹在滤过泡表面。
- 在蓝色滤光片下观察整个滤过泡。
- 如果有房水渗漏,可看到被房水稀释的荧光素流动(Seidel试验阳性)。
- 让患者闭眼,然后睁眼后立即观察整个滤过泡数秒,更容易判断。
- 确认渗漏的位置和范围也很重要。
滤过泡分类系统
Section titled “滤过泡分类系统”以下是基于外观的代表性滤过泡分类方法。
- Moorfields bleb grading system(MBGS):一种标准化评估滤过泡形态的分类方法8)
- Indiana bleb appearance grading scale(IBAGS):一种系统化对滤过泡外观进行分级的分类方法9)
两者均有助于评估滤过功能和预测感染风险。联合使用前段OCT可以更客观地评估滤过泡的内部结构和泡壁厚度10)。
微生物学检查
Section titled “微生物学检查”- 结膜拭子及培养:从脓性分泌物中采集标本,接种于血琼脂、巧克力琼脂、硫乙醇酸盐培养基等1)
- 前房水及玻璃体穿刺:II期及以上必须进行。培养同时进行玻璃体内抗生素注射。
- PCR:由于培养阴性率高达21-86%,PCR作为补充非常有用。有报告称检出率从47.6%提高到95.3%1)。
- 白内障术后眼内炎:发病时间和手术方式不同。白内障术后眼内炎通常发生在术后早期(约1周),而滤过泡相关感染常发生在术后数年。通过有无滤过泡感染征象进行鉴别。
- 急性前葡萄膜炎:滤过泡混浊及周围明显充血(white-on-red)的有无是鉴别的关键。非感染性葡萄膜炎不伴有滤过泡本身的白浊。
- 包裹性滤过泡(encapsulated bleb):术后数周发生的非感染性并发症。滤过泡腔被厚膜包围,导致眼压下降不良,但缺乏感染征象(white-on-red)。
5. 标准治疗方法
Section titled “5. 标准治疗方法”滤过泡炎(I~II期)的治疗
Section titled “滤过泡炎(I~II期)的治疗”若无玻璃体受累,应积极进行局部抗菌药物治疗。若感染局限于滤过泡和前房,可通过局部和全身抗菌药物处理。
- 强化滴眼液方案:万古霉素(25~50 mg/mL)或头孢唑林(50 mg/mL)与妥布霉素(14 mg/mL)每30分钟交替滴眼。48小时后根据改善情况逐渐减量。
- 替代方案:第四代氟喹诺酮类(如莫西沙星)每小时一次。
- 结膜下注射:根据滤过泡感染分期,可进行结膜下或前房内抗菌药物注射。
临床改善24小时后可考虑加用局部类固醇,但需谨慎判断,因为有预后恶化的报道。根据培养结果调整抗菌药物,并密切监测治疗反应。确认感染得到控制后再开始使用类固醇。
滤过泡相关性眼内炎(BAE)的治疗
Section titled “滤过泡相关性眼内炎(BAE)的治疗”在玻璃体穿刺取样的同时,进行玻璃体内抗菌药物注射。
| 药物 | 剂量 | 备注 |
|---|---|---|
| 万古霉素 | 1 mg/0.1 mL | 覆盖革兰阳性菌 |
| 头孢他啶 | 2.25 mg/0.1 mL | 覆盖革兰阴性菌 |
| 地塞米松 | 0.4mg/0.1mL | 辅助(抗炎) |
当感染扩散到玻璃体腔时,通常需要玻璃体切除术。有报告称玻璃体切除术(PPV)比穿刺注射法的视力预后更好,但近年也有数据显示两者的视力预后相当。一旦感染波及玻璃体腔,视力预后极差,因此需要迅速处理。需要注意的是,眼内炎玻璃体切除研究(EVS)针对的是白内障术后眼内炎,与BRI/BAE的患者背景、致病菌和发病机制不同,因此不能直接套用EVS的结果。特别是BAE常为迟发性且涉及高毒性菌,应考虑更积极的玻璃体切除术。
术后感染预防
Section titled “术后感染预防”青光眼诊疗指南(第5版)CQ6中,关于小梁切除术后抗菌药物的使用推荐如下4)。
术后早期抗菌药物使用
Section titled “术后早期抗菌药物使用”推荐预防性使用抗菌药物,但对于药物、方法和疗程尚未达成共识4)。参与研究的专家通常在术后13个月内持续滴用抗菌药物,在此期间未发生术后感染,因此强烈推荐术后持续使用抗菌药物13个月(推荐强度:强烈推荐实施;证据强度:C)4)。
术后长期抗菌药物使用
Section titled “术后长期抗菌药物使用”全国规模的滤过泡感染调查(104眼)比较了长期使用抗菌药物组和未使用组,结果显示抗菌药物可显著延迟滤过泡感染的发生6)。
- 未使用组:感染发生中位时间 3.9年
- 长期使用组:感染发生中位时间 6.4年
- 眼膏组:感染发生中位时间 10.5年
如果滤过泡壁薄,上眼睑抬起时有房水渗出,或晨起时泪液积聚等自觉症状,应积极考虑睡前使用新喹诺酮类抗菌眼膏4)。
长期使用组26眼中9眼检出耐药菌,但其中6眼为表皮葡萄球菌,不易导致重症眼内炎4)。从医疗经济角度也应避免滥用抗菌药物。
滤过泡渗漏的管理
Section titled “滤过泡渗漏的管理”如果发现渗漏(滤过泡感染的最大风险因素),需要进行适当的管理。
- 保守治疗:绷带式角膜接触镜、压迫缝合、氰基丙烯酸酯组织胶、加压眼罩
- 自体血注射:将自体血注射到滤过泡内及周围。可能引起眼压急剧升高。
- 手术治疗:结膜前徙术(成功率100%)、羊膜移植(成功率45%)。如果感染风险高或低眼压无法恢复,则适合采用游离结膜瓣或上方带蒂结膜瓣进行滤过泡重建。长期需要同时重新评估滤过泡形态和眼压管理 11)
青光眼诊疗指南(第5版)强烈建议术后1-3个月继续使用抗生素(证据强度C)4)。之后根据感染风险(如滤过泡渗漏的有无),考虑长期睡前使用新喹诺酮类眼膏。有报告称,长期使用可将感染发生的中位时间从非使用组的3.9年显著延迟至眼膏组的10.5年 6)。但应避免盲目使用,需与主治医生协商后决定是否继续。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”滤过泡相关性感染的病理源于青光眼滤过手术形成的滤过泡成为感染的入口。
感染建立的机制
Section titled “感染建立的机制”在小梁切除术中,房水从巩膜瓣下被引导至结膜下形成滤过泡。如果滤过泡壁变薄或渗漏,泪液或眼周常驻菌可能进入眼内。
抗代谢药物(MMC、5-FU)的使用通过以下复合机制增加感染风险:
- 减少结膜杯状细胞数量,降低黏蛋白产生,削弱泪液防御功能
- 促进结膜整体变薄和无血管化,减弱滤过泡壁的机械强度
- 削弱物理和免疫防御屏障,使细菌易于从结膜表面侵入眼内
- 抑制成纤维细胞增殖,延迟伤口愈合,降低结膜上皮修复能力
抗代谢药物在当前小梁切除术中对抑制瘢痕形成至关重要,但必须始终牢记其使用伴随的长期感染风险增加。
滤过泡壁变薄与渗漏
Section titled “滤过泡壁变薄与渗漏”滤过泡的形态随时间变化。小梁切除术后,伤口愈合过程中结膜下组织形成瘢痕。联合使用丝裂霉素C(MMC)可抑制早期过度组织反应,提高长期维持滤过泡的可能性,但在术后最初几个月瘢痕形成迅速进展时,巩膜瓣的流出阻力和滤过泡形态会迅速变化。如果在此期间管理不当,滤过泡壁变薄容易进展。
无血管的缺血性滤过泡房水渗漏风险特别高。无血管滤过泡更容易发生在以角膜缘为基底的结膜切开术中,这也与以角膜缘为基底的切口感染率较高(8% vs. 以穹窿为基底的0%)1)有关。房水渗漏(oozing或明显渗漏)和滤过泡感染(细菌进入滤过泡)是需要关注的长期并发症。对于渗出现象,可在注意感染的同时进行观察,但明显渗漏需要干预。
致病菌与病程阶段的关系
Section titled “致病菌与病程阶段的关系”致病菌的毒力与发病时间相关1)。早期发病型主要由低毒力菌(凝固酶阴性葡萄球菌)引起,与白内障术后眼内炎相似,来源于泪液和眼睑的正常菌群。这些细菌不产生外毒素,适当治疗预后良好。
相反,晚期发病型涉及毒力更强的细菌,如链球菌属(肺炎链球菌、草绿色链球菌群)、流感嗜血杆菌和沙雷菌属1)。这些细菌具有高外毒素产生能力和组织侵袭性,导致临床病程快速进展和视力预后不良。
Kandarakis等人(2022年)全面综述了文献中报道的BRI致病菌,鉴定出100多种微生物。在革兰阳性球菌中,链球菌属(约385株)和葡萄球菌属(约296株)占绝对优势,而在革兰阴性菌中,莫拉菌属(约79例)和嗜血杆菌属(约63例)是主要菌种1)。
Yang等人(2021年)报告了一名81岁男性,在小梁切除术后10年发生由犬咬二氧化碳嗜纤维菌引起的滤过泡炎。患者的脸部经常被其宠物狗舔舐,推测狗的口腔常驻菌通过滤过泡感染。通过小梁切除术修复获得了良好的视力预后(20/70)2)。
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”分子诊断技术的进步
Section titled “分子诊断技术的进步”Kandarakis等人(2022年)的综述指出,传统培养的阴性率高达21%至86%。实时PCR可将细菌检出率从47.6%提高到95.3%。此外,通过宏基因组学(高通量DNA测序)进行全面的微生物鉴定有望成为下一代诊断方法1)。
微创青光眼手术(MIGS)降低感染风险
Section titled “微创青光眼手术(MIGS)降低感染风险”MIGS的综述指出,与传统滤过手术相比,它有望减少创伤并降低严重术后并发症。但某些术式使用形成滤过泡的装置,因此需要根据手术类型评估感染风险3)。
罕见病原体的应对
Section titled “罕见病原体的应对”Yang等人(2021年)关于犬咬二氧化碳嗜纤维菌滤过泡炎的报道表明,与宠物动物的接触可能成为有滤过手术史眼睛的新感染风险因素。DNA测序使得以前难以培养的病原体得以鉴定2)。
术后抗菌药物使用的未来挑战
Section titled “术后抗菌药物使用的未来挑战”青光眼诊疗指南(第5版)指出,虽然术后长期使用抗菌药物可显著延迟感染发生,但关于给药药物、方法和持续时间尚未达成共识,期待高证据水平的研究4)。随着结膜菌群变化和耐药菌出现,长期随机对照试验的实施是未来的重要课题。
8. 参考文献
Section titled “8. 参考文献”- Kandarakis SA, Doumazos L, Mitsopoulou D, et al. A Review on Pathogens and Necessary Diagnostic Work for Bleb-Related Infections (BRIs). Diagnostics. 2022;12(9):2075.
- Yang MC, Ling J, Mosaed S. Capnocytophaga canimorsus blebitis: case report and review of literature. BMC Ophthalmol. 2021;21:59.
- Balas M, Mathew DJ, Bicket AK. Minimally Invasive Glaucoma Surgery: A Review of the Literature. Vision (Basel). 2023;7(3):54. doi:10.3390/vision7030054. PMID: 37606500.
- 日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
- Yamamoto T, Sawada A, Mayama C, et al. The 5-year incidence of bleb-related infection and its risk factors after filtering surgeries with adjunctive mitomycin C: collaborative bleb-related infection incidence and treatment study 2. Ophthalmology. 2014;121:1001-1006. doi:10.1016/j.ophtha.2013.11.001. PMID: 24491639.
- Sagara H, Yamamoto T, Imaizumi K, Sekiryu T. Impact of topically administered steroids, antibiotics, and sodium hyaluronate on bleb-related infection onset: the Japan Glaucoma Society survey of bleb-related infection report 4. J Ophthalmol. 2017;2017:7062565. doi:10.1155/2017/7062565. PMID: 29138694. PMCID: PMC5613473.
- Yamamoto T, Kuwayama Y, Kano K, et al. Clinical features of bleb-related infection: a 5-year survey in Japan. Acta Ophthalmol. 2013;91(7):619-624. doi:10.1111/j.1755-3768.2012.02480.x. PMID: 22883301.
- Wells AP, Ashraff NN, Hall RC, et al. Comparison of two clinical bleb grading systems. Ophthalmology. 2006;113(1):77-83. doi:10.1016/j.ophtha.2005.06.037. PMID: 16389104.
- Cantor LB, Mantravadi AV, WuDunn D, et al. Indiana Bleb Appearance Grading Scale. J Glaucoma. 2003;12(5):266-271. doi:10.1097/00134372-200310000-00012. PMID: 14520142.
- Kojima S, Inoue T, Kawaji T, Tanihara H. Filtration bleb revision guided by 3-dimensional anterior segment optical coherence tomography. J Glaucoma. 2014;23(5):312-315. doi:10.1097/IJG.0b013e3182741ee6. PMID: 23377583.
- Kim EA, Law SK, Coleman AL, et al. Long-Term Bleb-Related Infections After Trabeculectomy: Incidence, Risk Factors, and Influence of Bleb Revision. Am J Ophthalmol. 2015;159(6):1082-1091. doi:10.1016/j.ajo.2015.03.001. PMID: 25748577.
- Wallin Ö, Al-ahramy AM, Lundström M, Montan P. Endophthalmitis and severe blebitis following trabeculectomy: epidemiology and risk factors; a single-centre retrospective study. Acta Ophthalmol. 2014;92(5):426-431. doi:10.1111/aos.12257. PMID: 24020653.
