手术相关因素

术后脉络膜脱离(脉络膜渗出)
1. 什么是术后脉络膜脱离?
Section titled “1. 什么是术后脉络膜脱离?”脉络膜渗漏是指脉络膜毛细血管的浆液成分异常积聚在脉络膜上腔(脉络膜外腔)的病理状态。当睫状体和脉络膜与巩膜分离,液体在该间隙积聚并向玻璃体腔侧隆起时,称为脉络膜脱离。如果发生较大血管破裂,则成为出血性脉络膜脱离,甚至可能导致驱逐性出血。
脉络膜渗漏、睫状体脉络膜渗漏和浆液性脉络膜脱离几乎同义使用。脉络膜脱离是一个更广泛的概念,也包括出血性类型。脉络膜脱离的整体分类包括特发性脉络膜脱离、继发性脉络膜脱离和葡萄膜渗漏综合征三组。术后脉络膜脱离属于继发性。继发性脉络膜脱离的原因包括低眼压、脉络膜循环障碍、脉络膜炎症、恶性肿瘤等多种疾病。
浆液性与出血性的分类
Section titled “浆液性与出血性的分类”| 分类 | 内容物 | 主要发病机制 |
|---|---|---|
| 浆液性 | 浆液性液体 | 低眼压引起的静水压差 |
| 出血性 | 血液 | 后睫状动脉破裂 |
青光眼手术是脉络膜脱离最常见的原因。根据日本青光眼指南(第5版),小梁切除术后早期主要并发症的发生率包括浅前房(0.9–13%)、脉络膜脱离(5–14%)、前房积血(2.7–11%)和结膜切口渗漏(3.4–14%)1)。在TVT(管 vs 小梁切除术)研究中,小梁切除术后脉络膜渗漏的发生率为19%,青光眼引流植入物术后为16%4)。出血性脉络膜脱离在引流管植入手术中为1.2–2.7%,在小梁切除术中为0.6–1.4%。XEN45凝胶支架植入后也有0–15%的脉络膜渗漏报道2)。
白内障手术中也会发生术中脉络膜渗漏。在无缝线微切口白内障手术中,由于眼压降低时间短,发生率约为0.05%。危险因素包括高龄、高血压/动脉硬化、高眼压/青光眼、高度近视、小眼球和Sturge-Weber综合征。
可能导致术后视功能损害的低眼压黄斑病变的发生率为0.9–5%,滤过泡相关感染的发生率为0.97–5%1)。
小的周边脉络膜渗漏通常无症状,可自行消退。但大的渗漏可能导致视力下降和前房变浅。多数病例通过散瞳药和类固醇的保守治疗改善,但前房消失的重症病例或接吻性脉络膜渗漏需要外科引流。详情请参阅“标准治疗方法”一节。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”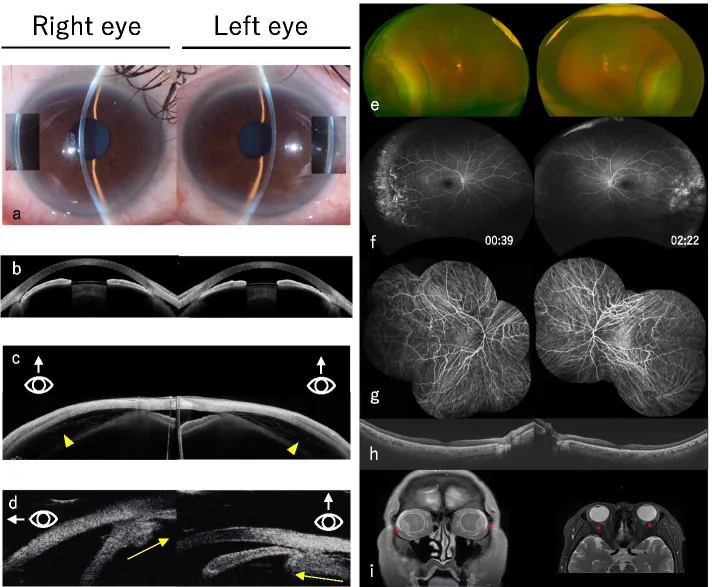
浆液性脉络膜渗漏:术后2~5天最常见。小的周边渗漏通常无症状。大的渗漏出现以下症状:
- 视力下降:由脉络膜隆起引起的屈光改变所致
- 周边视野狭窄:隆起的脉络膜压迫视网膜
- 近视化:由于晶状体虹膜隔前移
出血性脉络膜脱离:术后数日内出现急剧眼痛、恶心、视力下降时怀疑1)。表现为突然的剧烈搏动性疼痛和即刻视力丧失。睫状神经牵拉引起的疼痛可伴有恶心、呕吐。
术中发病(白内障手术时):伴有浅前房的急剧玻璃体压力升高是发病征兆。随着后囊升高,有后囊破裂的风险;当前房极度变浅时,手术难以继续。若眼底可见,可观察到脉络膜皱襞。
临床所见(医生检查确认的所见)
Section titled “临床所见(医生检查确认的所见)”浆液性和出血性的临床所见比较如下。
| 所见 | 浆液性 | 出血性 |
|---|---|---|
| 眼压 | 通常较低 | 通常较高 |
| 透照(Hagen征) | 阳性 | 阴性 |
| B型超声 | 无回声 | 高回声 |
眼底所见:检眼镜下,脉络膜脱离表现为茶褐色、表面光滑的凸透镜样硬性隆起。初期或轻度时,表现为睫状体平坦部和周边部脉络膜的隆起,无需压迫巩膜即可轻松观察锯齿缘。大的脉络膜脱离表现为由涡静脉附着处分隔的、最多4个多房性气球样隆起。
前房所见:前房深度可正常、变浅或消失。脉络膜脱离导致晶状体前移,引起浅前房。
合并低眼压黄斑病变时的所见:持续低眼压导致眼轴缩短,出现脉络膜皱褶、黄斑皱褶、视网膜血管迂曲和视乳头水肿1)。若持续存在,可能导致永久性视力损害。
继发性青光眼:继发性脉络膜脱离可引起急性青光眼发作。这是由于晶状体虹膜隔前移导致房角关闭,眼压急剧升高的病理状态。
3. 原因与风险因素
Section titled “3. 原因与风险因素”浆液性脉络膜渗出的成因
Section titled “浆液性脉络膜渗出的成因”术后低眼压是最常见的原因。根据Starling公式,眼压降低(间质压降低)导致毛细血管压相对升高,引起脉络膜上腔液体蓄积。炎症引起的脉络膜毛细血管通透性增加也起到作用6)。
脉络膜上腔的液体蓄积形成以下恶性循环:
- 术后低眼压→脉络膜上腔液体蓄积
- 睫状体功能下降→房水生成减少→进一步低眼压
- 晶状体前移→前房变浅→脉络膜脱离加重
- 房水流入葡萄膜巩膜流出通道→滤过泡形成不良
- 房水中蛋白浓度升高→促进滤过泡瘢痕化
白内障术中发病被认为是因为高龄导致的动脉硬化以及术中眼压急剧下降,导致短后睫状动脉迅速渗出浆液成分所致。
出血性脉络膜脱离的成因
Section titled “出血性脉络膜脱离的成因”后睫状动脉分支破裂导致血液迅速在脉络膜上腔蓄积。眼球突然减压,特别是从高眼压状态开始手术时风险较高。使用抗代谢药物(丝裂霉素C、5-FU)也会促进低眼压并起到作用1)。
患者相关因素
高龄、高血压、动脉硬化:增加出血风险。也与白内障术中的发生有关
高眼压、青光眼:术前高眼压的急剧减压是风险因素
高度近视、小眼球、Sturge-Weber综合征:小眼球中巩膜增厚压迫涡静脉参与发病
内眼手术史:尤其是玻璃体手术史是风险因素
葡萄膜炎:炎症导致脉络膜毛细血管通透性增加
使用抗凝药或抗血小板药:增加出血性变化的风险3)
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”脉络膜脱离表现为茶褐色、表面光滑、凸透镜样的硬性隆起。其特征是无需压迫即可轻松观察到锯齿缘。大的脉络膜脱离表现为由涡静脉附着处分隔的多房性隆起。
B型超声检查
Section titled “B型超声检查”该检查对于鉴别浆液性和出血性脉络膜脱离至关重要。
- 浆液性:无回声、光滑、厚实的半球形隆起
- 出血性:高回声隆起
它还可以检测临床上不明显的微小脉络膜上腔积液 5)。
超声生物显微镜(UBM)
Section titled “超声生物显微镜(UBM)”可以观察睫状体与巩膜的分离,用于显示睫状体的前旋。对眼前节的详细评估很有用。
不仅可以测量脉络膜厚度,还可以测量巩膜厚度,对诊断小眼球也有用。
需要与术后出现前房变浅、眼压异常的疾病进行鉴别。
- 视网膜脱离:脉络膜脱离通过其前部位置、向锯齿缘延伸、以及由涡静脉附着处分隔的多房性隆起与视网膜脱离相区别。与孔源性视网膜脱离不同,脉络膜脱离不会随眼球运动而明显移动。
- 驱逐性出血:术中急性发作,导致前房消失。脉络膜皱襞的有无有助于与脉络膜渗漏鉴别。驱逐性出血常伴有眼内容物的急剧脱出,预后不良。
- 灌注迷流综合征(IMS):白内障术中发生的玻璃体压力升高,但眼底无脉络膜皱襞,可与脉络膜渗漏区分。
- 恶性青光眼(房水迷流):存在浅前房,但无相应的低眼压、脉络膜脱离或睫状体上腔出血时需怀疑。房水流入玻璃体腔导致前房变浅,治疗选择包括散瞳药、房水生成抑制剂和玻璃体手术。
- 后巩膜炎:B型超声显示后巩膜和脉络膜增厚,球后组织水肿呈T征为特征。多见于中年女性,常为单眼,伴有眼痛和视力下降,常合并前巩膜炎或葡萄膜炎。
5. 标准治疗方法
Section titled “5. 标准治疗方法”预防的基本原则是尽量减少术中和术后低眼压1)。
- 小梁切除术:在巩膜瓣上放置多根缝线,术后通过激光缝线松解(LSL)管理眼压。术中多缝线以减少过度滤过是常见的管理方法1)。
- 激光缝线松解的时机:至少延迟1周。避免早期激光缝线松解。
- 前房稳定:使用粘弹剂或前房维持器。
- 无瓣青光眼引流装置:需要用可吸收缝线结扎引流管。
- 术后管理:停用局部和全身的房水生成抑制剂1)。
许多脉络膜渗出通过保守治疗可消退。部分病例因结膜下和巩膜瓣周围组织瘢痕化而自然改善1)。
- 散瞳药(硫酸阿托品水合物):使晶状体虹膜隔向后旋转,加深前房。
- 局部皮质类固醇:抑制炎症(推荐等级1B)1)。
- 加压眼罩:准确压迫巩膜瓣可改善过度滤过1)。
- 重症病例:联合口服泼尼松龙(1 mg/kg,逐渐减量)5)
- 前房消失时:向前房内注入空气或粘弹性物质以重建前房
白内障术中的处理:若能通过向前房内注入Healon V®(高粘度透明质酸钠)形成前房,则可继续手术。在微切口白内障手术中,随着眼压升高,切口自然闭合,因此等待20-30分钟前房可能加深,手术可继续进行。若Healon V®被从切口推出,则应中止手术;若无法形成前房,则于次日或之后重新手术。
此外,若单眼发生术中脉络膜渗出,对侧眼同样具有高风险,因此对侧眼手术最好在全身麻醉下进行,或考虑转诊至可行全身麻醉的机构。
外科引流的适应症如下5):
- 前房消失伴持续性晶状体角膜接触:角膜内皮损伤风险高
- 接吻型脉络膜脱离:脉络膜从视神经到晶状体均接触的严重脉络膜脱离
- 并发浆液性视网膜脱离:RPE泵机制失代偿导致的继发性视网膜脱离
- 持续性滤过泡渗漏伴低眼压
- 保守治疗无效的持续性脉络膜渗出
操作:在距角膜缘3.5-4.5 mm后方做全层巩膜切口,排出脉络膜上腔液体。术中在引流的同时向前房内注入灌注液或粘弹性物质以重建前房5)。
出血性脉络膜脱离的引流:出血可能自行吸收,但若需引流,最好等待7-10天至血液液化1)。
针对过度滤过的额外干预
Section titled “针对过度滤过的额外干预”对于过度滤过相关的低眼压,逐步考虑以下干预措施1):
- 经结膜巩膜瓣缝合:通过结膜直接使用尼龙线缝合巩膜瓣的方法,作为低眼压黄斑病变的治疗方法,长期有效性已被证实1)
- 自体血注射:有报告称将自体血注射到滤过泡内及周围可改善低眼压黄斑病变。但可能导致眼压急剧升高1)
- 开放性巩膜瓣缝合:若上述方法无效,则重新打开结膜,在直视下缝合巩膜瓣1)
- 巩膜开窗术:当出现明显的脉络膜脱离时,引流积聚在脉络膜上腔的液体1)
许多浆液性脉络膜渗出会随着术后伤口愈合和结膜下组织瘢痕化而消退。大多数病例通过散瞳药和类固醇滴眼液等保守治疗即可改善。但大的或持续的脉络膜渗出需要外科引流。出血性脉络膜脱离比浆液性更严重,需要更积极的干预。
Kissing choroidal(接触型脉络膜脱离)是指对侧的脉络膜脱离隆起至从视神经到晶状体相互接触的状态。伴有前房消失,视网膜血流障碍和角膜内皮损伤的风险高,是外科引流的绝对适应症。
6. 病理生理学·详细发病机制
Section titled “6. 病理生理学·详细发病机制”脉络膜的解剖特征
Section titled “脉络膜的解剖特征”脉络膜组织学上从外向内分为上脉络膜、血管层、脉络膜毛细血管层和Bruch膜四层。脉络膜在视神经和后睫状动脉进入眼球以及涡静脉离开眼球的部位与巩膜牢固结合。上脉络膜与巩膜的连接前方较松,后方较紧。这些连接部位决定了脉络膜脱离的多房形态。
巩膜与脉络膜之间的间隙称为脉络膜外腔,上脉络膜(一层薄的有色结缔组织膜)存在于该间隙中。由于上脉络膜与巩膜前方的连接较松,早期脉络膜脱离表现为睫状体平坦部和周边脉络膜的隆起。
Starling公式与脉络膜渗出
Section titled “Starling公式与脉络膜渗出”在正常的脉络膜毛细血管中,静水压保持平衡。当各种原因导致这种平衡被破坏时,血液中的白蛋白会漏出毛细血管,渗出液积聚在脉络膜上腔6)。
低眼压导致间质压(≈眼压)降低,毛细血管压相对升高,液体在脉络膜上腔积聚。一旦形成脉络膜渗出,含有蛋白质的血清在脉络膜上腔积聚,胶体渗透压的平衡限制了葡萄膜的再吸收。在脉络膜循环障碍中,脉络膜毛细血管的漏出增加;在脉络膜炎症中,毛细血管通透性增加,血液的液体成分漏出到血管外。
出血性脉络膜脱离的发病机制
Section titled “出血性脉络膜脱离的发病机制”后睫状动脉(短后睫状动脉)的分支因眼球突然减压而破裂,血液迅速在脉络膜上腔积聚。从高眼压状态突然降低眼压是最大的风险。伴有动脉硬化的老年人血管壁脆弱,破裂阈值降低。如果发生在术中,可能导致驱逐性出血,这是一种严重的并发症,导致眼内容物脱出。
RPE泵衰竭与浆液性视网膜脱离
Section titled “RPE泵衰竭与浆液性视网膜脱离”如果脉络膜脱离持续较长时间,视网膜色素上皮(RPE)的屏障机制失代偿,导致视网膜下液积聚,发生非孔源性视网膜脱离。如果伴随的非孔源性视网膜脱离长期存在,且中心凹下的视网膜色素上皮受损,即使手术获得解剖学改善,视力改善也很困难。
小眼球与葡萄膜渗漏综合征
Section titled “小眼球与葡萄膜渗漏综合征”在小眼球中,巩膜异常(增厚)压迫涡静脉,阻碍涡静脉引流,导致视网膜下液积聚。有报道称巩膜增厚是由于胶原纤维排列异常所致。
在葡萄膜渗漏综合征中,巩膜异常阻碍了富含蛋白质的液体从脉络膜血管外经巩膜向外移动6)。富含蛋白质的渗出液在脉络膜上腔积聚,胶体渗透压差导致液体持续滞留。本病缓解与复发交替,迁延不愈,长期脉络膜脱离逐渐导致脉络膜视网膜萎缩和视网膜色素上皮功能下降,引起视力障碍。
Gass于1983年报告巩膜部分切除术和巩膜开窗术对葡萄膜渗漏综合征有效,1990年报告约56%的病例视力改善两行以上。但若非孔源性视网膜脱离长期存在,即使手术获得解剖学改善,视力恢复也有限。
此外,像Hunter综合征这样的黏多糖代谢异常也可导致巩膜增厚,继发性脉络膜脱离。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”微创青光眼手术与脉络膜渗出
Section titled “微创青光眼手术与脉络膜渗出”微创青光眼手术相比传统滤过手术,脉络膜渗出的风险较低。然而,尽管XEN45凝胶支架的小内腔(约45 μm)理论上可以避免术后早期低眼压,但仍有脉络膜渗出的报道2)。
Cassottana等人(2023)报告了一例84岁男性在XEN45植入术后发生双侧脉络膜渗出的病例。右眼使用散瞳药和类固醇后一个月内改善,但左眼对保守治疗无效,两个月后需要经巩膜引流。高龄、术前多种药物使用、术后一周内眼压低于10 mmHg被确定为主要风险因素2)。
术后24至48小时内眼压低于10 mmHg被认为是预后不良因素2)。
单眼发病与对侧眼风险
Section titled “单眼发病与对侧眼风险”单眼脉络膜渗出可能是对侧眼相同手术的风险因素2)。在白内障手术中,如果一只眼发生术中脉络膜渗出,对侧眼的风险也很高,因此可考虑在全身麻醉下手术或转至具备全身麻醉条件的机构。
药物诱发的脉络膜渗出
Section titled “药物诱发的脉络膜渗出”Shaheen等人(2023)报告了一例局部使用多佐胺引起的急性浆液性和出血性脉络膜渗出病例。一名78岁男性在开始使用多佐胺-噻吗洛尔复方滴眼液两天后出现左眼脉络膜渗出,停用多佐胺并使用1%泼尼松龙和1%阿托品滴眼液后四天内完全消退。十年前也有类似发作,证实了特异性体质反应的再现性3)。
在人工晶状体眼中,由于缺乏晶状体屏障,药物向玻璃体的渗透增加,可能增加发病风险3)。口服碳酸酐酶抑制剂(乙酰唑胺、醋甲唑胺)未引起脉络膜渗出的病例也有报道,提示局部和全身用药的病理生理可能不同3)。
葡萄膜渗漏综合征的巩膜手术
Section titled “葡萄膜渗漏综合征的巩膜手术”对于葡萄膜渗漏综合征,部分巩膜切除术和巩膜开窗术的有效性已有报道。Gass报告约56%的病例视力改善两行或以上。然而,如果伴随的非孔源性视网膜脱离持续时间长,中心凹下视网膜色素上皮受损,即使手术获得解剖学改善,视力改善也可能困难。
- 影像诊断的进步:期待OCTA和广角OCT对术后脉络膜渗出的早期检测和定量评估的标准化。传统B超难以检测的微小渗出评估正成为可能。
- 按手术方式的管理指南:随着微创青光眼手术的普及,需要建立每种手术方式特有的脉络膜渗出发生率和处理指南。
- 对侧眼风险评估:单眼发病后对侧眼风险预测的生物标志物探索是未来的研究课题。
- 药物诱发机制的阐明:碳酸酐酶抑制剂的局部给药和全身给药可能具有不同的病理生理学,有报道称口服乙酰唑胺未发生脉络膜渗出的病例3)。有望提高药物选择的安全性。
微创青光眼手术相比传统滤过手术风险较低,但即使采用XEN凝胶支架等术式,也有0-15%的病例报告发生脉络膜渗出。高龄、术前使用多种青光眼药物、术后早期眼压降至10 mmHg以下时风险较高。详情请参见“原因与风险因素”一节。
8. 参考文献
Section titled “8. 参考文献”- 日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
- Cassottana P, Toma C, Maltese C, et al. A Case of Bilateral Choroidal Effusion after XEN Gel Stent Implantation. Gels. 2023;9(4):276.
- Shaheen A, Schultis S, Magraner M, et al. Acute serous and hemorrhagic choroidal effusion associated with topical dorzolamide therapy. Am J Ophthalmol Case Rep. 2023;31:101866.
- Gedde SJ, Herndon LW, Brandt JD, et al. Postoperative complications in the Tube Versus Trabeculectomy (TVT) study during five years of follow-up. Am J Ophthalmol. 2012;153(5):804-814.e1. doi:10.1016/j.ajo.2011.10.024. PMID: 22244522.
- Schrieber C, Liu Y. Choroidal effusions after glaucoma surgery. Curr Opin Ophthalmol. 2015;26(2):134-142. doi:10.1097/ICU.0000000000000131. PMID: 25643198.
- Brubaker RF, Pederson JE. Ciliochoroidal detachment. Surv Ophthalmol. 1983;27(5):281-289. doi:10.1016/0039-6257(83)90228-X. PMID: 6407132.
