低眼压 黄斑 病变是指眼压 持续降低导致眼底后极部出现脉络膜 视网膜 皱襞、视乳头水肿 、视网膜 静脉扩张迂曲,引起视力 下降和视物变形 的病症。主要原因是青光眼 滤过手术 后过度滤过和钝挫伤引起的睫状体分离 。滤过手术 后的发病率为0.9%~5% 1) 。
眼压 在8~10 mmHg以下可能发病,但5 mmHg以下发病率明显升高。好发于年轻人和高度近视 患者。OCT 是检测和评估脉络膜 视网膜 皱襞最简单、最优秀的方法,也有助于识别光感受器皱襞 9) 。许多病例通过保守治疗(加压眼罩、阿托品滴眼液)可自然缓解,但若无改善,则进行自体血注射 4, 5, 6) 或经结膜 巩膜 瓣缝合 3, 12) 。
低眼压 持续3个月以上容易留下永久性视力 障碍,因此建议在1~6个月内进行手术干预。外伤后睫状体分离 型,采用激光光凝(绿/黄色波长,光斑直径100~200 μm,200 mW以上)促进睫状体 与巩膜 的粘连形成。
低眼压 黄斑 病变(Hypotony Maculopathy)是由于各种原因导致持续低眼压 ,在眼底后极部形成脉络膜 视网膜 皱襞,引起视功能障碍的一种疾病。常伴有视乳头水肿 、视网膜 静脉扩张迂曲、脉络膜 静脉扩张,主观症状多为视力 下降和视物变形 。
该病于1954年由Dellaporta首次报道了与低眼压 相关的眼底改变,1972年Gass为明确与脉络膜皱襞 相关的视力 下降的病因,提出了“低眼压 黄斑 病变”的名称8) 。低眼压 本身在术后或外伤后相对常见,但只有部分病例会发展为黄斑 病变并导致视功能障碍。巩膜 硬度和眼轴长度 等个体因素影响发病。
低眼压 黄斑 病变可在眼压 8~10 mmHg或以下发病,5 mmHg以下发病率升高。统计学上,眼压 低于6.5 mmHg(低于平均眼压 3个标准差以上)被定义为“低眼压 ”。临床上,指低到足以引起视功能障碍的眼压 状态。
Gass假说认为,脉络膜 视网膜 皱襞引起的视网膜色素上皮 (RPE )和感光细胞 的机械性应变是视功能障碍的主要原因,该假说被广泛接受。低眼压 导致眼球壁向内塌陷时,脉络膜 和视网膜 出现冗余,形成皱襞。如果这种变化在短期内消退,视功能可以恢复,但如果长期持续,则会留下不可逆的视功能障碍。
Q
低眼压是指眼压低于多少 mmHg?
A
统计学上,低眼压 定义为眼压 低于6.5 mmHg,即低于平均眼压 3个标准差。但低眼压 黄斑 病变可在眼压 8~10 mmHg或以下发病,5 mmHg以下发病率明显升高。4 mmHg以下常导致严重视力 下降(矫正视力 0.2以下)。临床上,以影响视功能的低眼压 水平为问题所在。
最常见的原因是青光眼 滤过手术 后过度滤过,尤其是联合丝裂霉素C(MMC)的小梁切除术 后容易发生。根据青光眼 诊疗指南,术后1个月以后可能引起视功能障碍的并发症中,低眼压 黄斑 病变的发生率为0.95% 1) 。Costa & Arcieri(2007)的综述总结发病率为1.318% 8) 。其次常见的原因是钝挫伤引起的睫状体分离 。
已知好发于年轻人和高度近视 者2) 。年轻且近视 眼的巩膜 硬度低,因此在低眼压 下巩膜 容易向内塌陷,容易形成脉络膜皱襞 。老年患者容易发生脉络膜 渗漏,而年轻患者则倾向于发生低眼压性黄斑病变 。自从抗代谢药 物普及以来,滤过手术 后低眼压性黄斑病变 的报告有所增加。
低眼压性黄斑病变 的原因大致分为房水 流出增加和房水 生成减少。
青光眼 滤过手术 后过度滤过小梁切除术 后,眼压 显著下降时可能发生。涉及结膜 创口房水 渗漏、巩膜 瓣过度房水 流出、MMC对睫状体 的直接毒性等。钝挫伤后睫状体分离 :房角 发生睫状体分离 时,房水 流入脉络膜 上腔,同时房水 生成也减少。经葡萄膜巩膜 流出病理性增加导致显著低眼压 。葡萄膜炎 /睫状体 炎房水 生成减少导致低眼压 。前部增殖性玻璃体视网膜病变 进展 :周边视网膜 和睫状体 脱离迁延会导致房水 生成能力下降。视网膜脱离 手术后/玻璃体 手术后巩膜 切开部位渗漏或术后炎症引起的一过性低眼压 是原因。既往玻璃体 手术史、年轻、近视 是危险因素9) 。引流阀植入术后 :TVT研究显示,滤过泡渗漏 、低眼压性黄斑病变 和滤过泡感染在小梁切除术 组更常见,而引流阀组角膜内皮 损伤和植入物暴露倾向更多1) 。玻璃体内注射 抗VEGF后高度近视 或玻璃体 手术后巩膜 脆弱病例的发病报告11) 。双眼低眼压 :包括渗透性脱水、糖尿病昏迷、尿毒症、强直性肌营养不良等。
Fannin等人(2003)确定了低眼压性黄斑病变 的以下危险因素7) 。
年轻 :巩膜 硬度低,容易塌陷。巩膜 瓣愈合能力弱,过度滤过容易持续。男性 :发生率有高于女性的倾向。近视 (尤其是高度近视 )巩膜 薄而软,容易形成皱襞。首次青光眼 滤过手术 :在熟练掌握术后管理之前的阶段风险较高。使用抗纤维化药物 :MMC的风险高于5-FU。术前眼压 高 :术前眼压 越高,术后下降幅度越大。
滤过手术 时,应将MMC的浓度和作用时间控制在必要的最小限度,并避免接触结膜 边缘。建议术中用多根尼龙线牢固缝合巩膜 瓣,术后通过激光缝线松解(LSL )逐步调整滤过量1) 。
术后早期过度LSL 会增加低眼压 的风险,因此谨慎判断时机很重要。
青光眼 手术后应定期检查眼压 ,如感觉异常请立即就医。
Q
为什么年轻人和近视的人风险较高?
A
年轻人巩膜 瓣瘢痕形成较弱,术后容易持续过度滤过。近视 者,尤其是高度近视 ,巩膜 薄而脆弱,即使同样低眼压 ,也更容易形成脉络膜 视网膜 皱襞。这些因素叠加时风险进一步增加。
低眼压 黄斑 病变的发生与房水 动力学异常和眼球壁的机械变形密切相关。
导致低眼压 的房水 动力学异常大致可分为两类。
房水 流出增加睫状体分离裂隙 引起的房水 流出。睫状体分离 时,经葡萄膜巩膜 流出道病理性增加。房水 生成减少睫状体 炎症、睫状体 直接损伤(外伤、手术、药物毒性)、前部增殖性玻璃体视网膜病变 导致的睫状体 功能低下。
外伤后睫状体分离 时,睫状体 形成开放通道,房水 流入上脉络膜 腔,同时睫状体 上皮受损导致房水 生成减少。使用抗代谢药 物(MMC、5-FU)的滤过手术 中,巩膜 瓣周围的瘢痕形成受到抑制,房水 渗漏增加1) 。
发生低眼压 时,巩膜 壁向内塌陷,脉络膜 和视网膜 出现冗余,形成特征性的脉络膜 视网膜 皱襞。眼的前后径缩短,屈光 不正表现为远视 化。
Sakamoto等人(2018)报告,在小梁切除术 后低眼压 黄斑 病变的发生中,过度的巩膜 收缩比脉络膜 增厚是更主要的贡献因素2) 。持续低眼压 导致巩膜 胶原纤维松弛和收缩,眼轴长度 不可逆地缩短。
1972年Gass提出的假说认为,脉络膜 视网膜 皱襞对RPE 和感光细胞 产生机械性应变,这是视功能损害的本质。该假说至今仍被广泛接受。
近年来的OCT 研究发现了与脉络膜皱襞 不同的感光细胞 皱襞(photoreceptor folds)9) 。感光细胞 皱襞形成于脉络膜皱襞 的正下方,并伴有感光细胞 外节断裂(photoreceptor disruption)。这种感光细胞 的机械性损伤是不可逆中心视力 下降的主要原因;即使脉络膜皱襞 消退,如果感光细胞 损伤持续存在,视力 恢复也不良9) 。
低眼压 时筛板 向前隆起,轴浆流受限,急性期出现视乳头水肿 。在进展期青光眼 中,存活轴突较少时,即使低眼压 也可能不出现明显的视乳头肿胀。
眼压 降低导致眼球后部弯曲时,视网膜 静脉回流受阻,引起淤滞。临床上表现为视网膜 静脉扩张迂曲。
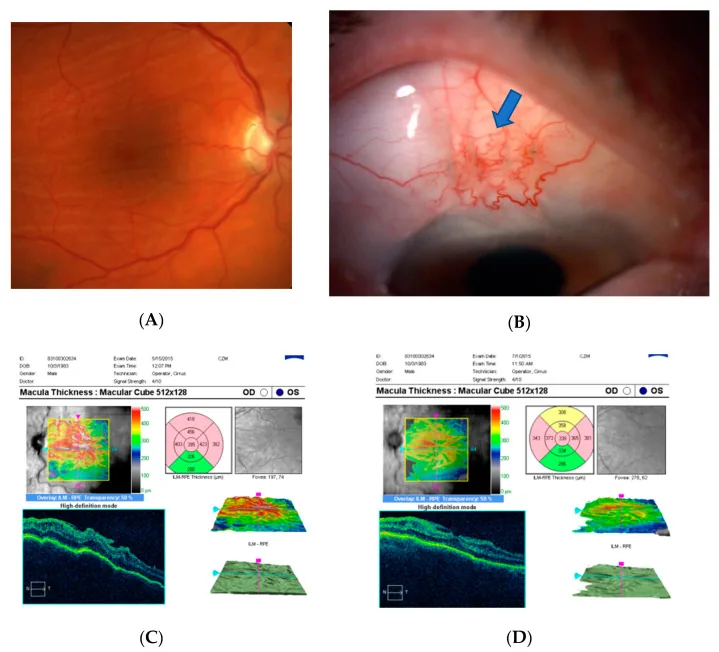
低眼压黄斑病变的眼底像和OCT所见 Kosior-Jarecka E, et al. Bleb Compressive Sutures in the Management of Hypotony Maculopathy after Glaucoma Surgery. J Clin Med. 2021. Figure 4. PM
CI D: PMC8196590. License: CC BY.
(A) 低眼压 黄斑 病变的眼底像,(B) 术后第1天的加压缝合(蓝色箭头),(C) 缝合前的黄斑 OCT ,(D) 缝合后的黄斑 OCT 。对应本文“4. 临床表现”部分讨论的低眼压 黄斑 病变。
视力 下降眼压 低于4 mmHg时,矫正视力 常降至0.2或以下。视物变形 黄斑 皱襞引起的扭曲。远视 化眼轴 缩短导致的屈光 改变。无症状 :早期或轻症病例可完全无症状,有时在常规OCT检查 中偶然发现。
低眼压 持续时间与最终视力 不一定相关,但早期恢复眼压 可改善视功能。
低眼压 黄斑 病变的眼底表现无论病因如何都具有共同特征,但伴随表现因病因不同而异。
脉络膜视网膜皱襞
后极部皱襞 :呈放射状或同心圆排列。是低眼压 黄斑 病变最具特征性的表现。
与视力 障碍的关系 :皱襞的方向、密度及与黄斑 中心的距离影响视力 预后。
血管迂曲
视网膜 动脉迂曲视网膜 血管冗余而迂曲。
视网膜 静脉扩张迂曲
视神经乳头改变
视乳头水肿 筛板 前隆引起的轴浆运输障碍有关。
视乳头血管迂曲 :慢性期可能残留视乳头周围血管迂曲。
眼前节所见
浅前房 房水 渗漏或睫状体分离 。
屈光 远视 化眼轴 缩短导致远视 。可能伴有脉络膜 脱离。
滤过术后型
脉络膜 视网膜 皱襞
视神经乳头水肿 充血 、肿胀。
视网膜 静脉扩张迂曲
浅前房 虹膜 、晶状体 、玻璃体 前移。
脉络膜 脱离
外伤型(睫状体分离)
黄斑 皱襞脉络膜 视网膜 皱襞。
视盘水肿 和充血
视网膜 血管扩张迂曲视网膜 静脉和动脉的迂曲。
浅前房 晶状体 虹膜 隔前移。
房角后退 睫状体分离 区域一致的房角 异常。
近年来的OCT 研究不仅发现了脉络膜皱襞 ,还发现了光感受器皱襞,光感受器层的机械损伤被认为是不可逆中心视力 下降的主要原因9) 。Henle纤维层的高反射也被报道为特征性OCT 表现9) 。
当低眼压 持续时,巩膜 过度收缩导致眼轴 缩短。Sakamoto等人(2018)报道,与小梁切除术 后低眼压 黄斑 病变的发生相比,过度巩膜 收缩比脉络膜 增厚贡献更大2) 。超声B超 可观察到后部巩膜 和脉络膜 增厚,不少病例伴有脉络膜 脱离。
Maheshwari等人(2022)报告了一例70岁男性原发性开角型青光眼 病例3) 。白内障 和青光眼 联合手术后出现严重低眼压 (1 mmHg)和360度脉络膜 脱离,导致低眼压 黄斑 病变。经结膜 巩膜 瓣缝合后脉络膜 脱离消退,眼压 和视力 均改善。
低眼压 黄斑 病变的诊断相对容易,基于病史、眼压测量 确认低眼压 以及特征性眼底表现。
眼压测量 低眼压 (典型≤5 mmHg,≤10 mmHg时怀疑)眼底检查 脉络膜 视网膜 皱襞、视盘水肿 、视网膜 静脉扩张迂曲
各检查方法的特点如下所示。
检查方法 主要评估对象 特点 OCT 脉络膜 视网膜 皱襞/感光细胞 皱襞简便且首选。可检测细微皱襞。 FA 皱襞部线状低荧光、视乳头荧光渗漏 也可用于评估视网膜 循环延迟。 ICG 脉络膜 静脉扩张、皱襞部低荧光FA 不清晰时补充使用。UBM /眼前节OCT 睫状体分离 的位置和范围对查找外伤型原因必不可少。 B超 脉络膜 增厚、脉络膜 脱离即使屈光 间质混浊也可使用。
OCT 是首选检查方法,其检出能力高于眼底检查 。仔细检查所有径向扫描非常重要。即使眼底临床检查正常,OCT 也可能检测到病理变化9) 。
荧光素眼底血管造影 (FA )的特征性表现为与皱褶处RPE 变薄相对应的线状低荧光,以及皱褶顶部脉络膜 荧光增强。吲哚青绿血管造影(ICG)作为FA 诊断困难病例的补充检查,可见脉络膜 静脉扩张迂曲和大量线状低荧光。
外伤后低眼压 黄斑 病变中,超声生物显微镜 (UBM )和前段OCT 对评估睫状体 脱离范围至关重要。房角镜检查 也可观察到睫状体 脱离。
Q
OCT检查能发现低眼压黄斑病变的哪些信息?
A
OCT 可高精度检测脉络膜 视网膜 皱褶,并能识别眼底检查 可能遗漏的细微皱褶。此外,还可评估与视功能预后相关的表现,如光感受器皱褶和Henle纤维层高反射9) 。OCT 对治疗后随访也有用,可客观判断皱褶改善和残留的光感受器损伤。
根据低眼压 的存在和特征性眼底表现组合进行诊断。询问青光眼 手术史、外伤史、玻璃体 手术史和抗VEGF注射史。
引起脉络膜 视网膜 皱褶的疾病鉴别诊断中,有”THIN RPE ”的口诀。
T(Tumors) :脉络膜 肿瘤、转移性肿瘤H(Hypotony) :低眼压 (本病)I(Inflammation / Idiopathic) :后巩膜炎 、特发性N(Neovascularization) :年龄相关性黄斑变性 等脉络膜新生血管 R(Retrobulbar mass / Retinal detachment) :眼眶 后方肿块、视网膜脱离 P(Papilledema) :颅内压增高引起的视乳头水肿 E(Extraocular hardware) :巩膜 扣带、放射敷贴器等
在考虑是否存在低眼压 、青光眼 手术史和外伤史的基础上进行鉴别诊断。
Q
低眼压黄斑病变的脉络膜视网膜皱襞在其他疾病中也能见到吗?
A
正如THIN RPE 助记符所示,肿瘤、炎症、视乳头水肿 、眼眶 占位性病变等多种疾病都可能出现脉络膜 视网膜 皱襞。需要在考虑是否存在低眼压 、青光眼 手术史和外伤史的基础上进行鉴别诊断。
低眼压 黄斑 病变的治疗以确定病因并处理为优先。由于许多病例可自然缓解,首先进行保守治疗,若无改善则逐步考虑积极干预。
重要的时间限制 :据报道,低眼压 黄斑 病变持续超过3个月容易留下永久性视力 损害。建议在视功能损害成为永久性之前进行手术治疗,一般需在1至6个月内做出判断。4 mmHg或以下的显著低眼压 持续2至3个月容易留下视物变形 和相对中心暗点 。另一方面,如果眼压 高于4 mmHg,即使持续半年左右,视功能也可能恢复。
根据病因采取不同的方法。
滤过术后过度滤过 :
加压眼垫 :用纱布等准确压迫巩膜 瓣 1) 佩戴大型软性隐形眼镜 :抑制滤过泡渗漏 硫酸阿托品水合物滴眼液 :睫状肌松弛、前房 加深 1) 类固醇 滴眼液(消炎)房水 生成减少
外伤后睫状体分离 :
1%阿托品滴眼液 : 持续保守治疗后,眼压 突然升高常导致睫状体分离 自然缓解。类固醇 滴眼液
睫状体 功能低下(PVR 后)
睫状体 功能低下(PVR 后)
如果保守治疗无效,考虑以下干预措施。
自体血注射 : 将自体血注射到滤过泡内及周围以减少滤过 4, 5, 6) 。需注意可能引起眼压 急剧升高 10) 。经结膜 巩膜 瓣缝合 : 通过结膜 直接用尼龙线缝合巩膜 瓣的方法,长期证明对低眼压 黄斑 病变有效 3, 12) 。前房 内注入粘弹剂或空气前房 容积,暂时升高眼压 。可重复进行,但效果常为暂时性。追加巩膜 缝合 : 手术再次打开结膜 ,在直视下缝合巩膜 瓣。如有明显脉络膜 脱离,需通过巩膜 开窗术排出脉络膜 上腔积液。
如果上述方法无效或眼压 未能恢复,手术选择如下。
激光光凝(睫状体分离 处) : 适用于睫状体分离 1-2周未缓解者。使用绿色或黄色波长激光,光斑100-200 μm,持续时间0.2-0.5秒,功率200 mW以上,使睫状体 轻微收缩并析出少量纤维蛋白。无效则数日后重复。眼压 恢复前常出现一过性高眼压 。睫状体 缝合术角膜缘 3.5 mm处制作半层巩膜 切口或巩膜 瓣,用可吸收缝线将脱离的睫状体 上皮缝合到巩膜 上。滤过泡重建(结膜 前徙术) : 切除变薄的滤过泡,通过结膜 前徙重建滤过泡 13) 。其他手术 :已报道的有透热凝固术、睫状体 冷冻凝固 术、巩膜扣带术 、环扎术、玻璃体 腔注气术、人工晶体 缝线固定术等。
治疗的阶段和时机总结如下。
时机 处理 早期(~1个月) 保守治疗(加压眼罩、SCL、阿托品、类固醇 ) 无改善 自体血注射、粘弹性物质注射、经结膜 巩膜 瓣缝合 1~3个月 激光光凝(睫状体分离 处)、继续观察 6个月内 手术(睫状体 缝合术、滤过泡重建、巩膜扣带术 等)
自体血注射后可能出现急剧的眼压 升高10) ,注射后的眼压 监测很重要。
激光光凝后的一过性高眼压 也需要注意。
如果眼压 持续低于4 mmHg达2-3个月,视力 恢复不良,且容易残留视物变形 和相对中心暗点 。早期恢复眼压 对预后至关重要。
Q
低眼压黄斑病变是否需要紧急手术?
A
低眼压 黄斑 病变有自然缓解的病例,因此首先尝试保守治疗。但如果低眼压 持续超过3个月,容易留下永久性视力 障碍,因此保守治疗无效时应在1-6个月内考虑手术干预。特别是眼压 低于4 mmHg的显著低眼压 ,最好在2个月内恢复眼压 。
Q
低眼压黄斑病变如果不治疗会怎样?
A
如果眼压 持续低于4 mmHg较长时间,视网膜 、巩膜 和脉络膜 内的纤维化可能进展,导致不可逆的视力 障碍。2个月内恢复眼压 是重要的参考指标。如果眼压 高于4 mmHg,即使持续半年左右也可能恢复。
如果早期恢复眼压 ,视功能有望改善。另一方面,如果感光细胞 皱襞或巩膜 、脉络膜 纤维化固定,则会残留不可逆的视力 障碍9) 。眼压 低于4 mmHg持续2-3个月时,容易残留视物变形 和相对中心暗点 。
脉络膜 脱离眼轴 缩短导致的不可逆远视 永久性感光细胞 损伤 :感光细胞 外节断裂导致中心视力 下降9) 视盘周围视网膜 劈裂 :在慢性低眼压 中有报道
Lee & Woo(2021)报告了两例因黄斑前膜 切除玻璃体 手术后发生低眼压性黄斑病变 的病例(53岁女性和20岁男性,韩国)。两例均在25G无缝线玻璃体 手术后出现无法测量的低眼压 ,OCT 识别出特征性的感光细胞 皱襞和Henle纤维层高反射。即使眼压 恢复正常,感光细胞 损伤仍然存在,一年后的视力 比术前更差。既往玻璃体 手术史、年轻、近视 被认为是低眼压性黄斑病变 的危险因素9) 。
Barbosa等人(2022)报告了一例70多岁女性在非穿透性青光眼 手术(深层巩膜切除术 )三年后发生眼压 2 mmHg的低眼压性黄斑病变 的病例。使用地塞米松滴眼液每日五次和环戊通每日两次,八周后完全恢复,但停用类固醇 两个月后复发。重新开始并维持类固醇 滴眼液后,14个月内保持了稳定的眼压 (14-17 mmHg)和良好的视力 14) 。这是一份将类固醇 应答者特性应用于治疗的有趣报告。
Maheshwari等人(2022)报告了一种不经结膜 切口、经结膜 缝合巩膜 瓣的微创技术3) 。在一例70岁男性青光眼 病例中,白内障 和青光眼 联合手术后出现严重低眼压 (1 mmHg)和360度脉络膜 脱离,该技术使脉络膜 脱离消退,眼压 和视力 均得到改善。该技术被介绍为一种微创且可在门诊进行的有前景的方法。
Lima-Fontes等人(2022)报告了一例52岁男性弹性纤维假性黄色瘤患者,在雷珠单抗 玻璃体腔内注射 (第78次注射后)发生低眼压性黄斑病变 的病例。原因是30G针头注射部位的巩膜 裂开。高度近视 、弹性纤维假性黄色瘤、反复注射、既往玻璃体 手术导致的玻璃体 缺失被认为是巩膜 脆弱的因素。通过巩膜 缝合和阿托品、地塞米松滴眼液恢复11) 。
Markopoulos等人(2023)报告了一名78岁男性,在小梁切除术 后因低眼压 (6 mmHg)出现视乳头周围视网膜 劈裂(PPRS)。使用地塞米松0.1%滴眼液每日两次和奈帕芬胺滴眼液每日三次治疗4周后,PPRS完全消失,眼压 恢复至16 mmHg。推测低眼压 导致毛细血管静水压梯度改变,促进液体进入细胞外间隙,是PPRS发生的机制15) 。
对于难治性低眼压 黄斑 病变,已有报告采用玻璃体切除术 联合内界膜 (ILM )剥离,以及使用全氟碳液(PFCL)平复脉络膜 视网膜 皱襞的方法。这些均处于病例报告水平,尚未确立为标准治疗。
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
Sakamoto M, Matsumoto Y, Mori S, et al. Excessive scleral shrinkage, rather than choroidal thickening, is a major contributor to the development of hypotony maculopathy after trabeculectomy. PLoS One. 2018;13:e0191862.
Maheshwari D, Shyam P, Pawar N, Ramakrishnan R. Transconjunctival flap sutures: A novel technique to combat hypotony. Indian J Ophthalmol. 2022;70(6):2223-2225.
Wise JB. Treatment of chronic postfiltration hypotony by intrableb injection of autologous blood. Arch Ophthalmol. 1993;111:827-830.
Nuyts RM, Greve EL, Geijssen HC, Langerhorst CT. Treatment of hypotonous maculopathy after trabeculectomy with mitomycin C. Am J Ophthalmol. 1994;118:322-331.
Okada K, Tsukamoto H, Masumoto M, et al. Autologous blood injection for marked overfiltration early after trabeculectomy with mitomycin C. Acta Ophthalmol Scand. 2001;79:305-308.
Fannin LA, Schiffman JC, Budenz DL. Risk factors for hypotony maculopathy. Ophthalmology. 2003;110:1185-1191.
Costa VP, Arcieri ES. Hypotony maculopathy. Acta Ophthalmol Scand. 2007;85:586-597.
Lee YJ, Woo SJ. Hypotony maculopathy and photoreceptor folds with disruptions after vitrectomy for epiretinal membrane removal: two case reports. J Med Case Reports. 2021;15:255.
Siegfried CJ, Grewal RK, Karalekas D, et al. Marked intraocular pressure rises complicating intrableb autologous blood injection. Arch Ophthalmol. 1996;114:492-493.
Lima-Fontes M, Godinho G, Cunha AM, et al. Hypotony Maculopathy Related to Anti-VEGF Intravitreal Injection. Int Med Case Rep J. 2022;15:517-520.
Eha J, Hoffmann EM, Pfeiffer N. Long-term results after transconjunctival resuturing of the scleral flap in hypotony following trabeculectomy. Am J Ophthalmol. 2013;155:864-869.
Satpute K, Bukke AN, Verma S, Dada T. Conjunctival advancement for management of hypotony maculopathy after trabeculectomy. BMJ Case Rep. 2022;15:e251718.
Barbosa RC, Bastos R, Tenedório P. Recurrent macular neurosensory detachment in hypotony maculopathy managed with topical corticosteroids. BMJ Case Rep. 2022;15:e248773.
Markopoulos I, Tzakos M, Tzimis V, Halkiadakis I. Peripapillary Retinoschisis as a Manifestation of Ocular Hypotony. Case Rep Ophthalmol. 2023;14:13-17.