低眼壓黃斑病變是指眼壓 持續降低導致眼底後極部出現脈絡膜 視網膜 皺襞、視神經乳頭水腫 、視網膜 靜脈擴張迂曲,引起視力 下降和視物變形的病症。
主要原因是青光眼 濾過手術 後過度濾過和鈍挫傷引起的睫狀體分離 。濾過手術 後的發生率為0.9%~5% 1) 。
眼壓 在8~10 mmHg以下可能發病,但5 mmHg以下發生率明顯升高。好發於年輕人和高度近視 患者。OCT 是檢測和評估脈絡膜 視網膜 皺襞最簡單、最優秀的方法,也有助於識別光感受器皺襞 9) 。許多病例通過保守治療(加壓眼罩、阿托品眼藥水)可自然緩解,但若無改善,則進行自體血注射 4, 5, 6) 或經結膜 鞏膜 瓣縫合 3, 12) 。
低眼壓 持續3個月以上容易留下永久性視力 障礙,因此建議在1~6個月內進行手術干預。外傷後睫狀體分離 型,採用雷射光凝(綠/黃色波長,光斑直徑100~200 μm,200 mW以上)促進睫狀體 與鞏膜 的粘連形成。
低眼壓 黃斑部 病變(Hypotony Maculopathy)是由於各種原因導致持續低眼壓 ,在眼底後極部形成脈絡膜 視網膜 皺褶,引起視功能障礙的一種疾病。常伴有視乳頭水腫 、視網膜 靜脈擴張迂曲、脈絡膜 靜脈擴張,主觀症狀多為視力 下降和變視症 。
該病於1954年由Dellaporta首次報告了與低眼壓 相關的眼底變化,1972年Gass為明確與脈絡膜 皺褶相關的視力 下降的病因,提出了「低眼壓 黃斑部 病變」的名稱8) 。低眼壓 本身在術後或外傷後相對常見,但只有部分病例會發展為黃斑部 病變並導致視功能障礙。鞏膜 硬度和眼軸長度 等個體因素影響發病。
低眼壓 黃斑部 病變可在眼壓 8~10 mmHg或以下發病,5 mmHg以下發病率升高。統計學上,眼壓 低於6.5 mmHg(低於平均眼壓 3個標準差以上)被定義為「低眼壓 」。臨床上,指低到足以引起視功能障礙的眼壓 狀態。
Gass假說認為,脈絡膜 視網膜 皺褶引起的視網膜色素上皮 (RPE )和感光細胞 的機械性應變是視功能障礙的主要原因,該假說被廣泛接受。低眼壓 導致眼球壁向內塌陷時,脈絡膜 和視網膜 出現冗餘,形成皺褶。如果這種變化在短期內消退,視功能可以恢復,但如果長期持續,則會留下不可逆的視功能障礙。
Q
低眼壓是指眼壓低於多少 mmHg?
A
統計學上,低眼壓 定義為眼壓 低於6.5 mmHg,即低於平均眼壓 3個標準差。但低眼壓 黃斑部 病變可在眼壓 8~10 mmHg或以下發病,5 mmHg以下發病率明顯升高。4 mmHg以下常導致嚴重視力 下降(矯正視力 0.2以下)。臨床上,以影響視功能的低眼壓 水平為問題所在。
最常見的原因是青光眼 濾過手術 後過度濾過,尤其是合併絲裂黴素C(MMC)的小樑切除術 後容易發生。根據青光眼 診療指引,術後1個月以後可能引起視功能障礙的併發症中,低眼壓 黃斑部 病變的發生率為0.95% 1) 。Costa & Arcieri(2007)的綜述總結發生率為1.318% 8) 。其次常見的原因是鈍挫傷引起的睫狀體分離 。
已知好發於年輕人和高度近視 者2) 。年輕且近視 眼的鞏膜 硬度低,因此在低眼壓 下鞏膜 容易向內塌陷,容易形成脈絡膜皺襞 。老年患者容易發生脈絡膜 滲漏,而年輕患者則傾向於發生低眼壓 性黃斑部 病變。自從抗代謝藥物 普及以來,濾過手術 後低眼壓 性黃斑部 病變的報告有所增加。
低眼壓 性黃斑部 病變的原因大致分為房水 流出增加和房水 生成減少。
青光眼 濾過手術 後過度濾過小樑切除術 後,眼壓 顯著下降時可能發生。涉及結膜 傷口房水 滲漏、鞏膜 瓣過度房水 流出、MMC對睫狀體 的直接毒性等。鈍挫傷後睫狀體分離 :隅角 發生睫狀體分離 時,房水 流入脈絡膜 上腔,同時房水 生成也減少。經葡萄膜鞏膜 流出病理性增加導致顯著低眼壓 。葡萄膜炎 /睫狀體 炎房水 生成減少導致低眼壓 。前部增殖性玻璃體視網膜病變 進展 :周邊視網膜 和睫狀體 脫離遷延會導致房水 生成能力下降。視網膜剝離 手術後/玻璃體 手術後鞏膜 切開部位滲漏或術後炎症引起的一過性低眼壓 是原因。既往玻璃體 手術史、年輕、近視 是危險因子9) 。引流閥植入術後 :TVT研究顯示,濾過泡滲漏 、低眼壓 性黃斑部 病變和濾過泡感染在小樑切除術 組更常見,而引流閥組角膜內皮 損傷和植入物暴露傾向較多1) 。玻璃體內注射 抗VEGF後高度近視 或玻璃體 手術後鞏膜 脆弱病例的發病報告11) 。雙眼低眼壓 :包括滲透性脫水、糖尿病昏迷、尿毒症、強直性肌營養不良等。
Fannin等人(2003)確定了低眼壓 性黃斑部 病變的以下危險因子7) 。
年輕 :鞏膜 硬度低,容易塌陷。鞏膜 瓣癒合能力弱,過度濾過容易持續。男性 :發生率有高於女性的傾向。近視 (尤其是高度近視 )鞏膜 薄而軟,容易形成皺褶。首次青光眼 濾過手術 :在熟練掌握術後管理之前的階段風險較高。使用抗纖維化藥物 :MMC的風險高於5-FU。術前眼壓 高 :術前眼壓 越高,術後下降幅度越大。
濾過手術 時,應將MMC的濃度和作用時間控制在必要的最小限度,並避免接觸結膜 邊緣。建議術中用多根尼龍線牢固縫合鞏膜 瓣,術後通過雷射縫線鬆解(LSL )逐步調整濾過量1) 。
術後早期過度LSL 會增加低眼壓 的風險,因此謹慎判斷時機很重要。
青光眼 手術後應定期檢查眼壓 ,如感覺異常請立即就醫。
Q
為什麼年輕人和近視的人風險較高?
A
年輕人鞏膜 瓣瘢痕形成較弱,術後容易持續過度濾過。近視 者,尤其是高度近視 ,鞏膜 薄而脆弱,即使同樣低眼壓 ,也更容易形成脈絡膜 視網膜 皺褶。這些因素疊加時風險進一步增加。
低眼壓黃斑病變的發生與房水 動力學異常和眼球壁的機械變形密切相關。
導致低眼壓 的房水 動力學異常大致可分為兩類。
房水 流出增加睫狀體分離裂隙 引起的房水 流出。睫狀體分離 時,經葡萄膜鞏膜 流出道病理性增加。房水 生成減少睫狀體 發炎、睫狀體 直接損傷(外傷、手術、藥物毒性)、前部增殖性玻璃體視網膜病變 導致的睫狀體 功能低下。
外傷後睫狀體分離 時,睫狀體 形成開放通道,房水 流入上脈絡膜 腔,同時睫狀體 上皮受損導致房水 生成減少。使用抗代謝藥物 (MMC、5-FU)的濾過手術 中,鞏膜 瓣周圍的瘢痕形成受到抑制,房水 滲漏增加1) 。
發生低眼壓 時,鞏膜 壁向內塌陷,脈絡膜 和視網膜 出現冗餘,形成特徵性的脈絡膜 視網膜 皺襞。眼的前後徑縮短,屈光 不正表現為遠視 化。
Sakamoto等人(2018)報告,在小梁切除術後低眼壓黃斑病變的發生中,過度的鞏膜 收縮比脈絡膜 增厚是更主要的貢獻因素2) 。持續低眼壓 導致鞏膜 膠原纖維鬆弛和收縮,眼軸長度 不可逆地縮短。
1972年Gass提出的假說認為,脈絡膜 視網膜 皺襞對RPE 和感光細胞 產生機械性應變,這是視功能障礙的本質。該假說至今仍被廣泛接受。
近年來的OCT 研究發現了與脈絡膜皺襞 不同的感光細胞 皺襞(photoreceptor folds)9) 。感光細胞 皺襞形成於脈絡膜皺襞 的正下方,並伴有感光細胞 外節斷裂(photoreceptor disruption)。這種感光細胞 的機械性損傷是不可逆中心視力 下降的主要原因;即使脈絡膜皺襞 消退,如果感光細胞 損傷持續存在,視力 恢復也不良9) 。
低眼壓 時篩板 向前隆起,軸漿流受限,急性期出現視乳頭水腫 。在進展期青光眼 中,存活軸突較少時,即使低眼壓 也可能不出現明顯的視乳頭腫脹。
眼壓 降低導致眼球後部彎曲時,視網膜 靜脈回流受阻,引起淤滯。臨床上表現為視網膜 靜脈擴張迂曲。
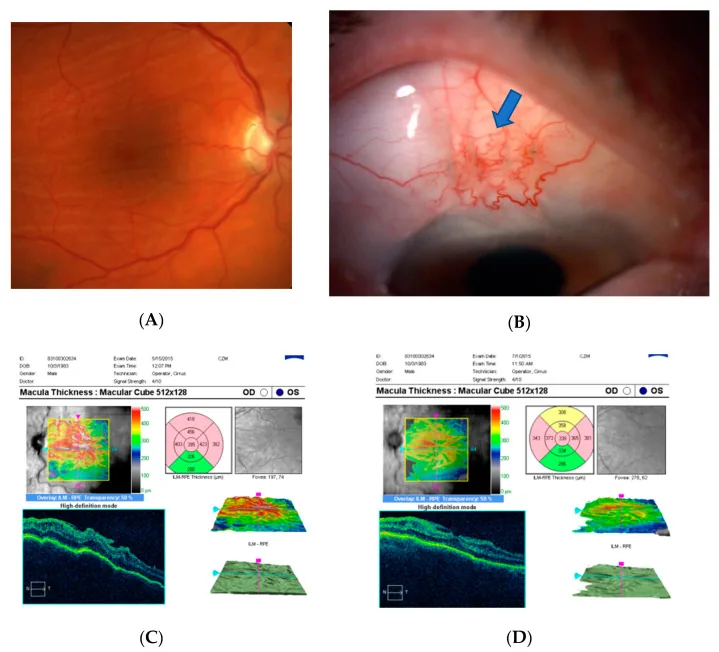
低眼壓黃斑病變的眼底像和OCT所見 Kosior-Jarecka E, et al. Bleb Compressive Sutures in the Management of Hypotony Maculopathy after Glaucoma Surgery. J Clin Med. 2021. Figure 4. PM
CI D: PMC8196590. License: CC BY.
(A) 低眼壓 黃斑部 病變的眼底像,(B) 術後第1天的加壓縫合(藍色箭頭),(C) 縫合前的黃斑 OCT ,(D) 縫合後的黃斑 OCT 。對應本文「4. 臨床表現」部分討論的低眼壓 黃斑部 病變。
視力 下降眼壓 低於4 mmHg時,矯正視力 常降至0.2或以下。變視症 黃斑 皺褶引起的扭曲。遠視 化眼軸 縮短導致的屈光 改變。無症狀 :早期或輕症病例可完全無症狀,有時在常規OCT檢查 中偶然發現。
低眼壓 持續時間與最終視力 不一定相關,但早期恢復眼壓 可改善視功能。
低眼壓 黃斑部 病變的眼底表現無論病因如何都具有共同特徵,但伴隨表現因病因不同而異。
脈絡膜視網膜皺褶
後極部皺褶 :呈放射狀或同心圓排列。是低眼壓 黃斑部 病變最具特徵性的表現。
與視力 障礙的關係 :皺褶的方向、密度及與黃斑 中心的距離影響視力 預後。
血管迂曲
視網膜 動脈迂曲視網膜 血管冗餘而迂曲。
視網膜 靜脈擴張迂曲
視神經乳頭變化
乳頭水腫 :急性期出現。與篩板 前凸引起的軸漿運輸障礙有關。
乳頭血管迂曲 :慢性期可能殘留乳頭周圍血管迂曲。
前眼部所見
淺前房 房水 滲漏或睫狀體分離 。
屈光 遠視 化眼軸 縮短導致遠視 。可能伴有脈絡膜 剝離。
濾過術後型
脈絡膜 視網膜 皺襞
視神經乳頭水腫 充血 、腫脹。
視網膜 靜脈擴張迂曲
淺前房 虹膜 、水晶體 、玻璃體 前移。
脈絡膜 剝離
外傷型(睫狀體分離)
黃斑 皺襞脈絡膜 視網膜 皺襞。
視神經 盤水腫與充血
視網膜 血管擴張迂曲視網膜 靜脈和動脈的迂曲。
淺前房 水晶體 虹膜 隔前移。
隅角後退 睫狀體分離 區域一致的隅角 異常。
近年來的OCT 研究不僅發現了脈絡膜皺襞 ,還發現了感光細胞 皺襞,感光細胞 層的機械損傷被認為是不可逆中心視力 下降的主要原因9) 。Henle纖維層的高反射也被報告為特徵性OCT 表現9) 。
當低眼壓 持續時,鞏膜 過度收縮導致眼軸 縮短。Sakamoto等人(2018)報告,與小樑切除術 後低眼壓黃斑病變的發生相比,過度鞏膜 收縮比脈絡膜 增厚貢獻更大2) 。超音波B掃描可觀察到後部鞏膜 和脈絡膜 增厚,不少病例伴有脈絡膜 剝離。
Maheshwari等人(2022)報告了一例70歲男性原發性開放隅角青光眼 病例3) 。白內障 和青光眼 聯合手術後出現嚴重低眼壓 (1 mmHg)和360度脈絡膜 剝離,導致低眼壓黃斑病變。經結膜 鞏膜 瓣縫合後脈絡膜 剝離消退,眼壓 和視力 均改善。
低眼壓黃斑病變的診斷相對容易,基於病史、眼壓測量 確認低眼壓 以及特徵性眼底表現。
眼壓測量 低眼壓 (典型≤5 mmHg,≤10 mmHg時懷疑)眼底檢查 脈絡膜 視網膜 皺襞、視盤水腫 、視網膜 靜脈擴張迂曲
各檢查方法的特點如下所示。
檢查方法 主要評估對象 特點 OCT 脈絡網膜皺襞/感光細胞 皺襞 簡便且為首選。可檢測細微皺襞。 FA 皺襞部線狀低螢光、視乳頭螢光滲漏 也可用於評估視網膜 循環延遲。 ICG 脈絡膜 靜脈擴張、皺襞部低螢光FA 不明確時補充使用。UBM /前眼部OCT 睫狀體分離 的位置和範圍對查找外傷型原因必不可少。 B超 脈絡膜 增厚、脈絡膜 剝離即使屈光 間質混濁也可使用。
OCT 是第一線檢查方法,其檢出能力高於眼底檢查 。仔細檢查所有徑向掃描非常重要。即使眼底臨床檢查正常,OCT 也可能檢測到病理變化9) 。
螢光素眼底血管攝影 (FA )的特徵性表現為與皺褶處RPE 變薄相對應的線狀低螢光,以及皺褶頂部脈絡膜 螢光增強。吲哚青綠血管攝影(ICG)作為FA 診斷困難病例的補充檢查,可見脈絡膜 靜脈擴張迂曲和大量線狀低螢光。
外傷後低眼壓黃斑病變中,超音波生物顯微鏡 (UBM )和前段OCT 對評估睫狀體 剝離範圍至關重要。隅角鏡檢查 也可觀察到睫狀體 剝離。
Q
OCT檢查能發現低眼壓黃斑病變的哪些資訊?
A
OCT 可高精度檢測脈絡膜 視網膜 皺褶,並能識別眼底檢查 可能遺漏的細微皺褶。此外,還可評估與視功能預後相關的表現,如光感受器皺褶和Henle纖維層高反射9) 。OCT 對治療後追蹤也有用,可客觀判斷皺褶改善和殘留的光感受器損傷。
根據低眼壓 的存在和特徵性眼底表現組合進行診斷。詢問青光眼 手術史、外傷史、玻璃體 手術史和抗VEGF注射史。
引起脈絡膜 視網膜 皺褶的疾病鑑別診斷中,有”THIN RPE ”的口訣。
T(Tumors) :脈絡膜 腫瘤、轉移性腫瘤H(Hypotony) :低眼壓 (本病)I(Inflammation / Idiopathic) :後鞏膜炎 、特發性N(Neovascularization) :年齡相關性黃斑部退化 等脈絡膜新生血管 R(Retrobulbar mass / Retinal detachment) :眼眶 後方腫塊、視網膜剝離 P(Papilledema) :顱內壓增高引起的視乳頭水腫 E(Extraocular hardware) :鞏膜 扣帶、放射敷貼器等
在考慮是否存在低眼壓 、青光眼 手術史和外傷史的基礎上進行鑑別診斷。
Q
低眼壓黃斑病變的脈絡膜視網膜皺襞在其他疾病中也能見到嗎?
A
正如THIN RPE 助記符所示,腫瘤、炎症、視乳頭水腫 、眼眶 佔位性病變等多種疾病都可能出現脈絡膜 視網膜 皺襞。需要在考慮是否存在低眼壓 、青光眼 手術史和外傷史的基礎上進行鑑別診斷。
低眼壓黃斑病變的治療以確定病因並處理為優先。由於許多病例可自然緩解,首先進行保守治療,若無改善則逐步考慮積極干預。
重要的時間限制 :據報導,低眼壓黃斑病變持續超過3個月容易留下永久性視力 損害。建議在視功能損害成為永久性之前進行手術治療,一般需在1至6個月內做出判斷。4 mmHg或以下的顯著低眼壓 持續2至3個月容易留下視物變形和相對中心暗點 。另一方面,如果眼壓 高於4 mmHg,即使持續半年左右,視功能也可能恢復。
根據病因採取不同的方法。
濾過術後過度濾過 :
加壓眼墊 :用紗布等準確壓迫鞏膜 瓣 1) 佩戴大型軟性隱形眼鏡 :抑制濾過泡滲漏 硫酸阿托品水合物滴眼液 :睫狀肌鬆弛、前房 加深 1) 類固醇 滴眼液(消炎)房水 生成減少
外傷後睫狀體分離 :
1%阿托品點眼 : 持續保守治療後,眼壓 突然升高常導致睫狀體分離 自然緩解。類固醇 點眼
睫狀體 功能低下(PVR 後)
睫狀體 功能低下(PVR 後)
如果保守治療無改善,考慮以下介入措施。
自體血注射 : 將自體血注射到濾過泡內及周圍以減少濾過 4, 5, 6) 。需注意可能引起眼壓 急劇升高 10) 。經結膜 鞏膜 瓣縫合 : 通過結膜 直接用尼龍線縫合鞏膜 瓣的方法,長期證明對低眼壓黃斑病變有效 3, 12) 。前房 內注入黏彈劑或空氣前房 容積,暫時升高眼壓 。可重複進行,但效果常為暫時性。追加鞏膜 縫合 : 手術再次打開結膜 ,在直視下縫合鞏膜 瓣。如有明顯脈絡膜 剝離,需通過鞏膜 開窗術排出脈絡膜 上腔積液。
如果上述方法無改善或眼壓 未能恢復,手術選擇如下。
雷射光凝(睫狀體分離 處) : 適用於睫狀體分離 1-2週未緩解者。使用綠色或黃色波長雷射,光斑100-200 μm,持續時間0.2-0.5秒,功率200 mW以上,使睫狀體 輕微收縮並析出少量纖維蛋白。無效則數日後重複。眼壓 恢復前常出現一過性高眼壓 。睫狀體 縫合術角膜緣 3.5 mm處製作半層鞏膜 切口或鞏膜 瓣,用可吸收縫線將剝離的睫狀體 上皮縫合到鞏膜 上。濾過泡重建(結膜 前徙術) : 切除變薄的濾過泡,通過結膜 前徙重建濾過泡 13) 。其他手術 :已報告的有透熱凝固術、睫狀體 冷凍凝固 術、鞏膜扣帶術 、環紮術、玻璃體 內氣體注入術、人工水晶體 縫合固定術等。
治療的階段與時機總結如下。
時機 處理 早期(~1個月) 保守治療(加壓眼罩、SCL、阿托品、類固醇 ) 無改善 自體血注射、黏彈性物質 注射、經結膜 鞏膜 瓣縫合 1~3個月 雷射光凝(睫狀體分離 處)、繼續觀察 6個月內 手術(睫狀體 縫合術、濾過泡重建、鞏膜扣帶術 等)
自體血注射後可能出現急劇的眼壓 升高10) ,注射後的眼壓 監測很重要。
雷射光凝後的一過性高眼壓 也需要注意。
如果眼壓 持續低於4 mmHg達2-3個月,視力 恢復不良,且容易殘留視物變形和相對中心暗點 。早期恢復眼壓 對預後至關重要。
Q
低眼壓黃斑病變是否需要緊急手術?
A
低眼壓黃斑病變有自然緩解的病例,因此首先嘗試保守治療。但如果低眼壓 持續超過3個月,容易留下永久性視力 障礙,因此保守治療無效時應在1-6個月內考慮手術介入。特別是眼壓 低於4 mmHg的顯著低眼壓 ,最好在2個月內恢復眼壓 。
Q
低眼壓黃斑病變如果不治療會怎樣?
A
如果眼壓 持續低於4 mmHg較長時間,視網膜 、鞏膜 和脈絡膜 內的纖維化可能進展,導致不可逆的視力 障礙。2個月內恢復眼壓 是重要的參考指標。如果眼壓 高於4 mmHg,即使持續半年左右也可能恢復。
如果早期恢復眼壓 ,視功能有望改善。另一方面,如果感光細胞 皺襞或鞏膜 、脈絡膜 纖維化固定,則會殘留不可逆的視力 障礙9) 。眼壓 低於4 mmHg持續2-3個月時,容易殘留視物變形和相對中心暗點 。
脈絡膜 剝離眼軸 縮短導致的不可逆遠視 永久性感光細胞 損傷 :感光細胞 外節斷裂導致中心視力 下降9) 視盤周圍視網膜 劈裂 :在慢性低眼壓 中有報導
Lee & Woo(2021)報告了兩例因黃斑前膜 切除玻璃體 手術後發生低眼壓 性黃斑 病變的病例(53歲女性和20歲男性,韓國)。兩例均在25G無縫線玻璃體 手術後出現無法測量的低眼壓 ,OCT 識別出特徵性的感光細胞 皺襞和Henle纖維層高反射。即使眼壓 恢復正常,感光細胞 損傷仍然存在,一年後的視力 比術前更差。既往玻璃體 手術史、年輕、近視 被認為是低眼壓 性黃斑 病變的危險因素9) 。
Barbosa等人(2022)報告了一例70多歲女性在非穿透性青光眼 手術(深層鞏膜切除術 )三年後發生眼壓 2 mmHg的低眼壓 性黃斑 病變的病例。使用地塞米松眼藥水每日五次和環戊通每日兩次,八週後完全恢復,但停用類固醇 兩個月後復發。重新開始並維持類固醇 眼藥水後,14個月內保持了穩定的眼壓 (14-17 mmHg)和良好的視力 14) 。這是一份將類固醇 應答者特性應用於治療的有趣報告。
Maheshwari等人(2022)報告了一種不經結膜 切口、經結膜 縫合鞏膜 瓣的微創技術3) 。在一例70歲男性青光眼 病例中,白內障 和青光眼 聯合手術後出現嚴重低眼壓 (1 mmHg)和360度脈絡膜 脫離,該技術使脈絡膜 脫離消退,眼壓 和視力 均得到改善。該技術被介紹為一種微創且可在門診進行之有前景的方法。
Lima-Fontes等人(2022)報告了一例52歲男性彈性纖維假性黃色瘤患者,在雷珠單抗 玻璃體內注射 (第78次注射後)發生低眼壓 性黃斑 病變的病例。原因是30G針頭注射部位的鞏膜 裂開。高度近視 、彈性纖維假性黃色瘤、反覆注射、既往玻璃體 手術導致的玻璃體 缺失被認為是鞏膜 脆弱的因素。通過鞏膜 縫合和阿托品、地塞米松眼藥水恢復11) 。
Markopoulos等人(2023)報告了一名78歲男性,在小樑切除術 後因低眼壓 (6 mmHg)出現視乳頭周圍視網膜 劈裂(PPRS)。使用地塞米松0.1%眼藥水每日兩次和奈帕芬胺眼藥水每日三次治療4週後,PPRS完全消失,眼壓 恢復至16 mmHg。推測低眼壓 導致毛細血管靜水壓梯度改變,促進液體進入細胞外間隙,是PPRS發生的機轉15) 。
對於難治性低眼壓黃斑病變,已有報告採用玻璃體切除術 合併內界膜 (ILM )剝離,以及使用全氟碳液(PFCL)平復脈絡膜 視網膜 皺襞的方法。這些均處於病例報告層級,尚未確立為標準治療。
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
Sakamoto M, Matsumoto Y, Mori S, et al. Excessive scleral shrinkage, rather than choroidal thickening, is a major contributor to the development of hypotony maculopathy after trabeculectomy. PLoS One. 2018;13:e0191862.
Maheshwari D, Shyam P, Pawar N, Ramakrishnan R. Transconjunctival flap sutures: A novel technique to combat hypotony. Indian J Ophthalmol. 2022;70(6):2223-2225.
Wise JB. Treatment of chronic postfiltration hypotony by intrableb injection of autologous blood. Arch Ophthalmol. 1993;111:827-830.
Nuyts RM, Greve EL, Geijssen HC, Langerhorst CT. Treatment of hypotonous maculopathy after trabeculectomy with mitomycin C. Am J Ophthalmol. 1994;118:322-331.
Okada K, Tsukamoto H, Masumoto M, et al. Autologous blood injection for marked overfiltration early after trabeculectomy with mitomycin C. Acta Ophthalmol Scand. 2001;79:305-308.
Fannin LA, Schiffman JC, Budenz DL. Risk factors for hypotony maculopathy. Ophthalmology. 2003;110:1185-1191.
Costa VP, Arcieri ES. Hypotony maculopathy. Acta Ophthalmol Scand. 2007;85:586-597.
Lee YJ, Woo SJ. Hypotony maculopathy and photoreceptor folds with disruptions after vitrectomy for epiretinal membrane removal: two case reports. J Med Case Reports. 2021;15:255.
Siegfried CJ, Grewal RK, Karalekas D, et al. Marked intraocular pressure rises complicating intrableb autologous blood injection. Arch Ophthalmol. 1996;114:492-493.
Lima-Fontes M, Godinho G, Cunha AM, et al. Hypotony Maculopathy Related to Anti-VEGF Intravitreal Injection. Int Med Case Rep J. 2022;15:517-520.
Eha J, Hoffmann EM, Pfeiffer N. Long-term results after transconjunctival resuturing of the scleral flap in hypotony following trabeculectomy. Am J Ophthalmol. 2013;155:864-869.
Satpute K, Bukke AN, Verma S, Dada T. Conjunctival advancement for management of hypotony maculopathy after trabeculectomy. BMJ Case Rep. 2022;15:e251718.
Barbosa RC, Bastos R, Tenedório P. Recurrent macular neurosensory detachment in hypotony maculopathy managed with topical corticosteroids. BMJ Case Rep. 2022;15:e248773.
Markopoulos I, Tzakos M, Tzimis V, Halkiadakis I. Peripapillary Retinoschisis as a Manifestation of Ocular Hypotony. Case Rep Ophthalmol. 2023;14:13-17.