چینخوردگی کوروئید و شبکیه
چینخوردگی قطب خلفی: به صورت شعاعی یا متحدالمرکز مرتب شده است. این مشخصترین یافته ماکولوپاتی هیپوتون است.
ارتباط با اختلال بینایی: جهت، تراکم و فاصله چینها از مرکز ماکولا بر پیشآگهی بینایی تأثیر میگذارد.

ماکولوپاتی هیپوتونی (Hypotony Maculopathy) وضعیتی است که در آن به دلیل افت فشار مداوم چشم به دلایل مختلف، چینهای مشیمیه-شبکیه در قطب خلفی چشم ایجاد شده و منجر به اختلال عملکرد بینایی میشود. این وضعیت با ادم پاپی، اتساع و پیچخوردگی وریدهای شبکیه و اتساع وریدهای مشیمیه همراه است و علائم ذهنی شامل کاهش بینایی و دگرگونبینی (مترامورفوپسی) میباشد.
این بیماری اولین بار در سال 1954 توسط Dellaporta به عنوان تغییرات فوندوس همراه با افت فشار چشم گزارش شد و در سال 1972، Gass اصطلاح «ماکولوپاتی هیپوتونی» را برای روشنسازی علت کاهش بینایی مرتبط با چینهای مشیمیه معرفی کرد8). افت فشار چشم به خودی خود پس از جراحی یا تروما نسبتاً شایع است، اما تنها بخشی از موارد به ماکولوپاتی و اختلال عملکرد بینایی منجر میشوند. عواملی مانند سفتی صلبیه و طول محور چشم در بروز آن نقش دارند.
ماکولوپاتی هیپوتونی میتواند در فشار داخل چشم 8 تا 10 میلیمتر جیوه یا کمتر رخ دهد و میزان بروز در فشار 5 میلیمتر جیوه یا کمتر افزایش مییابد. از نظر آماری، فشار داخل چشم کمتر از 6.5 میلیمتر جیوه (بیش از 3 انحراف معیار پایینتر از میانگین) به عنوان «هیپوتونی» تعریف میشود. از نظر بالینی، به وضعیتی اطلاق میشود که فشار چشم به اندازهای پایین باشد که باعث اختلال عملکرد بینایی شود.
فرضیه Gass که تغییر شکل مکانیکی اپیتلیوم رنگدانه شبکیه (RPE) و سلولهای گیرنده نوری ناشی از چینهای مشیمیه-شبکیه را عامل اصلی اختلال عملکرد بینایی میداند، به طور گسترده پذیرفته شده است. با افت فشار چشم، دیواره چشم به سمت داخل فرو میریزد و باعث ایجاد چینهای اضافی در مشیمیه و شبکیه میشود. اگر این تغییر در مدت کوتاهی برطرف شود، عملکرد بینایی بهبود مییابد، اما تداوم طولانی مدت آن منجر به اختلال غیرقابل برگشت بینایی میشود.
از نظر آماری، فشار داخل چشم کمتر از 6.5 میلیمتر جیوه (3 انحراف معیار پایینتر از میانگین) به عنوان هیپوتونی تعریف میشود. با این حال، ماکولوپاتی هیپوتونی میتواند در فشار 8 تا 10 میلیمتر جیوه یا کمتر رخ دهد و میزان بروز در فشار 5 میلیمتر جیوه یا کمتر به طور قابل توجهی افزایش مییابد. در فشار 4 میلیمتر جیوه یا کمتر، اغلب کاهش شدید بینایی (حدت بینایی اصلاح شده 0.2 یا کمتر) رخ میدهد. از نظر بالینی، افت فشار چشم به میزانی که باعث اختلال در عملکرد بینایی شود، مشکلساز است.
شایعترین علت، فیلتراسیون بیش از حد پس از جراحی فیلتراسیون گلوکوم است، به ویژه پس از ترابکولکتومی همراه با میتومایسین C (MMC). در راهنمای بالینی گلوکوم، فراوانی ماکولوپاتی هیپوتونی به عنوان عارضهای که میتواند یک ماه پس از جراحی باعث اختلال عملکرد بینایی شود، 0.9 تا 5 درصد گزارش شده است1). در مقاله مروری Costa & Arcieri (2007)، میزان بروز 1.3 تا 18 درصد ذکر شده است8). دومین علت شایع، دیالیز جسم مژگانی ناشی از تروماهای بلانت است.
شناخته شده است که این عارضه در افراد جوان و مبتلایان به نزدیکبینی شدید بیشتر رخ میدهد 2). در افراد جوان و نزدیکبین، به دلیل سفتی پایین صلبیه، صلبیه در برابر فشار پایین چشم به سمت داخل فرو میریزد و چینهای مشیمیه به راحتی تشکیل میشوند. بیماران مسنتر بیشتر مستعد ترشح مشیمیه هستند، در حالی که بیماران جوان تمایل بیشتری به ماکولوپاتی ناشی از فشار پایین چشم دارند. از زمانی که استفاده از داروهای ضد متابولیت رایج شده است، گزارشهای ماکولوپاتی ناشی از فشار پایین چشم پس از جراحی فیلتراسیون افزایش یافته است.
علل ماکولوپاتی ناشی از فشار پایین چشم به دو دسته اصلی افزایش خروج زلالیه و کاهش تولید زلالیه تقسیم میشوند.
Fannin و همکاران (2003) عوامل خطر زیر را برای ماکولوپاتی ناشی از فشار پایین چشم شناسایی کردند 7).
در افراد جوان، تشکیل اسکار دریچه صلبیه ضعیف است و فیلتراسیون بیش از حد پس از عمل ادامه مییابد. در افراد نزدیکبین، بهویژه نزدیکبینی شدید، صلبیه نازک و شکننده است و حتی با افت فشار یکسان، چینخوردگی مشیمیه-شبکیه به راحتی ایجاد میشود. ترکیب این عوامل خطر را بیشتر افزایش میدهد.
در بروز ماکولوپاتی ناشی از افت فشار چشم، ناهنجاریهای دینامیک زلالیه و تغییر شکل مکانیکی دیواره چشم نقش نزدیکی دارند.
ناهنجاریهای دینامیک زلالیه که منجر به افت فشار چشم میشوند، به دو دسته اصلی تقسیم میشوند.
در سیکلودایالیز پس از تروما، یک مسیر ارتباطی باز در جسم مژگانی ایجاد میشود که زلالیه به فضای فوقکوروئید تخلیه میشود و همزمان، آسیب به اپیتلیوم جسم مژگانی تولید زلالیه را کاهش میدهد. در جراحی فیلتراسیون با استفاده از آنتیمتابولیتها (MMC، 5-FU)، اسکار اطراف فلپ صلبیه مهار شده و نشت زلالیه افزایش مییابد1).
هنگامی که افت فشار چشم رخ میدهد، دیواره صلبیه به سمت داخل فرو میریزد و باعث ایجاد چینهای مشخص کوروئید و رتین میشود. طول قدامی-خلفی چشم کوتاه شده و به عنوان عیب انکساری، دوربینی ظاهر میشود.
Sakamoto و همکاران (2018) گزارش کردند که در ایجاد ماکولوپاتی هیپوتونیک پس از ترابکولکتومی، انقباض بیش از حد صلبیه عامل اصلیتر از ضخیم شدن کوروئید است2). با تداوم افت فشار، شل شدن و انقباض فیبرهای کلاژن صلبیه پیشرفت کرده و طول محوری چشم به طور غیرقابل برگشتی کوتاه میشود.
در فرضیهای که گس در سال 1972 مطرح کرد، چینهای کوروئید و رتین باعث ایجاد فشار مکانیکی بر RPE و سلولهای گیرنده نور میشوند که این امر ماهیت اختلال عملکرد بینایی است. این فرضیه هنوز هم به طور گسترده پذیرفته شده است.
در مطالعات اخیر OCT، چینهای گیرنده نور (photoreceptor folds) جدا از چینهای کوروئید شناسایی شدهاند9). چینهای گیرنده نور درست در زیر چینهای کوروئید تشکیل میشوند و با پارگی بخش خارجی گیرنده نور (photoreceptor disruption) همراه هستند. این آسیب مکانیکی گیرنده نور عامل اصلی کاهش غیرقابل برگشت بینایی مرکزی است و حتی اگر چینهای کوروئید برطرف شوند، اگر آسیب گیرنده نور باقی بماند، بهبود بینایی ضعیف خواهد بود9).
با افت فشار، صفحه کریبریفرم به سمت جلو برآمده شده و جریان آکسونی محدود میشود که در مرحله حاد باعث ادم پاپی میشود. در گلوکوم پیشرفته که آکسونهای زنده کمی وجود دارند، حتی با افت فشار نیز تورم پاپی ممکن است قابل توجه نباشد.
هنگامی که فشار چشم کاهش مییابد و بخش خلفی چشم خم میشود، بازگشت ورید شبکیه مختل شده و احتقان ایجاد میشود. این امر به صورت گشاد شدن و پیچ خوردگی وریدهای شبکیه از نظر بالینی مشاهده میشود.
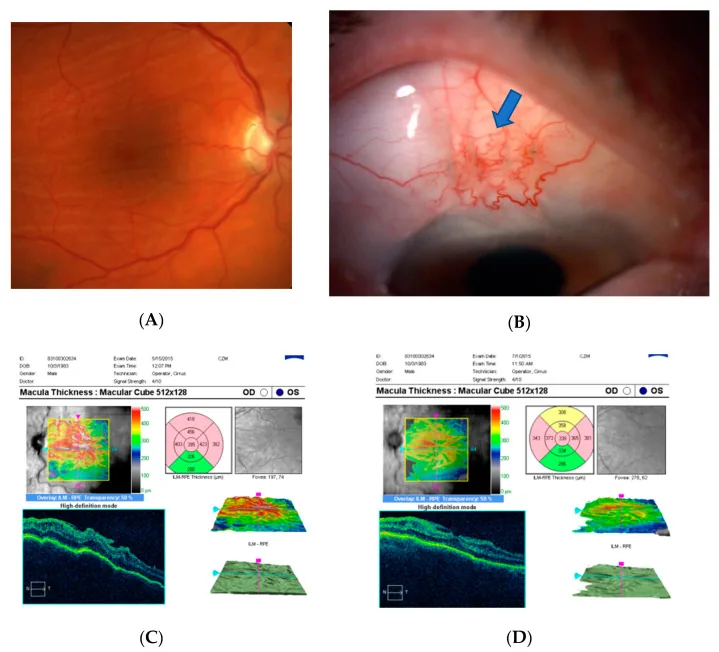
اگرچه مدت هیپوتونی لزوماً با حدت بینایی نهایی همبستگی ندارد، اما اگر فشار داخل چشم زودتر恢复正常 شود، بهبود عملکرد بینایی قابل انتظار است.
یافتههای فوندوس در ماکولوپاتی هیپوتون صرف نظر از علت، ویژگیهای مشترکی دارند، اما یافتههای همراه بر اساس علت متفاوت است.
چینخوردگی کوروئید و شبکیه
چینخوردگی قطب خلفی: به صورت شعاعی یا متحدالمرکز مرتب شده است. این مشخصترین یافته ماکولوپاتی هیپوتون است.
ارتباط با اختلال بینایی: جهت، تراکم و فاصله چینها از مرکز ماکولا بر پیشآگهی بینایی تأثیر میگذارد.
پیچخوردگی عروق
پیچخوردگی شریان شبکیه: به دلیل فروپاشی دیواره چشم، عروق شبکیه اضافی شده و پیچ میخورند.
اتساع و پیچخوردگی ورید شبکیه: نشاندهنده استاز وریدی است و به طور برجسته ظاهر میشود.
تغییرات دیسک بینایی
ادم پاپی: در مرحله حاد ظاهر میشود. ناشی از اختلال در انتقال آکسونی به دلیل برجستگی قدامی صفحه کریبریفرم است.
پیچخوردگی عروق پاپی: در مرحله مزمن، پیچخوردگی عروق اطراف پاپی ممکن است باقی بماند.
یافتههای بخش قدامی چشم
نوع پس از جراحی فیلتراسیون
چینهای مشیمیه-شبکیه: در قطب خلفی، چینهای شعاعی تا دایرهای شکل میگیرند.
ادم پاپی عصب بینایی: همراه با قرمزی و تورم پاپی.
اتساع و پیچخوردگی وریدهای شبکیه: منعکسکننده احتقان وریدی است.
اتاق قدامی کم عمق: به دلیل جابجایی قدامی عنبیه، عدسی و زجاجیه.
جداشدگی مشیمیه: در موارد فیلتراسیون بیش از حد، با فراوانی بالا همراه است.
نوع تروماتیک (جداشدگی جسم مژگانی)
چین ماکولا: چینهای مشیمیه-شبکیه در قطب خلفی.
ادم و قرمزی دیسک بینایی: تورم اطراف دیسک بینایی مشاهده میشود.
اتساع و پیچ خوردگی عروق شبکیه: پیچ خوردگی وریدها و شریانهای شبکیه.
اتاق قدامی کم عمق: به دلیل جابجایی قدامی.
فرورفتگی زاویه: ممکن است ناهنجاری زاویه مطابق با ناحیه جداشدگی جسم مژگانی مشاهده شود.
در مطالعات OCT اخیر، نه تنها چینهای مشیمیه بلکه چینهای فتورسپتور نیز شناسایی شدهاند و تصور میشود آسیب مکانیکی لایه فتورسپتور علت اصلی کاهش غیرقابل برگشت حدت بینایی مرکزی باشد 9). هایپررفلکتیویتی لایه الیاف هنله نیز به عنوان یافته OCT مشخصه گزارش شده است 9).
اگر فشار پایین چشم ادامه یابد، صلبیه بیش از حد منقبض شده و طول محوری چشم کوتاه میشود. ساکاموتو و همکاران (2018) گزارش کردند که انقباض بیش از حد صلبیه بیش از ضخیم شدن مشیمیه در ایجاد ماکولوپاتی هیپوتونیک پس از ترابکولکتومی نقش دارد 2). در سونوگرافی B-scan، ضخیم شدن صلبیه خلفی و مشیمیه ممکن است مشاهده شود و موارد همراه با جداشدگی مشیمیه نیز غیر معمول نیست.
ماهشواری و همکاران (2022) موردی از یک مرد 70 ساله با گلوکوم زاویه باز اولیه را گزارش کردند 3). پس از جراحی همزمان آب مروارید و گلوکوم، افت شدید فشار چشم (1 میلیمتر جیوه) و جداشدگی 360 درجه مشیمیه رخ داد و ماکولوپاتی هیپوتونیک ایجاد شد. با بخیه ترانس کنژنکتیوال فلپ صلبیه، جداشدگی مشیمیه برطرف شد و فشار چشم و بینایی بهبود یافت.
تشخیص ماکولوپاتی هیپوتونیک نسبتاً با شرح حال، تأیید فشار پایین چشم با تونومتری و یافتههای مشخص فوندوس آسان است.
ویژگیهای هر روش بررسی در زیر آورده شده است.
| روش بررسی | هدف اصلی ارزیابی | ویژگی |
|---|---|---|
| OCT | چینهای کوریورتینال و چینهای فتورسپتور | ساده و خط اول. قادر به تشخیص چینهای ریز نیز میباشد |
| FA | هیپوفلورسانس خطی در ناحیه چینها و نشت فلورسین از دیسک بینایی | همچنین برای ارزیابی تأخیر گردش خون شبکیه مفید است |
| ICG | اتساع وریدهای کوروئید و هیپوفلورسانس در ناحیه چینها | در مواردی که FA نامشخص است، تکمیلکننده است |
| UBM / OCT بخش قدامی | موقعیت و وسعت دیالیز جسم مژگانی | برای جستجوی علت در نوع تروماتیک ضروری است |
| سونوگرافی B-scan | ضخیم شدن کوروئید و جداشدگی کوروئید | حتی در موارد کدورت رسانههای انکساری قابل استفاده است |
OCT روش انتخابی اولیه است و قدرت تشخیصی بالاتری نسبت به معاینه فوندوس دارد. بررسی دقیق تمام اسکنهای شعاعی مهم است. حتی اگر فوندوس از نظر بالینی طبیعی به نظر برسد، OCT ممکن است تغییرات پاتولوژیک را تشخیص دهد 9).
در آنژیوگرافی فلورسئین (FA)، هیپوفلورسانس خطی مربوط به نازک شدن RPE در ناحیه چینها و افزایش فلورسانس مشیمیه در راس چینها مشخصه است. آنژیوگرافی با ایندوسیانین گرین (ICG) به عنوان آزمایش تکمیلی برای مواردی که تشخیص با FA دشوار است مفید بوده و اتساع و پیچخوردگی وریدهای مشیمیه و هیپوفلورسانس خطی متعدد را نشان میدهد.
در ماکولوپاتی هیپوتونی پس از تروما، میکروسکوپ اولتراسوند بیومیکروسکوپی (UBM) و OCT بخش قدامی برای ارزیابی وسعت سیکلودایالیز ضروری هستند. سیکلودایالیز با گونیوسکوپی نیز قابل مشاهده است.
OCT میتواند چینهای کوریورتینال را با دقت بالا تشخیص دهد و حتی چینهای ریزی که در معاینه فوندوس ممکن است نادیده گرفته شوند را شناسایی کند. علاوه بر این، میتواند یافتههای مرتبط با پیشآگهی بینایی مانند چینهای فوتورسپتور و هایپررفلکتیویتی لایه الیاف هنله را ارزیابی کند 9). همچنین برای پیگیری پس از درمان مفید است و میتواند بهبود چینها و آسیب باقیمانده فوتورسپتورها را به طور عینی تعیین کند.
تشخیص بر اساس وجود هیپوتونی و ترکیب یافتههای مشخص فوندوس انجام میشود. سابقه جراحی گلوکوم، تروما، ویترکتومی و تزریق anti-VEGF باید در شرح حال پرسیده شود.
برای تشخیص افتراقی بیماریهایی که باعث چینهای کوریورتینال میشوند، مخفف “THIN RPE” شناخته شده است.
تشخیص افتراقی با در نظر گرفتن وجود افت فشار چشم، سابقه جراحی گلوکوم، سابقه تروما و غیره انجام میشود.
همانطور که مخفف THIN RPE نشان میدهد، چینهای کوریورتینال میتوانند در بسیاری از بیماریها از جمله تومور، التهاب، ادم پاپی، ضایعات اشغالکننده فضای اربیت و غیره ایجاد شوند. تشخیص افتراقی باید با در نظر گرفتن وجود افت فشار چشم، سابقه جراحی گلوکوم، سابقه تروما و غیره انجام شود.
درمان ماکولوپاتی هیپوتونیک بر شناسایی و مدیریت علت زمینهای متمرکز است. از آنجایی که بسیاری از موارد خودبهخود بهبود مییابند، ابتدا درمان محافظهکارانه انجام میشود و در صورت عدم بهبود، مداخله تهاجمی به صورت مرحلهای در نظر گرفته میشود.
محدودیت زمانی مهم: گزارش شده است که تداوم ماکولوپاتی هیپوتونیک به مدت بیش از ۳ ماه میتواند منجر به اختلال دائمی بینایی شود. توصیه میشود قبل از دائمی شدن اختلال بینایی، درمان جراحی انجام شود و معمولاً تصمیمگیری در عرض ۱ تا ۶ ماه صورت میگیرد. افت فشار چشم قابل توجه (۴ میلیمتر جیوه یا کمتر) که به مدت ۲ تا ۳ ماه ادامه یابد، احتمال باقی ماندن متامورفوپسی و اسکوتوم مرکزی نسبی را افزایش میدهد. از سوی دیگر، اگر فشار چشم بالاتر از ۴ میلیمتر جیوه باشد، حتی اگر به مدت حدود شش ماه ادامه یابد، ممکن است بهبود عملکرد بینایی حاصل شود.
رویکرد بر اساس علت متفاوت است.
در صورت عدم بهبود با درمان محافظهکارانه، مداخلات زیر در نظر گرفته میشود.
در صورت عدم بهبود با روشهای فوق یا عدم بازیابی فشار چشم، گزینههای جراحی زیر ارائه میشود.
مراحل و زمانبندی درمان به شرح زیر است:
| زمان | اقدام |
|---|---|
| اوایل (تا ۱ ماه) | درمان محافظهکارانه (بانداژ فشاری، لنز تماسی نرم، آتروپین، استروئید) |
| بدون بهبود | تزریق خون خودی، تزریق ماده ویسکوالاستیک، بخیه فلپ صلبیه از راه ملتحمه |
| ۱ تا ۳ ماه | فتوکواگولاسیون لیزری (ناحیه جداشدگی جسم مژگانی)، ادامه پیگیری |
| ظرف ۶ ماه | جراحی (بخیه زدن جسم مژگانی، بازسازی فیلتراسیون، فرو رفتگی صلبیه و غیره) |
ماکولوپاتی ناشی از فشار پایین چشم گاهی خودبهخود بهبود مییابد، بنابراین ابتدا درمان محافظهکارانه امتحان میشود. با این حال، اگر فشار پایین بیش از ۳ ماه ادامه یابد، احتمال آسیب دائمی بینایی بیشتر است، بنابراین در صورت عدم پاسخ به درمان محافظهکارانه، مداخله جراحی در عرض ۱ تا ۶ ماه در نظر گرفته میشود. به ویژه در موارد افت فشار شدید با فشار ۴ میلیمتر جیوه یا کمتر، بازیابی فشار در عرض ۲ ماه مطلوب است.
اگر فشار داخل چشم به مدت طولانی ۴ میلیمتر جیوه یا کمتر باقی بماند، فیبروز داخل شبکیه، صلبیه و مشیمیه پیشرفت کرده و میتواند منجر به آسیب غیرقابل برگشت بینایی شود. بازیابی فشار در عرض ۲ ماه یک معیار مهم در نظر گرفته میشود. اگر فشار بالاتر از ۴ میلیمتر جیوه باشد، گاهی حتی پس از شش ماه نیز بهبودی ممکن است.
اگر فشار چشم زودتر بازیابی شود، بهبود عملکرد بینایی قابل انتظار است. از سوی دیگر، اگر چینخوردگی سلولهای بینایی یا فیبروز صلبیه و مشیمیه تثبیت شود، آسیب غیرقابل برگشت بینایی باقی میماند9). اگر فشار ۴ میلیمتر جیوه یا کمتر به مدت ۲ تا ۳ ماه ادامه یابد، دگرگونبینی و اسکوتوم مرکزی نسبی بیشتر باقی میمانند.
لی و وو (2021) دو مورد (زن 53 ساله و مرد 20 ساله از کره) از ماکولوپاتی هیپوتونیک پس از ویترکتومی برای برداشتن غشای اپیرتینال را گزارش کردند. در هر دو مورد، پس از ویترکتومی بدون بخیه با گیج 25، فشار داخل چشم غیرقابل اندازهگیری پایین بود و OCT چینخوردگی مشخص سلولهای بینایی (photoreceptor folds) و بازتابدهی بالای لایه الیاف هنله را نشان داد. حتی پس از نرمال شدن فشار چشم، آسیب سلولهای بینایی باقی ماند و دید پس از یک سال بدتر از قبل از عمل بود. سابقه ویترکتومی قبلی، سن پایین و نزدیکبینی به عنوان عوامل خطر ماکولوپاتی هیپوتونیک ذکر شدهاند 9).
باربوسا و همکاران (2022) موردی از یک زن 70 ساله را گزارش کردند که سه سال پس از جراحی گلوکوم غیرنافذ (اسکلرکتومی عمیق) دچار ماکولوپاتی هیپوتونیک با فشار چشم 2 میلیمتر جیوه شد. با قطره دگزامتازون 5 بار در روز و سیکلوپنتولات 2 بار در روز، پس از 8 هفته بهبودی کامل حاصل شد، اما دو ماه پس از قطع استروئید عود کرد. با از سرگیری و ادامه قطره استروئید با دوز نگهدارنده، فشار چشم (14-17 میلیمتر جیوه) و دید خوب به مدت 14 ماه پایدار ماند 14). این گزارش جالبی از استفاده از ویژگی پاسخدهندگان به استروئید در درمان است.
ماهشواری و همکاران (2022) یک روش کمتهاجمی برای بخیه زدن فلپ اسکلرا از طریق ملتحمه بدون برش آن گزارش کردند 3). در یک مورد گلوکوم در مرد 70 ساله که پس از جراحی همزمان آب مروارید و گلوکوم دچار هیپوتونی شدید (1 میلیمتر جیوه) و جداشدگی 360 درجه مشیمیه شده بود، با این روش جداشدگی مشیمیه برطرف شد و فشار چشم و دید بهبود یافت. این روش به عنوان روشی امیدوارکننده با تهاجم کم و قابل انجام در مطب معرفی شده است.
لیما-فونتس و همکاران (2022) موردی از یک مرد 52 ساله با شبهگزانتوم الاستیکوم را گزارش کردند که پس از تزریق داخل زجاجیهای رانیبیزوماب (پس از هفتاد و هشتمین تزریق) دچار ماکولوپاتی هیپوتونیک شد. علت آن باز شدن اسکلرا از محل تزریق با سوزن 30 گیج بود. نزدیکبینی شدید، شبهگزانتوم الاستیکوم، تزریقات مکرر و فقدان زجاجیه به دلیل ویترکتومی قبلی به عنوان عوامل ضعف اسکلرا در نظر گرفته شدند. با بخیه اسکلرا و قطره آتروپین و دگزامتازون بهبود یافت 11).
Markopoulos و همکاران (2023) یک مرد 78 ساله را گزارش کردند که پس از ترابکولکتومی با افت فشار چشم (6 میلیمتر جیوه) دچار جداشدگی شبکیه اطراف پاپی (peripapillary retinoschisis: PPRS) شد. با قطره دگزامتازون 0.1% دو بار در روز و نپافناک سه بار در روز، PPRS پس از 4 هفته کاملاً ناپدید شد و فشار چشم به 16 میلیمتر جیوه بازگشت. مکانیسم ایجاد PPRS به عنوان تغییر گرادیان فشار هیدرواستاتیک مویرگها در اثر افت فشار چشم و تسهیل حرکت مایع به فضای خارج سلولی بحث شده است15).
برای ماکولوپاتی هیپوتونیک مقاوم، روشهای ترکیبی ویترکتومی و برداشتن غشای محدود کننده داخلی (ILM) و همچنین روش صاف کردن چینهای کوریورتینال با استفاده از مایع پرفلوئوروکربن (PFCL) گزارش شده است. همه اینها در سطح گزارش موردی هستند و جایگاه آنها به عنوان درمان استاندارد تثبیت نشده است.