薄翳(nubecula)

角膜白斑(Corneal Leukoma)
1. 什么是角膜白斑?
Section titled “1. 什么是角膜白斑?”角膜白斑(corneal leukoma)是角膜基质中出现的瘢痕性白色混浊。它是各种角膜炎、外伤、炎症活动期消退后残留的不可逆混浊,特征为质地坚硬,不伴有水肿或浸润。
角膜瘢痕(corneal scar)根据程度分为三级。
斑翳(macula)
中等度的局限性混浊。
虹膜细节变得难以透见。
若累及瞳孔区,可导致视力下降。
白斑(leukoma)
浓密白色不透明混浊。
虹膜和瞳孔无法透见。
若位于瞳孔区,会导致严重视力障碍。
角膜是透光组织,即使微小的瘢痕也会直接导致光学功能下降。即使瘢痕性混浊轻微,也可能因不规则散光导致视功能显著下降。
角膜白斑是角膜实质的瘢痕,原则上不会自然消退。但轻度混浊(云翳水平)可能随着炎症消退而有所改善。累及瞳孔区的白斑对视力影响较大,请咨询眼科医生。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”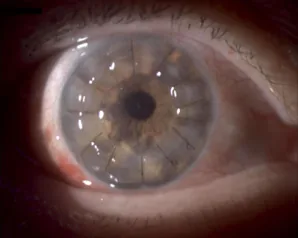
临床所见(医生检查时确认的发现)
Section titled “临床所见(医生检查时确认的发现)”- 角膜混浊:白色至灰白色的局限性或广泛性不透明区域
- 表面不规则:角膜地形图检查发现不规则散光
- 变薄:溃疡后瘢痕中基质变薄,有时伴有虹膜膨隆(粘连性白斑)
- 新生血管:在重症或迁延病例中,可见角膜缘血管侵入
- 前房所见:检查导致瘢痕形成的炎症是否残留(前房积脓、角膜后沉着物等)
3. 原因与风险因素
Section titled “3. 原因与风险因素”角膜白斑的原因多种多样。
感染性角膜炎是角膜白斑最常见的原因之一。
- 细菌性角膜炎:肺炎球菌可在眼球暴露后引起匍行性角膜溃疡1)。铜绿假单胞菌可导致伴有环形脓肿的重症溃疡,并迅速进展至穿孔1)。革兰阳性球菌形成类圆形局限性脓肿,革兰阴性杆菌易形成环形脓肿1)。
- 真菌性角膜炎:植物性外伤和长期使用类固醇眼药水是危险因素1)。丝状真菌表现为边缘羽毛状毛糙的灰白色溃疡(hyphate ulcer),角膜后表面的内皮斑具有特征性1)。
- 病毒性角膜炎:HSV和水痘-带状疱疹病毒通过免疫机制引起角膜基质浸润。经历地图状角膜炎和盘状角膜炎后形成瘢痕。
- 棘阿米巴角膜炎:常见于隐形眼镜佩戴者1)。早期放射状角膜神经炎进展为环形浸润,并留下瘢痕。
- 穿透性外伤:角膜基质伤口愈合过程中形成瘢痕。
- 化学性外伤:碱性物质可渗透至角膜基质深层,易导致广泛瘢痕。
- 分娩外伤(产道通过时):产钳分娩等使角膜受到外力,导致Descemet膜破裂引起角膜水肿,数周至数月后残留垂直方向的线状混浊和高度散光。
- 史蒂文斯-约翰逊综合征/中毒性表皮坏死松解症:急性期出现广泛角结膜上皮缺损。若角膜上皮干细胞消失,伴有结缔组织和血管的结膜组织覆盖角膜,导致严重混浊。
- 眼瘢痕性类天疱疮:睑球粘连和结膜侵入逐渐进展,导致角膜混浊。手术创伤有导致快速恶化的风险。
先天性和遗传性疾病
Section titled “先天性和遗传性疾病”- 先天性青光眼:眼压升高引起的角膜水肿导致混浊。
- 先天性遗传性角膜内皮营养不良(CHED):出生时即出现双侧角膜水肿和混浊。
- 先天性风疹综合征:宫内感染引起的角膜混浊。
角膜营养不良
Section titled “角膜营养不良”- 颗粒状角膜营养不良(I型和II型):由TGFBI基因突变引起。随着年龄增长,颗粒状混浊增加;II型(Avellino型)在角膜表层产生弥漫性混浊。
- 格子状角膜营养不良:淀粉样蛋白沉积导致线状或网状混浊。1型中央混浊更明显。
- 斑状角膜营养不良:常染色体隐性遗传。弥漫性毛玻璃样混浊遍布整个角膜基质,通常在10至30岁之间注意到视力下降。
- Fuchs角膜内皮营养不良:角膜内皮细胞变性导致大疱性角膜病变3)。多见于中老年人,女性发病率较高3)。
有报道称长期口服阿托伐醌(atovaquone)后,角膜上皮下至基质出现弥漫性白色颗粒状混浊4)。胺碘酮和氯喹等亲脂性药物因其阳离子两亲性结构也可引起角膜沉积4)。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”裂隙灯显微镜检查
Section titled “裂隙灯显微镜检查”这是评估角膜混浊的基本方法。观察混浊的位置(中央、旁中央、周边)、深度(上皮下、浅层基质、深层基质)、范围和密度。通过荧光素染色检查是否存在上皮缺损。
在角膜混浊的鉴别诊断中,区分感染性角膜炎的浸润性混浊和瘢痕性混浊非常重要。浸润性病变伴有周围水肿和前房炎症,提示活动性1)。环形浸润可见于真菌性角膜炎和棘阿米巴角膜炎,但放射状角膜神经炎和剧烈疼痛是棘阿米巴的特征2)。
眼前段光学相干断层扫描(AS-OCT)
Section titled “眼前段光学相干断层扫描(AS-OCT)”可以客观评估角膜病变的深度1)。还可以观察到角膜厚度增加或变薄、前房炎症细胞、角膜后沉着物(KP)、内皮斑等表现。通过治疗前后比较可以评估治疗效果。
对评估不规则散光有用1)。即使角膜白斑引起的混浊本身较轻,不规则散光也可能导致视功能显著下降。
体内共聚焦显微镜(IVCM)
Section titled “体内共聚焦显微镜(IVCM)”可以无创观察角膜内的细胞、神经纤维和微生物(真菌菌丝、棘阿米巴包囊)1)。在评估瘢痕组织的细胞构成时也有用,但需要熟练的操作和结果解读技能。
刮取培养和涂片镜检
Section titled “刮取培养和涂片镜检”当怀疑活动性感染性角膜炎时进行1)。通过革兰染色推测致病菌,通过血琼脂平板和巧克力琼脂平板培养进行确诊。
对于引起角膜基质混浊的疾病的鉴别,应考虑以下内容。
| 鉴别疾病 | 特征性表现 | 检查 |
|---|---|---|
| 药物性角膜沉积 | 用药史、漩涡状沉积 | 用药史确认、体内共聚焦显微镜 |
| Ascher环 | 双侧对称性环形基质混浊 | AS-OCT、排除诊断6) |
| 代谢性沉积 | LCAT缺乏症、丹吉尔病 | 血液检查、血脂检查 |
5. 标准治疗方法
Section titled “5. 标准治疗方法”角膜白斑的治疗旨在治疗病因和恢复视功能。
原发病的治疗
Section titled “原发病的治疗”如果导致角膜白斑的基础疾病仍处于活动期,则首先优先进行病因治疗。
- 感染性角膜炎:根据致病菌使用抗菌药物(氟喹诺酮类、头孢菌素类、氨基糖苷类)频繁滴眼是基本治疗1)。真菌性使用抗真菌药,病毒性使用抗病毒药。
- 炎症性疾病:使用类固醇滴眼液、免疫抑制剂进行抗炎治疗。
- 眼镜和隐形眼镜:对于轻度混浊或不规则散光,有时可通过硬性隐形眼镜进行矫正。
- 巩膜镜和PROSE装置:对于Stevens-Johnson综合征/中毒性表皮坏死松解症相关的角膜混浊和新生血管,佩戴PROSE装置已被报道可促使角膜混浊和新生血管消退7)。该装置的背面通道设计促进泪液交换,改善眼表环境7)。
- 治疗性激光角膜切除术:对于局限于角膜表层的混浊的首选方法。对颗粒状角膜营养不良I型和Avellino型的表层混浊有效。通常可进行约两次。
- 深板层角膜移植术(DALK):当角膜内皮健康但混浊波及基质时选择。排斥反应风险较低。
- 穿透性角膜移植术(PKP):适用于基质全层或内皮受累的情况。例如斑块状角膜营养不良的进展期。
- 角膜内皮移植术(DSAEK/DMEK):针对Fuchs角膜内皮营养不良等内皮疾病引起的混浊进行3)。若基质变化轻微,则为首选。
- 人工角膜(角膜假体):对于常规角膜移植困难的严重病例(如Stevens-Johnson综合征/中毒性表皮坏死松解症、眼瘢痕性类天疱疮),考虑使用Boston KPro等人工角膜。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”角膜瘢痕形成的机制
Section titled “角膜瘢痕形成的机制”角膜的透明性依赖于角膜基质内胶原纤维规则的格子状排列。角膜损伤后的瘢痕形成经历以下过程。
- 角膜细胞的凋亡:外伤或感染等引起的上皮损伤后,损伤部位的角膜细胞发生凋亡。
- 向肌成纤维细胞分化:泪液和上皮释放的TGF-β1和TGF-β2进入角膜基质,使存活的角膜细胞分化为肌成纤维细胞5)。
- 异常细胞外基质的产生:肌成纤维细胞产生无序的胶原和细胞外基质,导致透明性丧失5)。
- 上皮基底膜(EBM)损伤:正常的EBM控制TGF-β进入基质,但损伤导致这一屏障破坏,纤维化持续5)。
角膜基质混浊的分类
Section titled “角膜基质混浊的分类”角膜基质混浊分为以下三种类型。
- 炎性混浊(浸润性病变):细菌性或真菌性角膜炎等活动性感染灶。由中性粒细胞和淋巴细胞聚集引起。形成脓肿时,蛋白水解酶导致组织破坏,愈合后留下伴有变薄的瘢痕1)。
- 水肿性混浊:角膜内皮功能不全导致基质含水量增加。在Fuchs角膜内皮营养不良中,变性的内皮细胞在Descemet膜后表面突出异常胶原样物质(角膜滴状赘疣),随着病情进展,内皮的泵和屏障功能下降,导致大疱性角膜病变3)。
- 沉积性混浊:角膜营养不良(颗粒状、格子状、斑状)或代谢性疾病导致的物质沉积。在斑状角膜营养不良中,CHST6基因突变导致硫酸角质素的硫酸化受损,低硫酸化硫酸角质素弥漫性沉积在角膜基质细胞内外。
药物性角膜混浊的机制
Section titled “药物性角膜混浊的机制”具有阳离子两亲性结构的药物(如阿托伐醌)由疏水环和亲水性阳离子胺侧链组成,可穿过细胞膜引起磷脂积累4)。胺碘酮通过泪液、房水和角膜缘血管到达角膜,在溶酶体内形成药物-脂质复合物4)。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”氯沙坦滴眼液治疗角膜瘢痕
Section titled “氯沙坦滴眼液治疗角膜瘢痕”Dutra等人(2025)报告了3例因HSV或水痘-带状疱疹病毒角膜炎导致角膜瘢痕的患者,使用0.8 mg/mL氯沙坦滴眼液每日6次治疗5)。一名40岁女性HSV瘢痕患者(病例1)治疗16周后,BCVA从20/60改善至20/25,AS-OCT证实基质混浊消退。一名15岁男性水痘-带状疱疹病毒瘢痕患者(病例3)BCVA从20/200改善至20/205)。
氯沙坦是一种血管紧张素II受体拮抗剂,通过抑制TGF-β的非经典通路(ERK介导的信号传导)诱导肌成纤维细胞凋亡5)。肌成纤维细胞清除后,角膜成纤维细胞重新增殖,促进上皮基底膜再生和无序胶原的吸收与重排,从而恢复透明度5)。治疗效果可能需要6至9个月才能显现5)。
PROSE装置对史蒂文斯-约翰逊综合征/中毒性表皮坏死松解症的长期效果
Section titled “PROSE装置对史蒂文斯-约翰逊综合征/中毒性表皮坏死松解症的长期效果”Liao等人(2022)报告了两例(4眼)史蒂文斯-约翰逊综合征/中毒性表皮坏死松解症患者,通过持续佩戴背通道设计的PROSE装置,角膜混浊和新生血管消退7)。病例1(19岁女性,史蒂文斯-约翰逊综合征)左眼角膜混浊从1级改善至0级,BCVA从20/40提高至20/15。病例2(26岁男性,中毒性表皮坏死松解症)佩戴PROSE 17个月后,所有处方滴眼液均停用,角膜新生血管和混浊持续改善7)。
阿托伐醌引起的角膜基质混浊
Section titled “阿托伐醌引起的角膜基质混浊”Ashizuka等人(2025)报告了一名15岁男性,因再生障碍性贫血口服阿托伐醌14个月后出现双眼弥漫性角膜基质混浊4)。眼前节OCT显示均匀弥漫性混浊,角膜形态无变化,活体共聚焦显微镜证实角膜基质色素沉积。停用阿托伐醌一年后,角膜混浊仍存在4)。
Ascher环(特发性角膜环状混浊)
Section titled “Ascher环(特发性角膜环状混浊)”Megalla等人(2021)报告了一名70岁男性出现双侧对称性环状角膜基质混浊(Ascher环)6)。Ascher环是一种极为罕见的特发性基质混浊,于1964年首次描述,特征为双侧性且不影响视功能6)。尚未发现遗传模式或实验室异常,通过排除诊断确诊6)。
8. 参考文献
Section titled “8. 参考文献”- 日本眼感染症学会. 感染性角膜炎診療ガイドライン(第3版). 日眼会誌. 2023.
- Rhee MK, Ahmad S, Amescua G, et al.; American Academy of Ophthalmology Preferred Practice Pattern Cornea/External Disease Panel. Bacterial Keratitis Preferred Practice Pattern®. Ophthalmology. 2024;131(4):P87-P133. PMID: 38349295. doi:10.1016/j.ophtha.2023.12.035.
- Matthaei M, Hribek A, Clahsen T, Bachmann B, Cursiefen C, Jun AS. Fuchs Endothelial Corneal Dystrophy: Clinical, Genetic, Pathophysiologic, and Therapeutic Aspects. Annu Rev Vis Sci. 2019;5:151-175. PMID: 31525145. doi:10.1146/annurev-vision-091718-014852.
- Ashizuka T, Uematsu M, Mohamed TM, et al. A case of corneal opacity caused by atovaquone administration. Am J Ophthalmol Case Rep. 2025;37:102235.
- Dutra BAL, Drew-Bear LE, Herretes SP, et al. Topical Losartan Treatment of Herpes Simplex Virus- or Varicella-Zoster Virus-Induced Corneal Scarring: A Case Series. Case Rep Ophthalmol. 2025;16:281-289.
- Megalla M, Li E, Branden P, Chow J. Bilateral idiopathic corneal opacity: A report of Ascher ring and a review of the literature. Am J Ophthalmol Case Rep. 2021;23:101176.
- Liao J, Asghari B, Carrasquillo KG. Regression of corneal opacity and neovascularization in Stevens-Johnson syndrome and Toxic Epidermal Necrolysis with the use of prosthetic replacement of the ocular surface ecosystem (PROSE) treatment. Am J Ophthalmol Case Rep. 2022;26:101520.
