表层性血管新生

角膜新生血管(Corneal Neovascularization)
1. 角膜新生血管是什么
Section titled “1. 角膜新生血管是什么”角膜新生血管(corneal neovascularization; CoNV)是指原本无血管的角膜组织中,从角膜缘血管丛长出新的毛细血管侵入角膜组织的病理状态1)。它不是特定的疾病名称,而是针对感染、炎症、缺氧、外伤等多种病理状态产生的非特异性反应。
角膜具有“血管新生特权(corneal angiogenic privilege; CAP)”,通过血管新生抑制因子和促进因子的精密平衡维持无血管状态1)。当这种平衡被打破时,血管内皮细胞会增殖、迁移,侵入角膜实质。
新生血管根据解剖位置分为两型。
深层血管新生
从前睫状动脉侵入角膜实质内。
角膜实质炎(梅毒、结核)、实质型疱疹性角膜炎、大疱性角膜病变等持续性炎症或水肿可导致角膜新生血管。
未成熟的新生血管可引起脂质渗出、持续性炎症和瘢痕形成1)。随着病情进展,血管逐渐成熟,被周细胞覆盖,并对抗VEGF治疗产生抵抗1)。在角膜移植术后患者中,新生血管是排斥反应的危险因素。
如果不治疗,新生血管会逐渐成熟,难以自然消退,导致脂质性角膜病变(脂质在角膜内沉积)和角膜瘢痕,造成永久性视力下降。此外,若需进行角膜移植,新生血管的存在会增加移植片排斥反应的风险。早期就诊和病因治疗至关重要。
2. 主要症状与临床所见
Section titled “2. 主要症状与临床所见”临床所见(医生通过检查确认的发现)
Section titled “临床所见(医生通过检查确认的发现)”- 新生血管形态:从细微网状图案到怒张的活动性血管、成熟的高密度血管等多种多样
- 血管的位置与深度:通过裂隙灯显微镜的裂隙法、间接照明法评估是表层性还是深层性
- ghost vessel:血流中断的陈旧性血管。无需治疗
- 结膜侵入(conjunctivalization):结膜组织覆盖角膜表面。通过荧光素染色的延迟染色确认
- 脂质性角膜病变(lipid keratopathy):新生血管渗出的脂质沉积在角膜基质中形成的黄白色混浊
- Vogt角膜缘栅栏(POV)消失:提示角膜缘干细胞缺失的重要体征
3. 原因与风险因素
Section titled “3. 原因与风险因素”- 单纯疱疹病毒(HSV-1):发达国家角膜新生血管最常见的感染性原因1)。实质型角膜疱疹可导致深层血管新生
- 细菌性角膜炎:重症病例中,角膜溃疡和瘢痕可伴随血管侵入
- 真菌性角膜炎:治疗迁延病例可伴有新生血管
- 沙眼·盘尾丝虫病:发展中国家主要的感染性原因1)
低氧(隐形眼镜相关)
Section titled “低氧(隐形眼镜相关)”软性隐形眼镜的不当佩戴(过度佩戴)是主要原因。传统HEMA材质SCL佩戴者中约80~90%可见角膜上方血管侵入(10点至2点方向)。上皮损伤持续1个月以上时,该部位会有血管侵入。
碱性外伤可渗透至角膜基质深层,导致广泛的角膜缘干细胞损伤和新生血管形成。这是角膜移植成功率显著降低的群体之一。
角膜缘干细胞缺乏症(LSCD)
Section titled “角膜缘干细胞缺乏症(LSCD)”LSCD是角膜新生血管的主要途径之一1)3)。先天性、化学外伤、隐形眼镜过度佩戴、全身性炎症性疾病、医源性等原因导致角膜缘干细胞功能障碍时,正常上皮屏障丧失,血管侵入发生3)。轻症时荧光素染色可见漩涡状上皮病变,中症时出现表层新生血管和角膜血管翳3)。
是的,多数情况下可以预防。角膜新生血管的主要原因之一是隐形眼镜导致的缺氧。遵守佩戴时间、使用高透氧性镜片、定期接受眼科检查,可以大幅降低风险。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”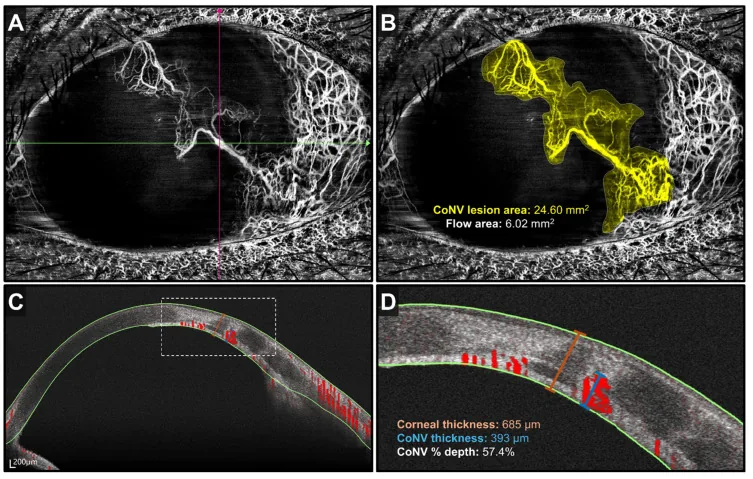
裂隙灯显微镜检查
Section titled “裂隙灯显微镜检查”角膜新生血管诊断中最基本的检查。评估血管的位置(象限)、深度(表层/深层)、活动性(有无血流)以及结膜侵入情况。
- 弥散法:将照射光宽度调大或通过扩散板观察,有助于辨别新生血管
- 间接照明法:利用虹膜或晶状体的反射光观察新生血管和角膜神经
- 荧光素染色:有助于评估上皮缺损和结膜侵入
荧光造影检查
Section titled “荧光造影检查”| 检查方法 | 主要评估指标 | 特点 |
|---|---|---|
| 裂隙灯显微镜 | 位置、深度、活动性 | 首选基本检查 |
| FA / ICGA | 灌注、渗漏、输入血管 | 有助于制定治疗方案 |
| AS-OCT / OCT-A | 深度与定量评估 | 非侵入性 |
5. 标准治疗方法
Section titled “5. 标准治疗方法”角膜新生血管的治疗包括病因治疗和对新生血管本身的干预两个方面2)。
- 停止佩戴CL:如果是低氧性原因,应停止佩戴,并考虑更换为高透氧性镜片。需判断是活动性血管还是陈旧性血管(ghost vessel)
- 感染治疗:针对引起感染的感染性角膜炎,给予抗菌药、抗病毒药、抗真菌药
- LSCD治疗:角膜缘移植、羊膜移植等手术治疗
- 类固醇滴眼液:通过抑制炎症细胞因子(IL-1、IL-6)、诱导淋巴细胞凋亡、抑制血管扩张来抑制新生血管2)。作为一线治疗,但长期使用需注意类固醇性青光眼和感染易感性增加
- 抗VEGF治疗:贝伐珠单抗(滴眼、结膜下注射、角膜基质内注射)被广泛使用1)2)。对未成熟的活跃血管有效,但对成熟血管(被周细胞覆盖的血管)效果有限1)。由于新生血管发生后2周内周细胞覆盖率达80%,早期治疗至关重要1)
- 免疫抑制剂:环孢素A滴眼液可抑制T细胞活化,具有类固醇减量效果2)。他克莫司、西罗莫司(mTOR抑制剂)也是可选方案1)
- 多西环素:通过抑制黏膜类天疱疮作用,抑制角膜新生血管2)
- 激光光凝术:使用氩激光或Nd:YAG激光凝固并闭塞血管。用于角膜移植前的预处理及脂质性角膜病变的治疗。存在角膜出血、变薄的风险,常出现血管再通或分流血管形成
- 细针透热疗法(FND):将细针插入角膜缘的营养血管,通过电凝使其闭塞。对成熟的粗大血管也有效,适用于氩激光难以闭塞的输入血管1)
- 光动力疗法(PDT):将光敏剂注入血管后,通过光照射产生活性氧,破坏血管壁。具有高特异性,但成本高且耗时
- MICE(MMC血管内化学栓塞术):使用33号针将丝裂霉素C(0.4 mg/mL)直接注入营养血管内6)。对于传统治疗抵抗的难治性角膜新生血管,已有报道显示可实现血管影化并改善脂质性角膜病变6)
6. 病理生理学·详细发病机制
Section titled “6. 病理生理学·详细发病机制”角膜血管新生特权(CAP)的维持机制
Section titled “角膜血管新生特权(CAP)的维持机制”角膜的无血管状态是由多种血管新生抑制机制协同维持的1)。
- 可溶性VEGF受体1(sVEGFR1):由角膜上皮和基质持续产生。它是一种内源性VEGF陷阱,能高亲和力捕获VEGF-A,竞争性抑制其与膜结合型VEGFR的结合1)
- 血小板反应蛋白(TSP-1/TSP-2):角膜细胞外基质中持续表达的血管生成抑制性糖蛋白。隔离VEGF并抑制VEGFR2信号。通过CD36/CD47诱导血管内皮细胞凋亡1)
- 内皮抑素:胶原蛋白XVIII的C端片段。抑制VEGF和bFGF通路,通过增强caspase-3活性促进血管内皮细胞凋亡。也抑制淋巴管生成1)
- 物理屏障:角膜缘屏障、致密的胶原排列、角膜相对低温环境限制血管侵入1)
血管生成促进因子与发病途径
Section titled “血管生成促进因子与发病途径”CAP的破坏主要通过两条途径发生1)2)。
途径1:炎症/低氧导致促进因子产生增加
角膜损伤后,巨噬细胞、上皮细胞和内皮细胞释放三种主要血管生成因子1)。
- VEGF-A:通过VEGFR-2促进VEC的增殖和迁移,诱导黏膜类天疱疮-2/黏膜类天疱疮-9,促进ECM重塑1)。是角膜新生血管中最重要的促进因子。
- bFGF(FGF-2):通过ERK/PI3K通路促进VEGF产生,并解离VE-钙黏蛋白结合,促进血管内皮细胞的出芽1)
- PDGF:募集周细胞和平滑肌细胞,稳定新生血管1)。PDGF介导的血管成熟可导致对抗VEGF治疗的耐药性
途径2:角膜缘干细胞缺乏症(LSCD)
角膜缘干细胞的丧失导致角膜上皮正常屏障功能受损,结膜组织侵入角膜和持续性炎症维持新生血管1)3)。
与淋巴管新生的关系
Section titled “与淋巴管新生的关系”角膜新生血管(血管新生)和淋巴管新生是相互关联但独立的过程4)。血管作为免疫效应细胞的输出通路(离心路),淋巴管作为抗原呈递细胞的输入通路(向心路)4)。两者同时进行与角膜移植中免疫特权的丧失和排斥反应有关4)。VEGF-A/VEGFR-2主要驱动血管新生,VEGF-C,D/VEGFR-3主要驱动淋巴管新生4)。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”AAV载体基因治疗
Section titled “AAV载体基因治疗”Xie等人(2024)综述了使用腺相关病毒(AAV)载体表达持续抗VEGF因子治疗角膜新生血管的研究5)。AAV2和AAV8对角膜基质细胞的转导效率最高,角膜基质内注射被认为是最有效的给药途径5)。AAV基因治疗单次给药即可发挥长期抗VEGF效果,但目前仍处于临床前阶段5)。
MMC血管内化学栓塞术(MICE)
Section titled “MMC血管内化学栓塞术(MICE)”Addeen等人(2023)报告了2例角膜移植后难治性新生血管患者接受MICE(使用33号针头血管内注入0.4 mg/mL MMC)治疗的病例6)。术后早期观察到血管幽灵化,疼痛减轻,生活质量改善6)。未观察到不良事件,但需确认长期安全性。
反义寡核苷酸(Aganirsen)
Section titled “反义寡核苷酸(Aganirsen)”Muller等人(2026)的综述报告,靶向IRS-1的反义寡核苷酸Aganirsen在临床前模型中显示出角膜新生血管的消退和缓解1)。CRISPR/Cas9编辑VEGF-A也显示出有希望的临床前数据1)。
眼科纳米系统
Section titled “眼科纳米系统”Zhang等人(2022)报告,纳米颗粒、脂质体、胶束等纳米载体可改善抗VEGF药物和类固醇的角膜内递送效率,实现持续释放、靶向性和低刺激性7)。临床应用仍有限,但有望减轻频繁给药的负担。
联合治疗的重要性
Section titled “联合治疗的重要性”角膜新生血管是一种多因素疾病,单一疗法往往难以获得足够疗效1)2)。针对VEGF、bFGF、PDGF、淋巴管新生等多条通路的联合疗法,可能成为未来治疗策略的核心1)。
8. 参考文献
Section titled “8. 参考文献”- Muller E, Feinberg L, Woronkowicz M, Roberts HW. Corneal Neovascularization: Pathogenesis, Current Insights and Future Strategies. Biology. 2026;15(2):136.
- Wu D, Chan KE, Lim BXH, et al. Management of corneal neovascularization: Current and emerging therapeutic approaches. Indian J Ophthalmol. 2024;72(Suppl 3):S354-S371.
- Drzyzga L, Spiewak D, Dorecka M, Wygledowska-Promienska D. Available Therapeutic Options for Corneal Neovascularization: A Review. Int J Mol Sci. 2024;25(10):5479.
- Zhang Z, Zhao R, Wu X, Ma Y, He Y. Research progress on the correlation between corneal neovascularization and lymphangiogenesis. Mol Med Rep. 2025;31(2):47.
- Xie M, Wang L, Deng Y, et al. Sustained and Efficient Delivery of Antivascular Endothelial Growth Factor by AAV for Treatment of Corneal Neovascularization. J Ophthalmol. 2024;2024:5487973.
- Addeen SZ, Oyoun Z, Alfhaily H, Anbari A. Outcomes of mitomycin C intravascular chemoembolization (MICE) in refractory corneal neovascularization after failed keratoplasty. Digit J Ophthalmol. 2023;29(4).
- Zhang C, Yin Y, Zhao J, et al. An Update on Novel Ocular Nanosystems with Possible Benefits in the Treatment of Corneal Neovascularization. Int J Nanomedicine. 2022;17:4911-4931.
