Neovascularización superficial

Neovascularización Corneal
1. ¿Qué es la neovascularización corneal?
Sección titulada «1. ¿Qué es la neovascularización corneal?»La neovascularización corneal (CoNV) es una condición patológica en la que nuevos capilares del plexo vascular limbal invaden el tejido corneal, que normalmente es avascular 1). No es una enfermedad específica, sino una respuesta inespecífica a diversas condiciones como infección, inflamación, hipoxia o traumatismo.
La cornea mantiene un “privilegio angiogénico corneal” (CAP), donde un equilibrio preciso entre factores inhibidores y promotores de la angiogénesis mantiene el estado avascular 1). Cuando este equilibrio se rompe, las células endoteliales vasculares proliferan, migran e invaden el estroma corneal.
Los nuevos vasos se clasifican en dos tipos según su ubicación anatómica.
Neovascularización profunda
Invade desde la arteria ciliar anterior hacia el estroma corneal.
Ocurre en queratitis intersticial (sífilis, tuberculosis), queratitis herpética estromal, queratopatía bullosa y otras inflamaciones o edemas persistentes.
Los vasos sanguíneos inmaduros causan exudación lipídica, inflamación persistente y cicatrización1). Con la progresión, los vasos maduran y se recubren de pericitos, volviéndose resistentes a la terapia anti-VEGF1). En pacientes trasplantados de córnea, la neovascularización es un factor de riesgo para el rechazo.
Si no se trata, los vasos maduran y se vuelven difíciles de regresar espontáneamente, causando queratopatía lipídica (depósitos de lípidos en la córnea) y cicatrices corneales que provocan una pérdida visual permanente. Además, si se requiere un trasplante de córnea, la presencia de vasos aumenta el riesgo de rechazo del injerto. Es importante la consulta temprana y el tratamiento de la causa.
2. Principales síntomas y hallazgos clínicos
Sección titulada «2. Principales síntomas y hallazgos clínicos»Síntomas subjetivos
Sección titulada «Síntomas subjetivos»- Disminución de la agudeza visual: ocurre cuando los vasos sanguíneos anormales o sus complicaciones (depósitos de lípidos, cicatrices) afectan el eje visual
- Enrojecimiento: hiperemia conjuntival asociada a la enfermedad subyacente
- Asintomático: cuando la lesión no afecta el eje visual, a menudo no hay síntomas subjetivos
Hallazgos clínicos (hallazgos que el médico confirma mediante el examen)
Sección titulada «Hallazgos clínicos (hallazgos que el médico confirma mediante el examen)»- Morfología de los vasos neovasculares: desde un patrón reticular fino hasta vasos activos tortuosos y vasos maduros de alta densidad
- Ubicación y profundidad de los vasos: se evalúa si son superficiales o profundos mediante el método de hendidura e iluminación indirecta con lámpara de hendidura
- vaso fantasma: vaso antiguo con flujo sanguíneo interrumpido. No requiere tratamiento
- conjuntivalización: cubrimiento de la córnea por tejido conjuntival. Se confirma con tinción retardada con fluoresceína
- queratopatía lipídica: opacidad blanco-amarillenta por depósito de lípidos en el estroma corneal, filtrados desde vasos sanguíneos nuevos
- desaparición de la empalizada de Vogt (POV): hallazgo importante que sugiere pérdida de células madre limbares
3. Causas y factores de riesgo
Sección titulada «3. Causas y factores de riesgo»Infecciones
Sección titulada «Infecciones»- Virus del herpes simple (VHS-1): la causa infecciosa más común de neovascularización corneal en países desarrollados1). La queratitis herpética estromal produce neovascularización profunda
- Queratitis bacteriana: en casos graves, se produce invasión vascular asociada a úlcera corneal y cicatrización
- Queratitis fúngica: en casos de tratamiento prolongado puede acompañarse de neovascularización
- Tracoma y oncocercosis: principales causas infecciosas en países en desarrollo1)
Hipoxia (relacionada con lentes de contacto)
Sección titulada «Hipoxia (relacionada con lentes de contacto)»El uso inadecuado (uso excesivo) de lentes de contacto blandos es la causa principal. En aproximadamente el 80-90% de los usuarios de lentes de contacto blandos de HEMA convencionales se observa invasión vascular desde la parte superior de la córnea (dirección de las 10 a las 2 en punto). Si el daño epitelial persiste durante más de un mes, los vasos sanguíneos invaden esa área.
Trauma químico
Sección titulada «Trauma químico»Las lesiones por álcali penetran profundamente en el estroma corneal, causando daño extenso a las células madre del limbo y neovascularización. Es uno de los grupos con una tasa de éxito significativamente baja en el trasplante de córnea.
Deficiencia de células madre del limbo (LSCD)
Sección titulada «Deficiencia de células madre del limbo (LSCD)»La LSCD es una de las principales vías de neovascularización corneal1)3). Cuando las células madre del limbo fallan debido a causas congénitas, trauma químico, uso excesivo de lentes de contacto, enfermedades inflamatorias sistémicas o iatrogénicas, se pierde la barrera epitelial normal y se produce invasión vascular3). En casos leves, se observa epiteliopatía en espiral con tinción de fluoresceína; en casos moderados, aparecen neovascularización superficial y pannus3).
Otras causas
Sección titulada «Otras causas»- Enfermedades inflamatorias: SJS/TEN, penfigoide ocular, catarro primaveral, queratitis rosácea
- Después de trasplante de córnea: neovascularización asociada al rechazo1)
- Enfermedades degenerativas: degeneración marginal de Terrien, distrofia corneal gelatinosa en gotas
Sí, en muchos casos se puede prevenir. Una de las principales causas de la neovascularización corneal es la falta de oxígeno debido a los lentes de contacto. Siguiendo el tiempo de uso recomendado, utilizando lentes de alta permeabilidad al oxígeno y realizando exámenes oftalmológicos regulares, se puede reducir significativamente el riesgo.
4. Métodos de diagnóstico y pruebas
Sección titulada «4. Métodos de diagnóstico y pruebas»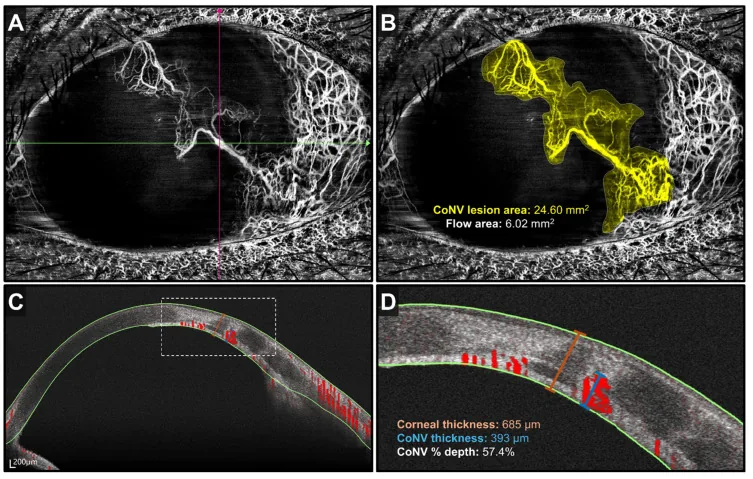
Examen con lámpara de hendidura
Sección titulada «Examen con lámpara de hendidura»Es la prueba más básica para el diagnóstico de la neovascularización corneal. Se evalúa la ubicación (cuadrante), profundidad (superficial/profunda), actividad (presencia de flujo sanguíneo) y presencia de invasión conjuntival de los vasos sanguíneos.
- Método de difusor: al aumentar el ancho del haz de luz o observar a través de un difusor, los vasos sanguíneos nuevos son más fáciles de distinguir
- Iluminación indirecta: observar los vasos sanguíneos nuevos y los nervios corneales mediante la luz reflejada del iris o del cristalino
- Tinción con fluoresceína: útil para evaluar la presencia de defectos epiteliales y la invasión conjuntival
Angiografía con fluoresceína
Sección titulada «Angiografía con fluoresceína»- Angiografía con fluoresceína (FA): evalúa funcionalmente la perfusión y la fuga vascular, diferenciando vasos activos de maduros 1)
- Angiografía con verde de indocianina (ICGA): excelente para visualizar vasos profundos y aferentes, útil para la orientación de la oclusión vascular 1)
Pruebas de imagen
Sección titulada «Pruebas de imagen»- OCT / OCT-A de segmento anterior: evalúa de forma no invasiva la profundidad y extensión de la red vascular corneal 1)
- Microscopía confocal in vivo (IVCM):Permite la cuantificación de células basales epiteliales en el diagnóstico de LSCD3)
| Método de examen | Principales parámetros evaluados | Características |
|---|---|---|
| Microscopio de lámpara de hendidura | Ubicación, profundidad y actividad | Examen básico de primera elección |
| AF / ICGA | Perfusión, fuga y vasos aferentes | Útil para la planificación del tratamiento |
| AS-OCT / OCT-A | Evaluación cuantitativa de profundidad | No invasivo |
5. Tratamiento estándar
Sección titulada «5. Tratamiento estándar»El tratamiento de la neovascularización corneal se basa en dos pilares: el tratamiento de la causa y la intervención sobre los propios vasos sanguíneos nuevos2).
Tratamiento de la causa
Sección titulada «Tratamiento de la causa»- Suspensión del uso de lentes de contacto: en caso de hipoxia, se debe suspender su uso y considerar el cambio a lentes de mayor permeabilidad al oxígeno. Es necesario determinar si los vasos son activos o antiguos (ghost vessel).
- Tratamiento de la infección: administración de antibióticos, antivirales o antifúngicos para la queratitis infecciosa causante.
- Tratamiento de LSCD: cirugía como trasplante de limbo o trasplante de membrana amniótica
Terapia farmacológica
Sección titulada «Terapia farmacológica»- Colirio de esteroides: suprime la neovascularización al inhibir citocinas inflamatorias (IL-1, IL-6), inducir apoptosis de linfocitos y suprimir la vasodilatación2). Es de primera elección, pero con uso prolongado se debe tener cuidado con el glaucoma esteroideo y el aumento de la susceptibilidad a infecciones
- Terapia anti-VEGF: se usa ampliamente bevacizumab (colirio, inyección subconjuntival o intracorneal)1)2). Es eficaz para vasos inmaduros activos, pero su efecto es limitado en vasos maduros (recubiertos por pericitos)1). Dado que el recubrimiento por pericitos alcanza el 80% dentro de las 2 semanas posteriores al inicio de la neovascularización, el tratamiento temprano es importante1)
- Fármacos inmunosupresores: la ciclosporina A en colirio suprime la activación de las células T y tiene un efecto ahorrador de corticosteroides2). El tacrolimús y el sirolimús (inhibidor de mTOR) también son opciones1)
- Doxiciclina: inhibe la neovascularización corneal mediante su acción inhibidora del penfigoide mucoso cicatricial2)
Tratamiento quirúrgico y procedimientos
Sección titulada «Tratamiento quirúrgico y procedimientos»- Fotocoagulación con láser: coagula y ocluye los vasos con láser de argón o Nd:YAG. Se utiliza como preparación previa al trasplante de córnea y para el tratamiento de la queratopatía lipídica. Existe riesgo de hemorragia corneal y adelgazamiento, y a menudo se observan recanalización vascular y formación de vasos derivados
- fine needle diathermy (FND): se inserta una aguja fina en los vasos nutricios del limbo y se coagula eléctricamente para ocluirlos. También es eficaz en vasos maduros y gruesos, y se realiza en vasos aferentes difíciles de ocluir con láser de argón1)
- terapia fotodinámica (PDT): tras inyectar una sustancia fotosensible en los vasos sanguíneos, se irradia con luz para generar especies reactivas de oxígeno que destruyen la pared vascular. Tiene alta especificidad, pero es costosa y requiere tiempo
- MICE (quimioembolización intravascular con MMC): técnica que consiste en inyectar directamente mitomicina C (0,4 mg/mL) en los vasos nutricios con una aguja de calibre 336). Se ha informado de la formación de vasos fantasma y mejora de la lipidosis corneal en neovascularización corneal refractaria a tratamientos convencionales6)
6. Fisiopatología y mecanismo detallado de la enfermedad
Sección titulada «6. Fisiopatología y mecanismo detallado de la enfermedad»Mecanismo de mantenimiento del privilegio antiangiogénico corneal (CAP)
Sección titulada «Mecanismo de mantenimiento del privilegio antiangiogénico corneal (CAP)»El estado avascular de la córnea se mantiene mediante la coordinación de múltiples mecanismos inhibidores de la angiogénesis1).
- Receptor 1 soluble del factor de crecimiento endotelial vascular (sVEGFR1): se produce de forma constitutiva en el epitelio y el estroma corneales. Captura con alta afinidad el VEGF-A e inhibe competitivamente su unión al VEGFR de membrana, actuando como una trampa endógena de VEGF1)
- Trombospondina (TSP-1/TSP-2): glucoproteína antiangiogénica expresada constitutivamente en la ECM corneal. Secuestra VEGF y suprime la señalización de VEGFR2. Induce apoptosis de las células endoteliales vasculares (VEC) a través de CD36/CD471)
- Endostatina: fragmento C-terminal del colágeno XVIII. Inhibe las vías de VEGF y bFGF, y promueve la apoptosis de VEC mediante el aumento de la actividad de caspasa-3. También suprime la linfangiogénesis1)
- Barrera física: la barrera limbal, la densa disposición del colágeno y el ambiente relativamente frío de la córnea limitan la invasión vascular1)
Factores proangiogénicos y vías patogénicas
Sección titulada «Factores proangiogénicos y vías patogénicas»La ruptura de la CAP ocurre principalmente a través de dos vías1)2).
Vía 1: Aumento de la producción de factores promotores debido a inflamación e hipoxia
El daño corneal provoca la liberación de tres factores angiogénicos principales por parte de macrófagos, células epiteliales y endoteliales1).
- VEGF-A: Promueve la proliferación y migración de las células endoteliales vasculares (VEC) a través de VEGFR-2, induce metaloproteinasas de matriz-2/metaloproteinasas de matriz-9 y estimula la remodelación de la matriz extracelular (ECM)1). Es el factor promotor más importante en la neovascularización corneal.
- bFGF (FGF-2): a través de la vía ERK/PI3K aumenta la producción de VEGF y disocia la unión de VE-cadherina, promoviendo la brotación de las CVE 1)
- PDGF: recluta pericitos y células de músculo liso, estabilizando los nuevos vasos sanguíneos 1). La maduración vascular inducida por PDGF genera resistencia a la terapia anti-VEGF
Vía 2: Deficiencia de células madre del limbo (LSCD)
La pérdida de células madre del limbo provoca la pérdida de la función de barrera normal del epitelio corneal, permitiendo la invasión del tejido conjuntival en la córnea y una inflamación persistente que mantiene los nuevos vasos sanguíneos 1)3).
Relación con la linfangiogénesis
Sección titulada «Relación con la linfangiogénesis»La neovascularización corneal (angiogénesis) y la linfangiogénesis son procesos independientes aunque interrelacionados4). Los vasos sanguíneos funcionan como vía de salida (eferente) para las células efectoras inmunitarias, mientras que los vasos linfáticos actúan como vía de entrada (aferente) para las células presentadoras de antígenos4). La progresión simultánea de ambos procesos contribuye a la pérdida del privilegio inmunitario y al rechazo en el trasplante de córnea4). VEGF-A/VEGFR-2 impulsa principalmente la angiogénesis, mientras que VEGF-C,D/VEGFR-3 impulsa la linfangiogénesis4).
7. Investigación actual y perspectivas futuras
Sección titulada «7. Investigación actual y perspectivas futuras»Terapia génica con vectores AAV
Sección titulada «Terapia génica con vectores AAV»Xie et al. (2024) revisaron el tratamiento de la neovascularización corneal mediante la expresión sostenida de factores anti-VEGF utilizando vectores de virus adenoasociados (AAV) 5). Se considera que AAV2 y AAV8 son los más eficientes para la transducción de queratocitos, y la inyección intraestromal corneal es la vía de administración más efectiva 5). La terapia génica con AAV puede proporcionar un efecto anti-VEGF a largo plazo con una sola dosis, pero actualmente se encuentra en etapa preclínica 5).
Quimioembolización intravascular con MMC (MICE)
Sección titulada «Quimioembolización intravascular con MMC (MICE)»Addeen et al. (2023) reportaron dos casos de MICE (inyección intravascular de MMC 0.4 mg/mL con aguja de 33G) para neovascularización refractaria después de trasplante de córnea 6). Se observó la formación de vasos fantasmas desde el postoperatorio temprano, con reducción del dolor y mejora en la calidad de vida 6). No se reportaron eventos adversos, aunque se requiere confirmación de la seguridad a largo plazo.
Oligonucleótido antisentido (Aganirsen)
Sección titulada «Oligonucleótido antisentido (Aganirsen)»En la revisión de Muller et al. (2026), se informó que Aganirsen, un oligonucleótido antisentido dirigido a IRS-1, mostró regresión y remisión de la neovascularización corneal en modelos preclínicos1). La edición de VEGF-A con CRISPR/Cas9 también muestra datos preclínicos prometedores1).
Nanosistemas oftálmicos
Sección titulada «Nanosistemas oftálmicos»Zhang et al. (2022) informaron que los nanotransportadores como nanopartículas, liposomas y micelas pueden mejorar la eficiencia de administración corneal de fármacos anti-VEGF y esteroides, logrando liberación sostenida, direccionamiento específico y baja irritación7). Aunque la aplicación clínica aún es limitada, se espera que reduzcan la carga de las administraciones frecuentes.
Importancia de la terapia combinada
Sección titulada «Importancia de la terapia combinada»La neovascularización corneal es una condición multifactorial, por lo que a menudo un solo tratamiento no es suficiente 1)2). La terapia combinada dirigida a múltiples vías como VEGF, bFGF, PDGF y linfangiogénesis podría convertirse en el centro de las estrategias terapéuticas futuras 1).
8. Referencias
Sección titulada «8. Referencias»- Muller E, Feinberg L, Woronkowicz M, Roberts HW. Corneal Neovascularization: Pathogenesis, Current Insights and Future Strategies. Biology. 2026;15(2):136.
- Wu D, Chan KE, Lim BXH, et al. Management of corneal neovascularization: Current and emerging therapeutic approaches. Indian J Ophthalmol. 2024;72(Suppl 3):S354-S371.
- Drzyzga L, Spiewak D, Dorecka M, Wygledowska-Promienska D. Available Therapeutic Options for Corneal Neovascularization: A Review. Int J Mol Sci. 2024;25(10):5479.
- Zhang Z, Zhao R, Wu X, Ma Y, He Y. Research progress on the correlation between corneal neovascularization and lymphangiogenesis. Mol Med Rep. 2025;31(2):47.
- Xie M, Wang L, Deng Y, et al. Sustained and Efficient Delivery of Antivascular Endothelial Growth Factor by AAV for Treatment of Corneal Neovascularization. J Ophthalmol. 2024;2024:5487973.
- Addeen SZ, Oyoun Z, Alfhaily H, Anbari A. Outcomes of mitomycin C intravascular chemoembolization (MICE) in refractory corneal neovascularization after failed keratoplasty. Digit J Ophthalmol. 2023;29(4).
- Zhang C, Yin Y, Zhao J, et al. An Update on Novel Ocular Nanosystems with Possible Benefits in the Treatment of Corneal Neovascularization. Int J Nanomedicine. 2022;17:4911-4931.
