Neovascolarizzazione superficiale

Neovascolarizzazione corneale (Corneal Neovascularization)
1. Cos’è la neovascolarizzazione corneale?
Sezione intitolata “1. Cos’è la neovascolarizzazione corneale?”La neovascolarizzazione corneale (CoNV) è una condizione in cui nuovi capillari dal plesso vascolare limbare invadono il tessuto corneale normalmente avascolare1). Non è una malattia specifica ma una risposta aspecifica a varie condizioni come infezione, infiammazione, ipossia e trauma.
La cornea possiede un «privilegio angiogenico corneale (CAP)» che mantiene lo stato avascolare grazie a un equilibrio preciso tra fattori inibitori e promotori dell’angiogenesi1). Quando questo equilibrio si rompe, le cellule endoteliali vascolari proliferano, migrano e invadono lo stroma corneale.
I neovasi sono classificati in due tipi in base alla posizione anatomica.
Neovascolarizzazione profonda
Invadono lo stroma corneale dalle arterie ciliari anteriori.
Si verifica in infiammazioni o edemi persistenti come cheratite interstiziale (sifilide, tubercolosi), cheratite erpetica stromale e cheratopatia bollosa.
I neovasi immaturi causano essudazione lipidica, infiammazione persistente e cicatrizzazione 1). Con il progredire, i vasi maturano, si ricoprono di periciti e diventano resistenti alla terapia anti-VEGF 1). Nei pazienti dopo trapianto di cornea, i neovasi rappresentano un fattore di rischio per il rigetto.
Senza trattamento, i neovasi maturano e regrediscono spontaneamente con difficoltà, portando a cheratopatia lipidica (depositi lipidici nella cornea) e cicatrici corneali, causa di un calo visivo permanente. Inoltre, in caso di necessità di trapianto di cornea, la presenza di neovasi aumenta il rischio di rigetto del graft. Sono importanti una visita precoce e il trattamento della causa.
2. Principali sintomi e segni clinici
Sezione intitolata “2. Principali sintomi e segni clinici”Sintomi soggettivi
Sezione intitolata “Sintomi soggettivi”- Riduzione dell’acuità visiva: si verifica quando i neovasi o le loro complicanze (depositi lipidici, cicatrici) interessano l’asse visivo
- Iperemia: iperemia congiuntivale associata alla malattia di base
- Asintomatico: spesso nessun sintomo soggettivo se la lesione non interessa l’asse visivo
Segni clinici (osservati dal medico all’esame)
Sezione intitolata “Segni clinici (osservati dal medico all’esame)”- Morfologia dei neovasi: varia da un fine reticolo a vasi attivi tortuosi, fino a vasi maturi densi
- Posizione e profondità dei vasi: valutate con lampada a fessura mediante metodo a fessura e illuminazione indiretta per determinare se superficiali o profondi
- Ghost vessel (vaso fantasma): vaso vecchio senza flusso sanguigno. Non richiede trattamento.
- Congiuntivalizzazione: rivestimento della cornea da tessuto congiuntivale. Confermato da colorazione ritardata alla fluoresceina.
- Cheratopatia lipidica: opacità giallo-biancastra dovuta a deposito di lipidi nello stroma corneale, fuoriusciti dai neovasi.
- Scomparsa della palizzata di Vogt (POV): segno importante che suggerisce una perdita delle cellule staminali limbari.
3. Cause e fattori di rischio
Sezione intitolata “3. Cause e fattori di rischio”Infezioni
Sezione intitolata “Infezioni”- Virus dell’herpes simplex (HSV-1) : causa infettiva più comune di neovascolarizzazione corneale nei paesi sviluppati 1). La cheratite erpetica stromale provoca neovascolarizzazione profonda.
- Cheratite batterica : nei casi gravi, l’ulcera corneale e la cicatrizzazione si accompagnano a invasione vascolare.
- Cheratite fungina : può associarsi a neovascolarizzazione nei casi prolungati.
- Tracoma e oncocercosi : principali cause infettive nei paesi in via di sviluppo 1).
Ipossia (correlata alle lenti a contatto)
Sezione intitolata “Ipossia (correlata alle lenti a contatto)”La causa principale è l’uso improprio (sovrautilizzo) delle lenti a contatto morbide. Circa l’80-90% degli utilizzatori di lenti morbide tradizionali in HEMA presenta invasione vascolare dalla parte superiore della cornea (direzione ore 10-2). Se la lesione epiteliale persiste per più di un mese, i vasi invadono l’area.
Trauma chimico
Sezione intitolata “Trauma chimico”Le ustioni alcaline penetrano in profondità nello stroma corneale, causando un’estesa compromissione delle cellule staminali limbari e neovascolarizzazione. È uno dei gruppi con il tasso di successo del trapianto di cornea significativamente più basso.
Insufficienza delle cellule staminali limbari (LSCD)
Sezione intitolata “Insufficienza delle cellule staminali limbari (LSCD)”La LSCD è una delle principali vie della neovascolarizzazione corneale 1)3). Quando le cellule staminali limbari diventano disfunzionali a causa di cause congenite, traumi chimici, uso eccessivo di lenti a contatto, malattie infiammatorie sistemiche o cause iatrogene, la normale barriera epiteliale viene persa e si verifica invasione vascolare 3). Nei casi lievi, la colorazione con fluoresceina mostra un’epiteliopatia a vortice; nei casi moderati compaiono neovascolarizzazione superficiale e panno 3).
Altre cause
Sezione intitolata “Altre cause”- Malattie infiammatorie : SJS/TEN, pemfigoide oculare, cheratocongiuntivite primaverile, cheratite da rosacea.
- Dopo trapianto di cornea : neovascolarizzazione associata a rigetto 1).
- Malattie degenerative: degenerazione marginale di Terrien, distrofia corneale goccioliforme gelatinosa
Sì, spesso è prevenibile. Una delle cause principali della neovascolarizzazione corneale è la mancanza di ossigeno dovuta alle lenti a contatto. Rispettando i tempi di utilizzo, utilizzando lenti ad alta permeabilità all’ossigeno e sottoponendosi a regolari visite oculistiche, è possibile ridurre significativamente il rischio.
4. Diagnosi e metodi di esame
Sezione intitolata “4. Diagnosi e metodi di esame”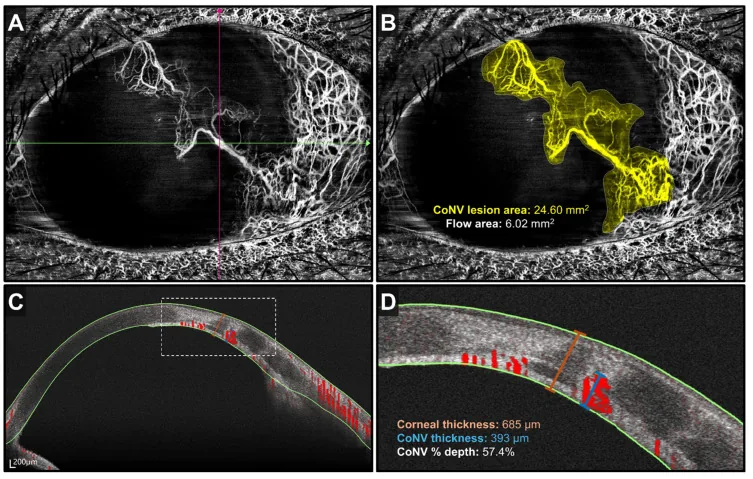
Esame con lampada a fessura
Sezione intitolata “Esame con lampada a fessura”Questo è l’esame più fondamentale per la diagnosi di neovascolarizzazione corneale. Si valutano la posizione (quadrante), la profondità (superficiale/profonda), l’attività (presenza di flusso sanguigno) e la presenza di invasione congiuntivale dei vasi.
- Metodo del diffusore: allargando il fascio luminoso o utilizzando un diffusore, i vasi neoformati sono più facili da distinguere
- Illuminazione indiretta: osservazione dei vasi neoformati e dei nervi corneali mediante luce riflessa dall’iride o dal cristallino
- Colorazione con fluoresceina : utile per rilevare difetti epiteliali e valutare l’invasione congiuntivale
Angiografia fluorescente
Sezione intitolata “Angiografia fluorescente”- Angiografia con fluoresceina (FA) : valuta funzionalmente la perfusione e la fuoriuscita vascolare, differenziando vasi attivi da vasi maturi1)
- Angiografia con verde indocianina (ICGA) : eccellente per visualizzare vasi profondi e afferenti, utile per il targeting dell’occlusione vascolare1)
Imaging
Sezione intitolata “Imaging”- OCT / OCT-A del segmento anteriore : consente una valutazione quantitativa non invasiva della profondità e dell’estensione della rete vascolare corneale1)
- Microscopia confocale in vivo (IVCM) : consente la quantificazione delle cellule basali epiteliali nella diagnosi di LSCD3)
| Metodo di esame | Principali parametri valutati | Caratteristiche |
|---|---|---|
| Lampada a fessura | Posizione, profondità, attività | Esame di base di prima linea |
| FA / ICGA | Perfusione, fuoriuscita, vasi afferenti | Utile per la pianificazione del trattamento |
| AS-OCT / OCT-A | Valutazione quantitativa e di profondità | Non invasivo |
5. Trattamento standard
Sezione intitolata “5. Trattamento standard”Il trattamento della neovascolarizzazione corneale si basa su due pilastri: trattamento della causa e intervento sui neovasi stessi2).
Trattamento della causa
Sezione intitolata “Trattamento della causa”- Sospensione dell’uso di lenti a contatto: in caso di ipossia, sospendere l’uso e considerare il passaggio a lenti ad alta permeabilità all’ossigeno. Distinguere tra vasi attivi e vasi vecchi (ghost vessel).
- Trattamento dell’infezione: somministrazione di antibiotici, antivirali o antimicotici per la cheratite infettiva causale.
- Trattamento della LSCD: trattamento chirurgico come il trapianto di limbo o il trapianto di membrana amniotica.
Terapia farmacologica
Sezione intitolata “Terapia farmacologica”- Collirio steroideo: sopprime la neovascolarizzazione inibendo le citochine infiammatorie (IL-1, IL-6), inducendo l’apoptosi dei linfociti e inibendo la vasodilatazione2). È la terapia di prima linea, ma con l’uso a lungo termine occorre prestare attenzione al glaucoma steroideo e all’aumentata suscettibilità alle infezioni.
- Terapia anti-VEGF: il bevacizumab (collirio, iniezione sottocongiuntivale o intrastromale) è ampiamente utilizzato1)2). Efficace sui vasi attivi immaturi, ma effetto limitato sui vasi maturi (rivestiti da periciti)1). Poiché la copertura dei periciti raggiunge l’80% entro due settimane dalla comparsa dei neovasi, il trattamento precoce è importante1).
- Immunosoppressori: il collirio di ciclosporina A sopprime l’attivazione dei linfociti T e ha un effetto di risparmio di steroidi2). Tacrolimus e sirolimus (inibitore di mTOR) sono anche opzioni1).
- Doxiciclina: sopprime la neovascolarizzazione corneale mediante inibizione del pemfigoide delle mucose2).
Trattamento chirurgico e procedurale
Sezione intitolata “Trattamento chirurgico e procedurale”- Fotocoagulazione laser: coagulazione e occlusione dei vasi con laser argon o Nd:YAG. Utilizzata come pretrattamento prima del trapianto di cornea e per il trattamento della cheratopatia lipidica. Rischio di emorragia e assottigliamento corneale; spesso si osservano ricanalizzazione vascolare e formazione di shunt.
- Diatermia con ago sottile (FND): inserimento di un ago sottile nei vasi nutritizi del limbo per coagulazione elettrica. Efficace anche su vasi maturi e spessi; utilizzata per vasi afferenti difficili da occludere con laser argon 1).
- Terapia fotodinamica (PDT): iniezione intravascolare di un fotosensibilizzatore, quindi irradiazione luminosa per generare specie reattive dell’ossigeno e distruggere la parete vascolare. Elevata specificità, ma costi elevati e tempi lunghi.
- MICE (chemoembolizzazione intravascolare con MMC): iniezione diretta di mitomicina C (0,4 mg/mL) nei vasi nutritizi con ago 33G 6). Per la neovascolarizzazione corneale refrattaria ai trattamenti convenzionali, è stato riportato un miglioramento della ghostizzazione vascolare e della cheratopatia lipidica 6).
6. Fisiopatologia e meccanismi dettagliati
Sezione intitolata “6. Fisiopatologia e meccanismi dettagliati”Meccanismi di mantenimento del privilegio angiogenico corneale (CAP)
Sezione intitolata “Meccanismi di mantenimento del privilegio angiogenico corneale (CAP)”Lo stato avascolare della cornea è mantenuto dal coordinamento di molteplici meccanismi inibitori dell’angiogenesi 1).
- Recettore solubile del VEGF 1 (sVEGFR1): prodotto costitutivamente dall’epitelio e dallo stroma corneale. Cattura il VEGF-A con alta affinità e inibisce competitivamente il legame al VEGFR di membrana, agendo come una trappola endogena del VEGF 1).
- Trombospondina (TSP-1/TSP-2): glicoproteina inibitoria dell’angiogenesi espressa costitutivamente nella matrice extracellulare corneale. Sequestra il VEGF e sopprime la segnalazione di VEGFR2. Induce l’apoptosi delle cellule endoteliali vascolari tramite CD36/CD47 1).
- Endostatina: frammento C-terminale del collagene XVIII. Inibisce le vie del VEGF e del bFGF, e promuove l’apoptosi delle cellule endoteliali vascolari tramite attivazione della caspasi-3. Sopprime anche la linfangiogenesi 1).
- Barriera fisica: la barriera limbare, la fitta disposizione del collagene e l’ambiente relativamente freddo della cornea limitano l’invasione vascolare1)
Fattori pro-angiogenici e vie di sviluppo
Sezione intitolata “Fattori pro-angiogenici e vie di sviluppo”La rottura del CAP avviene principalmente attraverso due vie1)2).
Via 1: Aumento della produzione di fattori promotori dovuto a infiammazione e ipossia
Il danno corneale porta al rilascio di tre principali fattori angiogenici da parte di macrofagi, cellule epiteliali e cellule endoteliali1).
- VEGF-A: attraverso VEGFR-2 promuove la proliferazione e la migrazione delle VEC, induce MMP-2/MMP-9 e stimola il rimodellamento della ECM1). Fattore promotore più importante nella neovascolarizzazione corneale
- bFGF (FGF-2): attraverso la via ERK/PI3K aumenta la produzione di VEGF, dissocia i legami della VE-caderina e promuove la germinazione delle VEC1)
- PDGF: recluta periciti e cellule muscolari lisce, stabilizzando i nuovi vasi1). La maturazione vascolare indotta da PDGF conferisce resistenza alla terapia anti-VEGF
Via 2: Insufficienza di cellule staminali limbari (LSCD)
La perdita di cellule staminali limbari porta alla perdita della normale funzione di barriera dell’epitelio corneale, e l’invasione del tessuto congiuntivale nella cornea insieme all’infiammazione persistente mantengono la neovascolarizzazione1)3).
Relazione con la linfangiogenesi
Sezione intitolata “Relazione con la linfangiogenesi”La neovascolarizzazione corneale (angiogenesi) e la linfangiogenesi sono processi interconnessi ma indipendenti4). I vasi sanguigni fungono da via efferente per le cellule effettrici immunitarie, mentre i vasi linfatici fungono da via afferente per le cellule presentanti l’antigene4). La progressione simultanea di entrambi è coinvolta nella perdita del privilegio immunitario e nel rigetto nel trapianto di cornea4). VEGF-A/VEGFR-2 guida principalmente l’angiogenesi, mentre VEGF-C,D/VEGFR-3 guida principalmente la linfangiogenesi4).
7. Ricerche recenti e prospettive future
Sezione intitolata “7. Ricerche recenti e prospettive future”Terapia genica con vettori AAV
Sezione intitolata “Terapia genica con vettori AAV”Xie et al. (2024) hanno revisionato il trattamento della neovascolarizzazione corneale mediante espressione sostenuta di fattori anti-VEGF utilizzando vettori di virus adeno-associati (AAV)5). AAV2 e AAV8 sono i più efficienti nel trasdurre le cellule dello stroma corneale, e l’iniezione intrastromale è considerata la via di somministrazione più efficace5). La terapia genica con AAV può fornire un effetto anti-VEGF a lungo termine dopo una singola somministrazione, ma attualmente è ancora in fase preclinica5).
Chemoembolizzazione intravascolare con MMC (MICE)
Sezione intitolata “Chemoembolizzazione intravascolare con MMC (MICE)”Addeen et al. (2023) hanno riportato due casi di MICE (iniezione intravascolare di MMC 0,4 mg/mL con ago 33 gauge) per neovascolarizzazione refrattaria dopo trapianto di cornea 6). Nelle fasi post-operatorie precoci si è osservata una fantomatizzazione dei vasi, con riduzione del dolore e miglioramento della qualità di vita 6). Non sono stati osservati eventi avversi, ma è necessaria la conferma della sicurezza a lungo termine.
Oligonucleotide antisenso (Aganirsen)
Sezione intitolata “Oligonucleotide antisenso (Aganirsen)”Nella revisione di Muller et al. (2026), l’oligonucleotide antisenso Aganirsen, che ha come bersaglio IRS-1, ha mostrato regressione e remissione della neovascolarizzazione corneale in modelli preclinici 1). Anche l’editing di VEGF-A tramite CRISPR/Cas9 mostra dati preclinici promettenti 1).
Nanosistemi oftalmici
Sezione intitolata “Nanosistemi oftalmici”Zhang et al. (2022) hanno riportato che nanovettori come nanoparticelle, liposomi e micelle possono migliorare l’efficienza di somministrazione di farmaci anti-VEGF e steroidi nella cornea, consentendo rilascio prolungato, targeting e bassa irritazione 7). L’applicazione clinica è ancora limitata, ma si spera di ridurre il carico delle somministrazioni frequenti.
Importanza della terapia combinata
Sezione intitolata “Importanza della terapia combinata”La neovascolarizzazione corneale è una condizione multifattoriale, quindi una singola terapia spesso non è sufficiente 1)2). Le terapie combinate che mirano a più vie (VEGF, bFGF, PDGF, linfangiogenesi) potrebbero diventare centrali nelle future strategie terapeutiche 1).
8. Riferimenti
Sezione intitolata “8. Riferimenti”- Muller E, Feinberg L, Woronkowicz M, Roberts HW. Corneal Neovascularization: Pathogenesis, Current Insights and Future Strategies. Biology. 2026;15(2):136.
- Wu D, Chan KE, Lim BXH, et al. Management of corneal neovascularization: Current and emerging therapeutic approaches. Indian J Ophthalmol. 2024;72(Suppl 3):S354-S371.
- Drzyzga L, Spiewak D, Dorecka M, Wygledowska-Promienska D. Available Therapeutic Options for Corneal Neovascularization: A Review. Int J Mol Sci. 2024;25(10):5479.
- Zhang Z, Zhao R, Wu X, Ma Y, He Y. Research progress on the correlation between corneal neovascularization and lymphangiogenesis. Mol Med Rep. 2025;31(2):47.
- Xie M, Wang L, Deng Y, et al. Sustained and Efficient Delivery of Antivascular Endothelial Growth Factor by AAV for Treatment of Corneal Neovascularization. J Ophthalmol. 2024;2024:5487973.
- Addeen SZ, Oyoun Z, Alfhaily H, Anbari A. Outcomes of mitomycin C intravascular chemoembolization (MICE) in refractory corneal neovascularization after failed keratoplasty. Digit J Ophthalmol. 2023;29(4).
- Zhang C, Yin Y, Zhao J, et al. An Update on Novel Ocular Nanosystems with Possible Benefits in the Treatment of Corneal Neovascularization. Int J Nanomedicine. 2022;17:4911-4931.
