Tân mạch nông

Tân mạch giác mạc (Corneal Neovascularization)
1. Tân mạch giác mạc là gì?
Phần tiêu đề “1. Tân mạch giác mạc là gì?”Tân mạch giác mạc (CoNV) là tình trạng các mao mạch mới từ đám rối mạch máu vùng rìa xâm nhập vào mô giác mạc vốn không có mạch máu1). Đây không phải là một bệnh cụ thể mà là phản ứng không đặc hiệu với nhiều tình trạng khác nhau như nhiễm trùng, viêm, thiếu oxy và chấn thương.
Giác mạc duy trì “đặc quyền chống tân mạch giác mạc (CAP)”, trong đó trạng thái không mạch máu được duy trì nhờ sự cân bằng chính xác giữa các yếu tố ức chế và kích thích tân mạch1). Khi sự cân bằng này bị phá vỡ, các tế bào nội mô mạch máu tăng sinh, di chuyển và xâm nhập vào nhu mô giác mạc.
Các mạch máu mới được phân loại thành hai loại dựa trên vị trí giải phẫu.
Tân mạch sâu
Xâm nhập từ động mạch thể mi trước vào trong nhu mô giác mạc.
Xảy ra do viêm giác mạc mô kẽ (giang mai, lao), viêm giác mạc herpes thể mô kẽ, viêm giác mạc bọng nước và các tình trạng viêm/phù nề dai dẳng khác.
Các mạch máu mới chưa trưởng thành gây rò rỉ lipid, viêm dai dẳng và sẹo hóa 1). Khi tiến triển, các mạch trưởng thành và được bao phủ bởi tế bào quanh mạch (pericyte), trở nên kháng trị liệu kháng VEGF 1). Ở bệnh nhân sau ghép giác mạc, mạch máu mới là yếu tố nguy cơ thải ghép.
Nếu không điều trị, các mạch máu mới sẽ trưởng thành và khó thoái triển tự nhiên, gây bệnh lipid giác mạc (lắng đọng lipid trong giác mạc) và sẹo giác mạc, dẫn đến giảm thị lực vĩnh viễn. Ngoài ra, nếu cần ghép giác mạc, sự hiện diện của mạch máu mới làm tăng nguy cơ thải ghép. Khám sớm và điều trị nguyên nhân là rất quan trọng.
2. Triệu chứng chính và dấu hiệu lâm sàng
Phần tiêu đề “2. Triệu chứng chính và dấu hiệu lâm sàng”Triệu chứng cơ năng
Phần tiêu đề “Triệu chứng cơ năng”- Giảm thị lực: Xảy ra khi mạch máu mới hoặc biến chứng của chúng (lắng đọng lipid, sẹo) ảnh hưởng đến trục thị giác
- Đỏ mắt: Xung huyết kết mạc kèm theo bệnh nguyên nhân
- Không triệu chứng: Thường không có triệu chứng cơ năng nếu tổn thương không lan đến trục thị giác
Dấu hiệu lâm sàng (bác sĩ phát hiện khi khám)
Phần tiêu đề “Dấu hiệu lâm sàng (bác sĩ phát hiện khi khám)”- Hình thái mạch máu mới: Từ dạng lưới mảnh đến mạch hoạt động căng phồng và mạch trưởng thành mật độ cao
- Vị trí và độ sâu của mạch: Đánh giá nông hay sâu bằng phương pháp khe sáng và chiếu sáng gián tiếp trên đèn khe
- Mạch ma (ghost vessel): Mạch cũ đã ngừng lưu thông máu. Không cần điều trị
- Kết mạc hóa (conjunctivalization): Tình trạng mô kết mạc phủ lên giác mạc. Được phát hiện bằng nhuộm fluorescein chậm
- Bệnh lipid giác mạc (lipid keratopathy): Đục màu trắng vàng do lắng đọng lipid rò rỉ từ mạch máu mới vào nhu mô giác mạc
- Mất hàng rào Vogt (POV): Dấu hiệu quan trọng gợi ý mất tế bào gốc vùng rìa
3. Nguyên nhân và Yếu tố Nguy cơ
Phần tiêu đề “3. Nguyên nhân và Yếu tố Nguy cơ”Nhiễm trùng
Phần tiêu đề “Nhiễm trùng”- Virus Herpes Simplex (HSV-1): Nguyên nhân nhiễm trùng phổ biến nhất gây tân mạch giác mạc ở các nước phát triển 1). Herpes giác mạc mô đệm gây tân mạch sâu
- Viêm giác mạc do vi khuẩn: Trường hợp nặng, xâm nhập mạch máu kèm loét giác mạc và sẹo
- Viêm giác mạc do nấm: Trường hợp kéo dài có thể kèm tân mạch
- Mắt hột và Bệnh giun chỉ Onchocerca: Nguyên nhân nhiễm trùng chính ở các nước đang phát triển 1)
Thiếu oxy (Liên quan đến kính áp tròng)
Phần tiêu đề “Thiếu oxy (Liên quan đến kính áp tròng)”Nguyên nhân chính là đeo kính áp tròng mềm quá mức. Khoảng 80-90% người đeo kính áp tròng mềm HEMA truyền thống có xâm nhập mạch máu từ phía trên giác mạc (hướng 10-2 giờ). Nếu tổn thương biểu mô kéo dài hơn một tháng, mạch máu sẽ xâm nhập vào khu vực đó.
Chấn thương hóa chất
Phần tiêu đề “Chấn thương hóa chất”Chấn thương kiềm thấm sâu vào nhu mô giác mạc, gây tổn thương rộng tế bào gốc vùng rìa và tân mạch. Đây là một trong những nhóm có tỷ lệ thành công ghép giác mạc thấp đáng kể.
Suy giảm tế bào gốc vùng rìa (LSCD)
Phần tiêu đề “Suy giảm tế bào gốc vùng rìa (LSCD)”LSCD là một trong những con đường chính của tân mạch giác mạc 1)3). Khi tế bào gốc vùng rìa bị rối loạn chức năng do bẩm sinh, chấn thương hóa chất, đeo kính áp tròng quá mức, bệnh viêm hệ thống hoặc do điều trị, hàng rào biểu mô bình thường bị mất và xảy ra xâm nhập mạch máu 3). Trường hợp nhẹ, thấy bệnh biểu mô xoắn ốc khi nhuộm fluorescein, trường hợp trung bình xuất hiện tân mạch nông và màng máu 3).
Nguyên nhân khác
Phần tiêu đề “Nguyên nhân khác”- Bệnh viêm: SJS/TEN, pemphigoid mắt, viêm kết mạc mùa xuân, viêm giác mạc do rosacea
- Sau ghép giác mạc: Tân mạch liên quan đến phản ứng thải ghép 1)
- Bệnh thoái hóa: Thoái hóa rìa giác mạc Terrien, loạn dưỡng giác mạc dạng giọt keo
Có, thường có thể phòng ngừa được. Một trong những nguyên nhân chính gây tân mạch giác mạc là thiếu oxy do kính áp tròng. Nguy cơ có thể giảm đáng kể bằng cách tuân thủ thời gian đeo, sử dụng kính có tính thấm oxy cao và khám mắt định kỳ.
4. Chẩn đoán và Phương pháp Xét nghiệm
Phần tiêu đề “4. Chẩn đoán và Phương pháp Xét nghiệm”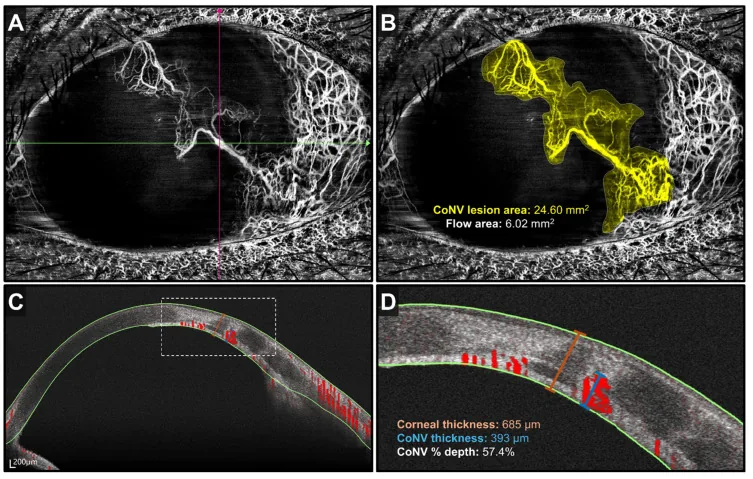
Khám bằng đèn khe
Phần tiêu đề “Khám bằng đèn khe”Đây là xét nghiệm cơ bản nhất trong chẩn đoán tân mạch giác mạc. Đánh giá vị trí của mạch máu (góc phần tư), độ sâu (nông/sâu), hoạt tính (có dòng chảy hay không) và sự xâm lấn kết mạc.
- Phương pháp khuếch tán: Sử dụng chùm sáng rộng hoặc qua đĩa khuếch tán, các mạch máu mới dễ phân biệt hơn
- Phương pháp chiếu sáng gián tiếp: Sử dụng ánh sáng phản xạ từ mống mắt hoặc thủy tinh thể, quan sát các mạch máu mới và dây thần kinh giác mạc
- Nhuộm fluorescein: Hữu ích để đánh giá sự hiện diện của khuyết tật biểu mô và xâm lấn kết mạc
Chụp mạch huỳnh quang
Phần tiêu đề “Chụp mạch huỳnh quang”- Chụp mạch huỳnh quang fluorescein (FA): Đánh giá chức năng tưới máu và rò rỉ mạch máu, phân biệt mạch hoạt động và mạch trưởng thành1)
- Chụp mạch xanh indocyanine (ICGA): Xuất sắc trong việc hiển thị mạch sâu và mạch hướng tâm, hữu ích cho việc nhắm mục tiêu tắc mạch1)
Chẩn đoán hình ảnh
Phần tiêu đề “Chẩn đoán hình ảnh”- OCT/OCT-A đoạn trước: Có thể đánh giá định lượng độ sâu và phạm vi của mạng lưới mạch máu giác mạc một cách không xâm lấn1)
- Kính hiển vi đồng tiêu in vivo (IVCM): Có thể định lượng tế bào đáy biểu mô trong chẩn đoán LSCD3)
| Phương pháp kiểm tra | Các mục đánh giá chính | Đặc điểm |
|---|---|---|
| Đèn khe | Vị trí, độ sâu, hoạt động | Kiểm tra cơ bản đầu tay |
| FA / ICGA | Tưới máu, rò rỉ, mạch hướng tâm | Hữu ích cho lập kế hoạch điều trị |
| AS-OCT / OCT-A | Đánh giá độ sâu và định lượng | Không xâm lấn |
5. Phương pháp điều trị tiêu chuẩn
Phần tiêu đề “5. Phương pháp điều trị tiêu chuẩn”Điều trị tân mạch giác mạc dựa trên hai trụ cột chính: điều trị nguyên nhân và can thiệp vào chính các mạch máu mới2).
Điều trị nguyên nhân
Phần tiêu đề “Điều trị nguyên nhân”- Ngừng đeo kính áp tròng: Nếu do thiếu oxy, ngừng đeo và cân nhắc chuyển sang loại kính có tính thấm oxy cao. Phân biệt giữa mạch hoạt động và mạch cũ (mạch ma).
- Điều trị nhiễm trùng: Dùng kháng sinh, kháng virus hoặc kháng nấm cho viêm giác mạc nhiễm trùng nguyên nhân.
- Điều trị LSCD: Phẫu thuật như ghép vùng rìa hoặc ghép màng ối.
Điều trị bằng thuốc
Phần tiêu đề “Điều trị bằng thuốc”- Thuốc nhỏ mắt steroid: Ức chế tân mạch bằng cách ức chế cytokine viêm (IL-1, IL-6), gây apoptosis tế bào lympho và ức chế giãn mạch2). Là lựa chọn đầu tay, nhưng sử dụng lâu dài cần chú ý glôcôm do steroid và tăng tính nhạy cảm với nhiễm trùng.
- Liệu pháp kháng VEGF: Bevacizumab (nhỏ mắt, tiêm dưới kết mạc hoặc tiêm nội mô) được sử dụng rộng rãi1)2). Hiệu quả với mạch hoạt động chưa trưởng thành, nhưng hiệu quả hạn chế với mạch trưởng thành (được bao phủ bởi tế bào quanh mạch)1). Vì sự bao phủ của tế bào quanh mạch đạt 80% trong vòng 2 tuần sau khi khởi phát tân mạch, điều trị sớm rất quan trọng1).
- Thuốc ức chế miễn dịch: Thuốc nhỏ mắt cyclosporin A ức chế hoạt hóa tế bào T và có tác dụng tiết kiệm steroid2). Tacrolimus và sirolimus (chất ức chế mTOR) cũng là lựa chọn1).
- Doxycycline: Ức chế tân mạch giác mạc thông qua tác dụng ức chế pemphigoid niêm mạc2).
Phẫu thuật và can thiệp thủ thuật
Phần tiêu đề “Phẫu thuật và can thiệp thủ thuật”- Quang đông laser: Các mạch máu được đông và tắc bằng laser argon hoặc Nd:YAG. Được sử dụng như một biện pháp chuẩn bị trước khi ghép giác mạc và điều trị bệnh lipid giác mạc. Có nguy cơ chảy máu và mỏng giác mạc, thường thấy tái thông mạch và hình thành shunt mạch.
- Diathermy kim nhỏ (FND): Một kim nhỏ được đưa vào các mạch dinh dưỡng của vùng rìa và được đông điện để gây tắc. Hiệu quả ngay cả với các mạch dày trưởng thành, và được thực hiện trên các mạch đến khó tắc bằng laser argon1).
- Liệu pháp quang động (PDT): Sau khi tiêm chất nhạy sáng vào mạch máu, chiếu sáng tạo ra các gốc oxy hoạt động phá hủy thành mạch. Có tính đặc hiệu cao nhưng tốn kém và mất thời gian.
- MICE (Thuyên tắc hóa học nội mạch bằng mitomycin C): Mitomycin C (0,4 mg/mL) được tiêm trực tiếp vào các mạch dinh dưỡng bằng kim 33G6). Đã có báo cáo về sự hình thành mạch ma và cải thiện bệnh lipid giác mạc trong tân mạch giác mạc kháng trị với điều trị thông thường6).
6. Sinh lý bệnh và cơ chế phát sinh chi tiết
Phần tiêu đề “6. Sinh lý bệnh và cơ chế phát sinh chi tiết”Cơ chế duy trì đặc quyền vô mạch (CAP)
Phần tiêu đề “Cơ chế duy trì đặc quyền vô mạch (CAP)”Trạng thái vô mạch của giác mạc được duy trì bởi sự phối hợp của nhiều cơ chế ức chế tân mạch1).
- Thụ thể VEGF hòa tan loại 1 (sVEGFR1): Được sản xuất liên tục bởi biểu mô và nhu mô giác mạc. Bẫy VEGF-A với ái lực cao, ức chế cạnh tranh liên kết với thụ thể gắn màng, là bẫy VEGF nội sinh1).
- Thrombospondin (TSP-1/TSP-2): Glycoprotein ức chế tân mạch được biểu hiện liên tục trong chất nền ngoại bào giác mạc. Cô lập VEGF và ức chế tín hiệu VEGFR2. Gây apoptosis tế bào nội mô mạch máu qua CD36/CD471).
- Endostatin: Mảnh đầu C của collagen XVIII. Ức chế các con đường VEGF và bFGF, thúc đẩy apoptosis tế bào nội mô mạch máu qua hoạt hóa caspase-3. Cũng ức chế tạo mạch bạch huyết1).
- Rào cản vật lý: Rào cản vùng rìa, sự sắp xếp collagen dày đặc và môi trường tương đối lạnh của giác mạc hạn chế sự xâm nhập của mạch máu1)
Yếu tố thúc đẩy tân mạch và con đường bệnh sinh
Phần tiêu đề “Yếu tố thúc đẩy tân mạch và con đường bệnh sinh”Sự phá vỡ CAP xảy ra chủ yếu qua hai con đường1)2).
Con đường 1: Tăng sản xuất yếu tố thúc đẩy do viêm và thiếu oxy
Tổn thương giác mạc dẫn đến giải phóng ba yếu tố tân mạch chính từ đại thực bào, tế bào biểu mô và tế bào nội mô1).
- VEGF-A: Thông qua VEGFR-2, thúc đẩy tăng sinh và di chuyển của VEC, cảm ứng MMP-2/MMP-9 để tái tạo ECM1). Là yếu tố thúc đẩy quan trọng nhất trong tân mạch giác mạc
- bFGF (FGF-2): Thông qua con đường ERK/PI3K, làm tăng sản xuất VEGF và phá vỡ liên kết VE-cadherin để thúc đẩy sự nảy mầm của VEC1)
- PDGF: Tuyển dụng tế bào quanh mạch và tế bào cơ trơn, ổn định mạch máu mới1). Sự trưởng thành mạch máu do PDGF gây ra kháng trị liệu kháng VEGF
Con đường 2: Suy giảm tế bào gốc vùng rìa (LSCD)
Mất tế bào gốc vùng rìa dẫn đến mất chức năng hàng rào bình thường của biểu mô giác mạc, và sự xâm nhập của mô kết mạc cùng viêm nhiễm dai dẳng duy trì tân mạch1)3).
Liên quan đến tạo mạch bạch huyết
Phần tiêu đề “Liên quan đến tạo mạch bạch huyết”Tân mạch giác mạc (tạo mạch máu) và tạo mạch bạch huyết là các quá trình liên quan nhưng độc lập4). Mạch máu hoạt động như đường dẫn ly tâm cho các tế bào hiệu ứng miễn dịch, trong khi mạch bạch huyết hoạt động như đường dẫn hướng tâm cho các tế bào trình diện kháng nguyên4). Sự tiến triển của cả hai đều liên quan đến mất đặc quyền miễn dịch và thải ghép trong ghép giác mạc4). VEGF-A/VEGFR-2 thúc đẩy tạo mạch máu, trong khi VEGF-C,D/VEGFR-3 thúc đẩy tạo mạch bạch huyết4).
7. Nghiên cứu mới nhất và triển vọng tương lai
Phần tiêu đề “7. Nghiên cứu mới nhất và triển vọng tương lai”Liệu pháp gen bằng vector AAV
Phần tiêu đề “Liệu pháp gen bằng vector AAV”Xie và cộng sự (2024) đã tổng quan về điều trị tân mạch giác mạc bằng vector virus liên quan đến adeno (AAV) để biểu hiện liên tục yếu tố kháng VEGF5). AAV2 và AAV8 là hiệu quả nhất trong việc chuyển nạp tế bào mô đệm giác mạc, và tiêm trong nhu mô giác mạc được coi là đường dùng hiệu quả nhất5). Liệu pháp gen AAV có thể mang lại hiệu quả kháng VEGF lâu dài với một liều duy nhất, nhưng hiện tại vẫn ở giai đoạn tiền lâm sàng5).
Phương pháp tắc mạch hóa chất nội mạch MMC (MICE)
Phần tiêu đề “Phương pháp tắc mạch hóa chất nội mạch MMC (MICE)”Addeen và cộng sự (2023) đã báo cáo hai trường hợp MICE (tiêm nội mạch MMC 0,4 mg/mL bằng kim 33-gauge) cho tân mạch kháng trị sau ghép giác mạc 6). Hiện tượng mạch máu mờ dần được quan sát thấy sớm sau phẫu thuật, giảm đau và cải thiện chất lượng cuộc sống 6). Không có tác dụng phụ nào được ghi nhận, nhưng cần xác nhận tính an toàn lâu dài.
Oligonucleotide antisense (Aganirsen)
Phần tiêu đề “Oligonucleotide antisense (Aganirsen)”Trong bài tổng quan của Muller và cộng sự (2026), đã báo cáo rằng Aganirsen, một oligonucleotide antisense nhắm mục tiêu IRS-1, cho thấy sự thoái lui và thuyên giảm tân mạch giác mạc trong các mô hình tiền lâm sàng 1). Chỉnh sửa VEGF-A bằng CRISPR/Cas9 cũng cho thấy dữ liệu tiền lâm sàng đầy hứa hẹn 1).
Hệ thống nano nhãn khoa
Phần tiêu đề “Hệ thống nano nhãn khoa”Zhang và cộng sự (2022) đã báo cáo rằng các chất mang nano như hạt nano, liposome và micelle có thể cải thiện hiệu quả phân phối thuốc kháng VEGF và steroid vào giác mạc, cho phép giải phóng kéo dài, nhắm đích và giảm kích ứng 7). Ứng dụng lâm sàng vẫn còn hạn chế, nhưng hy vọng sẽ giảm gánh nặng tiêm thuốc nhiều lần.
Tầm quan trọng của liệu pháp kết hợp
Phần tiêu đề “Tầm quan trọng của liệu pháp kết hợp”Vì tân mạch giác mạc là một bệnh lý đa yếu tố, đơn trị liệu thường không đạt hiệu quả đầy đủ 1)2). Liệu pháp kết hợp nhắm vào nhiều con đường như VEGF, bFGF, PDGF và tạo mạch bạch huyết có thể trở thành trọng tâm của các chiến lược điều trị trong tương lai 1).
8. Tài liệu tham khảo
Phần tiêu đề “8. Tài liệu tham khảo”- Muller E, Feinberg L, Woronkowicz M, Roberts HW. Corneal Neovascularization: Pathogenesis, Current Insights and Future Strategies. Biology. 2026;15(2):136.
- Wu D, Chan KE, Lim BXH, et al. Management of corneal neovascularization: Current and emerging therapeutic approaches. Indian J Ophthalmol. 2024;72(Suppl 3):S354-S371.
- Drzyzga L, Spiewak D, Dorecka M, Wygledowska-Promienska D. Available Therapeutic Options for Corneal Neovascularization: A Review. Int J Mol Sci. 2024;25(10):5479.
- Zhang Z, Zhao R, Wu X, Ma Y, He Y. Research progress on the correlation between corneal neovascularization and lymphangiogenesis. Mol Med Rep. 2025;31(2):47.
- Xie M, Wang L, Deng Y, et al. Sustained and Efficient Delivery of Antivascular Endothelial Growth Factor by AAV for Treatment of Corneal Neovascularization. J Ophthalmol. 2024;2024:5487973.
- Addeen SZ, Oyoun Z, Alfhaily H, Anbari A. Outcomes of mitomycin C intravascular chemoembolization (MICE) in refractory corneal neovascularization after failed keratoplasty. Digit J Ophthalmol. 2023;29(4).
- Zhang C, Yin Y, Zhao J, et al. An Update on Novel Ocular Nanosystems with Possible Benefits in the Treatment of Corneal Neovascularization. Int J Nanomedicine. 2022;17:4911-4931.
