Neovascularização superficial

Neovascularização Corneana (Corneal Neovascularization)
1. O que é neovascularização corneana?
Seção intitulada “1. O que é neovascularização corneana?”A neovascularização corneana (CoNV) é uma condição na quais novos capilares do plexo vascular limbar invadem o tecido corneano normalmente avascular1). Não é uma doença específica, mas uma reação inespecífica a várias condições como infecção, inflamação, hipóxia e trauma.
A córnea mantém um “privilégio angiogênico corneano (CAP)”, onde o estado avascular é mantido por um equilíbrio preciso entre fatores inibidores e pró-angiogênicos1). Quando esse equilíbrio é rompido, as células endoteliais vasculares proliferam, migram e invadem o estroma corneano.
Os novos vasos são classificados em dois tipos de acordo com a localização anatômica.
Neovascularização profunda
Invadem das artérias ciliares anteriores para dentro do estroma corneano.
Ocorre devido a ceratite intersticial (sífilis, tuberculose), ceratite herpética intersticial, ceratite bolhosa e outras inflamações/edemas persistentes.
Os vasos sanguíneos novos imaturos causam extravasamento lipídico, inflamação persistente e cicatrização 1). Com a progressão, os vasos amadurecem e são revestidos por pericitos, tornando-se resistentes à terapia anti-VEGF 1). Em pacientes pós-transplante de córnea, os novos vasos são um fator de risco para rejeição.
Se não tratada, os novos vasos amadurecem e tornam-se difíceis de regredir espontaneamente, causando lipidose corneana (depósito lipídico na córnea) e cicatriz corneana, resultando em perda permanente da visão. Além disso, se um transplante de córnea for necessário, a presença de novos vasos aumenta o risco de rejeição do enxerto. A consulta precoce e o tratamento da causa são importantes.
2. Principais sintomas e achados clínicos
Seção intitulada “2. Principais sintomas e achados clínicos”Sintomas subjetivos
Seção intitulada “Sintomas subjetivos”- Baixa acuidade visual: Ocorre quando os novos vasos ou suas complicações (depósito lipídico, cicatriz) afetam o eixo visual
- Hiperemia conjuntival: Vermelhidão ocular associada à doença de base
- Assintomático: Frequentemente sem sintomas subjetivos se a lesão não atingir o eixo visual
Achados clínicos (observados pelo médico ao exame)
Seção intitulada “Achados clínicos (observados pelo médico ao exame)”- Morfologia dos novos vasos: Variando de padrão reticular fino a vasos ativos ingurgitados e vasos maduros de alta densidade
- Localização e profundidade dos vasos: Avaliação se superficiais ou profundos usando o método de fenda e iluminação indireta na lâmpada de fenda
- Vaso fantasma (ghost vessel): Vaso antigo com fluxo sanguíneo interrompido. Não necessita tratamento
- Conjuntivalização: Condição em que o tecido conjuntival cobre a córnea. Detectada por coloração tardia com fluoresceína
- Lipidose corneana (lipid keratopathy): Opacidade amarelo-esbranquiçada devido ao depósito de lipídios extravasados dos novos vasos no estroma corneano
- Desaparecimento das paliçadas de Vogt (POV): Sinal importante que sugere perda de células-tronco do limbo
3. Causas e Fatores de Risco
Seção intitulada “3. Causas e Fatores de Risco”Infecções
Seção intitulada “Infecções”- Vírus Herpes Simples (HSV-1): Causa infecciosa mais comum de neovascularização corneana em países desenvolvidos 1). Herpes estromal causa neovascularização profunda
- Ceratite Bacteriana: Em casos graves, ocorre invasão vascular com úlcera de córnea e cicatriz
- Ceratite Fúngica: Em casos prolongados, pode haver neovascularização
- Tracoma e Oncocercose: Principais causas infecciosas em países em desenvolvimento 1)
Hipóxia (Relacionada a Lentes de Contato)
Seção intitulada “Hipóxia (Relacionada a Lentes de Contato)”A causa principal é o uso excessivo de lentes de contato gelatinosas. Cerca de 80-90% dos usuários de lentes de contato gelatinosas HEMA convencionais apresentam invasão vascular da parte superior da córnea (direção 10-2 horas). Se a lesão epitelial persistir por mais de um mês, os vasos sanguíneos invadem a área.
Trauma Químico
Seção intitulada “Trauma Químico”O trauma alcalino penetra profundamente no estroma corneano, causando dano extenso às células-tronco limbais e neovascularização. É um dos grupos com taxa de sucesso de transplante de córnea significativamente baixa.
Deficiência de Células-Tronco Limbais (LSCD)
Seção intitulada “Deficiência de Células-Tronco Limbais (LSCD)”A LSCD é uma das principais vias de neovascularização corneana 1)3). Quando as células-tronco limbais se tornam disfuncionais devido a causas congênitas, trauma químico, uso excessivo de lentes de contato, doenças inflamatórias sistêmicas ou iatrogênicas, a barreira epitelial normal é perdida e ocorre invasão vascular 3). Em casos leves, observa-se epiteliopatia espiralada com coloração por fluoresceína, e em casos moderados, surgem neovascularização superficial e pannus 3).
Outras Causas
Seção intitulada “Outras Causas”- Doenças Inflamatórias: SJS/NET, penfigoide ocular, conjuntivite vernal, ceratite rosácea
- Pós-Transplante de Córnea: Neovascularização associada à rejeição 1)
- Doenças degenerativas: Degeneração marginal de Terrien, distrofia corneana gelatinosa em gotas
Sim, muitas vezes pode ser prevenida. Uma das principais causas da neovascularização corneana é a falta de oxigênio devido às lentes de contato. O risco pode ser significativamente reduzido respeitando o tempo de uso, utilizando lentes de alta permeabilidade ao oxigênio e realizando exames oftalmológicos regulares.
4. Diagnóstico e Métodos de Exame
Seção intitulada “4. Diagnóstico e Métodos de Exame”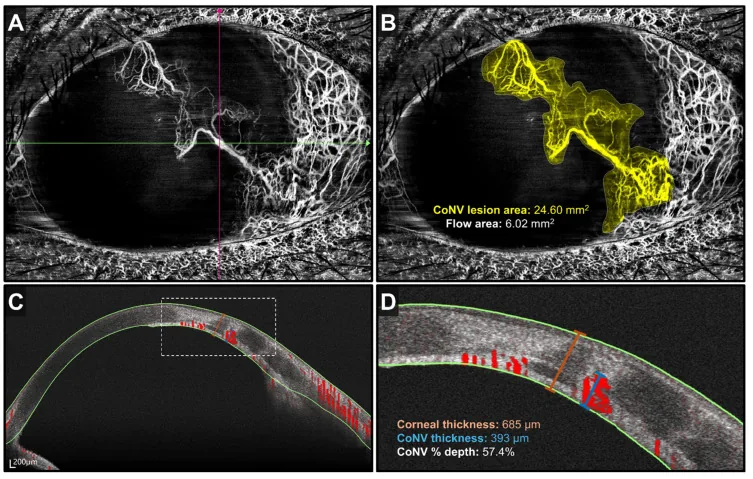
Exame com Lâmpada de Fenda
Seção intitulada “Exame com Lâmpada de Fenda”Este é o exame mais básico no diagnóstico da neovascularização corneana. Avalia-se a localização dos vasos (quadrante), profundidade (superficial/profunda), atividade (presença de fluxo sanguíneo) e invasão conjuntival.
- Método do difusor: Usando um feixe de luz largo ou através de um disco difusor, os novos vasos são mais facilmente distinguidos
- Método de iluminação indireta: Usando a luz refletida da íris ou do cristalino, observam-se os novos vasos e os nervos corneanos
- Coloração com fluoresceína: Útil para avaliar a presença de defeitos epiteliais e invasão conjuntival
Angiografia fluoresceínica
Seção intitulada “Angiografia fluoresceínica”- Angiografia fluoresceínica (FA): Avalia funcionalmente a perfusão e o extravasamento vascular, diferenciando vasos ativos de maduros1)
- Angiografia com verde de indocianina (ICGA): Excelente para visualizar vasos profundos e aferentes, útil para direcionamento de oclusão vascular1)
Exames de imagem
Seção intitulada “Exames de imagem”- OCT/OCT-A de segmento anterior: Pode avaliar quantitativamente a profundidade e extensão da rede vascular corneana de forma não invasiva1)
- Microscopia confocal in vivo (IVCM): Permite a quantificação de células basais epiteliais no diagnóstico de LSCD3)
| Método de exame | Principais itens avaliados | Características |
|---|---|---|
| Lâmpada de fenda | Localização, profundidade, atividade | Exame básico de primeira linha |
| FA / ICGA | Perfusão, extravasamento, vasos aferentes | Útil para planejamento terapêutico |
| AS-OCT / OCT-A | Avaliação de profundidade e quantitativa | Não invasivo |
5. Tratamento Padrão
Seção intitulada “5. Tratamento Padrão”O tratamento da neovascularização corneana baseia-se em dois pilares: tratamento da causa e intervenção nos próprios vasos neoformados2).
Tratamento da Causa
Seção intitulada “Tratamento da Causa”- Suspensão do uso de lentes de contato: Se for hipóxico, suspender o uso e considerar a troca para lentes de alta permeabilidade ao oxigênio. Distinguir entre vasos ativos e antigos (vasos fantasmas).
- Tratamento da infecção: Administração de antibióticos, antivirais ou antifúngicos para ceratite infecciosa causadora.
- Tratamento da LSCD: Cirurgia como transplante de limbo ou transplante de membrana amniótica.
Terapia Medicamentosa
Seção intitulada “Terapia Medicamentosa”- Colírio de corticosteroide: Suprime a neovascularização ao inibir citocinas inflamatórias (IL-1, IL-6), induzir apoptose de linfócitos e inibir vasodilatação2). É a primeira escolha, mas o uso prolongado requer atenção ao glaucoma esteroidal e aumento da suscetibilidade a infecções.
- Terapia anti-VEGF: Bevacizumabe (colírio, injeção subconjuntival ou intrastromal) é amplamente utilizado1)2). Eficaz contra vasos ativos imaturos, mas efeito limitado em vasos maduros (revestidos por pericitos)1). Como o revestimento por pericitos atinge 80% em 2 semanas após o início da neovascularização, o tratamento precoce é importante1).
- Imunossupressores: Colírio de ciclosporina A inibe a ativação de células T e tem efeito poupador de esteroides2). Tacrolimo e sirolimo (inibidor de mTOR) também são opções1).
- Doxiciclina: Inibe a neovascularização corneana por meio do efeito inibidor do penfigoide mucoso2).
Tratamento Cirúrgico e Procedimental
Seção intitulada “Tratamento Cirúrgico e Procedimental”- Fotocoagulação a laser: Os vasos sanguíneos são coagulados e ocluídos com laser de argônio ou Nd:YAG. Usado como preparação antes do transplante de córnea e para tratamento de lipidose corneana. Há risco de hemorragia e afinamento da córnea, e frequentemente ocorre recanalização vascular e formação de shunts.
- Diatermia por agulha fina (FND): Uma agulha fina é inserida nos vasos nutridores do limbo e coagulada eletricamente para oclusão. Eficaz mesmo em vasos espessos maduros, e é realizada em vasos aferentes difíceis de ocluir com laser de argônio1).
- Terapia fotodinâmica (PDT): Após injeção de substância fotossensível nos vasos, a irradiação luminosa gera espécies reativas de oxigênio que destroem a parede vascular. Possui alta especificidade, mas é cara e demorada.
- MICE (Quimioembolização intravascular com mitomicina C): Mitomicina C (0,4 mg/mL) é injetada diretamente nos vasos nutridores usando agulha 33G6). Foi relatada a formação de vasos fantasmas e melhora da lipidose corneana em neovascularização corneana refratária ao tratamento convencional6).
6. Fisiopatologia e mecanismo detalhado de ocorrência
Seção intitulada “6. Fisiopatologia e mecanismo detalhado de ocorrência”Mecanismos de manutenção do privilégio avascular (CAP)
Seção intitulada “Mecanismos de manutenção do privilégio avascular (CAP)”O estado avascular da córnea é mantido pela coordenação de múltiplos mecanismos inibidores da angiogênese1).
- Receptor solúvel de VEGF tipo 1 (sVEGFR1): Produzido constitutivamente pelo epitélio e estroma corneano. Captura VEGF-A com alta afinidade, inibindo competitivamente sua ligação aos receptores de membrana, sendo uma armadilha endógena de VEGF1).
- Trombospondina (TSP-1/TSP-2): Glicoproteína inibidora da angiogênese expressa constitutivamente na matriz extracelular da córnea. Sequestra VEGF e suprime a sinalização de VEGFR2. Induz apoptose de células endoteliais vasculares via CD36/CD471).
- Endostatina: Fragmento C-terminal do colágeno XVIII. Inibe as vias de VEGF e bFGF, promovendo apoptose de células endoteliais vasculares via ativação da caspase-3. Também inibe a linfangiogênese1).
- Barreira física: A barreira do limbo, o arranjo denso de colágeno e o ambiente relativamente frio da córnea limitam a invasão vascular1)
Fatores pró-angiogênicos e vias de patogênese
Seção intitulada “Fatores pró-angiogênicos e vias de patogênese”A ruptura do CAP ocorre principalmente por duas vias1)2).
Via 1: Aumento da produção de fatores pró-angiogênicos por inflamação e hipóxia
A lesão da córnea leva à liberação de três fatores angiogênicos principais de macrófagos, células epiteliais e células endoteliais1).
- VEGF-A: Através do VEGFR-2, promove proliferação e migração de VEC, induz MMP-2/MMP-9 para remodelamento da ECM1). É o fator pró-angiogênico mais importante na neovascularização da córnea
- bFGF (FGF-2): Através da via ERK/PI3K, aumenta a produção de VEGF e dissocia as junções de VE-caderina para promover a brotação de VEC1)
- PDGF: Recruta pericitos e células musculares lisas, estabilizando novos vasos1). A maturação vascular mediada por PDGF confere resistência à terapia anti-VEGF
Via 2: Deficiência de células-tronco do limbo (LSCD)
A perda de células-tronco do limbo leva à perda da função de barreira normal do epitélio corneano, e a invasão do tecido conjuntival e a inflamação persistente mantêm a neovascularização1)3).
Relação com a linfangiogênese
Seção intitulada “Relação com a linfangiogênese”A neovascularização da córnea (angiogênese) e a linfangiogênese são processos inter-relacionados, porém independentes4). Os vasos sanguíneos funcionam como via eferente para células efetoras imunes, enquanto os vasos linfáticos funcionam como via aferente para células apresentadoras de antígeno4). O progresso de ambos está envolvido na perda do privilégio imunológico e na rejeição do enxerto no transplante de córnea4). VEGF-A/VEGFR-2 impulsiona a angiogênese, enquanto VEGF-C,D/VEGFR-3 impulsiona a linfangiogênese4).
7. Pesquisas recentes e perspectivas futuras
Seção intitulada “7. Pesquisas recentes e perspectivas futuras”Terapia gênica com vetor AAV
Seção intitulada “Terapia gênica com vetor AAV”Xie et al. (2024) revisaram a terapia da neovascularização da córnea usando vetor de vírus adeno-associado (AAV) para expressão sustentada de fator anti-VEGF5). AAV2 e AAV8 são os mais eficientes para transdução de células do estroma corneano, e a injeção intraestromal é considerada a via de administração mais eficaz5). A terapia gênica com AAV pode proporcionar efeito anti-VEGF de longa duração com dose única, mas atualmente ainda está em estágio pré-clínico5).
Quimioembolização Intravascular com MMC (MICE)
Seção intitulada “Quimioembolização Intravascular com MMC (MICE)”Addeen et al. (2023) relataram dois casos de MICE (injeção intravascular de MMC 0,4 mg/mL com agulha 33-gauge) para neovascularização refratária após transplante de córnea 6). O fantasma vascular foi observado precocemente no pós-operatório, com redução da dor e melhora da qualidade de vida 6). Nenhum evento adverso foi observado, mas a segurança a longo prazo precisa ser confirmada.
Oligonucleotídeo Antissenso (Aganirsen)
Seção intitulada “Oligonucleotídeo Antissenso (Aganirsen)”Na revisão de Muller et al. (2026), foi relatado que o Aganirsen, um oligonucleotídeo antissenso direcionado ao IRS-1, mostrou regressão e remissão da neovascularização da córnea em modelos pré-clínicos 1). A edição de VEGF-A com CRISPR/Cas9 também mostrou dados pré-clínicos promissores 1).
Nanossistemas Oftálmicos
Seção intitulada “Nanossistemas Oftálmicos”Zhang et al. (2022) relataram que nanocarreadores como nanopartículas, lipossomas e micelas podem melhorar a eficiência da entrega de drogas anti-VEGF e esteroides na córnea, permitindo liberação sustentada, direcionamento e baixa irritação 7). A aplicação clínica ainda é limitada, mas espera-se reduzir o ônus das administrações frequentes.
Importância da Terapia Combinada
Seção intitulada “Importância da Terapia Combinada”Como a neovascularização da córnea é uma condição multifatorial, a monoterapia muitas vezes não é suficientemente eficaz 1)2). A terapia combinada visando múltiplas vias como VEGF, bFGF, PDGF e linfangiogênese pode se tornar o centro das estratégias de tratamento futuras 1).
8. Referências
Seção intitulada “8. Referências”- Muller E, Feinberg L, Woronkowicz M, Roberts HW. Corneal Neovascularization: Pathogenesis, Current Insights and Future Strategies. Biology. 2026;15(2):136.
- Wu D, Chan KE, Lim BXH, et al. Management of corneal neovascularization: Current and emerging therapeutic approaches. Indian J Ophthalmol. 2024;72(Suppl 3):S354-S371.
- Drzyzga L, Spiewak D, Dorecka M, Wygledowska-Promienska D. Available Therapeutic Options for Corneal Neovascularization: A Review. Int J Mol Sci. 2024;25(10):5479.
- Zhang Z, Zhao R, Wu X, Ma Y, He Y. Research progress on the correlation between corneal neovascularization and lymphangiogenesis. Mol Med Rep. 2025;31(2):47.
- Xie M, Wang L, Deng Y, et al. Sustained and Efficient Delivery of Antivascular Endothelial Growth Factor by AAV for Treatment of Corneal Neovascularization. J Ophthalmol. 2024;2024:5487973.
- Addeen SZ, Oyoun Z, Alfhaily H, Anbari A. Outcomes of mitomycin C intravascular chemoembolization (MICE) in refractory corneal neovascularization after failed keratoplasty. Digit J Ophthalmol. 2023;29(4).
- Zhang C, Yin Y, Zhao J, et al. An Update on Novel Ocular Nanosystems with Possible Benefits in the Treatment of Corneal Neovascularization. Int J Nanomedicine. 2022;17:4911-4931.
