표층성 혈관신생

각막 신생혈관 (Corneal Neovascularization)
1. 각막 신생혈관이란
섹션 제목: “1. 각막 신생혈관이란”각막 신생혈관(corneal neovascularization; CoNV)은 원래 무혈관인 각막 조직에 윤부 혈관총에서 새로운 모세혈관이 침입하는 병태입니다1). 특정 질환명이 아니라 감염·염증·저산소·외상 등 다양한 병태에 대한 비특이적 반응으로 발생합니다.
각막은 ‘혈관신생 특권(corneal angiogenic privilege; CAP)‘을 유지하고 있으며, 혈관신생 억제인자와 촉진인자의 정밀한 균형에 의해 무혈관 상태가 유지됩니다1). 이 균형이 깨지면 혈관내피세포가 증식·이주하여 각막 실질에 침입합니다.
신생혈관은 해부학적 위치에 따라 2가지 유형으로 분류됩니다.
심층성 혈관 신생
전모양체동맥에서 각막 실질 내로 침입합니다.
각막 실질염(매독·결핵), 실질형 헤르페스 각막염, 수포성 각막증 등의 지속적인 염증·부종으로 발생합니다.
미성숙한 신생혈관은 지질 삼출·지속적 염증·반흔화를 유발합니다1). 진행되면 혈관이 성숙하여 주피세포(pericyte)로 덮이게 되고 항VEGF 요법에 내성을 보이게 됩니다1). 각막 이식 후 환자에서는 신생혈관이 거부 반응의 위험 인자가 됩니다.
방치하면 신생혈관이 성숙하여 자연 퇴축이 어려워지고, 지질 각막증(각막 내 지질 침착)이나 각막 반흔을 일으켜 영구적인 시력 저하의 원인이 됩니다. 또한 각막 이식이 필요할 경우 신생혈관의 존재는 이식편 거부 반응 위험을 높입니다. 조기 진료와 원인 치료가 중요합니다.
2. 주요 증상과 임상 소견
섹션 제목: “2. 주요 증상과 임상 소견”자각 증상
섹션 제목: “자각 증상”- 시력 저하: 신생혈관이나 그 합병증(지질 침착, 반흔)이 시축에 걸린 경우 발생
- 충혈: 원인 질환에 따른 결막 충혈
- 무증상:시축에 병변이 미치지 않는 경우 자각 증상이 없는 경우가 많습니다
임상 소견(의사가 진찰 시 확인하는 소견)
섹션 제목: “임상 소견(의사가 진찰 시 확인하는 소견)”- 신생혈관의 형태:미세한 망상 패턴부터 확장된 활동성 혈관, 성숙한 고밀도 혈관까지 다양합니다
- 혈관의 위치와 깊이:표층성인지 심층성인지를 세극등현미경의 슬릿법·간접조명법으로 평가합니다
- ghost vessel: 혈류가 끊긴 오래된 혈관. 치료는 필요하지 않음
- 결막 침입(conjunctivalization): 각막 위에 결막 조직이 덮인 상태. 플루오레세인 염색의 지연 염색(delayed staining)으로 확인됨
- 지질 각막증(lipid keratopathy): 신생혈관에서 누출된 지질이 각막 실질에 침착된 황백색 혼탁
- Vogt 각막 윤부 울타리(POV) 소실: 윤부 줄기세포 소실을 시사하는 중요한 소견
3. 원인과 위험 요인
섹션 제목: “3. 원인과 위험 요인”감염증
섹션 제목: “감염증”- 단순 헤르페스 바이러스(HSV-1) : 선진국에서 각막 신생혈관의 가장 흔한 감염성 원인1). 실질형 각막 헤르페스에서는 심층성 혈관 신생이 발생함
- 세균성 각막염 : 중증 사례에서는 각막 궤양과 반흔에 동반하여 혈관 침입이 발생함
- 진균성 각막염: 치료가 지연된 경우 신생혈관을 동반할 수 있음
- 트라코마·온코세르카증: 개발도상국에서 주요 감염성 원인1)
저산소증 (콘택트렌즈 관련)
섹션 제목: “저산소증 (콘택트렌즈 관련)”소프트콘택트렌즈의 부적절한 착용(과다 착용)이 주요 원인이다. 기존 HEMA 재질 SCL 착용자의 약 8090%에서 각막 상방(10시2시 방향)에서 혈관 침입이 관찰된다. 상피 장애가 1개월 이상 지속되면 해당 부위에 혈관이 침입한다.
화학적 외상
섹션 제목: “화학적 외상”알칼리 외상은 각막 실질 깊숙이 침투하여 광범위한 윤부 줄기세포 장애와 신생혈관을 유발합니다. 각막 이식 성공률이 현저히 낮은 군 중 하나입니다.
윤부 줄기세포 결핍증(LSCD)
섹션 제목: “윤부 줄기세포 결핍증(LSCD)”LSCD는 각막 신생혈관의 주요 경로 중 하나입니다1)3). 선천적, 화학적 외상, 콘택트렌즈 과다 착용, 전신 염증성 질환, 의인성 등으로 윤부 줄기세포가 기능 부전에 빠지면 정상 상피 장벽이 소실되고 혈관 침입이 발생합니다3). 경증에서는 플루오레세인 염색으로 소용돌이 모양 상피증이 관찰되고, 중등증에서는 표층 신생혈관과 판누스가 나타납니다3).
기타 원인
섹션 제목: “기타 원인”- 염증성 질환: SJS/TEN, 안구 유천포창, 봄철 각결막염, 주사비 각막염
- 각막 이식 후: 거부 반응에 따른 신생혈관1)
- 변성 질환: Terrien 변연 각막 변성, 교양적 점상 각막 이영양증
네, 예방할 수 있는 경우가 많습니다. 각막 신생혈관의 주요 원인 중 하나는 콘택트렌즈로 인한 산소 부족입니다. 착용 시간을 지키고, 산소 투과성이 높은 렌즈를 사용하며, 정기적인 안과 검진을 받으면 위험을 크게 줄일 수 있습니다.
4. 진단과 검사 방법
섹션 제목: “4. 진단과 검사 방법”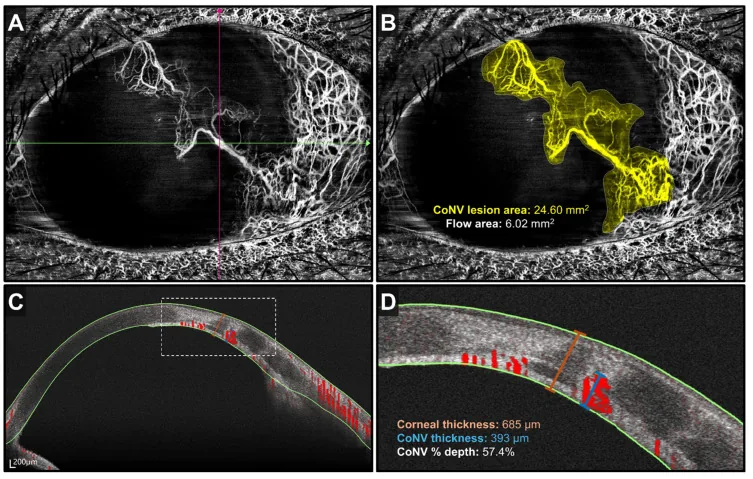
세극등 현미경 검사
섹션 제목: “세극등 현미경 검사”각막 신생혈관 진단에서 가장 기본적인 검사입니다. 혈관의 위치(사분면), 깊이(표층/심층), 활동성(혈류 유무), 결막 침범 유무를 평가합니다.
- 확산법: 조사광 폭을 넓히거나 확산판을 통해 관찰하면 신생혈관을 식별하기 쉽습니다
- 간접 조명법: 홍채나 수정체에서 반사된 빛으로 신생혈관, 각막 신경을 관찰합니다
- 플루오레세인 염색: 상피 결손 유무, 결막 침입 평가에 유용합니다
형광 조영 검사
섹션 제목: “형광 조영 검사”- 플루오레세인 형광 조영술(FA) : 혈관 관류와 누출을 기능적으로 평가하여 활동성 혈관과 성숙 혈관을 감별합니다1)
- 인도시아닌 그린 형광 조영술(ICGA) : 심층 혈관이나 유입 혈관의 묘사에 뛰어나며, 혈관 폐쇄술의 타겟팅에 유용합니다1)
영상 검사
섹션 제목: “영상 검사”- 전안부 OCT / OCT-A : 비침습적으로 각막 혈관망의 깊이와 범위를 정량 평가할 수 있습니다1)
- 생체 내 공초점 현미경(IVCM) : LSCD 진단에서 상피 기저 세포의 정량이 가능함3)
| 검사법 | 주요 평가 항목 | 특징 |
|---|---|---|
| 세극등 현미경 | 위치·깊이·활동성 | 일차 선택 기본 검사 |
| FA / ICGA | 관류·누출·영양 혈관 | 치료 계획에 유용 |
| AS-OCT / OCT-A | 깊이·정량적 평가 | 비침습적 |
5. 표준적인 치료법
섹션 제목: “5. 표준적인 치료법”각막 신생혈관의 치료는 원인 치료와 신생혈관 자체에 대한 중재의 두 가지 축으로 이루어집니다2).
원인 치료
섹션 제목: “원인 치료”- 콘택트렌즈 사용 중단: 저산소성인 경우 사용을 중단하고 산소 투과성이 높은 렌즈로 변경을 고려합니다. 활동성 혈관인지 오래된 혈관(ghost vessel)인지 확인합니다.
- 감염 치료: 원인이 되는 감염성 각막염에 대한 항균제, 항바이러스제, 항진균제 투여
- LSCD 치료:윤부이식·양막이식 등의 수술 치료
약물 요법
섹션 제목: “약물 요법”- 스테로이드 점안:염증성 사이토카인(IL-1, IL-6) 억제, 림프구 세포사멸 유도, 혈관 확장 억제를 통해 혈관 신생을 억제합니다2). 일차 선택이지만 장기 사용 시 스테로이드 녹내장이나 감염 감수성 증가에 주의해야 합니다
- 항VEGF 요법:베바시주맙(점안·결막하 주사·각막 실질 내 주사)이 널리 사용됩니다1)2). 미성숙 활동성 혈관에 효과적이지만, 성숙 혈관(주피세포로 덮인 혈관)에 대한 효과는 제한적입니다1). 신생혈관 발생 후 2주 이내에 주피세포 피복이 80%에 도달하므로 조기 치료가 중요합니다1)
- 면역억제제: 사이클로스포린 A 점안액은 T세포 활성화를 억제하고 스테로이드 절감 효과가 있습니다2). 타크로리무스, 시롤리무스(mTOR 억제제)도 선택지가 됩니다1)
- 독시사이클린: 점막 유사천포창 억제 작용을 통해 각막 신생혈관을 억제합니다2)
수술 요법 및 시술적 치료
섹션 제목: “수술 요법 및 시술적 치료”- 레이저 광응고술: 아르곤 또는 Nd:YAG 레이저로 혈관을 응고·폐쇄시킵니다. 각막 이식 전 전처치나 지질 각막증 치료에 사용됩니다. 각막 출혈·얇아짐의 위험이 있으며, 혈관 재개통이나 션트 혈관 형성이 종종 관찰됩니다
- fine needle diathermy (FND) : 윤부의 영양혈관에 가는 바늘을 삽입하여 전기적으로 응고 폐쇄합니다. 성숙한 굵은 혈관에도 효과적이며, 아르곤 레이저로 폐쇄가 어려운 구심혈관에 대해 시행됩니다1)
- 광역학 치료(PDT) : 광감작제를 혈관 내에 주입한 후, 광조사를 통해 활성산소종을 생성하여 혈관벽을 파괴합니다. 높은 특이성을 가지지만, 고비용과 시간이 소요됩니다
- MICE (MMC 혈관내 화학색전술) : 33게이지 바늘로 마이토마이신 C (0.4 mg/mL)를 영양혈관 내에 직접 주입하는 시술입니다6). 기존 치료에 저항하는 난치성 각막신생혈관에 대해, 혈관 고스트화와 지질각막증의 개선이 보고되었습니다6)
6. 병태생리학·상세한 발병 기전
섹션 제목: “6. 병태생리학·상세한 발병 기전”혈관신생 특권(CAP)의 유지 기전
섹션 제목: “혈관신생 특권(CAP)의 유지 기전”각막의 무혈관 상태는 여러 혈관신생 억제 기전이 협력하여 유지합니다1).
- 가용성 VEGF 수용체 1(sVEGFR1) : 각막 상피·실질에서 항상적으로 생성됩니다. VEGF-A를 고친화도로 포획하여 막결합형 VEGFR에 대한 결합을 경쟁적으로 억제하는 내인성 VEGF 트랩입니다1)
- 트롬보스폰딘(TSP-1/TSP-2) : 각막 ECM에 항상 발현하는 혈관신생 억제성 당단백질. VEGF를 격리하고 VEGFR2 신호를 억제합니다. CD36/CD47을 통해 VEC(혈관내피세포)의 세포자멸사를 유도합니다1)
- 엔도스타틴 : 콜라겐 XVIII의 C-말단 단편. VEGF·bFGF 경로를 억제하고, 카스파제 3 활성 증가로 VEC의 세포자멸사를 촉진합니다. 림프관 신생도 억제합니다1)
- 물리적 장벽 : 윤부 장벽, 치밀한 콜라겐 배열, 각막의 상대적 저온 환경이 혈관 침입을 제한합니다1)
혈관신생 촉진 인자와 발병 경로
섹션 제목: “혈관신생 촉진 인자와 발병 경로”CAP의 파괴는 주로 두 가지 경로를 통해 발생합니다1)2).
경로 1: 염증·저산소증에 의한 촉진 인자 생성 증가
각막 손상으로 인해 대식세포, 상피세포, 내피세포에서 세 가지 주요 혈관신생 인자가 방출됩니다1).
- VEGF-A: VEGFR-2를 통해 혈관내피세포의 증식 및 이동을 촉진하고, 점막유사천포창-2/점막유사천포창-9를 유도하여 세포외기질 리모델링을 촉진합니다1). 각막 신생혈관에서 가장 중요한 촉진 인자입니다.
- bFGF(FGF-2):ERK/PI3K 경로를 통해 VEGF 생성을 증가시키고 VE-카드헤린 결합을 해리시켜 VEC의 스프라우팅을 촉진합니다1)
- PDGF:주피세포·평활근세포를 동원하여 신생혈관을 안정화시킵니다1). PDGF에 의한 혈관 성숙은 항VEGF 요법에 대한 내성을 초래합니다
윤부줄기세포의 소실로 인해 각막상피의 정상적인 장벽 기능이 상실되고, 결막조직의 각막 침입과 지속적인 염증이 신생혈관을 유지합니다1)3).
림프관 신생과의 연관성
섹션 제목: “림프관 신생과의 연관성”각막 신생혈관(혈관 신생)과 림프관 신생은 상호 연관되면서도 독립적인 과정입니다4). 혈관은 면역 효과세포의 원심성 경로(원심로)로, 림프관은 항원 제시세포의 구심성 경로(구심로)로 기능합니다4). 두 과정의 동시 진행은 각막 이식에서 면역 특권 상실과 거부 반응에 관여합니다4). VEGF-A/VEGFR-2가 혈관 신생을, VEGF-C,D/VEGFR-3가 림프관 신생을 주로 유도합니다4).
7. 최신 연구와 향후 전망
섹션 제목: “7. 최신 연구와 향후 전망”AAV 벡터를 이용한 유전자 치료
섹션 제목: “AAV 벡터를 이용한 유전자 치료”Xie 등(2024)은 아데노-연관 바이러스(AAV) 벡터를 이용한 지속적 항-VEGF 인자 발현을 통한 각막 신생혈관 치료를 종설하였다5). AAV2와 AAV8이 각막 실질 세포의 형질도입에 가장 효율적이며, 각막 실질 내 주사가 가장 효과적인 투여 경로로 간주된다5). AAV 유전자 치료는 단회 투여로 장기간 항-VEGF 효과를 발휘할 수 있으나, 현재는 전임상 단계에 머물러 있다5).
MMC 혈관내 화학색전술(MICE)
섹션 제목: “MMC 혈관내 화학색전술(MICE)”Addeen 등(2023)은 각막 이식 후 난치성 신생혈관에 대한 MICE(33게이지 바늘로 MMC 0.4 mg/mL를 혈관 내 주입) 2례를 보고하였다6). 수술 후 조기에 혈관의 고스트화가 관찰되었고, 통증 감소와 삶의 질 개선이 얻어졌다6). 유해 사례는 관찰되지 않았으나, 장기 안전성 확인이 필요하다.
안티센스 올리고뉴클레오타이드(Aganirsen)
섹션 제목: “안티센스 올리고뉴클레오타이드(Aganirsen)”Muller 등(2026)의 종설에서는 IRS-1을 표적으로 하는 안티센스 올리고뉴클레오티드 Aganirsen이 각막 신생혈관의 퇴축과 관해를 전임상 모델에서 보였다고 보고되었습니다1). CRISPR/Cas9을 이용한 VEGF-A 편집도 유망한 전임상 데이터를 보여주고 있습니다1).
안과용 나노시스템
섹션 제목: “안과용 나노시스템”Zhang 등(2022)은 나노입자, 리포솜, 미셀 등의 나노캐리어가 항VEGF 약물이나 스테로이드의 각막 내 전달 효율을 개선하고, 지속 방출, 표적 지향성, 저자극성을 실현할 수 있다고 보고했습니다7). 임상 적용은 아직 제한적이지만, 빈번한 투여의 부담을 줄일 수 있을 것으로 기대됩니다.
병용 요법의 중요성
섹션 제목: “병용 요법의 중요성”각막 신생혈관은 다인성 병태이므로 단일 치료법으로는 충분한 효과를 얻기 어려운 경우가 많습니다1)2). VEGF, bFGF, PDGF, 림프관 신생 등 여러 경로를 표적으로 하는 병용 요법이 향후 치료 전략의 중심이 될 가능성이 있습니다1).
8. 참고 문헌
섹션 제목: “8. 참고 문헌”- Muller E, Feinberg L, Woronkowicz M, Roberts HW. Corneal Neovascularization: Pathogenesis, Current Insights and Future Strategies. Biology. 2026;15(2):136.
- Wu D, Chan KE, Lim BXH, et al. Management of corneal neovascularization: Current and emerging therapeutic approaches. Indian J Ophthalmol. 2024;72(Suppl 3):S354-S371.
- Drzyzga L, Spiewak D, Dorecka M, Wygledowska-Promienska D. Available Therapeutic Options for Corneal Neovascularization: A Review. Int J Mol Sci. 2024;25(10):5479.
- Zhang Z, Zhao R, Wu X, Ma Y, He Y. Research progress on the correlation between corneal neovascularization and lymphangiogenesis. Mol Med Rep. 2025;31(2):47.
- Xie M, Wang L, Deng Y, et al. Sustained and Efficient Delivery of Antivascular Endothelial Growth Factor by AAV for Treatment of Corneal Neovascularization. J Ophthalmol. 2024;2024:5487973.
- Addeen SZ, Oyoun Z, Alfhaily H, Anbari A. Outcomes of mitomycin C intravascular chemoembolization (MICE) in refractory corneal neovascularization after failed keratoplasty. Digit J Ophthalmol. 2023;29(4).
- Zhang C, Yin Y, Zhao J, et al. An Update on Novel Ocular Nanosystems with Possible Benefits in the Treatment of Corneal Neovascularization. Int J Nanomedicine. 2022;17:4911-4931.
