Néovascularisation superficielle

Néovascularisation cornéenne (Corneal Neovascularization)
1. Qu’est-ce que la néovascularisation cornéenne ?
Section intitulée « 1. Qu’est-ce que la néovascularisation cornéenne ? »La néovascularisation cornéenne (CoNV) est une condition dans laquelle de nouveaux capillaires provenant du plexus vasculaire limbique envahissent le tissu cornéen normalement avasculaire1). Ce n’est pas une maladie spécifique mais une réponse non spécifique à diverses conditions telles que l’infection, l’inflammation, l’hypoxie et les traumatismes.
La cornée possède un « privilège angiogénique cornéen (CAP) » qui maintient l’état avasculaire grâce à un équilibre précis entre les facteurs inhibiteurs et promoteurs de l’angiogenèse1). Lorsque cet équilibre est rompu, les cellules endothéliales vasculaires prolifèrent, migrent et envahissent le stroma cornéen.
Les néovaisseaux sont classés en deux types selon leur localisation anatomique.
Néovascularisation profonde
Ils envahissent le stroma cornéen à partir des artères ciliaires antérieures.
Survient dans les inflammations ou œdèmes persistants tels que la kératite interstitielle (syphilis, tuberculose), la kératite herpétique stromale et la kératopathie bulleuse.
Les néovaisseaux immatures provoquent une exsudation lipidique, une inflammation persistante et une cicatrisation 1). En progressant, les vaisseaux maturent, se couvrent de péricytes et deviennent résistants à la thérapie anti-VEGF 1). Chez les patients après une greffe de cornée, les néovaisseaux constituent un facteur de risque de rejet.
Sans traitement, les néovaisseaux maturent et régressent difficilement spontanément, entraînant une kératopathie lipidique (dépôts lipidiques dans la cornée) et des cicatrices cornéennes, causes de baisse permanente de l’acuité visuelle. De plus, en cas de nécessité de greffe de cornée, la présence de néovaisseaux augmente le risque de rejet du greffon. Une consultation précoce et un traitement de la cause sont importants.
2. Principaux symptômes et signes cliniques
Section intitulée « 2. Principaux symptômes et signes cliniques »Symptômes subjectifs
Section intitulée « Symptômes subjectifs »- Baisse de l’acuité visuelle : survient lorsque les néovaisseaux ou leurs complications (dépôts lipidiques, cicatrices) affectent l’axe visuel
- Hyperhémie : hyperhémie conjonctivale associée à la maladie causale
- Asymptomatique : souvent aucun symptôme subjectif si la lésion n’atteint pas l’axe visuel
Signes cliniques (observés par le médecin lors de l’examen)
Section intitulée « Signes cliniques (observés par le médecin lors de l’examen) »- Morphologie des néovaisseaux : varie d’un fin réseau à des vaisseaux actifs dilatés, en passant par des vaisseaux matures denses
- Localisation et profondeur des vaisseaux : évaluées par lampe à fente avec méthode de la fente et éclairage indirect pour déterminer si superficiels ou profonds
- Vaisseaux fantômes (ghost vessels) : vaisseaux anciens sans flux sanguin. Aucun traitement nécessaire.
- Conjonctivalisation : recouvrement de la cornée par du tissu conjonctival. Confirmé par un retard de coloration à la fluorescéine.
- Kératopathie lipidique : opacité jaune-blanche due au dépôt de lipides dans le stroma cornéen, provenant de la fuite des néovaisseaux.
- Disparition de la palissade de Vogt (POV) : signe important suggérant une perte des cellules souches limbiques.
3. Causes et facteurs de risque
Section intitulée « 3. Causes et facteurs de risque »Infections
Section intitulée « Infections »- Virus de l’herpès simplex (HSV-1) : cause infectieuse la plus fréquente de néovascularisation cornéenne dans les pays développés 1). La kératite herpétique stromale entraîne une néovascularisation profonde.
- Kératite bactérienne : dans les cas graves, l’ulcère cornéen et la cicatrisation s’accompagnent d’une invasion vasculaire.
- Kératite fongique : peut s’accompagner de néovascularisation dans les cas prolongés.
- Trachome et onchocercose : principales causes infectieuses dans les pays en développement 1).
Hypoxie (liée aux lentilles de contact)
Section intitulée « Hypoxie (liée aux lentilles de contact) »Le port inapproprié (surcharge) de lentilles de contact souples en est la cause principale. Environ 80 à 90 % des porteurs de lentilles souples en HEMA conventionnelles présentent une invasion vasculaire depuis la partie supérieure de la cornée (direction 10h-2h). Si l’épithéliopathie persiste plus d’un mois, des vaisseaux envahissent la zone.
Traumatisme chimique
Section intitulée « Traumatisme chimique »Les brûlures alcalines pénètrent profondément dans le stroma cornéen, provoquant une atteinte étendue des cellules souches limbiques et une néovascularisation. C’est l’un des groupes où le taux de réussite de la greffe de cornée est le plus faible.
Insuffisance en cellules souches limbiques (LSCD)
Section intitulée « Insuffisance en cellules souches limbiques (LSCD) »La LSCD est l’une des principales voies de la néovascularisation cornéenne 1)3). Lorsque les cellules souches limbiques deviennent dysfonctionnelles en raison de causes congénitales, de traumatismes chimiques, de surcharge en lentilles de contact, de maladies inflammatoires systémiques ou de causes iatrogènes, la barrière épithéliale normale est perdue et une invasion vasculaire se produit 3). Dans les cas légers, une épithéliopathie en tourbillon est observée à la coloration à la fluorescéine ; dans les cas modérés, une néovascularisation superficielle et un pannus apparaissent 3).
Autres causes
Section intitulée « Autres causes »- Maladies inflammatoires : SJS/TEN, pemphigoïde oculaire, kératoconjonctivite vernale, kératite rosacée.
- Après greffe de cornée : néovascularisation associée au rejet 1).
- Maladies dégénératives : Dégénérescence limbique de Terrien, dystrophie cornéenne en gouttes gélatineuses
Oui, cela peut souvent être évité. L’une des principales causes de la néovascularisation cornéenne est le manque d’oxygène dû aux lentilles de contact. En respectant la durée de port, en utilisant des lentilles à haute perméabilité à l’oxygène et en effectuant des examens ophtalmologiques réguliers, vous pouvez réduire considérablement le risque.
4. Diagnostic et méthodes d’examen
Section intitulée « 4. Diagnostic et méthodes d’examen »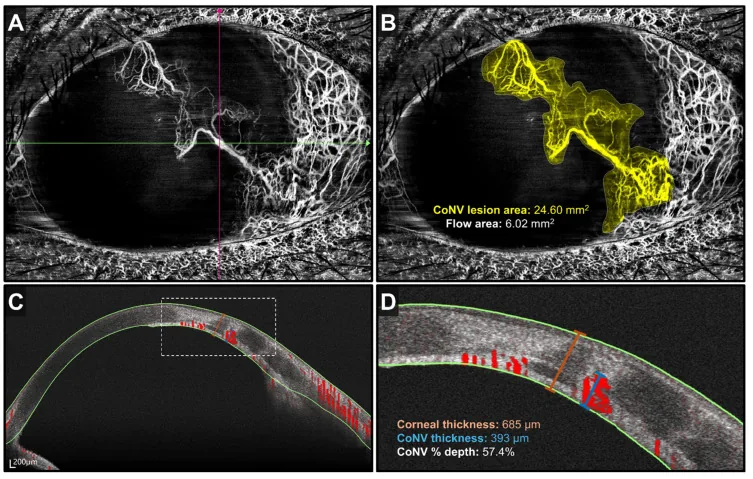
Examen à la lampe à fente
Section intitulée « Examen à la lampe à fente »C’est l’examen le plus fondamental pour le diagnostic de la néovascularisation cornéenne. Il évalue la localisation (quadrant), la profondeur (superficielle/profonde), l’activité (présence de flux sanguin) et la présence d’invasion conjonctivale des vaisseaux.
- Méthode du diffuseur : en élargissant le faisceau lumineux ou en utilisant un diffuseur, les vaisseaux néoformés sont plus faciles à distinguer
- Éclairage indirect : observer les vaisseaux néoformés et les nerfs cornéens à l’aide de la lumière réfléchie par l’iris ou le cristallin
- Coloration à la fluorescéine : utile pour détecter les défauts épithéliaux et évaluer l’invasion conjonctivale
Angiographie fluorescente
Section intitulée « Angiographie fluorescente »- Angiographie à la fluorescéine (FA) : évalue fonctionnellement la perfusion et la fuite vasculaires, et différencie les vaisseaux actifs des vaisseaux matures1)
- Angiographie au vert d’indocyanine (ICGA) : excellente pour visualiser les vaisseaux profonds et afférents, utile pour le ciblage de l’occlusion vasculaire1)
Imagerie
Section intitulée « Imagerie »- OCT / OCT-A du segment antérieur : permet une évaluation quantitative non invasive de la profondeur et de l’étendue du réseau vasculaire cornéen1)
- Microscopie confocale in vivo (IVCM) : permet la quantification des cellules basales épithéliales dans le diagnostic de LSCD3)
| Méthode d’examen | Principaux paramètres évalués | Caractéristiques |
|---|---|---|
| Lampe à fente | Localisation, profondeur, activité | Examen de base de première intention |
| FA / ICGA | Perfusion, fuite, vaisseaux afférents | Utile pour la planification du traitement |
| AS-OCT / OCT-A | Évaluation quantitative et de profondeur | Non invasif |
5. Traitement standard
Section intitulée « 5. Traitement standard »Le traitement de la néovascularisation cornéenne repose sur deux piliers : le traitement de la cause et l’intervention sur les néovaisseaux eux-mêmes2).
Traitement de la cause
Section intitulée « Traitement de la cause »- Arrêt du port de lentilles de contact : en cas d’hypoxie, arrêter le port et envisager le passage à des lentilles à haute perméabilité à l’oxygène. Distinguer les vaisseaux actifs des vaisseaux anciens (ghost vessels).
- Traitement de l’infection : administration d’antibiotiques, d’antiviraux ou d’antifongiques pour la kératite infectieuse causale.
- Traitement de la LSCD : traitement chirurgical tel que la greffe de limbe ou la greffe de membrane amniotique.
Traitement médicamenteux
Section intitulée « Traitement médicamenteux »- Collyre corticostéroïde : supprime la néovascularisation en inhibant les cytokines inflammatoires (IL-1, IL-6), en induisant l’apoptose des lymphocytes et en inhibant la vasodilatation2). C’est le traitement de première intention, mais une utilisation à long terme nécessite une attention au glaucome cortisonique et à l’augmentation de la sensibilité aux infections.
- Thérapie anti-VEGF : le bévacizumab (collyre, injection sous-conjonctivale ou intrastromale) est largement utilisé1)2). Efficace sur les vaisseaux actifs immatures, mais effet limité sur les vaisseaux matures (recouverts de péricytes)1). Comme le recouvrement par les péricytes atteint 80 % dans les deux semaines suivant l’apparition des néovaisseaux, un traitement précoce est important1).
- Immunosuppresseurs : le collyre de ciclosporine A supprime l’activation des lymphocytes T et a un effet d’épargne des corticoïdes2). Le tacrolimus et le sirolimus (inhibiteur de mTOR) sont également des options1).
- Doxycycline : supprime la néovascularisation cornéenne par inhibition de la pemphigoïde des muqueuses2).
Traitement chirurgical et procédural
Section intitulée « Traitement chirurgical et procédural »- Photocoagulation au laser : coagulation et occlusion des vaisseaux par laser argon ou Nd:YAG. Utilisée comme prétraitement avant greffe de cornée et pour le traitement de la kératopathie lipidique. Risques d’hémorragie cornéenne et d’amincissement ; une recanalisation vasculaire et la formation de shunts sont souvent observées.
- Fine needle diathermy (FND) : insertion d’une fine aiguille dans les vaisseaux nourriciers du limbe pour coagulation électrique. Efficace même sur les vaisseaux matures et épais, utilisée pour les vaisseaux afférents difficiles à occlure au laser argon 1).
- Thérapie photodynamique (PDT) : injection intravasculaire d’un photosensibilisateur, puis irradiation lumineuse pour générer des espèces réactives de l’oxygène et détruire la paroi vasculaire. Haute spécificité, mais coût élevé et temps nécessaire.
- MICE (chimioembolisation intravasculaire à la MMC) : injection directe de mitomycine C (0,4 mg/mL) dans les vaisseaux nourriciers à l’aide d’une aiguille 33G 6). Pour les néovascularisations cornéennes réfractaires aux traitements conventionnels, une amélioration de la vascularisation fantôme et de la kératopathie lipidique a été rapportée 6).
6. Physiopathologie et mécanismes détaillés
Section intitulée « 6. Physiopathologie et mécanismes détaillés »Mécanismes de maintien du privilège angiogénique cornéen (CAP)
Section intitulée « Mécanismes de maintien du privilège angiogénique cornéen (CAP) »L’état avasculaire de la cornée est maintenu par la coordination de multiples mécanismes inhibiteurs de l’angiogenèse 1).
- Récepteur soluble du VEGF de type 1 (sVEGFR1) : produit de manière constitutive par l’épithélium et le stroma cornéens. Il capture le VEGF-A avec une haute affinité et inhibe de manière compétitive la liaison au VEGFR membranaire, agissant comme un piège endogène du VEGF 1).
- Thrombospondine (TSP-1/TSP-2) : glycoprotéine inhibitrice de l’angiogenèse exprimée de manière constitutive dans la matrice extracellulaire cornéenne. Elle séquestre le VEGF et supprime la signalisation VEGFR2. Elle induit l’apoptose des cellules endothéliales vasculaires via CD36/CD47 1).
- Endostatine : fragment C-terminal du collagène XVIII. Elle inhibe les voies VEGF et bFGF, et favorise l’apoptose des cellules endothéliales vasculaires par activation de la caspase-3. Elle supprime également la lymphangiogenèse 1).
- Barrière physique : la barrière limbique, la disposition dense du collagène et l’environnement relativement froid de la cornée limitent l’invasion vasculaire1)
Facteurs pro-angiogéniques et voies de développement
Section intitulée « Facteurs pro-angiogéniques et voies de développement »La rupture du CAP se produit principalement par deux voies1)2).
Voie 1 : Augmentation de la production de facteurs promoteurs due à l’inflammation et à l’hypoxie
Les lésions cornéennes entraînent la libération de trois principaux facteurs angiogéniques par les macrophages, les cellules épithéliales et les cellules endothéliales1).
- VEGF-A : favorise la prolifération et la migration des VEC via VEGFR-2, induit la MMP-2/MMP-9 et stimule le remodelage de la MEC1). Facteur promoteur le plus important dans la néovascularisation cornéenne
- bFGF (FGF-2) : augmente la production de VEGF via la voie ERK/PI3K, dissocie les liaisons VE-cadhérine et favorise le bourgeonnement des VEC1)
- PDGF : recrute les péricytes et les cellules musculaires lisses, stabilisant les nouveaux vaisseaux1). La maturation vasculaire induite par le PDGF confère une résistance à la thérapie anti-VEGF
Voie 2 : Insuffisance limbique de cellules souches (LSCD)
La perte de cellules souches limbiques entraîne une perte de la fonction barrière normale de l’épithélium cornéen, et l’invasion conjonctivale de la cornée ainsi que l’inflammation persistante maintiennent la néovascularisation1)3).
Relation avec la lymphangiogenèse
Section intitulée « Relation avec la lymphangiogenèse »La néovascularisation cornéenne (angiogenèse) et la lymphangiogenèse sont des processus interdépendants mais indépendants4). Les vaisseaux sanguins servent de voie de sortie (efférente) pour les cellules immunitaires effectrices, tandis que les vaisseaux lymphatiques servent de voie d’entrée (afférente) pour les cellules présentatrices d’antigènes4). La progression simultanée des deux est impliquée dans la perte du privilège immunitaire et le rejet lors de la greffe de cornée4). VEGF-A/VEGFR-2 pilote principalement l’angiogenèse, tandis que VEGF-C,D/VEGFR-3 pilote principalement la lymphangiogenèse4).
7. Recherches récentes et perspectives futures
Section intitulée « 7. Recherches récentes et perspectives futures »Thérapie génique par vecteur AAV
Section intitulée « Thérapie génique par vecteur AAV »Xie et al. (2024) ont passé en revue le traitement de la néovascularisation cornéenne par expression soutenue de facteurs anti-VEGF à l’aide de vecteurs de virus adéno-associés (AAV)5). AAV2 et AAV8 sont les plus efficaces pour transduire les cellules du stroma cornéen, et l’injection intrastromale est considérée comme la voie d’administration la plus efficace5). La thérapie génique par AAV peut fournir un effet anti-VEGF à long terme après une seule administration, mais elle en est encore au stade préclinique5).
Chimio-embolisation intravasculaire à la MMC (MICE)
Section intitulée « Chimio-embolisation intravasculaire à la MMC (MICE) »Addeen et al. (2023) ont rapporté deux cas de MICE (injection intravasculaire de MMC 0,4 mg/mL avec une aiguille de calibre 33) pour des néovascularisations réfractaires après greffe de cornée 6). Une fantomisation vasculaire précoce a été observée, avec une réduction de la douleur et une amélioration de la qualité de vie 6). Aucun effet indésirable n’a été noté, mais la sécurité à long terme doit être confirmée.
Oligonucléotide antisens (Aganirsen)
Section intitulée « Oligonucléotide antisens (Aganirsen) »Dans une revue de Muller et al. (2026), l’oligonucléotide antisens Aganirsen ciblant IRS-1 a montré une régression et une rémission de la néovascularisation cornéenne dans des modèles précliniques 1). L’édition de VEGF-A par CRISPR/Cas9 montre également des données précliniques prometteuses 1).
Nanostructures ophtalmiques
Section intitulée « Nanostructures ophtalmiques »Zhang et al. (2022) ont rapporté que les nanovecteurs tels que les nanoparticules, liposomes et micelles peuvent améliorer l’efficacité de délivrance des anti-VEGF et des stéroïdes dans la cornée, permettant une libération prolongée, un ciblage et une faible irritation 7). L’application clinique est encore limitée, mais on espère réduire la charge des administrations fréquentes.
Importance des thérapies combinées
Section intitulée « Importance des thérapies combinées »La néovascularisation cornéenne étant multifactorielle, un traitement unique est souvent insuffisant 1)2). Les thérapies combinées ciblant plusieurs voies (VEGF, bFGF, PDGF, lymphangiogenèse) pourraient devenir centrales dans les stratégies futures 1).
8. Références
Section intitulée « 8. Références »- Muller E, Feinberg L, Woronkowicz M, Roberts HW. Corneal Neovascularization: Pathogenesis, Current Insights and Future Strategies. Biology. 2026;15(2):136.
- Wu D, Chan KE, Lim BXH, et al. Management of corneal neovascularization: Current and emerging therapeutic approaches. Indian J Ophthalmol. 2024;72(Suppl 3):S354-S371.
- Drzyzga L, Spiewak D, Dorecka M, Wygledowska-Promienska D. Available Therapeutic Options for Corneal Neovascularization: A Review. Int J Mol Sci. 2024;25(10):5479.
- Zhang Z, Zhao R, Wu X, Ma Y, He Y. Research progress on the correlation between corneal neovascularization and lymphangiogenesis. Mol Med Rep. 2025;31(2):47.
- Xie M, Wang L, Deng Y, et al. Sustained and Efficient Delivery of Antivascular Endothelial Growth Factor by AAV for Treatment of Corneal Neovascularization. J Ophthalmol. 2024;2024:5487973.
- Addeen SZ, Oyoun Z, Alfhaily H, Anbari A. Outcomes of mitomycin C intravascular chemoembolization (MICE) in refractory corneal neovascularization after failed keratoplasty. Digit J Ophthalmol. 2023;29(4).
- Zhang C, Yin Y, Zhao J, et al. An Update on Novel Ocular Nanosystems with Possible Benefits in the Treatment of Corneal Neovascularization. Int J Nanomedicine. 2022;17:4911-4931.
