前眼部病变

结节性多动脉炎(PAN)的神经眼科征象
一目了然的要点
Section titled “一目了然的要点”1. 结节性多动脉炎(PAN)的神经眼科征象
Section titled “1. 结节性多动脉炎(PAN)的神经眼科征象”结节性多动脉炎(Polyarteritis Nodosa; PAN)是一种主要累及中型动脉的全身性坏死性血管炎。动脉壁全层发生炎症,血管周围有炎性细胞浸润,导致纤维素样坏死。
发病率在活检确诊病例中为每年每10万人0.7例,患病率为每10万人6.3例,是一种罕见疾病。法国多民族人群的报告显示,每100万人患病率为33例,年发病率为0~1.6例1)。通常发生于40~60岁,男性略多(男女比1.5:1)1)。
全身症状中,神经症状常见,Pagnoux 2010年的348例中79%出现1)。眼部病变发生率为9~20%,表现为脉络膜血管炎、视网膜血管闭塞、缺血性视神经病变、脑神经麻痹等多种神经眼科征象。肺部病变原则上不出现,这是本病的特征之一。
与乙型肝炎病毒(HBV)相关,目前HBV相关PAN占全部病例的7~10%。在HBV疫苗普及前占36%,普及后有所下降。
眼部病变见于10%–20%的患者。脉络膜血管炎是最常见的眼部表现,脉络膜毛细血管板的局灶性急性缺血强烈提示血管炎。包括神经眼科表现(如脑神经麻痹、同向偏盲)在内,受累频率更高。
2. 主要症状与临床发现
Section titled “2. 主要症状与临床发现”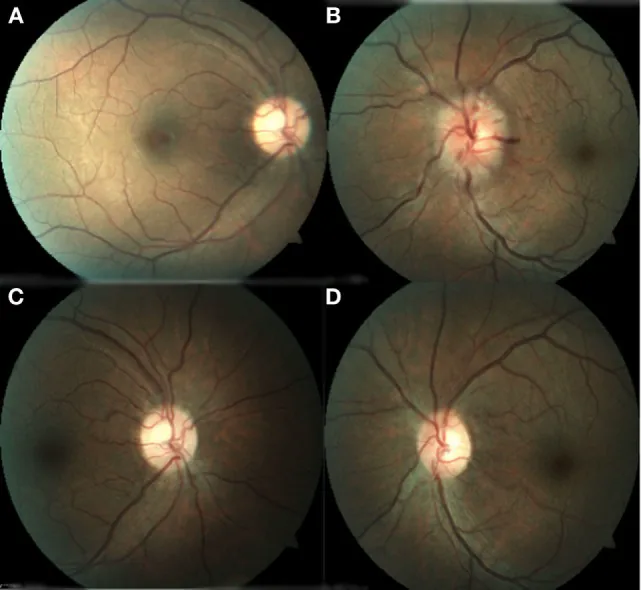
初发症状常以全身症状为先。
- 发热、体重减轻、全身乏力:PAN初发时常见,38℃以上发热可持续2周以上。
- 肌痛、关节痛:半数以上患者出现。
- 睾丸痛:强烈提示PAN的症状,约20%的患者出现5)。
- 周围神经病变:50%~75%的病例出现,表现为手脚麻木或无力。
眼部自觉症状如下。
- 视力下降:从缺血性视神经病变或视网膜血管闭塞引起的急剧下降,到慢性下降,程度不一。
- 一过性视力障碍:由视网膜血管一过性缺血引起。
- 视野异常:根据中枢神经系统血管炎的部位,出现同向偏盲等视野缺损。
- 复视:由眼外肌麻痹或脑神经麻痹引起。
眼部病变多样,分为前眼部、后眼部及神经眼科所见。
后段及神经眼科表现
全身脏器的主要患病率如下所示。
| 脏器 | 主要症状 | 患病率(%) |
|---|---|---|
| 周围神经 | 多发性单神经炎 | 50~70 |
| 肾脏 | 蛋白尿、高血压、肾功能衰竭 | 70 |
| 皮肤 | 紫癜、溃疡、网状青斑、坏疽 | 50 |
| 肌肉 | 肌肉痛 | 50~60 |
| 消化道 | 腹痛、消化道出血 | 30~35 |
| 关节 | 关节炎 | 20 |
| 生殖器 | 睾丸梗死 | 20 |
3. 病因与风险因素
Section titled “3. 病因与风险因素”PAN的病理生理学尚未完全阐明。推测环境刺激可能诱发遗传易感性。
基本病理是免疫复合物沉积于中等动脉血管壁,导致坏死。小动脉和中等动脉发生纤维素样坏死。
主要的风险因素和相关因素如下。
- HBV感染:与PAN有强烈关联,常在感染后6个月内发病。机制涉及血清免疫复合物沉积和补体消耗。HBV疫苗普及后,HBV相关PAN从1970年代的36%下降到7%。
- HCV感染:虽不如HBV强烈,但已有相关报道。
- CECR1突变(DADA2):导致腺苷脱氨酶2(ADA2)缺乏,发病年龄更早(多在10岁前),卒中频率更高。
- 药物:长期服用米诺环素超过3年可导致肾PAN。有病例仅停药后动脉瘤即消失3)。
- COVID-19 mRNA疫苗:接种后7至28天内发病的4例病例已有报道5)。
- 其他:也有报道与细小病毒B19、CMV、EBV、HIV感染、毛细胞白血病、VEXAS综合征相关1)。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”没有单一的检查可以确诊PAN。需结合临床表现、实验室检查、影像学和病理学结果进行诊断。
日本的诊断标准
Section titled “日本的诊断标准”根据厚生省难治性血管炎调查研究班(1998年)的标准,符合以下10项主要症状中的2项或以上,并且有血管造影或血管炎的病理发现,即可确诊。
- 发热(38℃以上,持续2周以上)和体重减轻(6个月内减少6kg以上)
- 高血压
- 进行性肾功能衰竭
- 脑梗死(出血)
- 缺血性心脏病、心包炎或心力衰竭
- 胸膜炎
- 消化道出血或肠梗阻
- 多发性单神经炎
- 皮肤症状(皮下结节、皮肤溃疡、坏疽、紫癜)
- 多关节炎或肌炎(肌痛、肌无力)
即使没有血管造影或病理结果,满足包括(1)在内的6项或以上项目,则视为疑似病例。
ACR 1990分类标准
Section titled “ACR 1990分类标准”满足以下10项中3项或以上即可分类1)。
体重减轻超过4kg、网状青斑、睾丸痛、弥漫性肌痛、单/多发性神经病变、舒张压超过90mmHg、肾功能衰竭、HBV阳性、血管造影异常(动脉瘤/闭塞)、活检显示动脉壁中性粒细胞浸润。
临床和血液检查
Section titled “临床和血液检查”- 炎症标志物:ESR升高、CRP升高、轻度白细胞增多、血小板增多、慢性贫血。
- ANCA:经典PAN通常为阴性。10%可能MPO-ANCA阳性,但阳性病例应考虑显微镜下多血管炎(MPA)。ANCA高值显著降低PAN的可能性。
- 病毒检测:检查HBV、HCV和HIV血清学。
- IL-6:与疾病活动性相关,高值病例常伴有关节痛和皮肤溃疡2)。
没有单一的检查可以确诊PAN。可见ESR和CRP升高等非特异性炎症表现,而ANCA和冷球蛋白通常为阴性,这有助于诊断。同时必须确认HBV、HCV和HIV血清学。确诊需要血管造影或组织活检。
- 特征性表现为中型动脉的斑片状全层纤维素样坏死,伴以中性粒细胞为主的炎症。
- 慢性病变中可见向淋巴细胞和巨噬细胞的转化以及血管新生。
- 坏死与纤维化的组合,以及邻近的微动脉瘤和血栓形成是典型表现。
- 联合肌肉和神经活检在有症状的PAN患者中80%可获得血管炎证据(单独肌肉活检为65%)。
- 如果活检发现肉芽肿或巨细胞,需考虑PAN以外的血管炎(如GPA、GCA)。
眼科及影像学检查
Section titled “眼科及影像学检查”- 荧光素眼底血管造影(FA):有助于显示脉络膜毛细血管层的多灶性急性缺血。可见臂-视网膜循环时间和视网膜内循环时间延长。
- 头部MRI:皮质及皮质下多发散在病变(灰质和白质)。钆增强FLAIR图像可确认小出血性病变与多发性梗死并存。
- MRA/CTA:显示肠系膜、肾、肝动脉多发微小动脉瘤(1-5mm)及共存狭窄病变。动脉狭窄与动脉瘤扩张交替出现是特征性表现6)。
- 内脏血管造影:在活检阴性或以内脏症状为主时进行。肠系膜、肝、肾动脉的局灶性节段性动脉瘤在高达90%的病例中被确认1)。
5. 标准治疗方法
Section titled “5. 标准治疗方法”PAN是一种危及生命的疾病,诊断后应立即与风湿病专家合作开始治疗。
全身治疗(日本标准)
Section titled “全身治疗(日本标准)”基本治疗是类固醇冲击疗法、口服类固醇和环磷酰胺输注的组合。
- 类固醇冲击疗法:用于急性期强力抑制炎症。
- 口服类固醇:冲击治疗后开始,逐渐减量至维持剂量5–10 mg/天。
- 环磷酰胺(安道生®)输注:与类固醇同时进行以诱导缓解。通常1–3次输注即可达到缓解。
- 维持治疗:缓解后改用甲氨蝶呤或硫唑嘌呤(依木兰®)。如有禁忌,使用霉酚酸酯。
根据疾病类型选择治疗也很重要。
- HBV-PAN:抗病毒药物+血浆置换(清除免疫复合物)是基础治疗。
- DADA2-PAN:TNF抑制剂有效。
- 药物诱发性PAN(如米诺环素):仅停用致病药物即可获得缓解3)。
根据眼部病变类型进行以下治疗。
- 干性角结膜炎:0.1%玻璃酸钠滴眼液,每日4-6次。
- 上巩膜炎/葡萄膜炎:0.1%地塞米松滴眼液,每日2-6次。
- 前段病变:使用类固醇或人工泪液等对症治疗。
- 活动性视网膜血管炎:全身使用类固醇。类固醇抵抗时加用免疫抑制剂。
- 进行性视网膜血管闭塞:抗凝治疗(华法林2-5mg/日,目标PT-INR 1.5-2)。
- 视网膜新生血管:及时进行视网膜光凝术。对于广泛视网膜血管闭塞,也可预防性进行。
- 增殖性玻璃体视网膜病变:考虑玻璃体切除术。
在免疫抑制治疗期间,需注意机会性感染如CMV视网膜炎、类固醇性中心性浆液性脉络膜视网膜病变,以及视网膜无灌注区出现的新生血管。建议定期进行包括荧光眼底造影在内的眼底检查。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”PAN的基本病变是中型动脉壁的全层炎症。
炎症级联反应被认为按以下方式进展。
- 内皮损伤的启动:环境刺激(感染、药物等)触发直接损伤或细胞因子/抗体介导的内皮损伤。
- 炎症细胞因子的释放:IL-2、IL-8和IFN-γ升高,白细胞被募集到动脉中膜。
- 内弹性膜破坏:中性粒细胞浸润破坏内弹性膜,导致内膜增厚、水肿和血栓形成。
- 动脉闭塞和动脉瘤形成:血栓形成导致的闭塞和动脉壁脆弱化导致的动脉瘤形成并存。血管造影上两者并存是PAN的典型表现。
在HBV相关PAN中,免疫复合物沉积和补体消耗是动脉炎的主要机制。
中枢神经系统动脉脆弱化导致动脉瘤形成,破裂可引起出血性梗死。慢性炎症导致狭窄和血栓形成,引起缺血性病变。在眼部,脉络膜、视网膜和视神经的血流障碍导致各种眼部表现。
在DADA2(CECR1突变)中,ADA2缺乏被认为导致M1型巨噬细胞过度活化,促进血管壁的炎症和破坏。
Boistault等人(2021)的报告中,一例难治性儿童PAN病例显示IL-6显著升高至106.43 pg/mL(正常0-4.3 pg/mL)2)。IL-6高值组以男性为主,关节痛和皮肤溃疡显著增多。
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”托珠单抗(IL-6受体抑制剂)
Section titled “托珠单抗(IL-6受体抑制剂)”已有报道将IL-6受体抑制剂托珠单抗(TCZ)应用于难治性PAN。
Boistault等人(2021年)总结了11例难治性PAN(中位年龄35岁,IQR 23.5-57.5岁,5例女性)使用TCZ治疗的报告2)。剂量为TCZ 8mg/kg每2-4周静脉滴注,或TCZ 162mg每周皮下注射,大多数病例达到了缓解。
在1例儿童PAN中,一名对高剂量类固醇联合环磷酰胺无效的4岁女童开始使用TCZ 8mg/kg每2周一次,数天内出现临床和生物学改善,21个月后仍维持完全缓解2)。选择TCZ的依据是IL-6水平相对于TNF-α较高。
COVID-19疫苗相关PAN
Section titled “COVID-19疫苗相关PAN”已有4例COVID-19 mRNA疫苗接种后发生PAN的报道。
Ohkubo等人(2022年)总结了接种疫苗后7-28天内发生PAN的病例5)。大多数发生在首次接种后,所有病例均通过类固醇和免疫抑制剂改善。推测其机制为脂质纳米颗粒(LNP)注射引起的炎症反应,导致中性粒细胞浸润和炎症细胞因子产生。
因果关系尚未确定,但疫苗的益处被认为远大于风险。
药物诱导性PAN的非免疫抑制管理
Section titled “药物诱导性PAN的非免疫抑制管理”Yokota等人(2022)首次在英文文献中报告了一例服用米诺环素3年以上后发生肾PAN的病例,仅通过停药就实现了功能和形态学缓解3)。7.5年后的再次造影显示肾动脉瘤消失,且未使用类固醇或免疫抑制剂进行治疗。
在药物诱导性PAN中,停用致病药物是首要措施,这一发现表明有可能在不使用免疫抑制治疗的情况下实现缓解,具有重要意义。
8. 参考文献
Section titled “8. 参考文献”- Ambrogetti R, Taha O, Awan B, et al. Pericarditis of Polyarteritis Nodosa. Cureus. 2023;15(10):e46717.
- Boistault M, Lopez Corbeto M, Quartier P, et al. A young girl with severe polyarteritis nodosa successfully treated with tocilizumab: a case report. Pediatr Rheumatol Online J. 2021;19:168.
- Yokota K, Kurihara I, Nakamura T, et al. Remission of Angiographically Confirmed Minocycline-induced Renal Polyarteritis Nodosa: A Case Report and Literature Review. Intern Med. 2022;61:103-110.
- Waisayarat J, Niyasom C, Vilaiyuk S, et al. Polyarteritis Nodosa with Cytomegalovirus Enteritis and Jejunoileal Perforation: Report of a Case with a Literature Review. Vasc Health Risk Manag. 2022;18:595-601.
- Ohkubo Y, Ohmura S, Ishihara R, et al. Possible case of polyarteritis nodosa with epididymitis following COVID-19 vaccination: A case report and review of the literature. Mod Rheumatol Case Rep. 2022;(epub).
- Robinson C, Yasin Z, Patel P, et al. A Rare Presentation of Polyarteritis Nodosa. Cureus. 2022;14(2):e21925.
