自身免疫性(最常见)

周边部溃疡性角膜炎
一目了然的要点
Section titled “一目了然的要点”1. 什么是周边部溃疡性角膜炎?
Section titled “1. 什么是周边部溃疡性角膜炎?”周边部溃疡性角膜炎(PUK)是一组在角膜缘附近角膜基质出现新月形破坏性炎症的疾病。其特征为角膜基质变性、炎性细胞浸润和上皮缺损,进展可导致角膜变薄、后弹力层膨出和穿孔。它是表现为周边角膜溃疡的疾病总称,包括特发性Mooren溃疡(蚕食性角膜溃疡)、类风湿关节炎等胶原病相关的溃疡、葡萄球菌过敏(卡他性角膜溃疡)和角膜泡疹等。
年发病率为每百万人0.2~3例,罕见,无性别差异8)。约50%伴有基础全身性疾病,其中约20%为感染性8)。类风湿关节炎(RA)是最常见的原因,占PUK患者的34%~42%2)。
类风湿关节炎的流行病学背景
Section titled “类风湿关节炎的流行病学背景”类风湿关节炎是胶原病中最常见的疾病。据报道,日本患病率女性为每1000人5.4人,男性为1.1人。多见于30-60岁女性,随着年龄增长男性比例增加。约70%的RA患者存在HLA-DR4遗传相关性。已知创伤或分娩后可诱发RA或使病情加重。
在RA中,合并血管炎的类型称为恶性类风湿关节炎。伴有巩膜炎、胸膜炎、间质性肺炎、心包炎、心肌炎、多发性单神经炎、肠系膜动脉栓塞、指尖溃疡,全身预后不良。大多数RA相关PUK并发于这种恶性类风湿关节炎,导致角膜迅速变薄和穿孔。
病理基本结构
Section titled “病理基本结构”PUK的发生被认为与角膜抗原的自身免疫反应、循环免疫复合物沉积以及对外来抗原的过敏反应有关。角膜周边的特殊性在于,角膜缘密集分布着血管网、免疫系统和神经系统,是免疫复合物易于沉积的环境。在胶原病相关的PUK中,血液中的自身抗体沉积在角膜缘及周边部,引发III型过敏反应,浸润的免疫细胞释放的细胞外基质降解酶参与溃疡形成。
Mooren溃疡定义为原因不明且不伴有全身性自身免疫疾病的周边部角膜溃疡。而PUK是伴随全身疾病发生的病变,两者的鉴别对于确定治疗方案至关重要。Mooren溃疡中巩膜炎合并较轻,但胶原病相关的周边部溃疡常继发于浅层巩膜炎或巩膜炎,灰白色病变向角膜中央进展,多伴有血管侵入。
2. 主要症状与临床所见
Section titled “2. 主要症状与临床所见”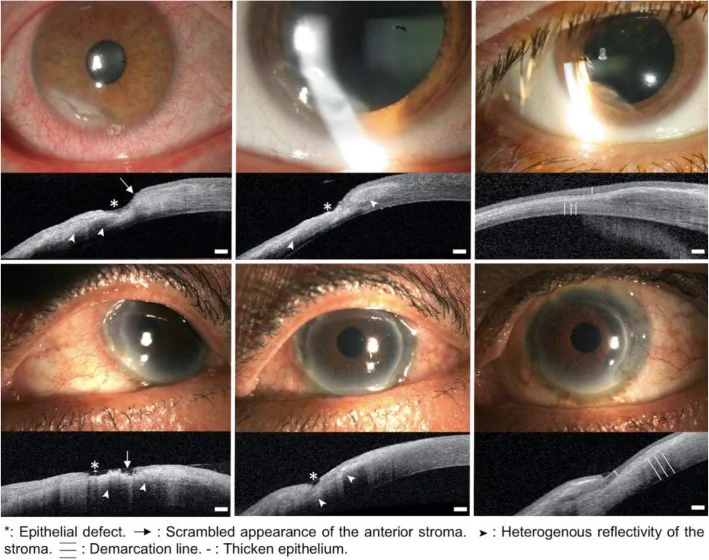
- 眼痛:角膜溃疡引起的剧烈疼痛。合并巩膜炎时,表现为向面部或颞部放射的深部痛,加重至影响睡眠。
- 充血:伴有睫状充血,多为局限性。合并巩膜炎时,表现为巩膜血管扩张迂曲导致的环形严重充血。
- 视力下降:根据角膜混浊和变薄的程度发生。
- 畏光、流泪:伴随角膜上皮损伤出现。
- 干涩感、异物感:类风湿关节炎合并病例常伴有重度干眼(继发性干燥综合征),出现眼表异物感和干涩感。
PUK的角膜表现为角膜缘附近局限的月牙形基质破坏。伴有胶原病的PUK,常继发于巩膜炎或表层巩膜炎,病变向角膜中央进展。
- 角膜基质浸润、溃疡:与角膜缘平行的月牙形浸润和基质坏死。溃疡前端呈深坑道状,称为undermining。
- 上皮缺损:溃疡部位上皮脱落,荧光素染色阳性。
- 角膜变薄:进展时角膜基质显著变薄。严重病例呈沙漏状角膜(hourglass cornea)4)。
- 旁中心角膜穿孔:重症病例在角膜中央附近发生穿孔。穿孔病例可见梨形瞳孔和虹膜组织脱出3)。
- 合并巩膜炎:约36%的PUK患者合并巩膜炎。巩膜炎是深层巩膜血管丛的炎症,引起巩膜水肿和细胞浸润。
- 角膜新生血管:慢性病例可见表层和深层血管侵入5)。
类风湿关节炎的眼部并发症谱
Section titled “类风湿关节炎的眼部并发症谱”类风湿关节炎相关的眼部并发症从干眼到巩膜穿孔,严重程度范围广泛。以下列出理解PUK的重要相关所见。
- 干燥性角结膜炎:作为继发性干燥综合征高频合并。
- 上巩膜炎:Tenon囊血管丛等浅层血管丛的炎症。疼痛轻微,视力正常。
- 巩膜炎(弥漫性/结节性):伴有眼痛的深层血管充血。主要为肉芽肿性炎症和血管炎。
- 坏死性巩膜炎:中央有黄白色缺血区域。预后不良,若不早期治疗可导致失明或难以保留眼球。
- 穿孔性巩膜软化症:发生于长期治疗RA的患者。巩膜逐渐变薄,变薄区域周围无充血或疼痛,葡萄膜暴露。
- 周边部角膜溃疡:多见于恶性类风湿关节炎,快速进展为变薄和穿孔。
3. 原因和风险因素
Section titled “3. 原因和风险因素”PUK继发于多种全身性疾病。大致分为自身免疫性、感染性和其他。
感染性及其他原因
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”- 裂隙灯显微镜检查:评估角膜周边浸润、溃疡和变薄的范围及深度。使用荧光素染色检查上皮缺损情况。
- 巩膜炎与结膜/表层巩膜充血的鉴别:滴用1:1000稀释的肾上腺素后,结膜充血和角膜缘充血消退,但巩膜炎引起的血管扩张不消退。
- 荧光素巩膜造影:评估巩膜无灌注区域的存在,用于与坏死性巩膜炎鉴别。
- 眼部超声(B超):用于评估后巩膜炎。可见巩膜增厚、巩膜结节、巩膜与Tenon囊分离、眼外肌炎等表现。
- 角膜刮片和培养:用于排除感染性病因。若高度怀疑感染,可考虑病变活检。
- 眼前节OCT(AS-OCT):当角膜混浊严重且裂隙灯检查难以评估深度时有用。AS-OCT可将PUK分为以下三期:
- 急性期:角膜上皮缺失,前基质结构破坏伴不均匀反射,病变区角膜厚度减少。
- 愈合过程期:再生中的不规则上皮呈低反射,基质反射趋于均匀。
- 愈合期:低反射上皮与高反射基质之间形成清晰边界,瘢痕性角膜增厚和变薄趋于稳定。
为确定基础疾病,系统进行以下检查。类风湿关节炎的诊断中,血沉升高、CRP升高、类风湿因子(RF)阳性有助诊断(约1/4病例RF阴性)。MMP-3可作为滑膜增殖的标志物,也用于评估疾病活动性。
| 检查项目 | 目的 |
|---|---|
| RF、抗CCP抗体 | 类风湿关节炎 |
| MMP-3 | RA疾病活动性 |
| ANA | SLE/胶原病 |
| ANCA(PR3/MPO) | ANCA相关性血管炎 |
| RPR/FTA-ABS | 梅毒 |
| CXR/PPD/IGRA | 结核/结节病 |
此外,根据需要增加外周血检查、肾功能、尿检、乙型/丙型肝炎病毒检查、骶髂关节X线、鼻窦CT等。若怀疑大血管炎,FDG-PET有用,据报道敏感性90%、特异性98%2)。
| 疾病 | 与PUK的区别 |
|---|---|
| Mooren溃疡 | 不伴全身疾病。无或轻度巩膜炎。 |
| Terrien角膜边缘变性 | 炎症表现轻微,进展缓慢。无上皮缺损。伴有脂肪沉积。 |
| 卡他性角膜溃疡 | 溃疡与角膜缘之间有透明带。对葡萄球菌的III型过敏反应。 |
卡他性角膜溃疡是由于对葡萄球菌外毒素的III型过敏反应,在角膜周边部发生的无菌性浸润和溃疡。好发于2、4、8、10点钟位置,与PUK不同的是,溃疡与角膜缘之间有1-2mm的透明带。Mooren溃疡单眼或双眼突然发病,表现为沿角膜缘的弧形溃疡,溃疡边缘有陡峭的挖掘,但溃疡与角膜缘之间没有透明带。
5. 标准治疗方法
Section titled “5. 标准治疗方法”PUK治疗的目标是控制炎症、预防继发感染、促进溃疡愈合和防止穿孔。如果合并胶原病,应优先治疗原发胶原病,并与风湿免疫科协作治疗。如果类风湿关节炎控制不佳,PUK无法控制。即使单独治疗PUK可能实现短期炎症控制,但如果全身疾病活动度高,复发和穿孔风险持续存在。因此,治疗计划应由眼科和内科共同制定。
- 人工泪液和泪点塞:用于治疗干眼和促进上皮化。推荐使用不含防腐剂的制剂。可联合使用透明质酸钠滴眼液(Hyalein®)和瑞巴派特滴眼液(Mucosta®)。
- 抗菌滴眼液:用于预防继发感染。
- 0.05%环孢素滴眼液:用于抑制局部炎症。由于市售免疫抑制剂滴眼液不适用于此,使用0.05%的自制制剂。对于Mooren溃疡,也有使用他克莫司滴眼液的报道。
- 地塞米松结膜下注射:将0.4 mL地塞米松注射液(Decadron®)注射到溃疡附近的结膜充血区域。
- 局部类固醇滴眼液:可能促进角膜溶解(角膜软化),因此使用需极其谨慎。合并巩膜炎的轻症病例,可开始使用0.1%倍他米松滴眼液,每日4-6次。
- 口服多西环素:利用其胶原酶抑制作用联合使用。也可联合使用维生素C以帮助胶原重塑。
- COX2抑制剂(塞来昔布):对于轻度巩膜炎,口服塞来昔布100 mg,每日两次。对疼痛非常有效,对炎症控制也有效。如无哮喘等禁忌症,应从初期积极联合使用。
- 氰基丙烯酸酯粘合剂:当穿孔迫在眉睫时,涂抹于溃疡底部 5)。
全身免疫抑制治疗是治疗的核心。
- 口服泼尼松龙:在PUK中,起始剂量为1-1.5 mg/kg/天。合并巩膜炎的初始治疗使用0.5-1 mg/kg/天。
- 类固醇冲击疗法:对于坏死性巩膜炎或快速进展性PUK,给予甲泼尼龙1克/天,连续3天的冲击治疗。
- 免疫抑制剂(类固醇节约剂):在穿孔迫近、类固醇抵抗或合并RA的病例中尽早引入。
- 生物制剂:在免疫抑制剂治疗抵抗的难治性病例中引入。
- 类风湿关节炎本身的DMARD治疗:早期积极使用改善病情抗风湿药以阻止关节破坏的进展。甲氨蝶呤等免疫抑制剂和抗TNF-α抗体等生物DMARD是核心。近年来,早期使用生物制剂可抑制骨破坏,显著改善长期生活质量(QOL)。短期联合使用NSAIDs和口服类固醇以缓解关节症状。
- 感染预防:使用免疫抑制剂或生物制剂前及使用期间,必须进行全身检查,筛查乙型肝炎病毒再激活和结核潜伏感染。
角膜穿孔或即将穿孔是外科干预的适应证。
- 结膜切除术(Brown手术):对蚕蚀性角膜溃疡有效。从溃疡两端各2个钟点位开始,切除角膜缘3~4 mm宽的充血结膜。也适用于胶原病相关的周边溃疡。
- 角膜上皮成形术:结膜切除后若巩膜暴露,病理性结膜可能重新伸展,因此将供体角膜制成的薄角膜上皮片像堤坝一样缝合在角膜缘2~3片。术后佩戴隐形眼镜。
- 表层角膜移植术:当病情严重且角膜穿孔不可避免时施行。使用保存角膜,用高尔夫刀充分刮除溃疡底部的增殖组织后进行移植。可与Brown手术或角膜上皮成形术联合使用。
- 板层角膜移植术:有报道对免疫检查点抑制剂相关PUK穿孔病例施行了板层微型角膜移植术5)。
- 羊膜移植:有报道对蚕蚀性角膜溃疡和胶原病并发PUK有效。
- Tenon囊悬吊移植:对于进展期PUK呈沙漏状角膜的病例,有报道改良Tenon囊悬吊环状补片移植4)。其优点是自体组织,无排斥反应。
- 补片移植术:对于穿孔性巩膜软化症,在穿孔部位进行补片移植等外科巩膜修复,以防止眼球萎缩。
术后需继续局部和全身使用类固醇或免疫抑制剂以抑制排斥反应。以巩膜炎为背景的穿孔病例,巩膜变薄范围广泛,术后病情易持续,因此必须联合全身免疫抑制治疗。
已有报道结膜下注射地塞米松植入物(Ozurdex)对PUK有效。对于不能耐受全身免疫抑制治疗的老年患者,三次注射可在11个月内控制炎症,且无巩膜融解或眼压升高8)。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”免疫复合物介导的角膜破坏
Section titled “免疫复合物介导的角膜破坏”PUK的发病机制涉及体液免疫和细胞免疫。在类风湿关节炎和血管炎中,关节滑膜和血管壁产生过量的炎性细胞因子,为全身性III型过敏反应奠定基础。自身抗体产生的免疫复合物沉积在角膜缘及周边部的血管中,激活补体经典途径。补体激活诱导中性粒细胞和巨噬细胞的趋化性,这些炎性细胞释放胶原酶和蛋白酶。
前炎性细胞因子(如TNF-α、IL-6)刺激角膜基质细胞产生基质金属蛋白酶(MMP)1)。MMP降解角膜周边部的胶原蛋白,导致角膜变薄和溃疡形成。在类风湿关节炎的关节病变中,关节滑膜出现淋巴细胞浸润、血管新生和滑膜增生,炎性细胞因子通过软骨细胞死亡和破骨细胞活化导致组织破坏;类似的破坏机制被认为也作用于角膜周边部。
Th17/IL-17通路
Section titled “Th17/IL-17通路”近年来,Th17细胞和IL-17的作用受到关注1)。TGF-β1、IL-6、IL-21等细胞因子促进Th17分化,IL-1进一步刺激Th17分化。Th17分泌的IL-17增强MMP产生,促进角膜基质降解1)。有报道称抑制Th17可减轻PUK的眼部并发症1)。
在肉芽肿性酒渣鼻中,表皮释放IL-37,激活肥大细胞释放糜酶、类胰蛋白酶和MMP等蛋白酶1)。这种炎性微环境被认为促进Th17极化,导致PUK发生1)。
预后与严重程度
Section titled “预后与严重程度”当合并周边部角膜溃疡或坏死性巩膜炎时,视力预后通常较差。坏死性巩膜炎好发于60多岁,双眼发病约占60%,若不及时进行适当治疗,可导致失明或眼球无法保留。在恶性类风湿关节炎中,全身性血管炎累及肺、心、肾,不仅影响视功能,也影响生命预后。穿孔性巩膜软化症典型地发生于长期治疗RA的患者,当出现典型表现时,往往已错过治疗时机。早期诊断和早期治疗干预是改善预后的关键。
角膜周边部为好发部位的原因
Section titled “角膜周边部为好发部位的原因”角膜缘是角膜上皮和结膜上皮的交界处,是血管系统、免疫系统和神经系统密集的区域。角膜缘含有丰富的朗格汉斯细胞,参与抗原呈递。中央角膜是无血管的,而周边部更容易从角膜缘血管网获得免疫复合物和炎症细胞。由于这一解剖学特性,在胶原病相关的周边部溃疡中,免疫复合物沉积在角膜缘至周边部,引发III型过敏反应,浸润的免疫细胞释放的细胞外基质降解酶参与溃疡形成。
角膜缘是血管网、免疫系统和神经系统密集的区域,朗格汉斯细胞也很丰富。中央角膜是无血管的,而周边部更容易从角膜缘血管网获得免疫复合物和炎症细胞。在自身免疫性疾病中,免疫复合物沉积在角膜缘血管,激活补体系统,中性粒细胞和巨噬细胞聚集并破坏角膜基质,因此病变好发于周边部。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”免疫检查点抑制剂相关PUK
Section titled “免疫检查点抑制剂相关PUK”随着免疫检查点抑制剂(ICI)的普及,作为irAE的PUK已有报道。在伊匹木单抗(抗CTLA-4抗体)和纳武利尤单抗(抗PD-1抗体)的联合治疗中,irAE的发生率超过90% 5)。ICI相关PUK可能对高剂量类固醇滴眼液和环孢素滴眼液耐药,已有需要板层角膜移植的病例报道 5)。肿瘤治疗的持续与irAE管理的平衡是一个挑战,与肿瘤内科的协作不可或缺。
结膜下地塞米松植入物
Section titled “结膜下地塞米松植入物”对于无法耐受全身免疫抑制治疗的患者,已尝试结膜下注射地塞米松植入物(Ozurdex)8)。重复给药实现了长期炎症控制,未出现巩膜融解或眼压升高 8)。作为一种避免全身副作用的局部治疗,期待未来的验证。
Th17靶向治疗的可能性
Section titled “Th17靶向治疗的可能性”由于Th17/IL-17通路与PUK的病理密切相关,针对Th17的治疗备受关注。在一例与肉芽肿性酒渣鼻相关的PUK病例中,异维A酸有效,提示异维A酸的Th17抑制作用和调节性T细胞促进作用可能参与其中 1)。
新型手术方法
Section titled “新型手术方法”针对进展期PUK的改良Tenon囊悬吊移植术已有报道 4)。由于使用自体组织,无排斥反应,即使在供体角膜难以获得的情况下也可实施 4)。
8. 参考文献
Section titled “8. 参考文献”- Hsiao FC, Meir YJ, Hsiao CH, et al. Peripheral ulcerative keratitis in a patient with granulomatous rosacea. Taiwan J Ophthalmol. 2023;13(1):80-83.
- Uchida S, Kaji Y, Ui M, et al. Peripheral ulcerative keratitis associated with large vessel vasculitis. Cureus. 2021;13(6):e15767.
- Dallalzadeh LO, Ang MJ, Beazer AP, Spencer DB, Afshari NA. Peripheral ulcerative keratitis secondary to severe hidradenitis suppurativa. Am J Ophthalmol Case Rep. 2022;25:101403.
- Anitha V, Ghorpade A, Ravindran M. A modified Tenon’s sling annular graft for advanced peripheral ulcerative keratitis with an hourglass cornea. Indian J Ophthalmol. 2022;70(2):655-657.
- Aschauer J, Donner R, Lammer J, Schmidinger G. Bilateral corneal perforation in Ipilimumab/Nivolumab-associated peripheral ulcerative keratitis. Am J Ophthalmol Case Rep. 2022;28:101686.
- Hsieh HH, Shen EP. Peripheral ulcerative keratitis secondary to chronic Citrobacter koseri canaliculitis. Taiwan J Ophthalmol. 2023;13(3):376-379.
- Acharya I, Jalloh MI, Trevisan CD, Haas CJ. Hidradenitis suppurativa and peripheral ulcerative keratitis. J Community Hosp Intern Med Perspect. 2024;14(6):89-93.
- Ghoraba HH, Or C, Ahluwalia A, et al. Subconjunctival dexamethasone implant (Ozurdex) for peripheral ulcerative keratitis. Am J Ophthalmol Case Rep. 2025;39:102379.
- Campagne O, Vinet E, Engel L, et al. Ocular manifestations of inflammatory bowel disease. Ocul Surf. 2023;29:326-339.
