干性角结膜炎

类风湿关节炎与眼部病变(干眼症、巩膜炎)
1. 类风湿关节炎与眼部病变是什么?
Section titled “1. 类风湿关节炎与眼部病变是什么?”类风湿关节炎(rheumatoid arthritis; RA)是一种以关节滑膜为主要病变部位的慢性炎症性自身免疫性疾病。它可引起肺、皮肤、眼等多系统症状,是胶原病中最常见的一种。
好发于30~60岁女性,男女比例约为1:3。老年发病时男性比例增加。日本患病率估计约为人口的0.5~1%(约60~120万人)。
约25~30%的RA患者出现某种眼部症状1)。眼部并发症的发生率与RA病程、疾病活动性和关节外症状的存在相关2)。
眼部并发症的分类
Section titled “眼部并发症的分类”RA相关的眼部病变分为以下五种类型。
| 眼部并发症 | 频率 | 主要特征 |
|---|---|---|
| 干燥性角结膜炎(干眼症) | 最常见 | 常合并干燥综合征 |
| 巩膜炎 | 较常见 | 眼痛、深层充血、可出现坏死型 |
| 表层巩膜炎 | 较常见 | 表层炎症,有自然缓解倾向 |
| 周边部角膜溃疡 | 相对较少 | 快速角膜变薄及穿孔风险 |
| 虹膜睫状体炎 | 罕见 | 前葡萄膜炎 |
恶性类风湿关节炎是一种伴有巩膜炎、胸膜炎、间质性肺炎、心包炎、心肌炎、多发性单神经炎、肠系膜动脉栓塞和指尖溃疡的重症类型,预后不良。
2. 主要症状与临床所见
Section titled “2. 主要症状与临床所见”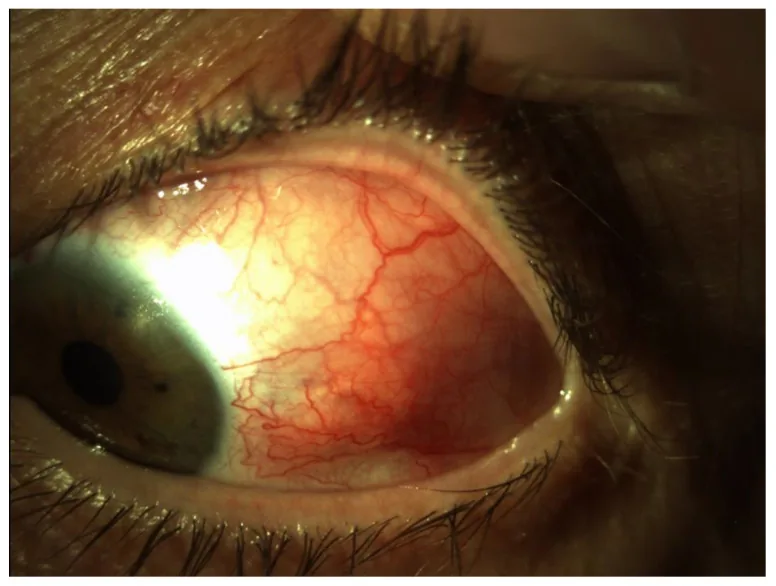
眼部并发症的种类不同,自觉症状也不同。
- 干燥性角结膜炎:眼干涩感、异物感、畏光、眼疲劳、视力波动
- 巩膜炎:剧烈眼痛(深部痛、搏动性)、充血、畏光、流泪
- 坏死性巩膜炎(穿孔性巩膜软化症):可能无痛,需注意漏诊
- 表层巩膜炎:区域性发红、轻度疼痛、有自然缓解倾向
- 周边部角膜溃疡:充血、视力下降、穿孔时突发剧烈眼痛
临床所见(眼科检查所见)
Section titled “临床所见(眼科检查所见)”巩膜炎
表层巩膜炎
周边角膜溃疡
巩膜炎根据Watson分类分为前部巩膜炎(弥漫型、结节型、坏死型)和后部巩膜炎,其中坏死型最为严重7)。约30%~50%的巩膜炎患者合并全身性自身免疫疾病,以RA最为常见5)。
3. 原因与风险因素
Section titled “3. 原因与风险因素”RA的眼部病变是由自身免疫机制引起的全身性血管炎和肉芽肿性炎症波及巩膜及角膜缘血管所致11)。
RA的病理生理与眼部波及
Section titled “RA的病理生理与眼部波及”- 自身免疫机制:滑膜淋巴细胞浸润、血管新生、血管翳形成导致软骨破坏和骨侵蚀。
- 炎症细胞因子:TNF-α、IL-1β、IL-6、IL-17主导组织破坏。
- 眼部波及:免疫复合物沉积于巩膜血管→补体激活和血管炎→肉芽肿性坏死性炎症
- 角膜边缘部:边缘血管网中的III型过敏反应→MMP(基质金属蛋白酶)产生→角膜实质胶原分解
- 泪腺功能低下:合并干燥综合征的病例中,淋巴细胞浸润导致泪腺和唾液腺分泌减少
眼部病变的风险因素
Section titled “眼部病变的风险因素”- RA病程长
- 类风湿因子(RF)高滴度、抗CCP抗体阳性
- 伴有关节外表现(肺、皮肤、神经)的恶性RA
- 合并干燥综合征(增加干性角结膜炎风险)
- 疾病活动性高(DAS28高值)
- 吸烟
有报道称,发生坏死性巩膜炎或周边部角膜溃疡的患者10年生存率降低8),这些眼部病变可作为全身血管炎活动性的指标。
4. 诊断和检查方法
Section titled “4. 诊断和检查方法”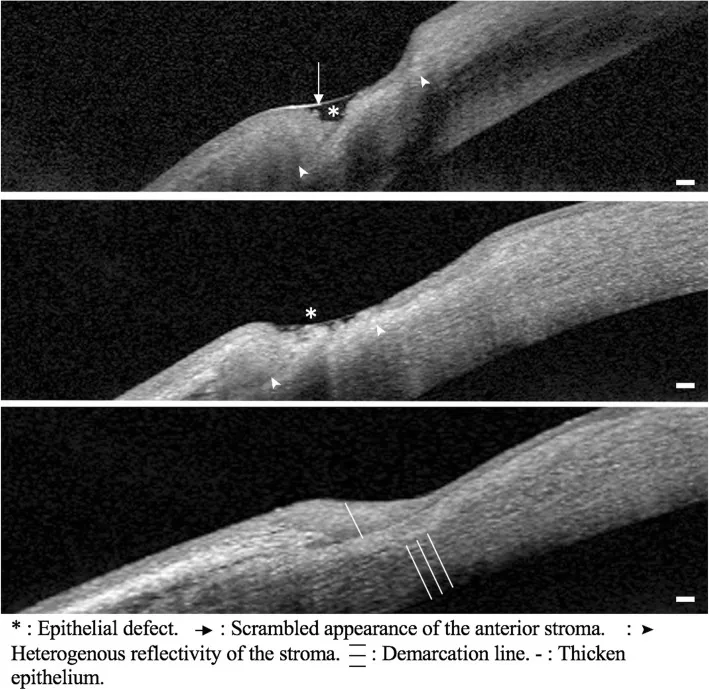
RA的诊断基于2010年ACR/EULAR分类标准9)。对关节肿胀数、血清学检查(RF、抗CCP抗体)、症状持续时间、急性期反应物(CRP、ESR)四个领域进行评分。
血液检查中,ESR升高、CRP升高、RF阳性(约75%,约25%阴性)、抗CCP抗体、MMP-3升高对诊断有用4)。X线检查中,手和手指的关节侵蚀和骨破坏是特征性表现。
通过以下检查评估眼部并发症。
| 检查方法 | 评估对象 | 所见标准 |
|---|---|---|
| Schirmer试验 | 泪液分泌量 | ≤5mm/5分钟表示分泌减少 |
| 泪膜破裂时间(BUT) | 泪膜稳定性 | ≤5秒表示不稳定 |
| 裂隙灯显微镜 | 巩膜、角膜、眼前段 | 检查坏死性变化和角膜变薄 |
| 眼压测量 | 青光眼、类固醇反应 | 使用类固醇时必须检查 |
| 眼底检查 | 后巩膜炎、视乳头水肿 | 排除后部病变 |
| B超扫描 | 后巩膜炎 | T征(Tenon囊水肿) |
| 眼眶MRI | 评估后巩膜炎范围 | 巩膜增厚和强化 |
后巩膜炎容易被漏诊,可表现为眼痛、视力下降、眼球突出和复视。B超扫描中的T征对诊断有帮助。
对于巩膜炎患者,建议进行系统性检查,包括RF、ANA、ANCA、补体和胸部X线,以筛查全身性疾病5)。
强烈建议定期进行眼科筛查。巩膜炎和周边角膜溃疡的早期发现和早期治疗直接影响视力预后。特别是在RA疾病活动性高或恶性RA期间,即使没有症状,眼科筛查也很重要。此外,使用羟氯喹的患者需要定期监测视网膜毒性。
5. 标准治疗方法
Section titled “5. 标准治疗方法”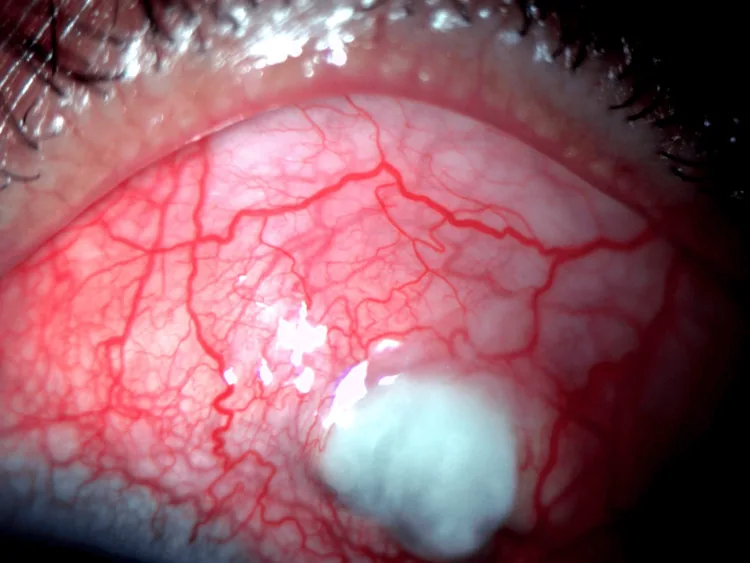
RA眼部病变的治疗需要眼科局部治疗和内科(风湿科)全身治疗相结合。
干燥性角结膜炎
Section titled “干燥性角结膜炎”对于轻至中度干燥性角结膜炎,逐步应用以下方法:
- 人工泪液滴眼:选择不含防腐剂的制剂(长期使用以避免防腐剂引起的角膜毒性)。
- 0.1%玻璃酸钠滴眼液:每日5-6次(角膜保护、泪液稳定)
- 泪点栓塞术:对中度以上病例有效。放置于上下泪点。
- 3%地夸磷索钠滴眼液:每日6次。促进水分和黏蛋白分泌。
- 瑞巴派特滴眼液:增强黏蛋白产生。对合并干燥综合征的病例有用。
合并干燥综合征的病例,干眼症往往更严重,可考虑加用环孢素滴眼液。
- NSAIDs滴眼和口服:氟比洛芬滴眼液、双氯芬酸滴眼液。轻度病例首选。
- 多数局灶性上巩膜炎可自行缓解,但反复发作的病例应评估全身性疾病活动性。
| 严重程度 | 治疗选择 |
|---|---|
| 轻度 | 口服NSAIDs(双氯芬酸钠75-100mg/日,吲哚美辛75mg/日) |
| 中度 | 泼尼松龙0.5-1mg/kg/日口服。有效后逐渐减量。 |
| 重症/坏死性 | 甲泼尼龙1g/日静脉冲击3天 + 免疫抑制剂 |
| 免疫抑制剂适应证 | 环磷酰胺(2mg/kg/日)或硫唑嘌呤(2mg/kg/日) |
| 难治性 | 生物制剂如利妥昔单抗、托珠单抗等 |
| 巩膜穿孔 | 保存角膜行板层角膜移植术或巩膜移植术 |
非甾体抗炎药对结节性和弥漫性巩膜炎可能有效,但坏死性巩膜炎需要更积极的免疫抑制治疗6)。
周边部角膜溃疡
Section titled “周边部角膜溃疡”- RA的全身控制:仅局部眼部治疗不够。必须与风湿科协作。
- 角膜保护:无防腐剂滴眼液和治疗性软性角膜接触镜(用于角膜保护)。
- 手术治疗:角膜穿孔时使用保存角膜行板层角膜移植术。
- 早期加强全身免疫抑制治疗对预防穿孔很重要10)。
与全身治疗的协作
Section titled “与全身治疗的协作”RA的全身治疗包括以下内容4)。
DMARDs(改善病情抗风湿药):
- 甲氨蝶呤(MTX)6~16mg/周是基础用药。联合叶酸可减轻副作用。
- 柳氮磺吡啶、布西拉明(瑞马替):用于不能耐受MTX的患者。
- 早期积极使用,以达标治疗策略实现DAS28缓解为目标。
生物制剂DMARDs:
- **抗TNF-α抗体:**英夫利西单抗、阿达木单抗、赛妥珠单抗、依那西普、戈利木单抗。
- **IL-6抑制剂:**托珠单抗(有报道对巩膜炎有效)。
- **T细胞共刺激抑制剂:**阿巴西普。
- **抗CD20抗体:**利妥昔单抗(有报道对难治性巩膜炎有效)。
- 注意严重感染和结核再激活风险。用药前必须进行筛查12)。
JAK抑制剂:
- 托法替布、巴瑞替尼、乌帕替尼。
- 近年来使用增加。有报道显示其疗效与生物制剂相当。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”RA的全身病理生理
Section titled “RA的全身病理生理”RA的发病涉及遗传易感性(HLA-DR4/DR1等)和环境因素(吸烟、牙周病菌导致的蛋白质瓜氨酸化等)的共同作用。产生针对瓜氨酸化蛋白的自身抗体(抗CCP抗体),作为免疫复合物沉积在关节内。
在滑膜中,组织破坏通过以下机制进行:
- T细胞、B细胞和巨噬细胞浸润滑膜
- 大量产生TNF-α、IL-1β、IL-6、IL-17等炎性细胞因子
- 血管新生导致血管翳(增厚的滑膜组织)形成
- 破骨细胞活化导致软骨破坏和骨侵蚀
眼部受累机制
Section titled “眼部受累机制”眼部病变是RA全身性血管炎和免疫反应在眼部的局部表现3)。
巩膜炎的机制:
- 免疫复合物沉积在巩膜血管→补体激活→中性粒细胞浸润→坏死性血管炎
- 肉芽肿性炎症(上皮样细胞、巨细胞)破坏巩膜实质
- MMP-1和MMP-3降解巩膜胶原蛋白
角膜边缘溃疡的机制:
- 免疫复合物沉积于角膜缘血管网(limbal plexus)
- III型超敏反应(Arthus反应)→补体和中性粒细胞介导的基质溶解
- MMP-1、MMP-2、MMP-9导致的胶原降解引起快速变薄
干燥性角结膜炎(合并干燥综合征)的机制:
- 以CD4阳性T细胞为主的淋巴细胞浸润泪腺和结膜杯状细胞
- 泪液分泌减少→角结膜上皮损伤→角结膜局部产生炎性细胞因子(IL-1β、TNF-α)→上皮损伤的恶性循环
- 继发性黏蛋白产生减少和泪膜破裂时间缩短
疾病活动性与眼部并发症的关系
Section titled “疾病活动性与眼部并发症的关系”巩膜炎和周边部角膜溃疡是RA的关节外表现之一,其加重和缓解与全身血管炎活动性平行。使用生物制剂或免疫抑制剂抑制RA疾病活动性也有助于改善眼部病变1)。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”生物制剂在眼部炎症中的应用
Section titled “生物制剂在眼部炎症中的应用”利妥昔单抗(抗CD20抗体)3)和托珠单抗(抗IL-6受体抗体)对难治性巩膜炎和周边部角膜溃疡的有效性已在病例报告和小规模研究中报道。通过生物制剂加强RA全身治疗可能有助于改善眼部并发症并预防复发。
抗TNF-α抗体诱导的葡萄膜炎
Section titled “抗TNF-α抗体诱导的葡萄膜炎”已有报道在使用抗TNF-α抗体期间出现矛盾性葡萄膜炎(脱髓鞘性葡萄膜炎样反应)的病例4)。需要在用药前后进行眼科监测,并在炎症加重时重新评估是否继续用药。
JAK抑制剂与眼部炎症
Section titled “JAK抑制剂与眼部炎症”JAK抑制剂(托法替布、巴瑞替尼等)作为RA全身治疗药物正逐渐普及,其对巩膜炎等眼部炎症的效果也在研究中。JAK-STAT通路通过IL-6和IFN-γ信号参与眼部炎症,有望应用于眼部局部治疗。
角膜生物工程与细胞疗法
Section titled “角膜生物工程与细胞疗法”对于严重的周边角膜溃疡穿孔病例,已尝试羊膜移植、人工角膜、培养角膜基质细胞移植等细胞工程方法。长期疗效评估仍是挑战。
8. 参考文献
Section titled “8. 参考文献”-
Sainz de la Maza M, Molina N, Gonzalez-Gonzalez LA, et al. Clinical characteristics of a large cohort of patients with scleritis and episcleritis. Ophthalmology. 2012;119(1):43-50.
-
Galor A, Thorne JE. Scleritis and peripheral ulcerative keratitis. Rheum Dis Clin North Am. 2007;33(4):835-854.
-
Artifoni M, Rothschild PR, Brézin A, et al. Ocular inflammatory diseases associated with rheumatoid arthritis. Nat Rev Rheumatol. 2014;10(2):108-116.
-
日本リウマチ学会 編. 関節リウマチ診療ガイドライン2020. メディカルレビュー社; 2021.
-
Akpek EK, Thorne JE, Qazi FA, Do DV, Jabs DA. Evaluation of patients with scleritis for systemic disease. Ophthalmology. 2004;111(3):501-506. doi:10.1016/j.ophtha.2003.06.006. PMID:15019326.
-
Jabs DA, Mudun A, Dunn JP, et al. Episcleritis and scleritis: clinical features and treatment results. Am J Ophthalmol. 2000;130(4):469-476.
-
Watson PG, Hayreh SS. Scleritis and episcleritis. Br J Ophthalmol. 1976;60(3):163-191.
-
Foster CS, Forstot SL, Wilson LA. Mortality rate in rheumatoid arthritis patients developing necrotizing scleritis or peripheral ulcerative keratitis. Ophthalmology. 1984;91(10):1253-1263.
-
Aletaha D, Neogi T, Silman AJ, et al. 2010 Rheumatoid arthritis classification criteria: an American College of Rheumatology/European League Against Rheumatism collaborative initiative. Arthritis Rheum. 2010;62(9):2569-2581.
-
Messmer EM, Foster CS. Vasculitic peripheral ulcerative keratitis. Surv Ophthalmol. 1999;43(5):379-396.
-
Smith JR, Mackensen F, Rosenbaum JT. Therapy insight: scleritis and its relationship to systemic autoimmune disease. Nat Clin Pract Rheumatol. 2007;3(4):219-226.
-
Bongartz T, Sutton AJ, Sweeting MJ, et al. Anti-TNF antibody therapy in rheumatoid arthritis and the risk of serious infections and malignancies. JAMA. 2006;295(19):2275-2285.
