乾性角結膜炎

類風濕性關節炎與眼部病變(乾眼症、鞏膜炎)
1. 類風濕性關節炎與眼部病變是什麼?
Section titled “1. 類風濕性關節炎與眼部病變是什麼?”類風濕性關節炎(rheumatoid arthritis; RA)是一種以關節滑膜為主要病變部位的慢性發炎性自體免疫疾病。它會引起肺、皮膚、眼睛等多種全身症狀,是膠原病中最常見的一種。
好發於30~60歲女性,男女比例約為1:3。老年發病時男性比例增加。日本盛行率估計約為人口的0.5~1%(約60~120萬人)。
約25~30%的RA患者出現某種眼部症狀1)。眼部併發症的發生率與RA病程、疾病活動性和關節外症狀的存在相關2)。
眼部併發症的分類
Section titled “眼部併發症的分類”RA相關的眼部病變分為以下五種類型。
| 眼部併發症 | 頻率 | 主要特徵 |
|---|---|---|
| 乾燥性角結膜炎(乾眼症) | 最常見 | 常合併乾燥症候群 |
| 鞏膜炎 | 較常見 | 眼痛、深層充血、可能出現壞死型 |
| 上鞏膜炎(表層鞏膜炎) | 較常見 | 表層發炎,有自然緩解傾向 |
| 周邊部角膜潰瘍 | 相對較少 | 快速角膜變薄及穿孔風險 |
| 虹膜睫狀體炎 | 罕見 | 前葡萄膜炎 |
惡性類風濕關節炎是一種伴有鞏膜炎、胸膜炎、間質性肺炎、心包炎、心肌炎、多發性單神經炎、腸繫膜動脈栓塞和指尖潰瘍的重症類型,預後不良。
2. 主要症狀與臨床所見
Section titled “2. 主要症狀與臨床所見”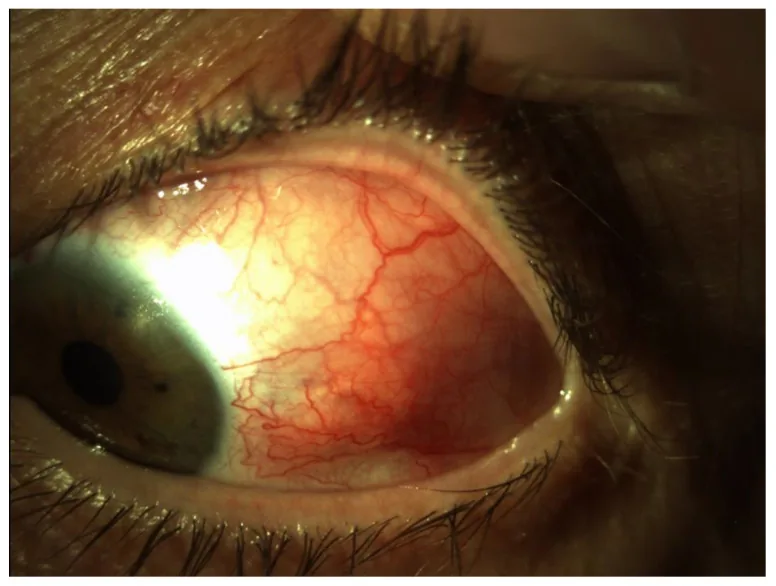
眼部併發症的種類不同,自覺症狀也不同。
- 乾燥性角結膜炎:眼乾澀感、異物感、畏光、眼疲勞、視力波動
- 鞏膜炎:劇烈眼痛(深部痛、搏動性)、充血、畏光、流淚
- 壞死性鞏膜炎(穿孔性鞏膜軟化症):可能無痛,需注意漏診
- 上鞏膜炎:區域性發紅、輕度疼痛、有自然緩解傾向
- 周邊部角膜潰瘍:充血、視力下降、穿孔時突發劇烈眼痛
臨床所見(眼科檢查所見)
Section titled “臨床所見(眼科檢查所見)”鞏膜炎
上鞏膜炎
周邊角膜潰瘍
鞏膜炎根據Watson分類分為前部鞏膜炎(瀰漫型、結節型、壞死型)和後部鞏膜炎,其中壞死型最為嚴重7)。約30%~50%的鞏膜炎患者合併全身性自體免疫疾病,以RA最為常見5)。
3. 原因與風險因素
Section titled “3. 原因與風險因素”RA的眼部病變是由自體免疫機制引起的全身性血管炎和肉芽腫性炎症波及鞏膜及角膜緣血管所致11)。
RA的病理生理與眼部波及
Section titled “RA的病理生理與眼部波及”- 自體免疫機制:滑膜淋巴細胞浸潤、血管新生、血管翳形成導致軟骨破壞和骨侵蝕。
- 發炎性細胞因子:TNF-α、IL-1β、IL-6、IL-17主導組織破壞。
- 眼部波及:免疫複合物沉積於鞏膜血管→補體活化及血管炎→肉芽腫性壞死性發炎
- 角膜邊緣部:邊緣血管網中的第三型過敏反應→MMP(基質金屬蛋白酶)產生→角膜實質膠原蛋白分解
- 淚腺功能低下:合併乾燥症候群的病例中,淋巴球浸潤導致淚腺及唾液腺分泌減少
眼部病變的風險因子
Section titled “眼部病變的風險因子”- RA病程長
- 類風濕因子(RF)高力價、抗CCP抗體陽性
- 伴有關節外表現(肺、皮膚、神經)的惡性RA
- 合併乾燥症候群(增加乾性角結膜炎風險)
- 疾病活動性高(DAS28高值)
- 吸菸
有報告指出,發生壞死性鞏膜炎或周邊部角膜潰瘍的患者10年存活率降低8),這些眼部病變可作為全身血管炎活動性的指標。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”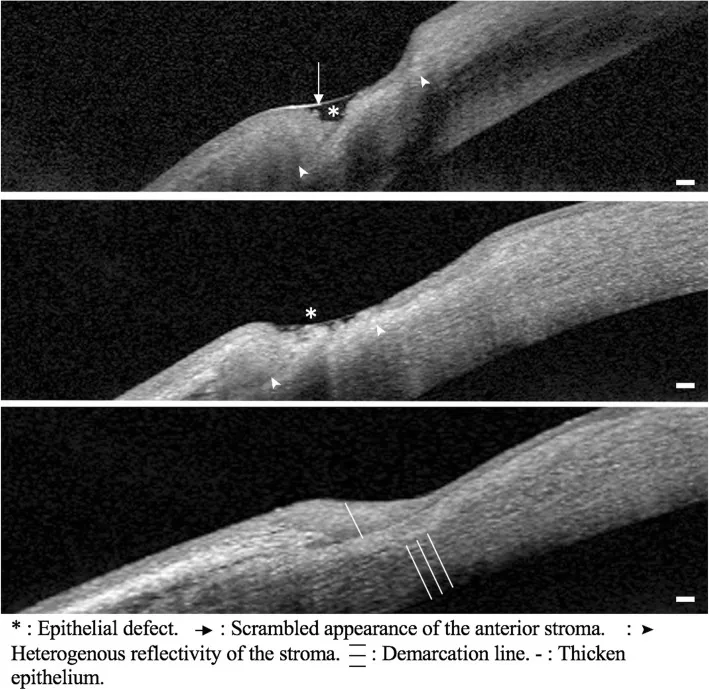
RA的診斷基於2010年ACR/EULAR分類標準9)。對關節腫脹數、血清學檢查(RF、抗CCP抗體)、症狀持續時間、急性期反應物(CRP、ESR)四個領域進行評分。
血液檢查中,ESR升高、CRP升高、RF陽性(約75%,約25%陰性)、抗CCP抗體、MMP-3升高對診斷有用4)。X光檢查中,手和手指的關節侵蝕和骨破壞是特徵性表現。
通過以下檢查評估眼部併發症。
| 檢查方法 | 評估對象 | 所見標準 |
|---|---|---|
| Schirmer試驗 | 淚液分泌量 | ≤5mm/5分鐘表示分泌減少 |
| 淚膜破裂時間(BUT) | 淚膜穩定性 | ≤5秒表示不穩定 |
| 裂隙燈顯微鏡 | 鞏膜、角膜、眼前段 | 檢查壞死性變化和角膜變薄 |
| 眼壓測量 | 青光眼、類固醇反應 | 使用類固醇時必須檢查 |
| 眼底檢查 | 後鞏膜炎、視乳頭水腫 | 排除後部病變 |
| B超掃描 | 後鞏膜炎 | T徵(Tenon囊水腫) |
| 眼眶MRI | 評估後鞏膜炎範圍 | 鞏膜增厚和增強效果 |
後鞏膜炎容易被忽略,可能表現為眼痛、視力下降、眼球突出和複視。B超掃描中的T徵對診斷有幫助。
對於鞏膜炎患者,建議進行系統性檢查,包括RF、ANA、ANCA、補體和胸部X光,以篩查全身性疾病5)。
強烈建議定期進行眼科篩查。鞏膜炎和周邊角膜潰瘍的早期發現和早期治療直接影響視力預後。特別是在RA疾病活動性高或惡性RA期間,即使沒有症狀,眼科篩查也很重要。此外,使用羥氯喹的患者需要定期監測視網膜毒性。
5. 標準治療方法
Section titled “5. 標準治療方法”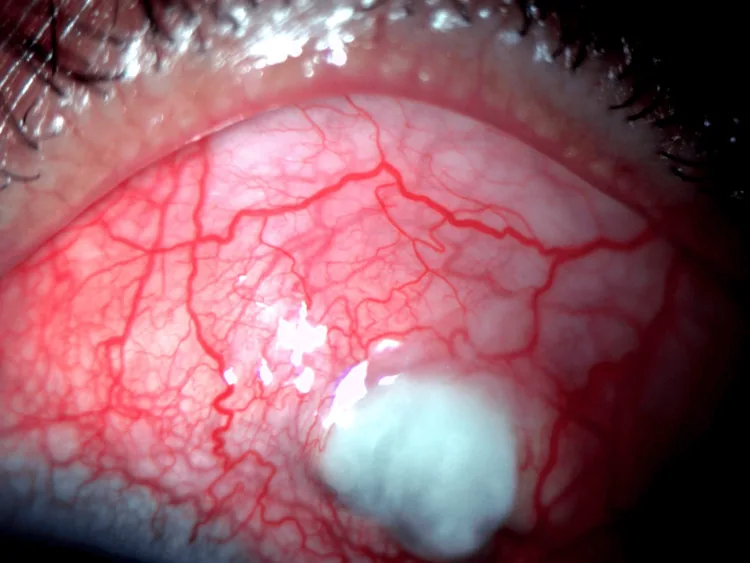
RA眼部病變的治療需要眼科局部治療和內科(風濕科)全身治療相結合。
乾燥性角結膜炎
Section titled “乾燥性角結膜炎”對於輕至中度乾燥性角結膜炎,逐步應用以下方法:
- 人工淚液點眼:選擇不含防腐劑的製劑(長期使用以避免防腐劑引起的角膜毒性)。
- 0.1%玻尿酸鈉滴眼液:每日5-6次(角膜保護、淚液穩定)
- 淚點栓塞術:對中度以上病例有效。放置於上下淚點。
- 3%地夸磷索鈉滴眼液:每日6次。促進水分和黏蛋白分泌。
- 瑞巴派特滴眼液:增強黏蛋白產生。對合併乾燥症候群的病例有用。
合併乾燥症候群的病例,乾眼症往往更嚴重,可考慮加用環孢素滴眼液。
- NSAIDs滴眼和口服:氟比洛芬滴眼液、雙氯芬酸滴眼液。輕度病例首選。
- 多數局灶性上鞏膜炎可自行緩解,但反覆發作的病例應評估全身性疾病活動性。
| 嚴重程度 | 治療選擇 |
|---|---|
| 輕度 | 口服NSAIDs(雙氯芬酸鈉75-100mg/日,吲哚美辛75mg/日) |
| 中度 | 潑尼松龍0.5-1mg/kg/日口服。有效後逐漸減量。 |
| 重症/壞死性 | 甲基潑尼松龍1g/日靜脈脈衝3天 + 免疫抑制劑 |
| 免疫抑制劑適應症 | 環磷醯胺(2mg/kg/日)或硫唑嘌呤(2mg/kg/日) |
| 難治性 | 生物製劑如利妥昔單抗、托珠單抗等 |
| 鞏膜穿孔 | 保存角膜行板層角膜移植術或鞏膜移植術 |
非類固醇抗發炎藥對結節性和瀰漫性鞏膜炎可能有效,但壞死性鞏膜炎需要更積極的免疫抑制治療6)。
周邊部角膜潰瘍
Section titled “周邊部角膜潰瘍”- RA的全身控制:僅局部眼部治療不夠。必須與風濕科協作。
- 角膜保護:無防腐劑眼藥水和治療性軟式隱形眼鏡(用於角膜保護)。
- 手術治療:角膜穿孔時使用保存角膜行板層角膜移植術。
- 早期加強全身免疫抑制治療對預防穿孔很重要10)。
與全身治療的協作
Section titled “與全身治療的協作”RA的全身治療包括以下內容4)。
DMARDs(疾病修飾抗風濕藥物):
- 甲氨蝶呤(MTX)6~16mg/週為基礎用藥。併用葉酸可減輕副作用。
- 柳氮磺吡啶、布西拉明(瑞馬替):用於無法耐受MTX的患者。
- 早期積極使用,以達標治療策略達到DAS28緩解為目標。
生物製劑DMARDs:
- **抗TNF-α抗體:**英夫利西單抗、阿達木單抗、賽妥珠單抗、依那西普、戈利木單抗。
- **IL-6抑制劑:**托珠單抗(有報告對鞏膜炎有效)。
- **T細胞共刺激抑制劑:**阿巴西普。
- **抗CD20抗體:**利妥昔單抗(有報告對難治性鞏膜炎有效)。
- 注意嚴重感染和結核再活化風險。給藥前必須進行篩查12)。
JAK抑制劑:
- 托法替布、巴瑞替尼、烏帕替尼。
- 近年來使用增加。有報告顯示其療效與生物製劑相當。
6. 病理生理學與詳細發病機制
Section titled “6. 病理生理學與詳細發病機制”RA的全身病理生理
Section titled “RA的全身病理生理”RA的發病涉及遺傳易感性(HLA-DR4/DR1等)和環境因素(吸煙、牙周病菌導致的蛋白瓜氨酸化等)的共同作用。產生針對瓜氨酸化蛋白的自體抗體(抗CCP抗體),作為免疫複合物沉積在關節內。
在滑膜中,組織破壞通過以下機制進行:
- T細胞、B細胞和巨噬細胞浸潤滑膜
- 大量產生TNF-α、IL-1β、IL-6、IL-17等炎性細胞因子
- 血管新生導致血管翳(增厚的滑膜組織)形成
- 破骨細胞活化導致軟骨破壞和骨侵蝕
眼部受累機制
Section titled “眼部受累機制”眼部病變是RA全身性血管炎和免疫反應在眼部的局部表現3)。
鞏膜炎的機制:
- 免疫複合物沉積在鞏膜血管→補體激活→中性球浸潤→壞死性血管炎
- 肉芽腫性炎症(類上皮細胞、巨細胞)破壞鞏膜實質
- MMP-1和MMP-3降解鞏膜膠原蛋白
角膜邊緣潰瘍的機轉:
- 免疫複合物沉積於角膜緣血管網(limbal plexus)
- 第三型過敏反應(Arthus反應)→補體及嗜中性球介導的基質溶解
- MMP-1、MMP-2、MMP-9導致的膠原蛋白分解引起快速變薄
乾性角結膜炎(合併乾燥症候群)的機轉:
- 以CD4陽性T細胞為主的淋巴球浸潤淚腺及結膜杯狀細胞
- 淚液分泌減少→角結膜上皮損傷→角結膜局部產生發炎性細胞激素(IL-1β、TNF-α)→上皮損傷的惡性循環
- 繼發性黏蛋白分泌減少及淚膜破裂時間縮短
疾病活動性與眼部併發症的關聯
Section titled “疾病活動性與眼部併發症的關聯”鞏膜炎及周邊部角膜潰瘍是RA的關節外表現之一,其惡化與緩解與全身血管炎活動性平行。使用生物製劑或免疫抑制劑抑制RA疾病活動性亦有助於改善眼部病變1)。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”生物製劑在眼部發炎中的應用
Section titled “生物製劑在眼部發炎中的應用”利妥昔單抗(抗CD20抗體)3)和托珠單抗(抗IL-6受體抗體)對難治性鞏膜炎及周邊部角膜潰瘍的有效性已在病例報告和小型研究中報導。透過生物製劑加強RA全身治療可能有助於改善眼部併發症並預防復發。
抗TNF-α抗體誘發的葡萄膜炎
Section titled “抗TNF-α抗體誘發的葡萄膜炎”已有報告指出在使用抗TNF-α抗體期間出現矛盾性葡萄膜炎(脫髓鞘性葡萄膜炎樣反應)的病例4)。需要在給藥前後進行眼科監測,並在發炎惡化時重新評估是否繼續給藥。
JAK抑制劑與眼部發炎
Section titled “JAK抑制劑與眼部發炎”JAK抑制劑(托法替布、巴瑞替尼等)作為RA全身治療藥物逐漸普及,其對鞏膜炎等眼部發炎的效果也在研究中。JAK-STAT路徑透過IL-6和IFN-γ訊息傳導參與眼部發炎,有望應用於眼部局部治療。
角膜生物工程與細胞療法
Section titled “角膜生物工程與細胞療法”對於嚴重的周邊角膜潰瘍穿孔病例,已嘗試羊膜移植、人工角膜、培養角膜基質細胞移植等細胞工程方法。長期療效評估仍是挑戰。
8. 參考文獻
Section titled “8. 參考文獻”-
Sainz de la Maza M, Molina N, Gonzalez-Gonzalez LA, et al. Clinical characteristics of a large cohort of patients with scleritis and episcleritis. Ophthalmology. 2012;119(1):43-50.
-
Galor A, Thorne JE. Scleritis and peripheral ulcerative keratitis. Rheum Dis Clin North Am. 2007;33(4):835-854.
-
Artifoni M, Rothschild PR, Brézin A, et al. Ocular inflammatory diseases associated with rheumatoid arthritis. Nat Rev Rheumatol. 2014;10(2):108-116.
-
日本リウマチ学会 編. 関節リウマチ診療ガイドライン2020. メディカルレビュー社; 2021.
-
Akpek EK, Thorne JE, Qazi FA, Do DV, Jabs DA. Evaluation of patients with scleritis for systemic disease. Ophthalmology. 2004;111(3):501-506. doi:10.1016/j.ophtha.2003.06.006. PMID:15019326.
-
Jabs DA, Mudun A, Dunn JP, et al. Episcleritis and scleritis: clinical features and treatment results. Am J Ophthalmol. 2000;130(4):469-476.
-
Watson PG, Hayreh SS. Scleritis and episcleritis. Br J Ophthalmol. 1976;60(3):163-191.
-
Foster CS, Forstot SL, Wilson LA. Mortality rate in rheumatoid arthritis patients developing necrotizing scleritis or peripheral ulcerative keratitis. Ophthalmology. 1984;91(10):1253-1263.
-
Aletaha D, Neogi T, Silman AJ, et al. 2010 Rheumatoid arthritis classification criteria: an American College of Rheumatology/European League Against Rheumatism collaborative initiative. Arthritis Rheum. 2010;62(9):2569-2581.
-
Messmer EM, Foster CS. Vasculitic peripheral ulcerative keratitis. Surv Ophthalmol. 1999;43(5):379-396.
-
Smith JR, Mackensen F, Rosenbaum JT. Therapy insight: scleritis and its relationship to systemic autoimmune disease. Nat Clin Pract Rheumatol. 2007;3(4):219-226.
-
Bongartz T, Sutton AJ, Sweeting MJ, et al. Anti-TNF antibody therapy in rheumatoid arthritis and the risk of serious infections and malignancies. JAMA. 2006;295(19):2275-2285.
