乾性角結膜炎
Schirmer試験:5mm/5分以下で分泌低下。
BUT(涙液破壊時間):5秒以下で不安定涙液層。
フルオレセイン染色:下方角膜・結膜の点状上皮障害。

関節リウマチ(rheumatoid arthritis; RA)は、関節滑膜を病変の主座とする慢性炎症性自己免疫疾患である。肺・皮膚・眼など全身に多彩な症状を呈し、膠原病のなかで最も頻度が高い。
30〜60歳の女性に好発し、男女比は約1:3である。高齢発症では男性の比率が増加する。日本の有病率は人口の約0.5〜1%(約60〜120万人)と推計される。
RA患者の約25〜30%に何らかの眼症状を認める1)。眼合併症の頻度はRA罹病期間・疾患活動性・関節外症状の有無に関連する2)。
RAに合併する眼病変は以下の5型に分類される。
| 眼合併症 | 頻度 | 主な特徴 |
|---|---|---|
| 乾性角結膜炎(ドライアイ) | 最多 | Sjögren症候群合併例が多い |
| 強膜炎 | 比較的多い | 眼痛・深層充血・壊死性形態あり |
| 上強膜炎(エピスクレラ炎) | 比較的多い | 表層性炎症・自然軽快傾向 |
| 周辺部角膜潰瘍 | 比較的少ない | 急速な角膜菲薄化・穿孔リスク |
| 虹彩毛様体炎 | 稀 | 前部ぶどう膜炎 |
悪性リウマチとは、強膜炎・胸膜炎・間質性肺炎・心膜炎・心筋炎・多発性単神経炎・腸間動脈塞栓症・指尖潰瘍を伴う重症型であり、予後が不良である。
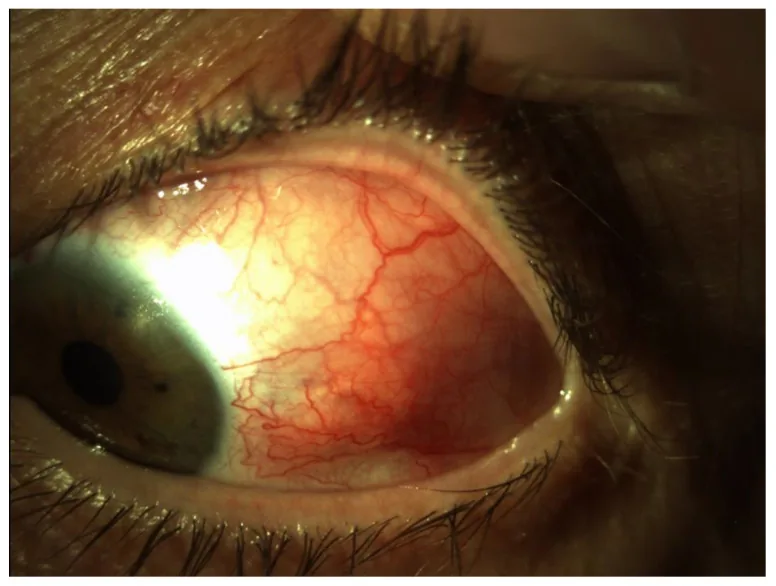
眼合併症の種類によって自覚症状は異なる。
乾性角結膜炎
Schirmer試験:5mm/5分以下で分泌低下。
BUT(涙液破壊時間):5秒以下で不安定涙液層。
フルオレセイン染色:下方角膜・結膜の点状上皮障害。
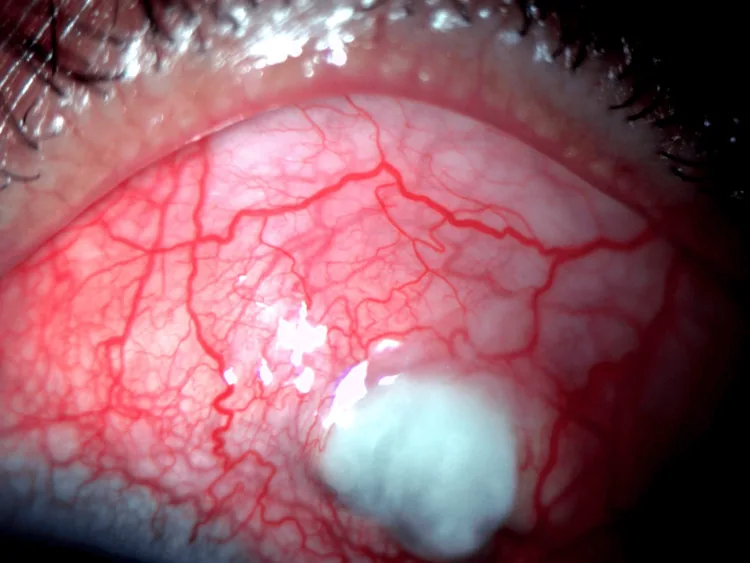
強膜炎
上強膜炎
周辺部角膜潰瘍
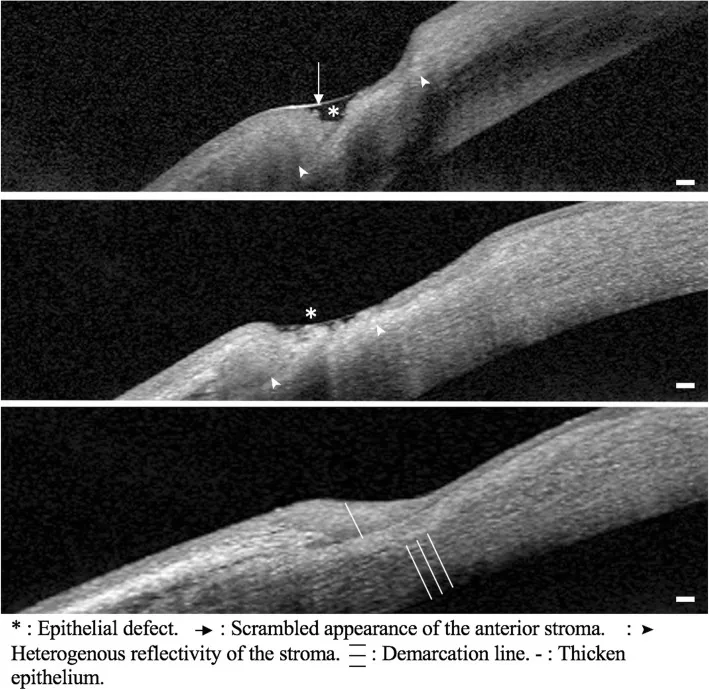
部位:角膜輪部から1〜2mmに沿った溝状菲薄化。
進行:弦月形に周方向に拡大し、急速に穿孔に至ることがある。
蛍光染色:上皮欠損部にフルオレセイン陽性。
強膜炎の分類はWatson分類に基づく前部強膜炎(びまん性・結節性・壊死性)と後部強膜炎に分けられ、壊死性が最も重篤である7)。強膜炎患者のうち約30〜50%に全身性自己免疫疾患を合併し、RAが最多である5)。
RAの眼病変は、自己免疫機序による全身性血管炎と肉芽腫性炎症が強膜・角膜辺縁部血管に波及することで生じる11)。
壊死性強膜炎や周辺部角膜潰瘍を発症した患者は、10年生存率が低下するとの報告があり8)、これらの眼病変は全身の血管炎活動性の指標となる。
RAの診断は2010年ACR/EULAR分類基準に基づく9)。関節の腫脹数・血清学的検査(RF・抗CCP抗体)・症状持続期間・急性期反応物質(CRP・赤沈)の4ドメインを点数化する。
血液検査では赤沈亢進・CRP上昇・RF陽性(約75%、約25%では陰性)・抗CCP抗体・MMP-3上昇が診断に有用である4)。X線検査では手・指の関節びらん・骨侵食像が特徴的である。
以下の検査により眼合併症を評価する。
| 検査法 | 評価対象 | 所見の目安 |
|---|---|---|
| Schirmer試験 | 涙液分泌量 | 5mm/5分以下で分泌低下 |
| 涙液破壊時間(BUT) | 涙液安定性 | 5秒以下で不安定 |
| 細隙灯顕微鏡 | 強膜・角膜・前眼部 | 壊死性変化・角膜菲薄化の確認 |
| 眼圧測定 | 緑内障・ステロイド応答 | ステロイド使用時は必須 |
| 眼底検査 | 後部強膜炎・乳頭浮腫 | 後部病変の除外 |
| Bスキャン超音波 | 後部強膜炎 | T-sign(テノン嚢水腫) |
| MRI眼窩 | 後部強膜炎の範囲評価 | 強膜の肥厚・増強効果 |
後部強膜炎は見逃されやすく、眼痛・視力低下・眼球突出・複視を呈することがある。Bスキャン超音波でのT-signが診断に有用である。
強膜炎患者では全身性疾患の精査として、RF・ANA・ANCA・補体・胸部X線等の系統的検索が推奨される5)。
定期的な眼科検診が強く推奨される。強膜炎や周辺部角膜潰瘍は早期発見・早期治療が視力予後に直結する。特にRA疾患活動性が高い時期や悪性RAでは、症状がなくても眼科的スクリーニングが重要である。また、ヒドロキシクロロキン使用患者では網膜毒性の定期モニタリングも必要となる。
RAの眼病変治療は眼科的局所治療と内科(リウマチ科)の全身治療の両輪で行う。
軽症から中等症の乾性角結膜炎には以下を段階的に適用する。
Sjögren症候群合併例ではドライアイが重症化しやすく、シクロスポリン点眼液の追加を検討する場合がある。
| 重症度 | 治療選択 |
|---|---|
| 軽症 | NSAIDs内服(ジクロフェナクナトリウム 75〜100mg/日、インドメタシン 75mg/日) |
| 中等症 | プレドニゾロン0.5〜1mg/kg/日 経口投与。有効後に漸減 |
| 重症・壊死性 | メチルプレドニゾロン1g/日 3日間静注パルス療法 + 免疫抑制薬 |
| 免疫抑制薬適応 | シクロホスファミド(2mg/kg/日)またはアザチオプリン(2mg/kg/日) |
| 難治性 | リツキシマブ・トシリズマブ等の生物学的製剤 |
| 強膜穿孔 | 保存角膜による表層角膜移植術・強膜移植術 |
結節性・びまん性強膜炎では非ステロイド性抗炎症薬が有効なことがあるが、壊死性強膜炎に対してはより積極的な免疫抑制療法が必要となる6)。
RAの全身治療として以下を適用する4)。
DMARDs(疾患修飾性抗リウマチ薬):
生物学的DMARDs:
JAK阻害薬:
RA発症には遺伝的素因(HLA-DR4/DR1等)と環境因子(喫煙・歯周病菌による蛋白シトルリン化等)が複合して関与する。シトルリン化蛋白に対する自己抗体(抗CCP抗体)が産生され、免疫複合体として関節内に沈着する。
滑膜では以下の機序で組織破壊が進行する。
眼病変はRA全身の血管炎・免疫反応の眼局所における発現である3)。
強膜炎の機序:
角膜辺縁部潰瘍の機序:
乾性角結膜炎(Sjögren症候群合併)の機序:
強膜炎・周辺部角膜潰瘍はRA関節外症状の一つであり、全身の血管炎活動性と並行して増悪・寛解する。生物学的製剤や免疫抑制薬によるRAの疾患活動性抑制は、眼病変の改善にも寄与する1)。
難治性強膜炎・周辺部角膜潰瘍に対するリツキシマブ(抗CD20抗体)3)やトシリズマブ(抗IL-6受容体抗体)の有効性が症例報告・小規模研究で報告されている。生物学的製剤によるRA全身治療の強化が眼合併症の改善・再発抑制に貢献する可能性がある。
抗TNF-α抗体投与中に逆説的なぶどう膜炎(demyelinating uveitis-like reaction)が発症する症例が報告されている4)。投与前後の眼科的モニタリングと、炎症増悪時には投与継続の可否を再検討する必要がある。
JAK阻害薬(トファシチニブ・バリシチニブ等)はRA全身治療薬として普及しつつあり、強膜炎等の眼炎症への効果についても研究が進んでいる。JAK-STAT経路はIL-6・IFN-γシグナルを介した眼炎症に関与しており、眼局所への応用が期待される。
重篤な周辺部角膜潰瘍の穿孔例に対し、羊膜移植・人工角膜・培養角膜実質細胞移植などの細胞工学的アプローチが試みられている。長期成績の評価が課題である。
Sainz de la Maza M, Molina N, Gonzalez-Gonzalez LA, et al. Clinical characteristics of a large cohort of patients with scleritis and episcleritis. Ophthalmology. 2012;119(1):43-50.
Galor A, Thorne JE. Scleritis and peripheral ulcerative keratitis. Rheum Dis Clin North Am. 2007;33(4):835-854.
Artifoni M, Rothschild PR, Brézin A, et al. Ocular inflammatory diseases associated with rheumatoid arthritis. Nat Rev Rheumatol. 2014;10(2):108-116.
日本リウマチ学会 編. 関節リウマチ診療ガイドライン2020. メディカルレビュー社; 2021.
Akpek EK, Thorne JE, Qazi FA, Do DV, Jabs DA. Evaluation of patients with scleritis for systemic disease. Ophthalmology. 2004;111(3):501-506. doi:10.1016/j.ophtha.2003.06.006. PMID:15019326.
Jabs DA, Mudun A, Dunn JP, et al. Episcleritis and scleritis: clinical features and treatment results. Am J Ophthalmol. 2000;130(4):469-476.
Watson PG, Hayreh SS. Scleritis and episcleritis. Br J Ophthalmol. 1976;60(3):163-191.
Foster CS, Forstot SL, Wilson LA. Mortality rate in rheumatoid arthritis patients developing necrotizing scleritis or peripheral ulcerative keratitis. Ophthalmology. 1984;91(10):1253-1263.
Aletaha D, Neogi T, Silman AJ, et al. 2010 Rheumatoid arthritis classification criteria: an American College of Rheumatology/European League Against Rheumatism collaborative initiative. Arthritis Rheum. 2010;62(9):2569-2581.
Messmer EM, Foster CS. Vasculitic peripheral ulcerative keratitis. Surv Ophthalmol. 1999;43(5):379-396.
Smith JR, Mackensen F, Rosenbaum JT. Therapy insight: scleritis and its relationship to systemic autoimmune disease. Nat Clin Pract Rheumatol. 2007;3(4):219-226.
Bongartz T, Sutton AJ, Sweeting MJ, et al. Anti-TNF antibody therapy in rheumatoid arthritis and the risk of serious infections and malignancies. JAMA. 2006;295(19):2275-2285.