Grado 1
Diámetro máximo del edema: ≤3 mm
Características de la lesión: Edema estromal localizado, limitado a una parte de la córnea.

El hidrops corneal agudo (ACH) es una complicación rara de los trastornos ectásicos corneales. Es una condición en la que una rotura en la membrana de Descemet y el endotelio corneal permite que el humor acuoso fluya rápidamente hacia el estroma corneal, causando edema corneal agudo.
La enfermedad subyacente más común es el queratocono, pero también ocurre en el queratoglobo y la degeneración marginal pelúcida (PMD).
Las tasas de incidencia son las siguientes1):
La edad de inicio varía de 5 a 59 años, con un pico entre los 20 y 40 años1). El riesgo en hombres es hasta el doble que en mujeres. También se observan diferencias étnicas, con mayor prevalencia en isleños del Pacífico en Nueva Zelanda y en personas del sur de Asia y negras en el Reino Unido.
Hallazgos recientes indican que el hidrops corneal agudo (ACH) no ocurre solo con un defecto de la membrana de Descemet; también es necesario un defecto en el estroma corneal posterior. Un informe señaló que el ACH no ocurrió en 16 ojos con defectos de la membrana de Descemet durante DMEK, pero ocurrió en los 5 ojos con perforación del estroma posterior 1).
Se reporta que ocurre en aproximadamente el 2.4–3% de los pacientes con queratocono, 6–11.5% de los pacientes con degeneración marginal pelúcida corneal y alrededor del 11% de los pacientes con queratoglobo 1). El riesgo es mayor cuanto más grave es la ectasia corneal, y se necesita especial atención en pacientes con el hábito de frotarse los ojos.
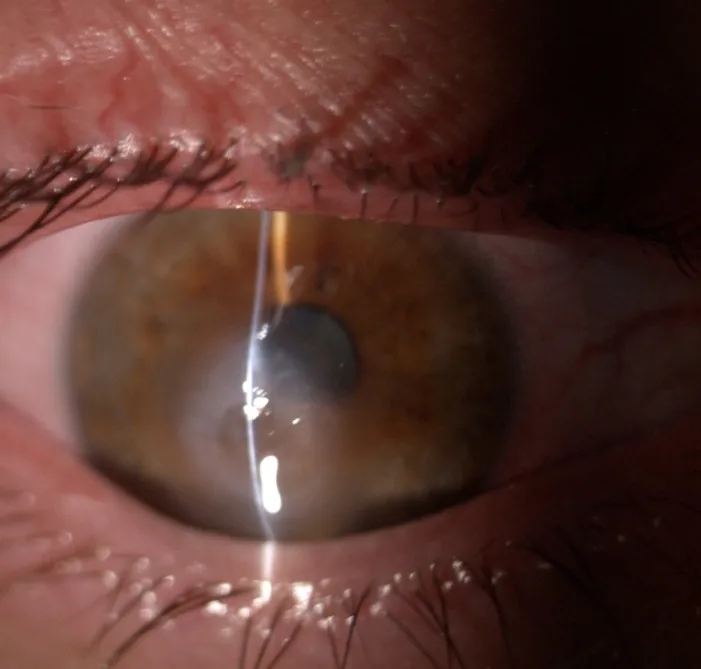
Los principales síntomas subjetivos del ACH son los siguientes.
Los desencadenantes incluyen acciones que aumentan temporalmente la presión intraocular, como frotarse los ojos, estornudar, toser, sonarse la nariz y el ejercicio vigoroso. A menudo ocurre espontáneamente.
En la lámpara de hendidura se observan hiperemia conjuntival, edema estromal corneal, edema epitelial, hendiduras intraestromales (intrastromal clefts) y ampollas epiteliales1).
La clasificación por grados según la extensión del edema se muestra a continuación1).
Grado 1
Diámetro máximo del edema: ≤3 mm
Características de la lesión: Edema estromal localizado, limitado a una parte de la córnea.
Grado 2
Diámetro máximo del edema: 3–5 mm
Características de la lesión: Extensión moderada del edema, puede afectar el eje visual.
Grado 3
Diámetro máximo del edema: >5 mm
Características de la lesión: Edema extenso, que presenta opacidad severa incluyendo el eje visual. El caso más joven (niña de 5 años) reportó edema corneal total de limbo a limbo8).
Para la evaluación de la transparencia corneal, también se utiliza una clasificación de 5 grados desde Grado 0 (cámara anterior e iris completamente invisibles) hasta Grado 4 (completamente transparente)1).
La OCT de segmento anterior (AS-OCT) puede visualizar de forma no invasiva la rotura y desprendimiento de la membrana de Descemet, las hendiduras de líquido intraestromal (intrastromal fluid clefts) y el aumento del grosor corneal1). El tamaño y la profundidad del desgarro son predictores del tiempo de resolución de la ACH. La prueba de Seidel puede ser positiva, pero esto se debe a la fuga de humor acuoso desde la córnea edematosa, no a una perforación.
Se han reportado casos de ACH en pacientes con oftalmopatía de Graves, y la elevación de la presión intraocular y la inflamación de la superficie ocular pueden ser factores de riesgo7).
En cuanto al riesgo de infección, un informe indica que el 2.7% (3/112 casos) de los casos de ACH se complicaron con queratitis infecciosa 5). Todos los casos complicados fueron varones con dermatitis atópica grave, con una edad promedio de 46 años. Los cultivos detectaron MSCNS y MSSA.
Frotarse el ojo aplica una fuerza mecánica sobre la membrana de Descemet, y en una córnea ya adelgazada y ectásica, puede desencadenar directamente una rotura de la membrana de Descemet 1). Los pacientes con dermatitis atópica tienen un riesgo particularmente alto porque tienden a frotarse los ojos debido al picor. Si hay picor, es importante controlar los síntomas con gotas oftálmicas u otros medicamentos.
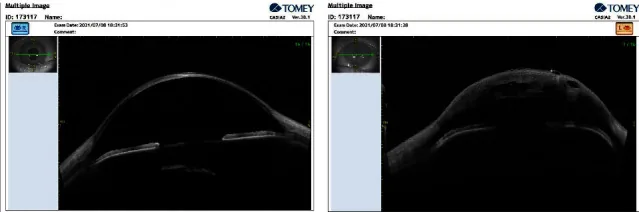
El diagnóstico de HCA se basa en los hallazgos clínicos y se complementa con diversas pruebas de imagen.
Es la base del diagnóstico. Se identifican inyección conjuntival, edema estromal, edema epitelial y hendiduras intraestromales 1). Se realiza una prueba de Seidel para diferenciar de la perforación.
A continuación se muestran las características de las principales modalidades de exploración.
| Método de exploración | Contenido principal de evaluación | Características |
|---|---|---|
| AS-OCT | Ruptura de DM, hendiduras estromales | Sin contacto, cuantitativo |
| Microscopía ultrasónica biomicroscópica | Sitio de ruptura, grosor corneal | Monitoreo de resolución |
| Microscopía confocal in vivo (IVCM) | Células inflamatorias, edema | Evaluación a nivel celular |
El tratamiento de la ACH comienza con manejo conservador; se considera tratamiento quirúrgico si la mejoría es escasa o se necesita una resolución temprana.
Se utilizan los siguientes medicamentos1)9).
La resolución espontánea con tratamiento conservador toma de 2 a 4 meses (máximo 5 a 36 semanas)1). En ojos sometidos a cross-linking corneal (CXL), la resolución es significativamente más rápida, reportándose resolución completa en 3 semanas7).
Se realiza para promover la resolución temprana, aliviar los síntomas y minimizar la cicatrización corneal.
Inyección de gas en la cámara anterior
Descemetopexia neumática: Se inyecta aire, SF6 o C3F8 en la cámara anterior para desplegar y reaplicar el borde de la membrana de Descemet mediante un efecto de taponamiento 1).
Tiempo de resolución: 2 a 7 semanas (significativamente más corto que los 64 a 117 días del tratamiento conservador).
Frecuencia de reinyección: Aire 77.8%, SF6 66.7%, C3F8 0 a 35.7% requieren reinyección.
Suturas de compresión
Suturas de compresión: Las suturas comprimen y cierran el desgarro de la membrana de Descemet. Incluye suturas de espesor total (FTS) y suturas de espesor parcial (PTS) 2).
Tiempo de resolución: La revisión de la literatura reporta de 1 hora a 45 días; la mayoría dentro de las 2 semanas 2).
Combinado con aire intracameral: Se ha reportado resolución completa en 2 semanas con 3 FTS más aire (50% de llenado de la cámara anterior) 3).
Trasplante de córnea
Queratoplastia endotelial automatizada con descemetorrexis (DSAEK)/Queratoplastia endotelial de membrana de Descemet (DMEK): Se considera para desgarros grandes de la membrana de Descemet 1).
Queratoplastia lamelar anterior profunda (pDALK): Puede lograr el cierre de la DM, la recuperación de la curvatura corneal y la recuperación visual en una sola cirugía.
Queratoplastia penetrante (PKP): Se realiza para cicatrices visualmente significativas después de ACH. La supervivencia del injerto a largo plazo después de ACH es menor que en casos sin ACH 3).
Se muestra un ejemplo representativo de prescripción de gotas oftálmicas después de suturas de compresión 3).
| Medicamento | Dosis/Frecuencia |
|---|---|
| moxifloxacino 0.5% | 4 veces al día |
| acetato de prednisolona 1% | reducir gradualmente según sea necesario |
| NaCl 5% | una vez al acostarse |
Muchos casos se resuelven en 2 a 4 meses solo con tratamiento conservador 1). Sin embargo, después de la resolución pueden persistir cicatrices corneales y neovascularización, lo que lleva a un deterioro visual permanente. La inyección de gas intracameral o las suturas de compresión pueden acortar la resolución a aproximadamente 2 semanas y minimizar la formación de cicatrices. Es importante discutir las opciones de tratamiento con su médico.
Es una cirugía en la que se inyecta aire o un gas especial (SF6, C3F8, etc.) en la cámara anterior, y su efecto de taponamiento sostiene la rotura de la membrana de Descemet desde el interior para promover la readhesión 1). Puede acortar el tiempo de resolución de 64–117 días con tratamiento conservador a 2–7 semanas. Sin embargo, puede ocurrir glaucoma por bloqueo pupilar o la necesidad de reinyección.
Tradicionalmente, se ha asumido la siguiente vía: microtraumatismo como frotarse el ojo → rotura de la membrana de Descemet → penetración del humor acuoso en el estroma → separación de las capas lamelares → edema 1).
Estudios recientes han demostrado que el defecto de la membrana de Descemet por sí solo no causa ACH; también es esencial un defecto en el estroma corneal posterior 1). Este hallazgo es importante para explicar por qué la ACH ocurre solo en casos de ectasia corneal severa.
En especímenes de trasplante de córnea de espesor total (PKP) de córneas con ACH, se observan lamelas estromales poco compactadas. La laminina y el colágeno tipo IV se localizan adyacentes a la membrana de Descemet enrollada, y se cree que esto juega un papel importante en la migración y reendotelización de las células endoteliales 1).
El tercio anterior del estroma corneal permanece ligeramente hinchado debido al entrecruzamiento lamelar. Los dos tercios posteriores consisten en fibrillas unidireccionales no entrelazadas y pueden hincharse hasta tres veces 7).
Las células endoteliales corneales adyacentes migran hacia el área de rotura de la membrana de Descemet, restauran la función de bomba endotelial, lo que lleva a la deshidratación corneal, y finalmente la reparación se completa mediante la formación de cicatriz 1). Las suturas de compresión aproximan físicamente los bordes de la membrana de Descemet, promoviendo la migración de células endoteliales.
Estudios con microscopía confocal in vivo han mostrado que los casos donde las células inflamatorias persisten más de 4 semanas tienen un alto riesgo de neovascularización corneal 1).
Varshney et al. (2021) reportaron un caso de AHC que complicó una queratitis después de CXL 7). En la córnea tratada con CXL, la resolución ocurrió rápidamente en 21 días, significativamente más corta que los 2–4 meses habituales. Se sugirió que el mecanismo es el aumento del entrecruzamiento de colágeno por CXL → aumento de la fuerza cohesiva interlamelar en el estroma anterior → aumento de la resistencia a la hinchazón. Las córneas entrecruzadas tienen mayor resistencia a la digestión enzimática, lo que se cree que contribuye a la resolución temprana.
Se ha reportado una técnica que utiliza OCT intraoperatorio (iOCT) para ajustar la profundidad y tensión de la sutura en tiempo real.
Kaur et al. (2025) realizaron suturas de compresión de espesor parcial guiadas por iOCT (PTS, profundidad objetivo 50–60%) en 7 casos (mediana de edad 16 años, grosor corneal preoperatorio 1120–2363 μm)2). La sutura se realizó mientras se confirmaba la compactación estromal con apariencia de “oruga” mediante iOCT; todos los casos se resolvieron en 2 semanas y las suturas se retiraron después de 8–12 semanas. La PTS mostró una eficacia comparable a las suturas de espesor total (FTS) con un menor riesgo de daño endotelial.
Una revisión de la literatura (19 estudios) informó que el tiempo de resolución de las suturas de compresión varió de 1 hora a 45 días, y la mayoría se resolvió dentro de las 2 semanas2).
Liu et al. informaron un procedimiento en dos etapas: epiqueratofaquia asistida por TKP (primera etapa para reparación de la membrana de Descemet) seguida de DALK con el mismo injerto (segunda etapa) después de 2.1±0.7 meses para lograr la recuperación visual2).
Petrelli et al. realizaron una resección en cuña lamelar para la perforación corneal después de ACH cuando la adhesión con cianoacrilato no tuvo éxito2). Esto logró una mejora refractiva evitando el trasplante de córnea.
Alio et al. realizaron una inyección en cámara anterior de 0,3 ml de plasma rico en plaquetas enriquecido (EPRP) en casos refractarios a SF6, logrando la resolución en una semana 1). Se supuso que el mecanismo era la promoción de la regeneración de células endoteliales por factores de crecimiento.
Para casos con desgarros grandes de la membrana de Descemet, se ha informado un método que utiliza un parche DMEK pequeño de 5 mm de diámetro para sellar temporalmente el desgarro 1). Se han reportado casos en los que la córnea logró deturgencia natural incluso después del desprendimiento parcial del injerto.
Ontiveros-Holguín & Pacheco-Padrón (2022) reportaron un caso de ACH y migración de ICRS después de la implantación de segmentos de anillo intracorneales (ICRS) 8). Se resolvió después de 8 semanas solo con tratamiento conservador. Se considera el primer informe de ACH después de la implantación de ICRS que se recupera solo con manejo conservador.
Es una sutura de compresión realizada mientras se confirma la profundidad y la tensión de la sutura en tiempo real mediante OCT intraoperatorio (iOCT) 3). Dado que permite un control objetivo de la profundidad de la sutura, que antes dependía de la experiencia, se puede lograr una compresión corneal efectiva mientras se reduce el riesgo de daño endotelial. En el informe de Kaur et al., todos los casos se resolvieron en dos semanas.