Степень 1
Максимальный диаметр отека: ≤ 3 мм
Характер поражения: Локализованный отек стромы. Ограничен частью роговицы.

Острый гидропс роговицы (ОГР) — редкое осложнение эктазий роговицы. Это разрыв десцеметовой мембраны и эндотелия роговицы, приводящий к быстрому поступлению водянистой влаги в строму роговицы и резкому отеку роговицы.
Наиболее частым основным заболеванием является кератоконус, но он также возникает при кератоглобусе и пеллюцидной краевой дегенерации (ПКД).
Частота встречаемости следующая 1):
Возраст начала варьирует от 5 до 59 лет, чаще встречается в возрасте 20–40 лет 1). Риск у мужчин до двух раз выше, чем у женщин. Отмечаются этнические различия: в Новой Зеландии выше распространенность среди жителей тихоокеанских островов, в Великобритании — среди выходцев из Южной Азии и чернокожих.
Согласно новейшим данным, одного только дефекта десцеметовой мембраны недостаточно для развития ОРГ; также необходим дефект задней стромы роговицы. В одном исследовании сообщается, что из 16 глаз с дефектом десцеметовой мембраны во время DMEK ни один не развил ОРГ, тогда как из 5 глаз с перфорацией задней стромы все развили ОРГ 1).
Считается, что она возникает примерно у 2,4–3% пациентов с кератоконусом, у 6–11,5% пациентов с пеллюцидной краевой дегенерацией роговицы и примерно у 11% пациентов с кератоглобусом 1). Чем тяжелее эктазия роговицы, тем выше риск, и особое внимание требуется пациентам с привычкой тереть глаза.
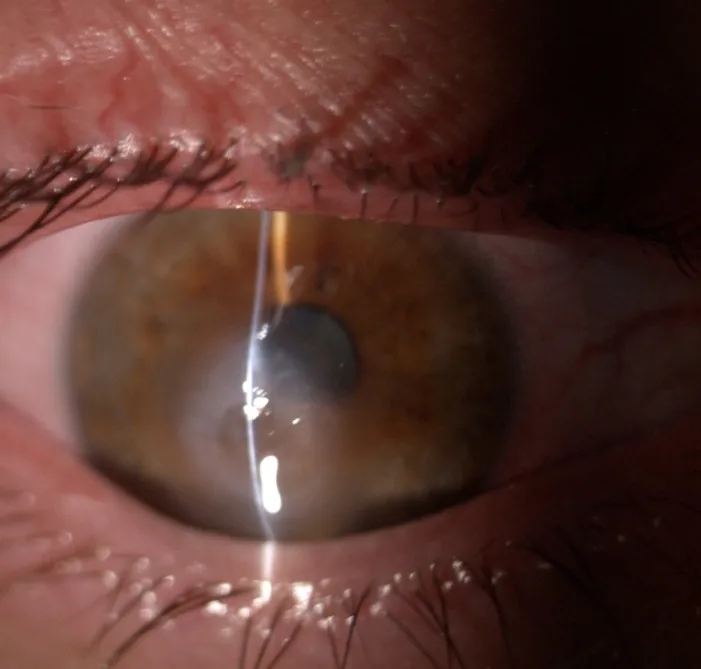
Основные субъективные симптомы ОРГ следующие:
К провоцирующим факторам относятся действия, временно повышающие внутриглазное давление, такие как трение глаз, чихание, кашель, сморкание или интенсивные физические нагрузки. Это также может происходить спонтанно.
При биомикроскопии с щелевой лампой выявляются конъюнктивальная гиперемия, отек стромы роговицы, отек эпителия, интрастромальные щели и эпителиальные пузыри1).
Классификация по степени выраженности отека представлена ниже1).
Степень 1
Максимальный диаметр отека: ≤ 3 мм
Характер поражения: Локализованный отек стромы. Ограничен частью роговицы.
Степень 2
Максимальный диаметр отека: 3–5 мм
Характер поражения: Умеренный отек. Может затрагивать зрительную ось.
Степень 3
Максимальный диаметр отека: > 5 мм
Характер поражения: Обширный отек. Выраженное помутнение, включая зрительную ось. У самого молодого пациента (девочка 5 лет) описан тотальный отек роговицы от лимба до лимба8).
Для оценки прозрачности роговицы также используется 5-балльная классификация от степени 0 (передняя камера и радужка полностью не видны) до степени 4 (полностью прозрачна)1).
Оптическая когерентная томография переднего сегмента (AS-OCT) позволяет неинвазивно визуализировать разрыв и отслойку десцеметовой мембраны, интрастромальные полости с жидкостью и увеличение толщины роговицы1). Размер и глубина разрыва являются прогностическими показателями времени разрешения АСН. Проба Зейделя может быть положительной, что обусловлено истечением водянистой влаги через отечную роговицу, а не перфорацией.
Сообщалось о случаях АСН у пациентов с эндокринной офтальмопатией, при этом повышение внутриглазного давления и воспаление поверхности глаза могут быть факторами риска7).
Что касается риска инфекции, сообщается, что 2,7% (3/112) случаев ACH осложнились инфекционным кератитом5). Все случаи были мужчинами с тяжелым атопическим дерматитом, средний возраст 46 лет. При посеве были обнаружены MSCNS и MSSA.
Трение глаз оказывает механическое воздействие на десцеметову мембрану и может стать прямой причиной ее разрыва при уже истонченной и расширенной роговице 1). Пациенты с атопическим дерматитом особенно склонны тереть глаза из-за зуда, что создает высокий риск. При зуде важно контролировать симптомы с помощью глазных капель и т.д.
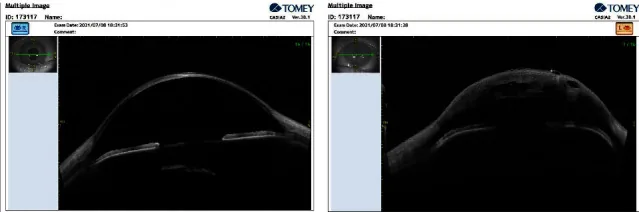
Диагноз ОВР ставится на основании клинических данных и дополняется различными методами визуализации.
Основа диагностики. Выявляются конъюнктивальная гиперемия, стромальный отек, эпителиальный отек и интрастромальные щели 1). Проводится проба Зайдля для дифференциации с перфорацией.
Ниже приведены характеристики основных методов визуализации.
| Метод исследования | Основные оцениваемые параметры | Особенности |
|---|---|---|
| AS-OCT | Разрыв ДМ и стромальные расщелины | Бесконтактный, количественный |
| Ультразвуковая биомикроскопия | Место разрыва, толщина роговицы | Мониторинг разрешения |
| Конфокальная микроскопия in vivo (IVCM) | Воспалительные клетки, отек | Оценка на клеточном уровне |
Лечение АСН начинается с консервативной терапии; при недостаточном улучшении или необходимости раннего разрешения рассматривается хирургическое лечение.
Используются следующие препараты1)9).
Спонтанное разрешение при консервативном лечении занимает 2–4 месяца (максимум 5–36 недель)1). С другой стороны, в глазах, подвергшихся кросслинкингу роговицы (CXL), разрешение происходит значительно быстрее, с сообщениями о полном разрешении в течение 3 недель7).
Выполняется с целью ускорения разрешения, облегчения симптомов и минимизации рубцевания роговицы.
Инъекция газа в переднюю камеру
пневматическая десцеметопексия: введение воздуха, SF6 или C3F8 в переднюю камеру для расправления и повторного прилегания краев десцеметовой мембраны за счет тампонирующего эффекта1).
Время разрешения: 2–7 недель (значительно короче, чем 64–117 дней при консервативном лечении).
Частота повторных инъекций: воздух 77,8%, SF6 66,7%, C3F8 0–35,7% требуют повторной инъекции.
Компрессионные швы
compression sutures: швы для сжатия и закрытия разрыва десцеметовой мембраны. Существуют сквозные (FTS) и частичные (PTS) швы2).
Время разрешения: по данным обзора литературы, от 1 часа до 45 дней. Большинство случаев разрешаются в течение 2 недель2).
Комбинация с воздухом в передней камере: полное разрешение в течение 2 недель было зарегистрировано при использовании 3 FTS + воздух (заполнение передней камеры на 50%)3).
Трансплантация роговицы
Эндотелиальная кератопластика (DSAEK/DMEK): рассматривается при больших разрывах десцеметовой мембраны1).
Глубокая передняя послойная кератопластика (pDALK): позволяет закрыть ДМ, восстановить кривизну роговицы и зрение за одну операцию.
Сквозная кератопластика (PKP): выполняется при рубцах, ухудшающих зрение после АСН. Выживаемость трансплантата после PKP при АСН ниже, чем в случаях без АСН3).
Приведен пример типичного рецепта глазных капель после наложения компрессионных швов3).
| Препарат | Доза и частота |
|---|---|
| Моксифлоксацин 0,5% | 4 раза в день |
| Преднизолона ацетат 1% | Постепенное снижение по показаниям |
| NaCl 5% | 1 раз перед сном |
Многие случаи разрешаются только консервативным лечением в течение 2–4 месяцев1). Однако после разрешения могут остаться рубцы роговицы и неоваскуляризация, приводящие к стойкому нарушению зрения. Инъекция газа в переднюю камеру или компрессионный шов могут сократить время разрешения до примерно 2 недель и минимизировать образование рубцов. Важно обсудить с лечащим врачом для определения тактики лечения.
Это хирургическая процедура, при которой в переднюю камеру вводится воздух или специальный газ (SF6, C3F8 и т. д.), и за счет тампонирующего эффекта область разрыва десцеметовой мембраны поддерживается изнутри, способствуя повторному прикреплению 1). Разрешение, которое при консервативном лечении занимает 64–117 дней, может быть сокращено до 2–7 недель. Однако может возникнуть зрачковый блок-глаукома или потребоваться повторная инъекция.
Традиционно предполагалось, что микроповреждения (например, трение глаз) → разрыв десцеметовой мембраны → проникновение водянистой влаги в строму → разделение ламеллярных слоев → отек 1).
Последние исследования показывают, что только дефект десцеметовой мембраны не вызывает ACH; также необходим дефект задней стромы роговицы 1). Это открытие важно для объяснения того, почему ACH возникает только в случаях тяжелой эктазии роговицы.
В образцах роговицы ACH при сквозной кератопластике (PKP) обнаруживаются рыхло упакованные стромальные ламеллы. Ламинин и коллаген IV типа локализуются рядом со свернутой десцеметовой мембраной, что, как полагают, играет важную роль в миграции и реэндотелизации эндотелиальных клеток 1).
Передняя треть стромы роговицы из-за ламеллярного переплетения набухает лишь незначительно. Задние две трети состоят из непереплетенных однонаправленных фибрилл и могут набухать до трехкратного размера 7).
Соседние эндотелиальные клетки роговицы мигрируют в область разрыва десцеметовой мембраны и восстанавливают функцию эндотелиального насоса, что приводит к дегидратации роговицы и окончательному восстановлению с образованием рубца 1). Компрессионный шов физически сближает края десцеметовой мембраны, способствуя миграции эндотелиальных клеток.
Исследования с использованием прижизненной конфокальной микроскопии показали, что в случаях, когда воспалительные клетки сохраняются более 4 недель, риск неоваскуляризации роговицы высок 1).
Varshney et al. (2021) сообщили о случае ACH, осложнившего кератит после CXL 7). В роговице, уже прошедшей CXL, разрешение наступило быстро, в течение 21 дня, что значительно короче обычных 2–4 месяцев. Предполагаемый механизм: усиление сшивки коллагена под действием CXL → увеличение межламеллярной прочности передней стромы → повышение устойчивости к набуханию. Сшитая роговица более устойчива к ферментативному перевариванию, что способствует раннему разрешению.
Сообщается о технике регулировки глубины и натяжения шва в реальном времени с использованием интраоперационной ОКТ (iOCT).
Kaur et al. (2025) выполнили частичный компрессионный шов (PTS, целевая глубина 50–60%) под контролем iOCT у 7 пациентов (медиана возраста 16 лет, предоперационная толщина роговицы 1120–2363 мкм)2). Швы накладывались при визуализации стромальной компрессии, имеющей вид «гусеницы», с помощью iOCT; все случаи разрешились в течение 2 недель, швы были удалены через 8–12 недель. PTS показал эффективность, аналогичную полнослойному шву (FTS), при меньшем риске повреждения эндотелия.
Обзор литературы (19 исследований) показал время разрешения компрессионного шва от 1 часа до 45 дней, причем большинство случаев разрешилось в течение 2 недель2).
Liu et al. сообщили о двухэтапной операции: TKP-ассистированная эпикератофакия (восстановление десцеметовой мембраны на первом этапе) с последующей DALK с использованием того же трансплантата (второй этап) через 2,1 ± 0,7 месяца, что позволило добиться улучшения зрения2).
Petrelli et al. выполнили ламеллярную клиновидную резекцию после неудачной аппликации цианоакрилатного клея при перфорации роговицы после ACH2). Это позволило избежать трансплантации роговицы и улучшить рефракцию.
Alio et al. ввели 0,3 мл обогащенной тромбоцитами плазмы (EPRP) в переднюю камеру у пациентов, рефрактерных к SF6, и добились разрешения в течение недели 1). Предполагается, что механизм заключается в стимуляции регенерации эндотелиальных клеток факторами роста.
Для случаев с большим разрывом десцеметовой мембраны сообщается о методе временного закрытия разрыва с помощью небольшого патча DMEK диаметром 5 мм 1). Описаны случаи, когда после частичного отслоения трансплантата роговица спонтанно восстанавливала детургесценцию.
Ontiveros-Holguín & Pacheco-Padrón (2022) сообщили о случае ACH и миграции ICRS после имплантации интракорнеальных кольцевых сегментов (ICRS) 8). ACH разрешилась через 8 недель только при консервативном лечении. Это считается первым сообщением об ACH после имплантации ICRS, которая восстановилась только при консервативном лечении.
Это компрессионный шов, выполняемый под контролем интраоперационной ОКТ (iOCT) для проверки глубины и натяжения шва в реальном времени 3). В отличие от традиционного метода, основанного на опыте, глубина шва может контролироваться объективно, что позволяет эффективно сжимать роговицу при снижении риска повреждения эндотелия. В отчете Kaur et al. все случаи разрешились в течение 2 недель.