Grado 1
Diametro massimo dell’edema: ≤ 3 mm
Caratteristiche della lesione: Edema stromale localizzato. Limitato a una parte della cornea.

L’idrope corneale acuto (ACH) è una rara complicanza delle ectasie corneali. Consiste in una rottura della membrana di Descemet e dell’endotelio corneale, che provoca un rapido afflusso di umore acqueo nello stroma corneale e un improvviso edema corneale.
La malattia di base più comune è il cheratocono, ma si verifica anche nel cheratoglobo e nella degenerazione marginale pellucida (DMP).
L’incidenza è la seguente 1):
L’età di insorgenza varia da 5 a 59 anni, con un picco tra i 20 e i 40 anni 1). Il rischio negli uomini è fino al doppio rispetto alle donne. Si osservano differenze etniche: in Nuova Zelanda la prevalenza è più alta tra gli isolani del Pacifico, nel Regno Unito tra gli asiatici del sud e i neri.
Secondo le conoscenze più recenti, un semplice difetto della membrana di Descemet non è sufficiente a causare l’ACH; è necessario anche un difetto dello stroma corneale posteriore. Uno studio riporta che su 16 occhi con difetto della membrana di Descemet durante DMEK, nessuno ha sviluppato ACH, mentre su 5 occhi con perforazione dello stroma posteriore, tutti hanno sviluppato ACH 1).
Si stima che si verifichi in circa il 2,4–3% dei pazienti con cheratocono, nel 6–11,5% dei pazienti con degenerazione marginale pellucida e in circa l’11% dei pazienti con cheratoglobo 1). Maggiore è la gravità dell’ectasia corneale, maggiore è il rischio, e particolare attenzione è necessaria nei pazienti con l’abitudine di strofinarsi gli occhi.
I principali sintomi soggettivi dell’ACH sono i seguenti:
I fattori scatenanti includono azioni che aumentano temporaneamente la pressione intraoculare, come strofinarsi gli occhi, starnutire, tossire, soffiarsi il naso o fare esercizio fisico intenso. Può anche verificarsi spontaneamente.
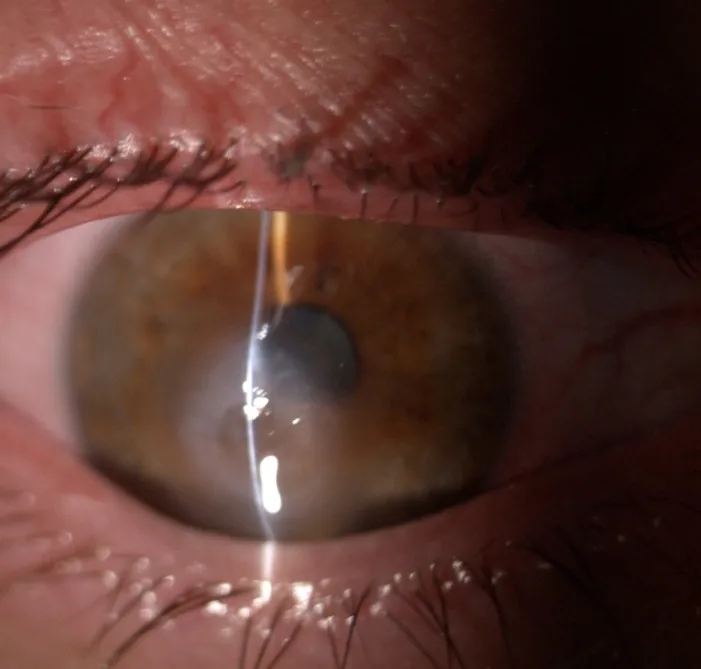
All’esame con lampada a fessura si osservano iperemia congiuntivale, edema stromale corneale, edema epiteliale, fessure intrastromali e bolle epiteliali1).
La classificazione in gradi in base all’estensione dell’edema è mostrata di seguito1).
Grado 1
Diametro massimo dell’edema: ≤ 3 mm
Caratteristiche della lesione: Edema stromale localizzato. Limitato a una parte della cornea.
Grado 2
Diametro massimo dell’edema: 3–5 mm
Caratteristiche della lesione: Edema moderato. Può interessare l’asse visivo.
Grado 3
Diametro massimo dell’edema: > 5 mm
Caratteristiche della lesione: Edema esteso. Opacità grave che include l’asse visivo. Il caso più giovane (bambina di 5 anni) ha riportato un edema corneale totale da limbo a limbo8).
Per la valutazione della trasparenza corneale viene utilizzata anche una classificazione a 5 gradi, dal Grado 0 (camera anteriore e iride completamente invisibili) al Grado 4 (completamente trasparente)1).
L’OCT del segmento anteriore (AS-OCT) consente di visualizzare in modo non invasivo la rottura e il distacco della membrana di Descemet, le cavità di liquido intrastromali e l’aumento dello spessore corneale1). Le dimensioni e la profondità della rottura sono indicatori predittivi del tempo di risoluzione dell’ACH. Il test di Seidel può essere positivo, ma ciò è dovuto a una perdita di umore acqueo dalla cornea edematosa e non a una perforazione.
Sono stati riportati casi di ACH in pazienti con oftalmopatia basedowiana, e l’aumento della pressione intraoculare e l’infiammazione della superficie oculare possono essere fattori di rischio7).
Per quanto riguarda il rischio di infezione, è stato riportato che il 2,7% (3/112) dei casi di ACH ha sviluppato cheratite infettiva5). Tutti i casi erano uomini con dermatite atopica grave, età media 46 anni. La coltura ha evidenziato MSCNS e MSSA.
Strofinarsi gli occhi esercita una forza meccanica sulla membrana di Descemet e può essere un fattore scatenante diretto della rottura della membrana di Descemet in una cornea già assottigliata ed ectasica 1). I pazienti con dermatite atopica sono particolarmente a rischio perché tendono a strofinarsi gli occhi a causa del prurito. In caso di prurito, è importante controllare i sintomi con colliri, ecc.
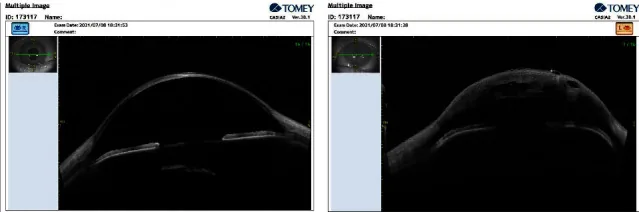
La diagnosi di ACH si basa sui reperti clinici ed è integrata da vari esami di imaging.
Base della diagnosi. Si valutano iperemia congiuntivale, edema stromale, edema epiteliale e fessure intrastromali 1). Il test di Seidel viene eseguito per differenziare una perforazione.
Di seguito sono riportate le caratteristiche delle principali modalità di esame.
| Metodo di esame | Principali elementi valutati | Caratteristiche |
|---|---|---|
| AS-OCT | Rottura della DM e fessure stromali | Non a contatto, quantitativo |
| Microscopia ultrasonica biomicroscopica | Sede della rottura, spessore corneale | Monitoraggio della risoluzione |
| Microscopia confocale in vivo (IVCM) | Cellule infiammatorie, edema | Valutazione a livello cellulare |
Il trattamento dell’ACH inizia con una terapia conservativa; in caso di miglioramento insufficiente o se è necessaria una risoluzione precoce, si considera il trattamento chirurgico.
Vengono utilizzati i seguenti farmaci1)9).
La risoluzione spontanea con trattamento conservativo richiede 2-4 mesi (massimo 5-36 settimane)1). D’altra parte, negli occhi sottoposti a cross-linking corneale (CXL), la risoluzione è notevolmente più rapida, con casi di risoluzione completa in 3 settimane riportati7).
Viene eseguita con l’obiettivo di accelerare la risoluzione, alleviare i sintomi e minimizzare le cicatrici corneali.
Iniezione di gas in camera anteriore
pneumatic descemetopexy: iniezione di aria, SF6 o C3F8 in camera anteriore per dispiegare e riapporre i bordi della membrana di Descemet tramite effetto tamponante1).
Tempo di risoluzione: 2-7 settimane (significativamente più breve rispetto ai 64-117 giorni del trattamento conservativo).
Frequenza di reiniezione: aria 77,8%, SF6 66,7%, C3F8 0-35,7% richiedono reiniezione.
Suture compressive
compression sutures: suture per comprimere e chiudere l’area di rottura della membrana di Descemet. Esistono suture a tutto spessore (FTS) e a spessore parziale (PTS)2).
Tempo di risoluzione: secondo una revisione della letteratura, da 1 ora a 45 giorni. La maggior parte si risolve entro 2 settimane2).
Associazione con aria in camera anteriore: è stata riportata risoluzione completa entro 2 settimane con 3 FTS + aria (riempimento al 50% della camera anteriore)3).
Trapianto di cornea
Cheratoplastica endoteliale (DSAEK/DMEK): presa in considerazione in caso di ampia rottura della membrana di Descemet1).
Cheratoplastica lamellare anteriore profonda (pDALK): consente di chiudere la DM, ripristinare la curvatura corneale e la vista in un unico intervento.
Cheratoplastica perforante (PKP): eseguita per cicatrici corneali che compromettono la vista dopo ACH. La sopravvivenza a lungo termine del trapianto dopo PKP per ACH è inferiore rispetto ai casi non ACH3).
Viene mostrato un esempio di prescrizione di colliri tipica dopo suture compressive3).
| Farmaco | Dose e frequenza |
|---|---|
| Moxifloxacina 0,5% | 4 volte al giorno |
| Prednisolone acetato 1% | Riduzione graduale secondo necessità |
| NaCl 5% | 1 volta prima di coricarsi |
Molti casi si risolvono con il solo trattamento conservativo entro 2-4 mesi1). Tuttavia, dopo la risoluzione possono rimanere cicatrici corneali e neovascolarizzazione, causando deficit visivo permanente. L’iniezione di gas in camera anteriore o la sutura compressiva possono ridurre il tempo di risoluzione a circa 2 settimane e minimizzare la formazione di cicatrici. È importante discutere con il medico curante per decidere la strategia terapeutica.
Si tratta di un intervento chirurgico in cui viene iniettata aria o un gas speciale (SF6, C3F8, ecc.) nella camera anteriore e, grazie al suo effetto tamponante, la zona di rottura della membrana di Descemet viene sostenuta dall’interno per favorire la riadesione 1). La risoluzione, che con il trattamento conservativo richiede 64-117 giorni, può essere ridotta a 2-7 settimane. Tuttavia, possono verificarsi glaucoma da blocco pupillare o la necessità di una reiniezione.
Tradizionalmente, si ipotizzava un percorso di microtraumi (ad esempio, sfregamento degli occhi) → rottura della membrana di Descemet → infiltrazione di umore acqueo nello stroma → separazione degli strati lamellari → edema 1).
Studi recenti mostrano che un difetto isolato della membrana di Descemet non causa ACH; è necessario anche un difetto dello stroma corneale posteriore 1). Questa scoperta è importante per spiegare perché l’ACH si verifica solo nei casi di grave ectasia corneale.
Nei campioni di cheratoplastica perforante (PKP) di cornee con ACH, si osservano lamelle stromali lassamente impaccate. La laminina e il collagene di tipo IV sono localizzati in prossimità della membrana di Descemet arrotolata e si ritiene che svolgano un ruolo importante nella migrazione e nella riendotelizzazione delle cellule endoteliali 1).
Il terzo anteriore dello stroma corneale si gonfia solo leggermente a causa dell’intreccio lamellare. I due terzi posteriori, costituiti da fibrille non intrecciate e unidirezionali, possono gonfiarsi fino a tre volte 7).
Le cellule endoteliali corneali adiacenti migrano verso l’area di rottura della membrana di Descemet e ripristinano la funzione di pompa endoteliale, portando alla disidratazione corneale e alla riparazione finale con formazione di cicatrice 1). La sutura compressiva avvicina fisicamente i bordi della membrana di Descemet, favorendo la migrazione delle cellule endoteliali.
Studi con microscopia confocale in vivo hanno mostrato che nei casi in cui le cellule infiammatorie persistono per più di 4 settimane, il rischio di neovascolarizzazione corneale è elevato 1).
Varshney et al. (2021) hanno riportato un caso di ACH complicante una cheratite dopo CXL 7). Nella cornea già trattata con CXL, la risoluzione è stata rapida in 21 giorni, notevolmente più breve dei soliti 2-4 mesi. Il meccanismo suggerito è il rafforzamento dei cross-link del collagene da parte del CXL → aumento della forza coesiva interlamellare dello stroma anteriore → aumento della resistenza al rigonfiamento. La cornea cross-linkata è più resistente alla digestione enzimatica, contribuendo alla risoluzione precoce.
È stata riportata una tecnica per regolare in tempo reale la profondità e la tensione della sutura utilizzando l’OCT intraoperatorio (iOCT).
Kaur et al. (2025) hanno eseguito una sutura compressiva parziale (PTS, profondità target 50-60%) guidata da iOCT in 7 pazienti (età mediana 16 anni, spessore corneale preoperatorio 1120-2363 μm)2). Le suture sono state posizionate sotto visualizzazione iOCT della compattazione stromale con aspetto a ‘bruco’; tutti i casi si sono risolti entro 2 settimane e le suture sono state rimosse dopo 8-12 settimane. La PTS ha mostrato un’efficacia simile alla sutura a tutto spessore (FTS) con un minor rischio di danno endoteliale.
Una revisione della letteratura (19 studi) ha riportato un tempo di risoluzione della sutura compressiva da 1 ora a 45 giorni, con la maggior parte dei casi risolti entro 2 settimane2).
Liu et al. hanno riportato una chirurgia in due fasi: epicheratofachia assistita da TKP (riparazione della membrana di Descemet nella prima fase) seguita da DALK con lo stesso innesto (seconda fase) dopo 2,1 ± 0,7 mesi, ottenendo un recupero visivo2).
Petrelli et al. hanno eseguito una resezione cuneiforme lamellare dopo fallimento della colla cianoacrilica per una perforazione corneale post-ACH2). Ciò ha permesso di evitare un trapianto di cornea migliorando la rifrazione.
Alio et al. hanno iniettato 0,3 ml di plasma ricco di piastrine arricchito (EPRP) nella camera anteriore in casi refrattari a SF6, ottenendo la risoluzione in una settimana 1). Si ipotizza che il meccanismo sia la promozione della rigenerazione delle cellule endoteliali da parte dei fattori di crescita.
Per i casi con ampia rottura della membrana di Descemet, è stato riportato un metodo che utilizza un piccolo patch DMEK di 5 mm per chiudere temporaneamente la rottura 1). Sono stati descritti casi in cui la cornea ha mostrato una deturgescenza spontanea dopo un distacco parziale del graft.
Ontiveros-Holguín & Pacheco-Padrón (2022) hanno riportato un caso di ACH e migrazione di ICRS dopo impianto di segmenti anulari intracorneali (ICRS) 8). L’ACH si è risolta dopo 8 settimane con solo trattamento conservativo. È considerata la prima segnalazione di ACH dopo impianto di ICRS risolta solo con trattamento conservativo.
È una sutura compressiva eseguita utilizzando l’OCT intraoperatorio (iOCT) per verificare in tempo reale la profondità e la tensione della sutura 3). A differenza del metodo convenzionale che si basava sull’esperienza, la profondità della sutura può essere controllata oggettivamente, consentendo una compressione corneale efficace riducendo il rischio di danno endoteliale. Nel rapporto di Kaur et al., tutti i casi si sono risolti entro 2 settimane.