Grad 1
Maximaler Durchmesser des Ödems: ≤ 3 mm
Läsionscharakter: Lokalisiertes Stromaödem. Beschränkt auf einen Teil der Hornhaut.

Das akute Hornhautödem (ACH) ist eine seltene Komplikation von Hornhautektasien. Es handelt sich um einen Riss der Descemet-Membran und des Hornhautendothels, der zu einem schnellen Einstrom von Kammerwasser in das Hornhautstroma und einer plötzlichen Hornhautschwellung führt.
Die häufigste Grunderkrankung ist der Keratokonus, es tritt aber auch bei Keratoglobus und pelluzider marginaler Degeneration (PMD) auf.
Die Inzidenz ist wie folgt 1):
Das Erkrankungsalter reicht von 5 bis 59 Jahren, mit einem Häufigkeitsgipfel zwischen dem 20. und 40. Lebensjahr 1). Männer haben ein bis zu doppelt so hohes Risiko wie Frauen. Es gibt ethnische Unterschiede: In Neuseeland ist die Prävalenz bei Pazifikinsulanern höher, in Großbritannien bei Südasiaten und Schwarzen.
Nach neuesten Erkenntnissen reicht ein reiner Defekt der Descemet-Membran nicht aus, um einen ACH zu verursachen; auch ein Defekt des hinteren Hornhautstromas ist erforderlich. Eine Studie berichtet, dass bei 16 Augen mit einem Descemet-Membran-Defekt während einer DMEK kein ACH auftrat, während bei 5 Augen mit einer Perforation des hinteren Stromas in allen Fällen ein ACH auftrat 1).
Es wird angenommen, dass es bei etwa 2,4–3 % der Patienten mit Keratokonus, 6–11,5 % der Patienten mit pelluzider marginaler Hornhautdegeneration und etwa 11 % der Patienten mit Keratoglobus auftritt 1). Je schwerwiegender die Hornhautektasie, desto höher das Risiko, und bei Patienten mit der Angewohnheit, sich die Augen zu reiben, ist besondere Vorsicht geboten.
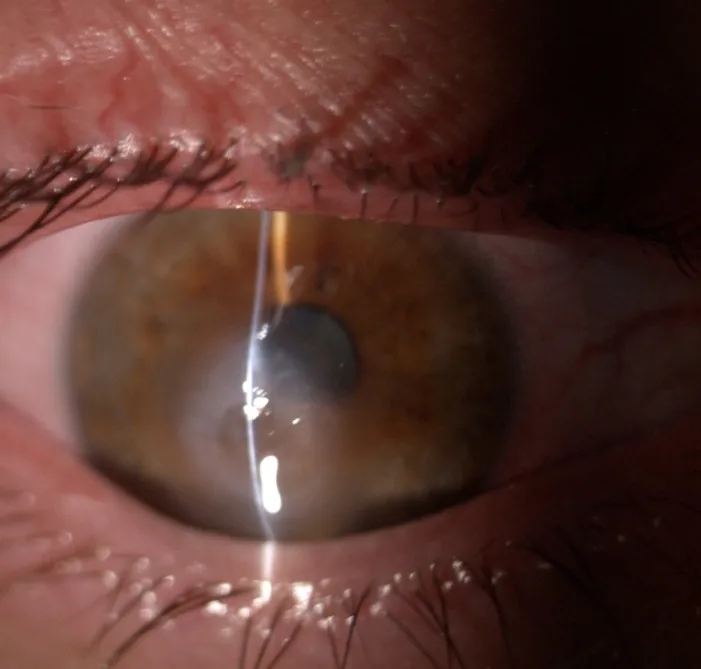
Die wichtigsten subjektiven Symptome des ACH sind:
Zu den Auslösern gehören Handlungen, die den Augeninnendruck vorübergehend erhöhen, wie Augenreiben, Niesen, Husten, Nasenputzen oder starke körperliche Anstrengung. Es kann auch spontan auftreten.
Im Spaltlampenmikroskop zeigen sich konjunktivale Hyperämie, Hornhautstromaödem, Epithelödem, intrastromale Spalten und Epithelblasen1).
Die Gradeinteilung nach Ausdehnung des Ödems ist unten aufgeführt1).
Grad 1
Maximaler Durchmesser des Ödems: ≤ 3 mm
Läsionscharakter: Lokalisiertes Stromaödem. Beschränkt auf einen Teil der Hornhaut.
Grad 2
Maximaler Durchmesser des Ödems: 3–5 mm
Läsionscharakter: Mäßiges Ödem. Kann die Sehachse beeinträchtigen.
Grad 3
Maximaler Durchmesser des Ödems: > 5 mm
Läsionscharakter: Ausgedehntes Ödem. Schwere Trübung einschließlich der Sehachse. Der jüngste Fall (5-jähriges Mädchen) berichtete über ein limbus-zu-limbus Hornhautödem8).
Zur Beurteilung der Hornhauttransparenz wird auch eine 5-stufige Klassifikation von Grad 0 (Vorderkammer und Iris vollständig unsichtbar) bis Grad 4 (vollständig transparent) verwendet1).
Die optische Kohärenztomographie des vorderen Augenabschnitts (AS-OCT) ermöglicht die nicht-invasive Visualisierung von Descemet-Membranruptur und -abhebung, intrastromalen Flüssigkeitshohlräumen und erhöhter Hornhautdicke1). Größe und Tiefe der Ruptur sind prädiktive Indikatoren für die ACH-Auflösungszeit. Der Seidel-Test kann positiv sein, was jedoch auf einen Kammerwasseraustritt durch das ödematöse Hornhautgewebe und nicht auf eine Perforation zurückzuführen ist.
Es wurden Fälle von ACH bei Patienten mit Morbus Basedow berichtet, wobei erhöhter Augeninnendruck und Augenoberflächenentzündung Risikofaktoren darstellen können7).
Hinsichtlich des Infektionsrisikos wird berichtet, dass 2,7 % (3/112) der ACH-Fälle eine infektiöse Keratitis entwickelten5). Alle Fälle waren Männer mit schwerer atopischer Dermatitis, Durchschnittsalter 46 Jahre. In der Kultur wurden MSCNS und MSSA nachgewiesen.
Das Reiben der Augen übt eine mechanische Kraft auf die Descemet-Membran aus und kann bei bereits ausgedünnter und erweiterter Hornhaut ein direkter Auslöser für einen Riss der Descemet-Membran sein 1). Patienten mit atopischer Dermatitis neigen aufgrund von Juckreiz besonders dazu, sich die Augen zu reiben, und haben ein besonders hohes Risiko. Bei Juckreiz ist es wichtig, die Symptome mit Augentropfen usw. zu kontrollieren.
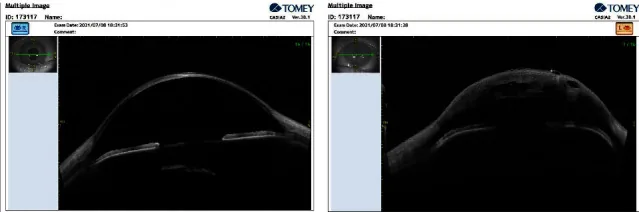
Die Diagnose eines ACH basiert auf klinischen Befunden und wird durch verschiedene bildgebende Verfahren ergänzt.
Grundlage der Diagnose. Es werden konjunktivale Hyperämie, Stromaödem, Epithelödem und intrastromale Spalten untersucht 1). Der Seidel-Test wird zur Abgrenzung einer Perforation durchgeführt.
Nachfolgend sind die Merkmale der wichtigsten Untersuchungsmodalitäten aufgeführt.
| Untersuchungsmethode | Hauptbewertungsinhalte | Merkmale |
|---|---|---|
| AS-OCT | DM-Ruptur und Stroma-Spalten | Kontaktlos, quantitativ |
| Ultraschall-Biomikroskopie | Rupturstelle, Hornhautdicke | Rückbildungsüberwachung |
| In-vivo-Konfokalmikroskopie (IVCM) | Entzündungszellen, Ödem | Zelluläre Beurteilung |
Die Behandlung der ACH beginnt mit einer konservativen Therapie; bei unzureichender Besserung oder wenn eine frühzeitige Rückbildung erforderlich ist, wird eine operative Behandlung in Betracht gezogen.
Die folgenden Medikamente werden verwendet1)9).
Die spontane Rückbildung unter konservativer Behandlung dauert 2–4 Monate (maximal 5–36 Wochen)1). Andererseits ist die Rückbildung in Augen, die einer Hornhaut-Crosslinking (CXL) unterzogen wurden, deutlich schneller, mit berichteten Fällen vollständiger Rückbildung innerhalb von 3 Wochen7).
Sie wird durchgeführt, um eine frühzeitige Rückbildung, Symptomlinderung und Minimierung von Hornhautnarben zu erreichen.
Gasinjektion in die Vorderkammer
pneumatische Descemetopexie: Injektion von Luft, SF6 oder C3F8 in die Vorderkammer, um die Ränder der Descemet-Membran durch Tamponade-Effekt zu entfalten und wieder anzulegen1).
Rückbildungszeit: 2–7 Wochen (deutlich kürzer als die 64–117 Tage der konservativen Behandlung).
Häufigkeit der Reinjektion: Luft 77,8 %, SF6 66,7 %, C3F8 0–35,7 % benötigen eine Reinjektion.
Kompressionsnähte
compression sutures: Nähte zur Kompression und zum Verschluss der Descemet-Membran-Rissstelle. Es gibt durchgreifende (FTS) und partielle (PTS) Nähte2).
Rückbildungszeit: Laut Literaturübersicht 1 Stunde bis 45 Tage. Die meisten Fälle innerhalb von 2 Wochen2).
Kombination mit Vorderkammerluft: Vollständige Rückbildung innerhalb von 2 Wochen wurde mit 3 FTS + Luft (50% Füllung der Vorderkammer) berichtet3).
Hornhauttransplantation
Endothelkeratoplastik (DSAEK/DMEK): Wird bei großen Descemet-Membran-Rissen in Betracht gezogen1).
Tiefe anteriore lamelläre Keratoplastik (pDALK): Ermöglicht den Verschluss der DM, Wiederherstellung der Hornhautkrümmung und des Sehvermögens in einem einzigen Eingriff.
Durchgreifende Keratoplastik (PKP): Wird bei sehbehindernden Narben nach ACH durchgeführt. Die langfristige Transplantatüberlebensrate nach PKP bei ACH ist niedriger als bei Nicht-ACH-Fällen3).
Ein Beispiel für ein typisches Augentropfen-Rezept nach Kompressionsnähten wird gezeigt3).
| Medikament | Dosis und Häufigkeit |
|---|---|
| Moxifloxacin 0,5 % | 4-mal täglich |
| Prednisolonacetat 1 % | Nach Bedarf ausschleichen |
| NaCl 5 % | 1-mal vor dem Schlafengehen |
Viele Fälle bilden sich allein mit konservativer Behandlung innerhalb von 2–4 Monaten zurück1). Allerdings können nach der Rückbildung Hornhautnarben und Neovaskularisation zurückbleiben, die zu dauerhaften Sehstörungen führen. Eine Gasinjektion in die Vorderkammer oder eine Kompressionsnaht kann die Rückbildung auf etwa 2 Wochen verkürzen und die Narbenbildung minimieren. Es ist wichtig, mit dem behandelnden Arzt zu besprechen, um die Therapiestrategie festzulegen.
Es handelt sich um einen chirurgischen Eingriff, bei dem Luft oder ein spezielles Gas (SF6, C3F8 usw.) in die Vorderkammer injiziert wird. Durch den Tamponade-Effekt wird die Rissstelle der Descemet-Membran von innen gestützt und die Wiederanhaftung gefördert 1). Die Rückbildung, die bei konservativer Behandlung 64–117 Tage dauert, kann auf 2–7 Wochen verkürzt werden. Es kann jedoch zu einem Pupillarblockglaukom oder einer erneuten Injektion kommen.
Bisher wurde angenommen, dass Mikrotrauma (z. B. Augenreiben) → Riss der Descemet-Membran → Eindringen von Kammerwasser in das Stroma → Trennung der Lamellenschichten → Ödem führt 1).
Neuere Studien zeigen, dass ein alleiniger Defekt der Descemet-Membran keine ACH verursacht; auch ein Defekt des hinteren Hornhautstromas ist erforderlich 1). Diese Erkenntnis ist wichtig, um zu erklären, warum ACH nur bei schwerer Hornhautektasie auftritt.
In Vollhaut-Hornhauttransplantat (PKP)-Präparaten von ACH-Hornhäuten finden sich locker gepackte Stromalamellen. Laminin und Kollagen Typ IV sind in der Nähe der aufgerollten Descemet-Membran lokalisiert und spielen vermutlich eine wichtige Rolle bei der Migration und Regeneration der Endothelzellen 1).
Das vordere Drittel des Hornhautstromas schwillt aufgrund der lamellaren Verflechtung nur geringfügig an. Die hinteren zwei Drittel bestehen aus nicht verflochtenen, unidirektionalen Fibrillen und können bis zum Dreifachen anschwellen 7).
Angrenzende Hornhautendothelzellen wandern in den Rissbereich der Descemet-Membran und stellen die Endothelpumpenfunktion wieder her, was zu einer Hornhautdehydratation und schließlich zur Reparatur durch Narbenbildung führt 1). Die Kompressionsnaht bringt die Ränder der Descemet-Membran physisch näher zusammen und fördert so die Migration der Endothelzellen.
Studien mit In-vivo-Konfokalmikroskopie haben gezeigt, dass Fälle, in denen Entzündungszellen länger als 4 Wochen verbleiben, ein hohes Risiko für Hornhautneovaskularisation aufweisen 1).
Varshney et al. (2021) berichteten über einen Fall von ACH als Komplikation einer Keratitis nach CXL 7). In der bereits mit CXL behandelten Hornhaut kam es innerhalb von 21 Tagen zu einer raschen Rückbildung, deutlich kürzer als die üblichen 2–4 Monate. Als Mechanismus wird eine verstärkte Kollagenvernetzung durch CXL → erhöhte interlamelläre Kohäsionskraft des vorderen Stromas → erhöhte Quellresistenz vermutet. Die vernetzte Hornhaut ist resistenter gegen enzymatischen Abbau, was zur frühen Rückbildung beiträgt.
Eine Technik zur Echtzeitanpassung von Nahttiefe und -spannung mittels intraoperativer OCT (iOCT) wurde berichtet.
Kaur et al. (2025) führten bei 7 Patienten (Altersmedian 16 Jahre, präoperative Hornhautdicke 1120–2363 μm) eine iOCT-gesteuerte partielle Kompressionsnaht (PTS, Zielteife 50–60 %) durch2). Die Nähte wurden unter iOCT-Sichtkontrolle des stromalen Compactions mit „raupenartigem“ Aussehen platziert; alle Fälle klangen innerhalb von 2 Wochen ab, die Fäden wurden nach 8–12 Wochen entfernt. Die PTS zeigte eine ähnliche Wirksamkeit wie die Vollschichtnaht (FTS) bei geringerem Risiko einer Endothelschädigung.
Eine Literaturübersicht (19 Studien) ergab eine Rückbildungszeit der Kompressionsnaht von 1 Stunde bis 45 Tagen, wobei die meisten Fälle innerhalb von 2 Wochen abklangen2).
Liu et al. berichteten über eine zweistufige Operation: TKP-gestützte Epikeratophakie (Reparatur der Descemet-Membran im ersten Schritt) gefolgt von DALK mit demselben Transplantat (zweiter Schritt) nach 2,1 ± 0,7 Monaten, wodurch eine Sehverbesserung erreicht wurde2).
Petrelli et al. führten nach erfolgloser Cyanacrylat-Klebung einer Hornhautperforation nach ACH eine lamelläre Keilresektion durch2). Dadurch wurde eine Hornhauttransplantation vermieden und die Refraktion verbessert.
Alio et al. injizierten 0,3 ml angereichertes plättchenreiches Plasma (EPRP) in die Vorderkammer bei SF6-refraktären Fällen und erzielten eine Rückbildung innerhalb einer Woche 1). Die Förderung der Endothelzellregeneration durch Wachstumsfaktoren wurde als Mechanismus vermutet.
Für Fälle mit großem Descemet-Membranriss wurde eine Methode berichtet, bei der ein 5 mm großer DMEK-Patch verwendet wird, um die Rissstelle vorübergehend zu verschließen 1). Es wurden Fälle beschrieben, bei denen die Hornhaut nach einer teilweisen Transplantatablösung spontan eine Deturgeszenz zeigte.
Ontiveros-Holguín & Pacheco-Padrón (2022) berichteten über einen Fall von ACH und ICRS-Wanderung nach Implantation intrakornealer Ringsegmente (ICRS) 8). Die ACH bildete sich nach 8 Wochen unter alleiniger konservativer Behandlung zurück. Dies gilt als erster Bericht einer ACH nach ICRS-Implantation, die sich allein durch konservative Behandlung erholte.
Es handelt sich um eine Kompressionsnaht, die unter intraoperativer OCT (iOCT) durchgeführt wird, um die Nahttiefe und -spannung in Echtzeit zu überprüfen 3). Im Gegensatz zur herkömmlichen Methode, die auf Erfahrung beruhte, kann die Nahttiefe objektiv kontrolliert werden, was eine effektive Hornhautkompression bei reduziertem Endothelschadenrisiko ermöglicht. Im Bericht von Kaur et al. bildeten sich alle Fälle innerhalb von 2 Wochen zurück.