Grade 1
Diamètre maximal de l’œdème : ≤ 3 mm
Caractéristiques de la lésion : Œdème stromal localisé, limité à une partie de la cornée.

L’hydrops cornéen aigu (ACH) est une complication rare des ectasies cornéennes. Il s’agit d’une rupture de la membrane de Descemet et de l’endothélium cornéen, entraînant un afflux rapide d’humeur aqueuse dans le stroma cornéen et un œdème cornéen brutal.
La maladie sous-jacente la plus fréquente est le kératocône, mais il survient également dans le kératoglobe et la dégénérescence marginale pellucide (DMP).
L’incidence est la suivante 1) :
L’âge de survenue varie de 5 à 59 ans, avec un pic entre 20 et 40 ans 1). Le risque chez les hommes est jusqu’à deux fois plus élevé que chez les femmes. Des différences ethniques sont observées : en Nouvelle-Zélande, la prévalence est plus élevée chez les insulaires du Pacifique, et au Royaume-Uni chez les personnes d’origine sud-asiatique et noire.
Selon les connaissances les plus récentes, une simple rupture de la membrane de Descemet ne suffit pas à provoquer un ACH ; une perte de substance du stroma cornéen postérieur est également nécessaire. Une étude rapporte que sur 16 yeux ayant subi une rupture de la membrane de Descemet lors d’une DMEK, aucun ACH n’est survenu, tandis que sur 5 yeux présentant une perforation du stroma postérieur, tous ont développé un ACH 1).
On estime qu’il survient chez environ 2,4 à 3 % des patients atteints de kératocône, 6 à 11,5 % des patients atteints de dégénérescence marginale pellucide, et environ 11 % des patients atteints de kératoglobe 1). Le risque est d’autant plus élevé que l’ectasie cornéenne est sévère, et une attention particulière est nécessaire chez les patients ayant l’habitude de se frotter les yeux.
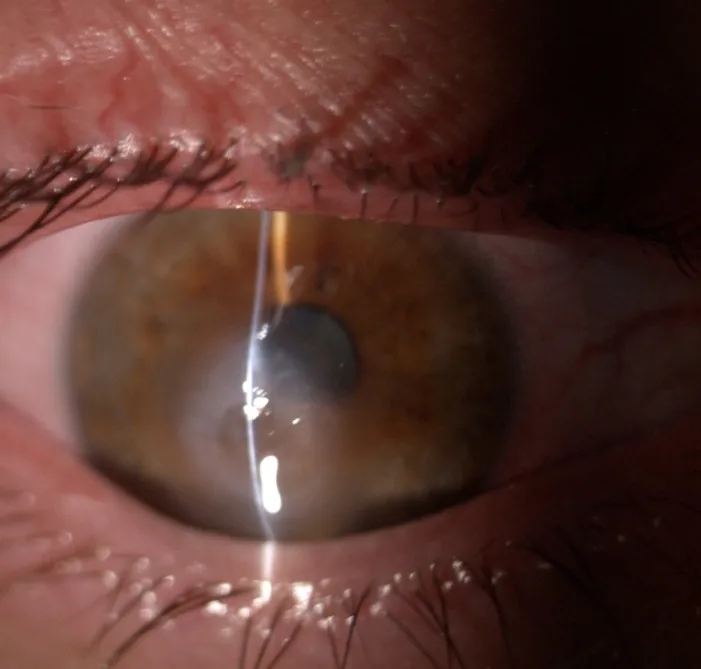
Les principaux symptômes subjectifs de l’ACH sont les suivants :
Les facteurs déclenchants incluent des actions qui augmentent temporairement la pression intraoculaire, comme se frotter les yeux, éternuer, tousser, se moucher ou faire un exercice intense. Cela peut aussi survenir spontanément.
À la lampe à fente, on observe une hyperhémie conjonctivale, un œdème stromal cornéen, un œdème épithélial, des fentes intrastromales et des bulles épithéliales1).
La classification par grade selon l’étendue de l’œdème est présentée ci-dessous1).
Grade 1
Diamètre maximal de l’œdème : ≤ 3 mm
Caractéristiques de la lésion : Œdème stromal localisé, limité à une partie de la cornée.
Grade 2
Diamètre maximal de l’œdème : 3 à 5 mm
Caractéristiques de la lésion : Œdème modéré, pouvant affecter l’axe visuel.
Grade 3
Diamètre maximal de l’œdème : > 5 mm
Caractéristiques de la lésion : Œdème étendu, opacité sévère incluant l’axe visuel. Le cas le plus jeune (fille de 5 ans) a rapporté un œdème cornéen total de limbe à limbe8).
Pour l’évaluation de la transparence cornéenne, une classification en 5 grades de Grade 0 (chambre antérieure et iris totalement invisibles) à Grade 4 (totalement transparent) est également utilisée1).
L’OCT du segment antérieur (AS-OCT) permet de visualiser de manière non invasive la rupture et le décollement de la membrane de Descemet, les poches de liquide intrastromales et l’augmentation de l’épaisseur cornéenne1). La taille et la profondeur de la rupture sont des facteurs prédictifs du temps de résolution de l’ACH. Le test de Seidel peut être positif, mais cela est dû à une fuite d’humeur aqueuse à travers la cornée œdémateuse et non à une perforation.
Des cas d’ACH survenant chez des patients atteints d’ophtalmopathie basedowienne ont été rapportés, l’augmentation de la pression intraoculaire et l’inflammation de la surface oculaire pouvant être des facteurs de risque7).
En ce qui concerne le risque d’infection, une étude rapporte que 2,7 % (3/112) des cas d’ACH ont développé une kératite infectieuse5). Tous les cas étaient des hommes atteints de dermatite atopique sévère, âgés en moyenne de 46 ans. Les cultures ont révélé MSCNS et MSSA.
Se frotter les yeux exerce une force mécanique sur la membrane de Descemet, ce qui peut directement provoquer une rupture de cette membrane chez les patients dont la cornée est déjà amincie et dilatée 1). Les patients atteints de dermatite atopique sont particulièrement à risque car ils ont tendance à se frotter les yeux en raison des démangeaisons. En cas de démangeaisons, il est important de contrôler les symptômes à l’aide de collyres.
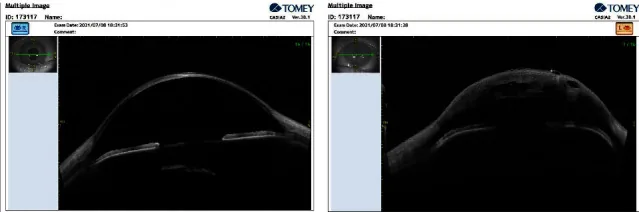
Le diagnostic de l’ACH repose sur les signes cliniques et est complété par divers examens d’imagerie.
C’est l’examen de base du diagnostic. On recherche une hyperhémie conjonctivale, un œdème stromal, un œdème épithélial et des fentes intrastromales 1). Le test de Seidel est réalisé pour différencier une perforation.
Les caractéristiques des principales modalités d’examen sont présentées ci-dessous.
| Méthode d’examen | Principaux éléments évalués | Caractéristiques |
|---|---|---|
| AS-OCT | Rupture de DM et clivages stromaux | Non contact, quantitatif |
| Microscope ultrasonique biomicroscopique | Site de rupture, épaisseur cornéenne | Surveillance de la résolution |
| Microscopie confocale in vivo (IVCM) | Cellules inflammatoires, œdème | Évaluation au niveau cellulaire |
Le traitement de l’ACH commence par un traitement conservateur ; en cas d’amélioration insuffisante ou si une résolution précoce est nécessaire, un traitement chirurgical est envisagé.
Les médicaments suivants sont utilisés1)9).
La résolution spontanée sous traitement conservateur prend 2 à 4 mois (maximum 5 à 36 semaines)1). En revanche, dans les yeux ayant subi une cross-linking cornéen (CXL), la résolution est nettement plus rapide, avec des cas de résolution complète en 3 semaines rapportés7).
Elle est réalisée dans le but d’accélérer la résolution, de soulager les symptômes et de minimiser les cicatrices cornéennes.
Injection de gaz dans la chambre antérieure
pneumatic descemetopexy : injection d’air, de SF6 ou de C3F8 dans la chambre antérieure pour déployer et réappliquer les bords de la membrane de Descemet par effet de tamponnement1).
Délai de résolution : 2 à 7 semaines (significativement plus court que les 64 à 117 jours du traitement conservateur).
Fréquence de réinjection : air 77,8 %, SF6 66,7 %, C3F8 0 à 35,7 % nécessitent une réinjection.
Sutures de compression
compression sutures : sutures pour comprimer et fermer la zone de rupture de la membrane de Descemet. Il existe des sutures transfixiantes (FTS) et des sutures partielles (PTS)2).
Délai de résolution : d’après une revue de la littérature, de 1 heure à 45 jours. La plupart des cas se résolvent en moins de 2 semaines2).
Association avec de l’air intracamérulaire : une résolution complète en moins de 2 semaines a été rapportée avec 3 FTS + air (remplissage à 50 % de la chambre antérieure)3).
Greffe de cornée
Kératoplastie endothéliale (DSAEK/DMEK) : envisagée en cas de rupture importante de la membrane de Descemet1).
Kératoplastie lamellaire antérieure profonde (pDALK) : permet de fermer la DM, de restaurer la courbure cornéenne et la vision en une seule intervention.
Kératoplastie transfixiante (PKP) : réalisée pour les cicatrices cornéennes opaques après ACH. La survie du greffon à long terme après PKP pour ACH est inférieure à celle des cas non-ACH3).
Un exemple de prescription de collyres typique après sutures de compression est présenté3).
| Médicament | Dose et fréquence |
|---|---|
| moxifloxacine 0,5 % | 4 fois/jour |
| acétate de prednisolone 1 % | Réduction progressive selon les besoins |
| NaCl 5 % | 1 fois au coucher |
De nombreux cas disparaissent en 2 à 4 mois avec un traitement conservateur seul1). Cependant, des cicatrices cornéennes et des néovaisseaux peuvent persister après la disparition, entraînant une déficience visuelle permanente. L’injection de gaz dans la chambre antérieure ou la suture compressive peuvent réduire la disparition à environ 2 semaines et minimiser la formation de cicatrices. Il est important de discuter avec le médecin traitant pour décider de la stratégie thérapeutique.
Il s’agit d’une intervention chirurgicale consistant à injecter de l’air ou un gaz spécial (SF6, C3F8, etc.) dans la chambre antérieure, dont l’effet de tamponnade soutient la zone de rupture de la membrane de Descemet de l’intérieur pour favoriser la réadhésion 1). La résolution, qui nécessite 64 à 117 jours avec un traitement conservateur, peut être réduite à 2 à 7 semaines. Cependant, un glaucome par bloc pupillaire ou une réinjection peuvent survenir.
Traditionnellement, on supposait un mécanisme de microtraumatisme (par exemple, frottement des yeux) → rupture de la membrane de Descemet → infiltration de l’humeur aqueuse dans le stroma → séparation des couches lamellaires → œdème 1).
Des études récentes montrent qu’un défaut isolé de la membrane de Descemet ne provoque pas d’ACH ; un défaut du stroma cornéen postérieur est également nécessaire 1). Cette découverte est importante pour expliquer pourquoi l’ACH ne survient que dans les cas d’ectasie cornéenne sévère.
Dans les spécimens de kératoplastie transfixiante (PKP) de cornées ACH, on observe des lamelles stromales lâchement disposées. La laminine et le collagène de type IV sont localisés à proximité de la membrane de Descemet enroulée, ce qui jouerait un rôle important dans la migration et la régénération des cellules endothéliales 1).
Le tiers antérieur du stroma cornéen ne gonfle que légèrement en raison de l’entrelacement lamellaire. Les deux tiers postérieurs, constitués de fibrilles non entrecroisées et unidirectionnelles, peuvent gonfler jusqu’à trois fois leur épaisseur 7).
Les cellules endothéliales cornéennes adjacentes migrent vers la zone de rupture de la membrane de Descemet, rétablissant la fonction de pompe endothéliale, ce qui entraîne une déshydratation cornéenne et une réparation finale par formation de cicatrice 1). La suture compressive rapproche physiquement les bords de la membrane de Descemet, favorisant la migration des cellules endothéliales.
Des études en microscopie confocale in vivo ont montré que les cas où les cellules inflammatoires persistent plus de 4 semaines présentent un risque élevé de néovascularisation cornéenne 1).
Varshney et al. (2021) ont rapporté un cas d’ACH compliquant une kératite après CXL 7). Dans la cornée déjà traitée par CXL, la résolution a été rapide en 21 jours, nettement plus courte que les 2 à 4 mois habituels. Le mécanisme suggéré est le renforcement des liaisons croisées de collagène par le CXL, augmentant la force de cohésion interlamellaire du stroma antérieur et la résistance au gonflement. La cornée réticulée est plus résistante à la digestion enzymatique, ce qui contribuerait à la résolution précoce.
Une technique permettant d’ajuster en temps réel la profondeur et la tension des sutures à l’aide de l’OCT peropératoire (iOCT) a été rapportée.
Kaur et al. (2025) ont réalisé une suture compressive partielle (PTS, profondeur cible 50-60 %) guidée par iOCT chez 7 patients (âge médian 16 ans, épaisseur cornéenne préopératoire 1120-2363 μm)2). Les sutures ont été placées sous visualisation iOCT de la compaction stromale d’aspect « chenille », et toutes ont disparu en 2 semaines, les sutures étant retirées après 8 à 12 semaines. La PTS a montré une efficacité similaire à la suture transfixiante (FTS) avec un risque moindre de lésion endothéliale.
Une revue de la littérature (19 études) a rapporté un délai de résolution de la suture compressive allant de 1 heure à 45 jours, la plupart des cas se résolvant en 2 semaines2).
Liu et al. ont rapporté une chirurgie en deux étapes : une TKP-assisted epikeratophakia (réparation de la membrane de Descemet lors de la première étape) suivie d’une DALK utilisant le même greffon (deuxième étape) 2,1 ± 0,7 mois plus tard, permettant une récupération visuelle2).
Petrelli et al. ont réalisé une résection cunéiforme lamellaire après échec de la colle cyanoacrylate pour une perforation cornéenne post-ACH2). Cela a permis d’éviter une greffe de cornée tout en améliorant la réfraction.
Alio et al. ont injecté 0,3 ml de plasma riche en plaquettes enrichi (EPRP) dans la chambre antérieure chez des cas réfractaires au SF6, et ont obtenu une résolution en une semaine 1). La promotion de la régénération des cellules endothéliales par les facteurs de croissance a été suggérée comme mécanisme.
Pour les cas présentant une large rupture de la membrane de Descemet, une méthode utilisant un petit patch DMEK de 5 mm pour fermer temporairement la rupture a été rapportée 1). Des cas où la cornée a spontanément retrouvé sa détersion après un décollement partiel du greffon ont été décrits.
Ontiveros-Holguín & Pacheco-Padrón (2022) ont rapporté un cas d’ACH et de migration d’ICRS après implantation d’anneaux intracornéens (ICRS) 8). L’ACH a disparu après 8 semaines avec un traitement conservateur seul. Il s’agit du premier rapport d’ACH après implantation d’ICRS guéri uniquement par traitement conservateur.
Il s’agit d’une suture compressive réalisée sous guidage par OCT peropératoire (iOCT) pour vérifier en temps réel la profondeur et la tension de la suture 3). Contrairement à la méthode conventionnelle qui reposait sur l’expérience, la profondeur de suture peut être contrôlée objectivement, permettant une compression cornéenne efficace tout en réduisant le risque de lésion endothéliale. Dans le rapport de Kaur et al., tous les cas ont disparu en moins de 2 semaines.