
Complicanze oftalmiche dei corticosteroidi
1. Cosa sono le complicanze oftalmologiche dei corticosteroidi
Sezione intitolata “1. Cosa sono le complicanze oftalmologiche dei corticosteroidi”I corticosteroidi surrenalici (glucocorticoidi) sono farmaci essenziali per il trattamento di un’ampia gamma di malattie, tra cui malattie autoimmuni, malattie infiammatorie oculari e infiammazioni post-operatorie. Tuttavia, il loro uso a lungo termine o ad alte dosi può causare gravi effetti collaterali agli occhi.
La cataratta steroidea è la più frequente opacità del cristallino indotta da farmaci e, una volta insorta, può portare a un grave deficit visivo in tempi relativamente brevi. Si verifica più spesso con la somministrazione sistemica, ma può manifestarsi anche con terapia inalatoria o colliri a lungo termine. I pazienti in terapia steroidea necessitano di regolari controlli oculistici.
Le principali malattie e situazioni in cui gli steroidi vengono utilizzati in oftalmologia sono le seguenti:
- Reazioni allergiche e di ipersensibilità: raffreddore da fieno, cheratocongiuntivite primaverile, congiuntivite allergica
- Uveite (anteriore, posteriore, panuveite): Prevenzione delle recidive e controllo dell’infiammazione
- Sclerite ed episclerite: Infiammazione autoimmune
- Arterite a cellule giganti: Somministrazione sistemica d’emergenza per proteggere la vista
- Gestione dell’infiammazione post-operatoria: Dopo chirurgia della cataratta o trapianto di cornea
- Malattie erpetiche oculari: riduzione dell’infiammazione nella cheratite stromale (in combinazione con antivirali)
- Malattie orbitali: oftalmopatia tiroidea, pseudotumore infiammatorio orbitario
Con la somministrazione a breve termine, le complicanze oculari sono rare, ma l’aumento della pressione intraoculare può manifestarsi circa due settimane dopo l’inizio del trattamento. La cataratta di solito si verifica con l’uso a lungo termine, ma nei cosiddetti steroidi-responder la pressione oculare può aumentare anche in breve tempo; pertanto, si raccomanda un monitoraggio regolare della pressione intraoculare indipendentemente dalla durata del trattamento.
2. Principali sintomi e segni clinici
Sezione intitolata “2. Principali sintomi e segni clinici”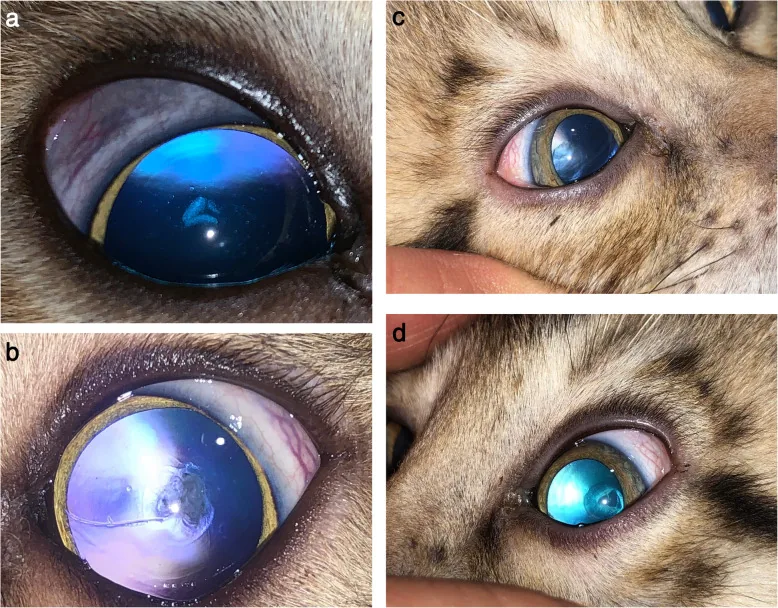
Sintomi soggettivi
Sezione intitolata “Sintomi soggettivi”Cataratta sottocapsulare posteriore (cataratta steroidea):
- Riduzione dell’acuità visiva (la riduzione diventa significativa quando l’opacità raggiunge un diametro di 3 mm o più)
- Fotofobia e abbagliamento (ipersensibilità alla luce e fastidio visivo)
- Marcata riduzione della sensibilità al contrasto nonostante una buona acuità visiva
- Spesso si avverte un deficit visivo già quando l’opacità è ancora piccola
- Spesso è asintomatico (difficile da percepire anche con pressione oculare elevata)
- Con pressione oculare elevata si possono lamentare pesantezza oculare, fastidio e visione offuscata
- Difetti del campo visivo (in fase avanzata, perdita della visione periferica)
Stadi di progressione dell’opacità
Sezione intitolata “Stadi di progressione dell’opacità”| Stadio | Reperto |
|---|---|
| Iniziale | Sottile opacità puntiforme o vacuoli subito sotto la capsula posteriore sull’asse visivo |
| Stadio avanzato | Le opacità puntiformi confluiscono in un’opacità sottocapsulare posteriore a forma di disco, ben definita e omogenea (diametro 2-3 mm). Granuli policromatici blu, verdi e rossi. |
| Ulteriore progressione | Estensione nella corteccia anteriore. Ci vuole tempo per espandersi oltre il confine. |
| Fase tardiva | Aumento dell’intensità di retrodispersione nel nucleo fetale → complicanza di cataratta nucleare |
La cataratta steroidea è comunemente riconosciuta come cataratta sottocapsulare posteriore, ma il rischio di cataratta nucleare è elevato e la loro coesistenza non è rara. La PSC progredisce più rapidamente rispetto ad altri tipi di cataratta; tre grandi studi hanno dimostrato che la PSC progredisce più velocemente della cataratta nucleare e corticale3).
Reperti del glaucoma steroideo:
- Angolo aperto (nessuna anomalia angolare)
- Aumento della pressione intraoculare (spesso superiore a 30 mmHg)
- Accumulo di matrice extracellulare nel trabecolato
- Nei casi cronici, escavazione della papilla ottica e assottigliamento dello strato di fibre nervose retiniche
| Complicanze | Opacità/segni tipici | Sintomi soggettivi precoci |
|---|---|---|
| Cataratta steroidea | Opacità sottocapsulare posteriore a disco (4 stadi di progressione) | Abbagliamento/fotofobia |
| Glaucoma steroideo | Allargamento dell’escavazione del disco ottico | Quasi asintomatico |
La tipica cataratta steroidea si presenta come un opacità a forma di disco sotto la capsula posteriore sull’asse visivo, caratterizzata da granuli policromatici. Anche nella cataratta senile può verificarsi opacità sottocapsulare posteriore, ma se si osserva una cataratta sottocapsulare posteriore entro i 40 anni, è necessario indagare attivamente una storia di uso di steroidi. In alcuni casi, può essere difficile distinguerla dalla cataratta complicata da uveite.
3. Cause e fattori di rischio
Sezione intitolata “3. Cause e fattori di rischio”Rischio per via di somministrazione
Sezione intitolata “Rischio per via di somministrazione”Il rischio di complicanze oculari da steroidi varia a seconda della via di somministrazione. La somministrazione sistemica comporta il rischio più elevato, ma anche la somministrazione topica può causare la condizione con l’uso a lungo termine1).
- Somministrazione sistemica (orale/endovenosa): Rischio più elevato sia per cataratta che per glaucoma. L’insorgenza con dosi di prednisolone equivalenti a 10 mg/die o inferiori è relativamente rara. Si verifica spesso in casi di somministrazione sistemica ad alte dosi per oltre un anno.
- Colliri steroidei: Rischio inferiore rispetto alla somministrazione sistemica, ma l’uso prolungato può causare cataratta sottocapsulare posteriore e aumento della pressione intraoculare3)
- Steroidi inalatori (terapia dell’asma): Rischio di cataratta sottocapsulare posteriore8)
- Steroidi nasali: Secondo una revisione sistematica, non esiste un rischio significativo di cataratta o aumento della pressione intraoculare9)
- Iniezione intravitreale di triamcinolone: provoca un aumento della pressione intraoculare in oltre il 50% dei casi, di cui l’1-2% richiede un intervento chirurgico2)
Fattori di rischio per la cataratta
Sezione intitolata “Fattori di rischio per la cataratta”Le linee guida AAO per la pratica clinica della cataratta (Preferred Practice Pattern) indicano che l’uso sistemico di steroidi è un fattore di rischio per la cataratta sottocapsulare posteriore e che gli utilizzatori a lungo termine di corticosteroidi per via inalatoria o orale hanno un rischio maggiore di sviluppare la cataratta3).
- I bambini sono più suscettibili degli adulti a sviluppare la cataratta steroidea
- I pazienti che ricevono una terapia sistemica a lungo termine per malattie sistemiche (collagenopatie, LES, artrite reumatoide, sindrome nefrosica, post-trapianto renale) sono a rischio particolarmente elevato
Fattori di rischio del glaucoma
Sezione intitolata “Fattori di rischio del glaucoma”- Glaucoma primario ad angolo aperto preesistente
- Precedente aumento della pressione intraoculare dovuto a somministrazione di steroidi (responder agli steroidi)
- Diabete di tipo 1
- Bambini e anziani (alta reattività)
- Uso a lungo termine superiore a 3 mesi2)
4. Diagnosi e metodi di esame
Sezione intitolata “4. Diagnosi e metodi di esame”Diagnosi della cataratta
Sezione intitolata “Diagnosi della cataratta”L’osservazione del cristallino con la lampada a fessura (slit lamp) è fondamentale.
- Punti di osservazione: presenza di opacità a forma di piatto sotto la capsula posteriore e granuli policromatici, diametro dell’opacità (≥2 mm causa deficit visivo)
- Metodo di retroilluminazione: facilita l’identificazione di opacità sottocapsulari posteriori e vacuoli
- Valutazione della funzione visiva: anche con buona acuità visiva corretta, la sensibilità al contrasto può essere significativamente ridotta, portando talvolta a un intervento chirurgico precoce
- Classificazione LOCS III: valuta l’opacità in 4 categorie: nucleare (NO/NC), corticale (C) e sottocapsulare posteriore (PSC). La PSC valuta il grado di opacità sottocapsulare posteriore con retroilluminazione4)
Nella diagnosi, la cosa più importante è un’anamnesi dettagliata dell’uso di steroidi, verificando la via di somministrazione (sistemica, collirio, inalazione, spray nasale), il dosaggio e la durata del trattamento. Nei pazienti con uveite che usano steroidi, può essere difficile distinguere dalla cataratta complicata da uveite. Anche la storia di esposizione a radiazioni e traumi oculari deve essere verificata come fattori di rischio per la cataratta sottocapsulare posteriore 3).
Diagnosi del glaucoma
Sezione intitolata “Diagnosi del glaucoma”- Misurazione della pressione intraoculare: la misurazione con tonometro ad applanazione di Goldmann è lo standard
- Esame dell’angolo: presenza di angolo aperto o anomalie angolari
- Esame del campo visivo: valutazione del danno del campo visivo mediante perimetria statica di Humphrey
- Valutazione del nervo ottico: valutazione della morfologia della testa del nervo ottico e dello strato di fibre nervose retiniche mediante OCT
L’acuità visiva misura la capacità di discriminare stimoli ad alto contrasto (nitidi in bianco e nero), mentre la sensibilità al contrasto è la capacità di distinguere sottili differenze di luminosità. Nella cataratta sottocapsulare posteriore, la sensibilità al contrasto è spesso significativamente ridotta anche se l’acuità visiva è relativamente buona, causando difficoltà nelle attività quotidiane (camminare in luoghi poco illuminati, guidare, ecc.). Se la riduzione della sensibilità al contrasto è marcata, può essere indicato un intervento chirurgico anche in presenza di buona acuità visiva.
5. Trattamento standard
Sezione intitolata “5. Trattamento standard”Trattamento della cataratta steroidea
Sezione intitolata “Trattamento della cataratta steroidea”Gestione conservativa:
- Il trattamento farmacologico della cataratta non ha prove sufficienti di efficacia e non è raccomandato3)
- Per piccole opacità centrali è possibile migliorare temporaneamente l’acuità visiva con colliri midriatici, ma occorre prestare attenzione al peggioramento dell’abbagliamento.
- Valutare la riduzione alla dose minima efficace di steroidi o la sospensione (conciliandola con la gestione della malattia di base).
Indicazioni chirurgiche:
- L’intervento chirurgico è spesso necessario quando l’opacità sottocapsulare posteriore ha un diametro di 2 mm o più e causa compromissione della funzione visiva.
- Se la sensibilità al contrasto è marcatamente ridotta, si considera l’intervento chirurgico anche in presenza di buona acuità visiva
- Poiché la PSC progredisce rapidamente, spesso è necessario un intervento precoce
Metodo chirurgico:
- Prevalentemente facoemulsificazione + impianto di IOL
- Attenzione intraoperatoria (importante): negli occhi con opacità sottocapsulare posteriore, la capsula posteriore può essere fragile, pertanto è necessario prestare attenzione alla rottura capsulare posteriore
- Nei casi con uveite di base, l’intervento chirurgico viene eseguito in un periodo relativamente stabile continuando la somministrazione orale di steroidi. L’impianto di IOL non presenta problemi
- Se esiste la possibilità che sia necessario un intervento di filtrazione per il glaucoma secondario, si esegue l’intervento con incisione corneale preservando la congiuntiva superiore
Gestione postoperatoria:
- Il controllo dell’infiammazione della malattia di base (come l’uveite) è importante
- Durante la somministrazione continuativa di steroidi, il rischio di cataratta secondaria (PCO) è elevato
Trattamento del glaucoma steroideo
Sezione intitolata “Trattamento del glaucoma steroideo”Prima scelta: riduzione o sospensione degli steroidi
- Se possibile, dare priorità alla riduzione o alla sospensione degli steroidi. Tuttavia, a causa della gestione della malattia di base, la riduzione può essere difficile.
- In alcuni casi, i cambiamenti tissutali possono essere irreversibili, quindi è importante un intervento precoce.
Terapia ipotensiva oculare (simile al glaucoma primario ad angolo aperto):
- Utilizzare nell’ordine: analoghi delle prostaglandine, beta-bloccanti, inibitori dell’anidrasi carbonica (collirio o orali), agonisti dei recettori α₂.
- Se la pressione intraoculare non è controllabile con colliri o farmaci orali, è necessario un intervento chirurgico2)
Trattamento chirurgico:
- Trabeculotomia: è un’opzione per il glaucoma steroideo quando il controllo della pressione intraoculare con farmaci è insufficiente. Studi multicentrici riportano che è efficace nel controllo della pressione intraoculare negli occhi con glaucoma steroideo13)
- Trabeculoplastica laser selettiva: è efficace, ma non deve essere eseguita in caso di uveite associata
- Trabeculectomia (chirurgia filtrante): eseguita quando l’incisione è insufficiente
In molti casi, la sospensione o la riduzione degli steroidi porta a una diminuzione della pressione intraoculare. Tuttavia, se l’uso prolungato ha causato cambiamenti tissutali irreversibili nel trabecolato (accumulo di matrice extracellulare), la pressione potrebbe non migliorare dopo la sospensione, rendendo necessari farmaci ipotensivi oculari o un intervento chirurgico. Se la sospensione è difficile a causa della malattia di base, l’oculista e il medico curante collaborano per la gestione.
L’intervento chirurgico in sé può dare buoni risultati, come nella normale chirurgia della cataratta. Tuttavia, durante la somministrazione continua di steroidi, il rischio di cataratta secondaria (PCO) è elevato, ed è necessario un follow-up regolare anche dopo l’operazione. La PCO può essere trattata con capsulotomia posteriore con laser Nd:YAG. Poiché la capsula posteriore può essere fragile, è richiesta una tecnica chirurgica attenta per evitare la rottura della capsula posteriore durante l’intervento.
6. Fisiopatologia e meccanismi dettagliati di insorgenza
Sezione intitolata “6. Fisiopatologia e meccanismi dettagliati di insorgenza”Meccanismo della cataratta steroidea
Sezione intitolata “Meccanismo della cataratta steroidea”Il meccanismo di insorgenza della cataratta steroidea non è stato completamente chiarito, ma sono stati riportati diversi meccanismi5)6)10).
- Teoria della formazione di un intermedio di base di Schiff: Si forma una base di Schiff tra il gruppo C-20 chetonico dello steroide e un gruppo nucleofilo delle proteine del cristallino. Successivamente avviene un riarrangiamento di Heyns del gruppo C-21 idrossilico, generando un addotto amminico stabile. Si ritiene che questo addotto sia osservato solo nella cataratta steroidea indotta5)
- Anomalie metaboliche e della funzione di membrana: Alterazione del trasporto ionico nelle cellule epiteliali del cristallino
- Danno ossidativo: Denaturazione delle proteine del cristallino (aggregazione della cristallina) dovuta alla produzione di radicali liberi
- Meccanismo mediato dal recettore dei glucocorticoidi: Il recettore dei glucocorticoidi influenza oltre 5.000 geni, causando anomalie nelle molecole di adesione cellulare10)
- Formazione di addotti proteici
- Riduzione della trasparenza delle fibre del cristallino nella capsula posteriore e aggregazione della cristallina
- Migrazione verso la capsula posteriore delle cellule danneggiate dell’equatore del cristallino6)
La cataratta sottocapsulare posteriore si verifica sull’asse visivo, causando disturbi visivi relativamente precoci. Se il diametro dell’opacità è di almeno 1 mm, la funzione visiva è compromessa; con 2 mm o più, la sensibilità al contrasto diminuisce notevolmente anche se l’acuità visiva corretta è buona; con 3 mm o più, spesso anche l’acuità visiva diminuisce.
Meccanismo del glaucoma steroideo
Sezione intitolata “Meccanismo del glaucoma steroideo”I glucocorticoidi aumentano la pressione intraoculare riducendo il deflusso dell’umore acqueo dalla camera anteriore.
- Aumento della produzione di matrice extracellulare nelle cellule del trabecolato: gli steroidi inibiscono la degradazione della matrice extracellulare (fibronectina, laminina, collagene, ecc.) delle cellule del trabecolato e ne promuovono la deposizione. Ciò ostruisce la struttura reticolare del trabecolato, compromettendo il deflusso dell’umore acqueo.
- Induzione della miocilina (myocilin): la miocilina è una proteina di 55 kDa indotta nelle cellule del trabecolato quando esposte a steroidi, ed è coinvolta nella riduzione del deflusso dell’umore acqueo e nell’aumento della pressione intraoculare indotto da steroidi2)
- Modificazioni del citoscheletro: la riorganizzazione del citoscheletro di actina provoca alterazioni morfologiche della via di deflusso dell’umore acqueo
La risposta pressoria oculare agli steroidi varia da individuo a individuo; nei giovani, nei casi di ipertensione oculare e in quelli con grave danno del nervo ottico può essere necessario un intervento chirurgico11). Nei responder agli steroidi, indipendentemente dalla via di somministrazione e dalla durata, è necessario un monitoraggio regolare della pressione intraoculare12).
Meccanismo dell’aumento del rischio infettivo
Sezione intitolata “Meccanismo dell’aumento del rischio infettivo”Il recettore dei glucocorticoidi sopprime la trascrizione di citochine e chemochine, inibendo la migrazione e l’attivazione delle cellule immunitarie. Ciò riduce l’immunità locale contro funghi, virus e batteri. In particolare, le infezioni fungine tendono a peggiorare sotto immunosoppressione da steroidi7).
7. Ricerche recenti e prospettive future
Sezione intitolata “7. Ricerche recenti e prospettive future”Sicurezza oftalmica degli steroidi intranasali
Sezione intitolata “Sicurezza oftalmica degli steroidi intranasali”Revisioni sistematiche recenti hanno mostrato che gli steroidi intranasali non sono significativamente associati al rischio di cataratta o aumento della pressione intraoculare9). Tuttavia, è stato sottolineato che anche steroidi considerati a “bassa penetrazione intraoculare”, come il fluorometolone e il loteprednolo, comportano un rischio di aumento della pressione intraoculare e cataratta con l’uso a lungo termine, richiedendo cautela.
Impianto a rilascio prolungato di fluocinolone acetonide
Sezione intitolata “Impianto a rilascio prolungato di fluocinolone acetonide”La ricerca sui dispositivi a rilascio prolungato di fluocinolone acetonide intravitreale sta avanzando e si suggerisce che possano essere utili per la gestione a lungo termine dell’uveite2). Tuttavia, rispetto ai corticosteroidi sistemici, gli effetti collaterali locali (aumento della pressione intraoculare e cataratta) sono più frequenti e richiedono una gestione personalizzata.
Identificazione genetica dei responder agli steroidi
Sezione intitolata “Identificazione genetica dei responder agli steroidi”Si ritiene che la risposta della pressione intraoculare agli steroidi sia geneticamente determinata e sono in corso studi per identificare geni correlati, come il gene della miocilina. In futuro, si prevede la realizzazione di una medicina personalizzata che, utilizzando informazioni genetiche, possa identificare precocemente i soggetti ad alto rischio di glaucoma steroideo12).
Sì, si raccomanda vivamente una visita oculistica regolare. L’aumento della pressione intraoculare spesso non presenta sintomi evidenti, e la cataratta iniziale è spesso asintomatica. Indipendentemente dalla via di somministrazione (sistemica, topica, inalatoria), i pazienti in trattamento a lungo termine necessitano di una valutazione oculistica (pressione intraoculare, cristallino, nervo ottico) almeno 1-2 volte l’anno. In particolare, il controllo della pressione intraoculare a 2 settimane-1 mese dall’inizio del trattamento è importante.
8. Riferimenti bibliografici
Sezione intitolata “8. Riferimenti bibliografici”-
McGhee CNJ, Dean S, Danesh-Meyer H. Locally administered ocular corticosteroids: benefits and risks. Drug Saf. 2002;25(1):33-55. PMID: 11820911. doi:10.2165/00002018-200225010-00004.
-
Okoye O, Okonkwo O. Inflammatory glaucoma. Community Eye Health. 2019;32(106):S1-S4.
-
Miller KM, Oetting TA, Tweeten JP, et al. Cataract in the Adult Eye Preferred Practice Pattern. Ophthalmology. 2022;129(1):P1-P126.
-
Chylack LT Jr, Wolfe JK, Singer DM, et al. The Lens Opacities Classification System III. Arch Ophthalmol. 1993;111(6):831-836. PMID: 8512486. doi:10.1001/archopht.1993.01090060119035.
-
Urban RC Jr, Cotlier E. Corticosteroid-induced cataracts. Surv Ophthalmol. 1986;31(2):102-110. PMID: 3541262. doi:10.1016/0039-6257(86)90077-9.
-
Jobling AI, Augusteyn RC. What causes steroid cataracts? A review of steroid-induced posterior subcapsular cataracts. Clin Exp Optom. 2002;85(2):61-75. PMID: 11952401. doi:10.1111/j.1444-0938.2002.tb03011.x.
-
Carnahan MC, Goldstein DA. Ocular complications of topical, peri-ocular, and systemic corticosteroids. Curr Opin Ophthalmol. 2000;11(6):478-483. PMID: 11141645.
-
Cumming RG, Mitchell P, Leeder SR. Use of inhaled corticosteroids and the risk of cataracts. N Engl J Med. 1997;337(1):8-14. PMID: 9203425. doi:10.1056/NEJM199707033370102.
-
Valenzuela CV, Liu JC, Vila PM, et al. Intranasal corticosteroids do not lead to ocular changes: a systematic review and meta-analysis. Laryngoscope. 2019;129(1):6-12. PMID: 30229924. PMCID: PMC6320292. doi:10.1002/lary.27209.
-
James ER. The etiology of steroid cataract. J Ocul Pharmacol Ther. 2007;23(5):403-420. PMID: 17900234. doi:10.1089/jop.2006.0067.
-
Sihota R, Konkal VL, Dada T, Agarwal HC, Singh R. Prospective, long-term evaluation of steroid-induced glaucoma. Eye (Lond). 2008;22(1):26-30. PMID: 16823461. doi:10.1038/sj.eye.6702474.
-
Phulke S, Kaushik S, Kaur S, Pandav SS. Steroid-induced glaucoma: an avoidable irreversible blindness. J Curr Glaucoma Pract. 2017;11(2):67-72. PMID: 28924342. PMCID: PMC5577123. doi:10.5005/jp-journals-10028-1226.
-
Japanese Steroid-Induced Glaucoma Multicenter Study Group. Success rates of trabeculotomy for steroid-induced glaucoma: a comparative, multicenter, retrospective cohort study. Am J Ophthalmol. 2011;151(6):1047-1056.e1. doi:10.1016/j.ajo.2010.11.028.
