
Complications ophtalmologiques des corticostéroïdes
1. Qu’est-ce que les complications ophtalmiques des corticostéroïdes ?
Section intitulée « 1. Qu’est-ce que les complications ophtalmiques des corticostéroïdes ? »Les corticostéroïdes (glucocorticoïdes) sont des médicaments essentiels pour traiter un large éventail de maladies, notamment les maladies auto-immunes, les maladies inflammatoires oculaires et l’inflammation postopératoire. Cependant, leur utilisation à long terme ou à fortes doses peut entraîner des effets secondaires oculaires graves.
La cataracte cortisonique est l’opacification du cristallin la plus fréquente due aux médicaments. Une fois qu’elle se développe, elle peut entraîner une perte de vision sévère en relativement peu de temps. Elle survient souvent après une administration systémique, mais peut également se développer après une inhalation ou une instillation de collyre à long terme. Les patients sous corticostéroïdes nécessitent des examens ophtalmologiques réguliers.
Les principales maladies et situations dans lesquelles les corticostéroïdes sont utilisés en ophtalmologie sont les suivantes :
- Réactions allergiques et d’hypersensibilité : rhinite allergique, conjonctivite printanière, conjonctivite allergique
- Uvéite (antérieure, postérieure, panuvéite) : Prévention des récidives et suppression de l’inflammation
- Sclérite et épisclérite : Inflammation auto-immune
- Artérite à cellules géantes : Administration systémique d’urgence pour protéger la vision
- Gestion de l’inflammation postopératoire : Après chirurgie de la cataracte ou greffe de cornée
- Maladies herpétiques oculaires : anti-inflammatoire pour la kératite stromale (en association avec des antiviraux)
- Maladies orbitaires : orbitopathie thyroïdienne, pseudotumeur inflammatoire orbitaire
Les complications ophtalmiques sont rares lors d’une administration à court terme, mais une augmentation de la pression intraoculaire peut apparaître environ deux semaines après le début du traitement. La cataracte survient généralement lors d’un traitement à long terme, mais chez les répondeurs aux stéroïdes, la pression intraoculaire peut augmenter même après une courte période. Il est donc recommandé de mesurer régulièrement la pression intraoculaire, quelle que soit la durée du traitement.
2. Principaux symptômes et signes cliniques
Section intitulée « 2. Principaux symptômes et signes cliniques »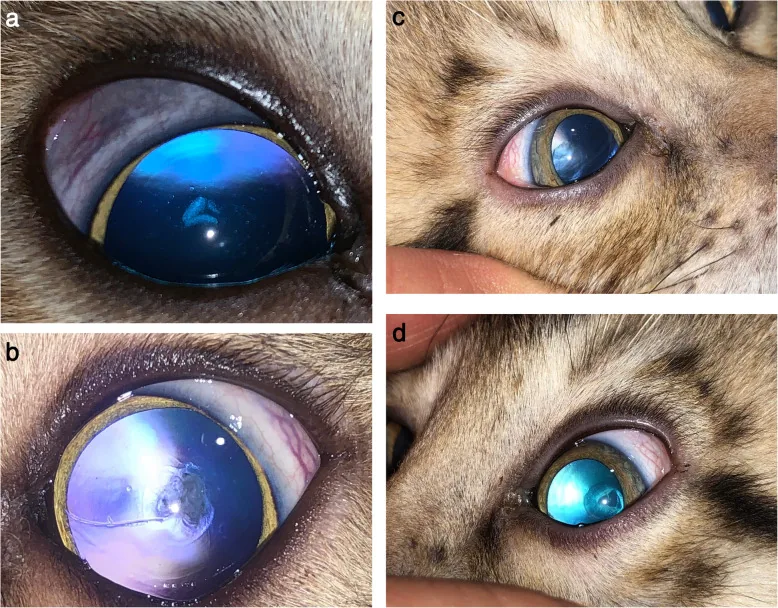
Symptômes subjectifs
Section intitulée « Symptômes subjectifs »Cataracte sous-capsulaire postérieure (cataracte stéroïdienne) :
- Baisse de l’acuité visuelle (l’opacité devient significative lorsque le diamètre atteint 3 mm ou plus)
- Photophobie et éblouissement (sensibilité à la lumière et éclat gênant)
- Diminution marquée de la sensibilité au contraste malgré une bonne acuité visuelle
- Souvent, les patients ressentent un trouble fonctionnel dès le début de l’opacité
- Souvent asymptomatique (la pression oculaire élevée est difficile à ressentir)
- En cas d’hypertension oculaire, le patient peut se plaindre de lourdeur, d’inconfort ou de vision trouble
- Déficit du champ visuel (à un stade avancé, perte de vision périphérique)
Stades de progression de l’opacité
Section intitulée « Stades de progression de l’opacité »| Stade | Observation |
|---|---|
| Initial | Légères opacités ponctuées ou vacuoles juste sous la capsule postérieure sur l’axe visuel |
| Stade avancé | Les opacités ponctuées fusionnent pour former une opacité sous-capsulaire postérieure en forme de soucoupe, bien délimitée et homogène (diamètre 2-3 mm). Granules polychromes bleus, verts et rouges. |
| Progression supplémentaire | Extension vers le cortex antérieur. Il faut du temps pour dépasser la ligne de démarcation. |
| Stade tardif | Augmentation de l’intensité de la rétrodiffusion dans le noyau embryonnaire → association d’une cataracte nucléaire |
La cataracte stéroïdienne est généralement reconnue comme une cataracte sous-capsulaire postérieure, mais le risque de cataracte nucléaire est également élevé et leur association n’est pas rare. La PSC progresse plus rapidement que les autres types de cataracte ; trois grandes études ont montré que la PSC progresse plus rapidement que la cataracte nucléaire et la cataracte corticale3).
Signes du glaucome stéroïdien :
- Angle ouvert (aucune anomalie angulaire détectée)
- Augmentation de la pression intraoculaire (souvent >30 mmHg)
- Accumulation de matrice extracellulaire dans le trabéculum
- Dans les cas chroniques, élargissement de l’excavation de la papille optique et amincissement de la couche des fibres nerveuses rétiniennes
| Complications | Opacités/observations typiques | Symptômes subjectifs précoces |
|---|---|---|
| Cataracte cortisonique | Opacité sous-capsulaire postérieure en disque (progression en 4 stades) | Éblouissement, photophobie |
| Glaucome stéroïdien | Élargissement de l’excavation papillaire | Presque asymptomatique |
La cataracte stéroïdienne typique se présente sous la forme d’une opacité en forme de soucoupe sous-capsulaire postérieure sur l’axe visuel, souvent accompagnée de granules polychromes, ce qui est caractéristique. Bien que l’opacité sous-capsulaire postérieure puisse également survenir dans la cataracte liée à l’âge, si elle est observée avant l’âge de 40 ans, il est nécessaire de rechercher activement des antécédents d’utilisation de stéroïdes. Il peut parfois être difficile de la distinguer d’une cataracte compliquée d’uvéite.
3. Causes et facteurs de risque
Section intitulée « 3. Causes et facteurs de risque »Risque selon la voie d’administration
Section intitulée « Risque selon la voie d’administration »Le risque de complications ophtalmiques liées aux stéroïdes varie selon la voie d’administration. L’administration systémique présente le risque le plus élevé, mais même l’administration locale peut entraîner l’apparition de la maladie en cas d’utilisation prolongée1).
- Administration systémique (orale/intraveineuse) : risque le plus élevé pour la cataracte et le glaucome. L’apparition à une dose équivalente de prednisolone inférieure à 10 mg/jour est relativement rare. Survient souvent chez les patients sous fortes doses systémiques prolongées pendant plus d’un an.
- Collyres stéroïdiens : risque plus faible que l’administration systémique, mais une utilisation à long terme peut entraîner une cataracte sous-capsulaire postérieure et une augmentation de la pression intraoculaire3).
- Stéroïdes inhalés (traitement de l’asthme) : risque de cataracte sous-capsulaire postérieure8).
- Stéroïdes nasaux : une revue systématique n’a pas trouvé de risque significatif de cataracte ou d’augmentation de la pression intraoculaire9).
- Injection intravitréenne de triamcinolone : une augmentation de la pression intraoculaire survient dans plus de 50 % des cas, dont 1 à 2 % nécessitent une intervention chirurgicale2)
Facteurs de risque de cataracte
Section intitulée « Facteurs de risque de cataracte »Le guide de pratique clinique de l’AAO (Preferred Practice Pattern) indique que l’utilisation systémique de stéroïdes est un facteur de risque de cataracte sous-capsulaire postérieure, et que les utilisateurs à long terme de corticostéroïdes inhalés ou oraux présentent un risque élevé de développer une cataracte3).
- Les enfants sont plus susceptibles que les adultes de développer une cataracte stéroïdienne
- Les patients recevant un traitement systémique à long terme pour des maladies systémiques (collagénose, lupus érythémateux disséminé, polyarthrite rhumatoïde, syndrome néphrotique, après transplantation rénale) présentent un risque particulièrement élevé
Facteurs de risque du glaucome
Section intitulée « Facteurs de risque du glaucome »- Glaucome primitif à angle ouvert préexistant
- Antécédents d’élévation de la pression intraoculaire due à un traitement antérieur par stéroïdes (répondeur aux stéroïdes)
- Diabète de type 1
- Enfants et personnes âgées (réactivité élevée)
- Utilisation à long terme de plus de 3 mois2)
4. Diagnostic et méthodes d’examen
Section intitulée « 4. Diagnostic et méthodes d’examen »Diagnostic de la cataracte
Section intitulée « Diagnostic de la cataracte »L’observation du cristallin à l’aide d’un microscope à lampe à fente (lampe à fente) est fondamentale.
- Points d’observation : présence d’une opacité en forme de soucoupe sous-capsulaire postérieure et de granules polychromes, diamètre de l’opacité (≥2 mm entraînant un trouble visuel fonctionnel)
- Transillumination : facilite la détection des opacités sous-capsulaires postérieures et des vacuoles
- Évaluation de la fonction visuelle : même avec une bonne acuité visuelle corrigée, la sensibilité au contraste peut être significativement réduite, justifiant parfois une chirurgie précoce
- Classification LOCS III : évaluation de l’opacité en quatre catégories : nucléaire (NO/NC), corticale (C) et sous-capsulaire postérieure (PSC). Pour la PSC, le degré d’opacité sous-capsulaire postérieure est évalué par transillumination4)
L’élément le plus important du diagnostic est l’interrogatoire détaillé sur l’utilisation de stéroïdes, en précisant la voie d’administration (systémique, collyre, inhalation, spray nasal), la dose et la durée du traitement. Chez les patients atteints d’uvéite utilisant des stéroïdes, la distinction avec une cataracte compliquée d’uvéite peut être difficile. Les antécédents d’exposition aux radiations et de traumatisme oculaire sont également à vérifier comme facteurs de risque de cataracte sous-capsulaire postérieure3).
Diagnostic du glaucome
Section intitulée « Diagnostic du glaucome »- Mesure de la pression intraoculaire : la mesure par tonomètre à aplanation de Goldmann est la référence
- Examen de l’angle iridocornéen : recherche d’un angle ouvert ou de anomalies de l’angle
- Examen du champ visuel : évaluation des défauts du champ visuel par périmétrie statique de Humphrey
- Évaluation du nerf optique : évaluation de la forme de la papille et de la couche des fibres nerveuses rétiniennes par OCT
L’acuité visuelle mesure la capacité à distinguer des cibles à haut contraste (noir et blanc net), tandis que la sensibilité au contraste est la capacité à percevoir de faibles différences de luminosité. Dans la cataracte sous-capsulaire postérieure, la sensibilité au contraste est souvent considérablement réduite même si l’acuité visuelle est relativement bonne, ce qui entraîne des difficultés dans la vie quotidienne (marche dans des endroits faiblement éclairés, conduite, etc.). Si la diminution de la sensibilité au contraste est marquée, une intervention chirurgicale peut être indiquée même si l’acuité visuelle est bonne.
5. Traitement standard
Section intitulée « 5. Traitement standard »Traitement de la cataracte stéroïdienne
Section intitulée « Traitement de la cataracte stéroïdienne »Traitement conservateur :
- Le traitement médicamenteux de la cataracte n’a pas de preuve suffisante d’efficacité et n’est pas recommandé3)
- Pour une petite opacité centrale, il est possible d’améliorer temporairement l’acuité visuelle avec des mydriatiques, mais il faut être attentif à l’aggravation de l’éblouissement.
- Envisager une réduction à la dose minimale efficace ou l’arrêt des stéroïdes (en conciliant avec la gestion de la maladie sous-jacente).
Indications chirurgicales :
- Une intervention chirurgicale est souvent nécessaire lorsque l’opacité sous-capsulaire postérieure a un diamètre ≥ 2 mm et entraîne une altération de la fonction visuelle.
- Si la sensibilité au contraste est nettement diminuée, envisager une chirurgie même si l’acuité visuelle est bonne
- La PSC progresse rapidement, donc une chirurgie précoce est souvent nécessaire
Méthode chirurgicale :
- Phacoémulsification + insertion d’IOL est la principale méthode
- Attention peropératoire (important) : Les yeux avec opacité sous-capsulaire postérieure peuvent avoir une capsule fragile, nécessitant une attention particulière pour éviter une rupture capsulaire.
- Dans les cas d’uvéite sous-jacente, l’intervention chirurgicale est réalisée pendant une période relativement calme, tout en poursuivant la corticothérapie orale. L’implantation d’un IOL ne pose pas de problème.
- Si une chirurgie filtrante pour glaucome secondaire peut être nécessaire, préservez la conjonctive supérieure et réalisez l’intervention par incision cornéenne.
Gestion postopératoire :
- Le contrôle de l’inflammation de la maladie sous-jacente (uvéite, etc.) est important
- En cas d’administration continue de stéroïdes, le risque de cataracte secondaire (PCO) est également élevé
Traitement du glaucome stéroïdien
Section intitulée « Traitement du glaucome stéroïdien »Premier choix : réduction ou arrêt des stéroïdes
- Si possible, privilégier la réduction ou l’arrêt des stéroïdes. Cependant, la réduction peut être difficile en raison de la gestion de la maladie sous-jacente.
- Les modifications tissulaires peuvent être irréversibles, d’où l’importance d’une intervention précoce.
Traitement hypotenseur oculaire (similaire à celui du glaucome primitif à angle ouvert) :
- Utilisation dans l’ordre : prostaglandines, bêta-bloquants, inhibiteurs de l’anhydrase carbonique (collyres ou oraux), agonistes des récepteurs α₂.
- Si la pression intraoculaire n’est pas contrôlée par les collyres ou les médicaments oraux, une intervention chirurgicale peut être nécessaire2)
Traitement chirurgical :
- Trabéculotomie : C’est une option pour le glaucome stéroïdien lorsque la pression intraoculaire n’est pas suffisamment contrôlée par les médicaments. Des études multicentriques rapportent son efficacité pour contrôler la pression intraoculaire dans les yeux atteints de glaucome stéroïdien13)
- Trabéculoplastie sélective au laser : Elle est souvent efficace, mais ne doit pas être réalisée en cas d’uvéite associée
- Trabéculectomie (chirurgie filtrante) : réalisée lorsque l’incision est insuffisante
Dans de nombreux cas, l’arrêt ou la réduction des stéroïdes entraîne une baisse de la pression intraoculaire. Cependant, si l’utilisation à long terme a provoqué des modifications tissulaires irréversibles du trabéculum (accumulation de matrice extracellulaire), la pression peut ne pas s’améliorer après l’arrêt, et des médicaments hypotenseurs ou une intervention chirurgicale peuvent être nécessaires. Si l’arrêt est difficile en raison de la maladie sous-jacente, l’ophtalmologiste et le médecin traitant doivent collaborer pour la prise en charge.
La chirurgie elle-même peut espérer de bons résultats, comme pour une chirurgie de la cataracte standard. Cependant, en cas d’administration continue de stéroïdes, le risque de cataracte secondaire (PCO) est élevé, et un suivi régulier après l’opération est nécessaire. La PCO peut être traitée par capsulotomie postérieure au laser Nd:YAG. Comme la capsule postérieure peut être fragile, une technique chirurgicale attentive pour éviter une rupture capsulaire peropératoire est requise.
6. Physiopathologie et mécanisme détaillé de l’apparition
Section intitulée « 6. Physiopathologie et mécanisme détaillé de l’apparition »Mécanisme de la cataracte stéroïdienne
Section intitulée « Mécanisme de la cataracte stéroïdienne »Le mécanisme d’apparition de la cataracte stéroïdienne n’est pas complètement élucidé, mais plusieurs mécanismes ont été rapportés5)6)10).
- Théorie de la formation d’un intermédiaire base de Schiff : Une base de Schiff se forme entre le groupe cétone C-20 du stéroïde et un groupe nucléophile des protéines du cristallin. Ensuite, un réarrangement de Heyns du groupe hydroxyle C-21 se produit, générant un adduit de substitution amine stable. Cet adduit ne serait observé que dans la cataracte stéroïdienne5)
- Anomalies métaboliques et dysfonctionnement membranaire : Altération du transport ionique dans les cellules épithéliales du cristallin
- Stress oxydatif : Dénaturation des protéines du cristallin (agrégation de cristallines) due à la production de radicaux libres
- Mécanisme médié par le récepteur des glucocorticoïdes : Le récepteur des glucocorticoïdes influence plus de 5 000 gènes, entraînant des anomalies des molécules d’adhésion cellulaire10)
- Formation d’adduits protéiques
- Diminution de la transparence des fibres du cristallin dans la région capsulaire postérieure et agrégation de cristalline
- Migration vers la face postérieure de la capsule des cellules endommagées de la zone équatoriale du cristallin6)
La cataracte sous-capsulaire postérieure, se développant sur l’axe visuel, entraîne une altération de la fonction visuelle relativement tôt. Un diamètre d’opacité de 1 mm ou plus affecte la fonction visuelle ; à partir de 2 mm, la sensibilité au contraste diminue nettement même si l’acuité visuelle corrigée est bonne ; à partir de 3 mm, l’acuité visuelle diminue souvent également.
Mécanisme du glaucome stéroïdien
Section intitulée « Mécanisme du glaucome stéroïdien »Les glucocorticoïdes augmentent la pression intraoculaire en réduisant l’écoulement de l’humeur aqueuse depuis la chambre antérieure.
- Augmentation de la production de matrice extracellulaire dans les cellules trabéculaires : Les stéroïdes inhibent la dégradation de la matrice extracellulaire (fibronectine, laminine, collagène, etc.) des cellules trabéculaires et favorisent son dépôt. Cela obstrue la structure en treillis du trabéculum et altère l’écoulement de l’humeur aqueuse.
- Induction de la myociline : La myociline est une protéine de 55 kDa induite dans les cellules trabéculaires lors de l’exposition aux stéroïdes, et elle est impliquée dans la réduction de l’écoulement de l’humeur aqueuse et l’augmentation de la pression intraoculaire induite par les stéroïdes2)
- Modifications du cytosquelette : la réorganisation du cytosquelette d’actine entraîne des changements morphologiques dans la voie d’écoulement de l’humeur aqueuse
La réponse de la pression intraoculaire aux stéroïdes varie selon les individus ; chez les jeunes, les patients présentant une pression intraoculaire élevée ou une atteinte sévère du nerf optique, une intervention chirurgicale peut être nécessaire11). Chez les répondeurs aux stéroïdes, une vérification régulière de la pression intraoculaire est nécessaire, indépendamment de la voie d’administration et de la durée du traitement12).
Mécanisme d’augmentation du risque infectieux
Section intitulée « Mécanisme d’augmentation du risque infectieux »Les récepteurs des glucocorticoïdes inhibent la transcription des cytokines et des chimiokines, et entravent la migration et l’activation des cellules immunitaires. Cela réduit l’immunité locale contre les champignons, les virus et les bactéries. Les infections fongiques en particulier sont susceptibles de s’aggraver sous immunosuppression induite par les stéroïdes7).
7. Recherches récentes et perspectives futures
Section intitulée « 7. Recherches récentes et perspectives futures »Sécurité ophtalmique des corticostéroïdes nasaux
Section intitulée « Sécurité ophtalmique des corticostéroïdes nasaux »Une revue systématique récente a montré que les corticostéroïdes nasaux ne sont pas significativement associés à un risque de cataracte ou d’augmentation de la pression intraoculaire9). Cependant, même les stéroïdes considérés comme ayant une « faible pénétration intraoculaire », tels que le fluorométholone et le lotéprednol, présentent un risque d’augmentation de la pression intraoculaire et de cataracte en cas d’utilisation à long terme, ce qui nécessite une attention particulière.
Implant à libération prolongée d’acétonide de fluocinolone
Section intitulée « Implant à libération prolongée d’acétonide de fluocinolone »La recherche sur les dispositifs à libération prolongée d’acétonide de fluocinolone intravitréen progresse, suggérant leur utilité potentielle pour la gestion à long terme de l’uvéite2). Cependant, par rapport aux stéroïdes systémiques, les effets secondaires locaux (augmentation de la pression intraoculaire, cataracte) sont plus fréquents, nécessitant une gestion individualisée.
Identification génétique des répondeurs aux stéroïdes
Section intitulée « Identification génétique des répondeurs aux stéroïdes »La réponse de la pression intraoculaire aux stéroïdes est considérée comme génétiquement déterminée, et l’identification de gènes associés tels que le gène de la myociline progresse. À l’avenir, on espère réaliser une médecine personnalisée permettant d’identifier à l’avance les personnes à haut risque de glaucome stéroïdien à l’aide d’informations génétiques12).
Oui, une consultation ophtalmologique régulière est fortement recommandée. L’augmentation de la pression intraoculaire est souvent asymptomatique, et la cataracte est également souvent asymptomatique au début. Indépendamment de la voie d’administration (systémique, collyre, inhalation), les patients sous traitement à long terme nécessitent une évaluation ophtalmologique (pression intraoculaire, cristallin, nerf optique) au moins 1 à 2 fois par an. En particulier, un contrôle de la pression intraoculaire 2 semaines à 1 mois après le début du traitement est important.
8. Références
Section intitulée « 8. Références »-
McGhee CNJ, Dean S, Danesh-Meyer H. Locally administered ocular corticosteroids: benefits and risks. Drug Saf. 2002;25(1):33-55. PMID: 11820911. doi:10.2165/00002018-200225010-00004.
-
Okoye O, Okonkwo O. Inflammatory glaucoma. Community Eye Health. 2019;32(106):S1-S4.
-
Miller KM, Oetting TA, Tweeten JP, et al. Cataract in the Adult Eye Preferred Practice Pattern. Ophthalmology. 2022;129(1):P1-P126.
-
Chylack LT Jr, Wolfe JK, Singer DM, et al. The Lens Opacities Classification System III. Arch Ophthalmol. 1993;111(6):831-836. PMID: 8512486. doi:10.1001/archopht.1993.01090060119035.
-
Urban RC Jr, Cotlier E. Corticosteroid-induced cataracts. Surv Ophthalmol. 1986;31(2):102-110. PMID: 3541262. doi:10.1016/0039-6257(86)90077-9.
-
Jobling AI, Augusteyn RC. What causes steroid cataracts? A review of steroid-induced posterior subcapsular cataracts. Clin Exp Optom. 2002;85(2):61-75. PMID: 11952401. doi:10.1111/j.1444-0938.2002.tb03011.x.
-
Carnahan MC, Goldstein DA. Ocular complications of topical, peri-ocular, and systemic corticosteroids. Curr Opin Ophthalmol. 2000;11(6):478-483. PMID: 11141645.
-
Cumming RG, Mitchell P, Leeder SR. Use of inhaled corticosteroids and the risk of cataracts. N Engl J Med. 1997;337(1):8-14. PMID: 9203425. doi:10.1056/NEJM199707033370102.
-
Valenzuela CV, Liu JC, Vila PM, et al. Intranasal corticosteroids do not lead to ocular changes: a systematic review and meta-analysis. Laryngoscope. 2019;129(1):6-12. PMID: 30229924. PMCID: PMC6320292. doi:10.1002/lary.27209.
-
James ER. The etiology of steroid cataract. J Ocul Pharmacol Ther. 2007;23(5):403-420. PMID: 17900234. doi:10.1089/jop.2006.0067.
-
Sihota R, Konkal VL, Dada T, Agarwal HC, Singh R. Prospective, long-term evaluation of steroid-induced glaucoma. Eye (Lond). 2008;22(1):26-30. PMID: 16823461. doi:10.1038/sj.eye.6702474.
-
Phulke S, Kaushik S, Kaur S, Pandav SS. Steroid-induced glaucoma: an avoidable irreversible blindness. J Curr Glaucoma Pract. 2017;11(2):67-72. PMID: 28924342. PMCID: PMC5577123. doi:10.5005/jp-journals-10028-1226.
-
Japanese Steroid-Induced Glaucoma Multicenter Study Group. Success rates of trabeculotomy for steroid-induced glaucoma: a comparative, multicenter, retrospective cohort study. Am J Ophthalmol. 2011;151(6):1047-1056.e1. doi:10.1016/j.ajo.2010.11.028.
