
عوارض چشمی کورتیکواستروئیدها
۱. عوارض چشمی کورتیکواستروئیدها چیست؟
Section titled “۱. عوارض چشمی کورتیکواستروئیدها چیست؟”کورتیکواستروئیدها (گلوکوکورتیکوئیدها) داروهای ضروری برای درمان طیف وسیعی از بیماریها از جمله بیماریهای خودایمنی، بیماریهای التهابی چشم و التهاب پس از جراحی هستند. با این حال، استفاده طولانیمدت یا با دوز بالا از آنها میتواند عوارض جانبی جدی برای چشم ایجاد کند.
شایعترین نوع کدورت عدسی ناشی از دارو، آب مروارید استروئیدی است که پس از بروز، در مدت نسبتاً کوتاهی باعث کاهش شدید بینایی میشود. این عارضه بیشتر با مصرف سیستمیک رخ میدهد، اما با استنشاق طولانیمدت یا قطره چشمی نیز ممکن است ایجاد شود. بیماران تحت درمان با استروئید نیاز به معاینات منظم چشم پزشکی دارند.
بیماریها و شرایط اصلی که در چشم پزشکی از استروئیدها استفاده میشود به شرح زیر است:
- واکنشهای آلرژیک و حساسیتی: تب یونجه، کاتار بهاری، ورم ملتحمه آلرژیک
- یووئیت (قدامی، خلفی، کامل): پیشگیری از عود و مهار التهاب
- اسکلریت و اپیاسکلریت: التهاب خودایمنی
- آرتریت سلول ژانت: تجویز سیستمیک اورژانسی برای حفظ بینایی
- مدیریت التهاب پس از جراحی: پس از جراحی آب مروارید و پیوند قرنیه
- بیماریهای هرپسی چشم: کاهش التهاب کراتیت استرومایی (همراه با داروهای ضد ویروس)
- بیماریهای اوربیت: تیروئید اگزوفتالمی، شبهتومور التهابی اوربیت
عوارض چشمی در مصرف کوتاهمدت استروئیدها نادر است، اما افزایش فشار چشم ممکن است حدود دو هفته پس از شروع درمان ظاهر شود. آب مروارید معمولاً در مصرف طولانیمدت ایجاد میشود، اما در پاسخدهندگان به استروئید، فشار چشم حتی در مدت کوتاه نیز افزایش مییابد؛ بنابراین اندازهگیری منظم فشار چشم بدون توجه به مدت مصرف توصیه میشود.
2. علائم اصلی و یافتههای بالینی
Section titled “2. علائم اصلی و یافتههای بالینی”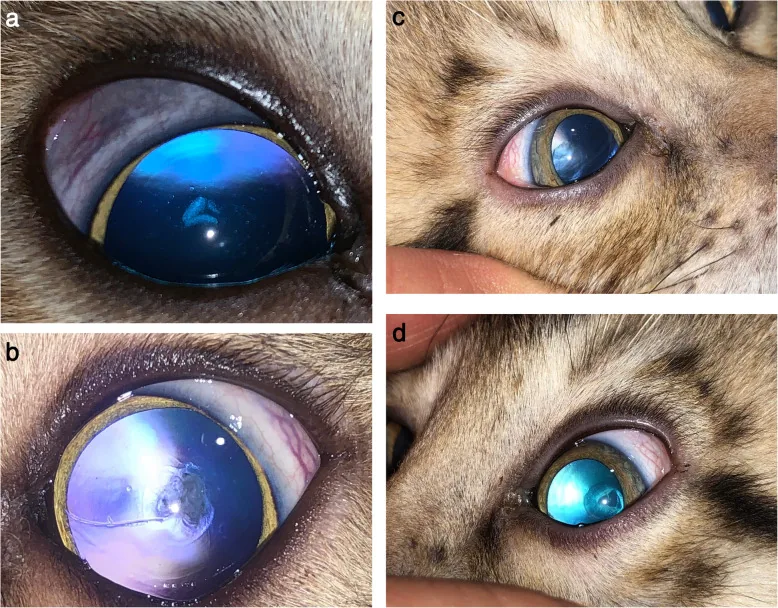
علائم ذهنی
Section titled “علائم ذهنی”آبمروارید زیرکپسولی خلفی (آبمروارید استروئیدی):
- کاهش بینایی (زمانی که کدورت به قطر ۳ میلیمتر یا بیشتر برسد، کاهش بینایی قابل توجه است)
- فوتوفوبیا و گِلِیر (حساسیت به نور و خیرگی)
- کاهش قابل توجه حساسیت کنتراست حتی با وجود دید خوب
- اغلب از مراحل اولیه کدورت، اختلال عملکرد بینایی احساس میشود
- در بسیاری از موارد بدون علامت است (حتی با فشار بالای چشم بهسختی قابل احساس است)
- در صورت افزایش فشار چشم ممکن است سنگینی، ناراحتی و تاری دید ایجاد شود
- اختلال میدان بینایی (در مراحل پیشرفته، میدان بینایی از نواحی محیطی کاهش مییابد)
مراحل پیشرفت کدورت
Section titled “مراحل پیشرفت کدورت”| مرحله | یافته |
|---|---|
| اولیه | کدورتهای نقطهای خفیف و واکوئلها درست در زیر کپسول خلفی روی محور بینایی |
| مرحله پیشرفته | نقاط کدر به هم پیوسته و یک کدورت زیرکپسولی خلفی بشقابمانند با مرز مشخص و داخلی همگن (قطر ۲-۳ میلیمتر). گرانولهای چندرنگ آبی، سبز و قرمز |
| پیشرفت بیشتر | گسترش به داخل قشر قدامی. برای عبور از مرز و بزرگتر شدن به زمان نیاز دارد |
| مرحله پایانی | افزایش شدت پراکندگی نور از ناحیه هسته جنینی → همراهی با آبمروارید هستهای |
آبمروارید استروئیدی معمولاً به عنوان آبمروارید زیرکپسولی خلفی شناخته میشود، اما خطر آبمروارید هستهای نیز بالا بوده و همراهی آن غیرمعمول نیست. PSC سریعتر از سایر انواع آبمروارید پیشرفت میکند و سه مطالعه بزرگ نشان دادهاند که PSC سریعتر از آبمروارید هستهای و قشری پیشرفت میکند3).
یافتههای گلوکوم استروئیدی:
- زاویه باز (بدون ناهنجاری زاویه)
- افزایش فشار داخل چشم (اغلب بالای 30 میلیمتر جیوه)
- تجمع ماتریکس خارج سلولی در ترابکول
- در موارد طولانی، گودرفتگی پیشرونده دیسک بینایی و نازک شدن لایه فیبرهای عصبی شبکیه
| عوارض | کدورت/یافتههای معمول | علائم اولیه |
|---|---|---|
| آبمروارید استروئیدی | کدورت دیسکی شکل زیر کپسول خلفی (پیشرفت ۴ مرحلهای) | خیرگی و حساسیت به نور |
| گلوکوم استروئیدی | گودیدگی عصب بینایی | تقریباً بدون علامت |
آبمروارید استروئیدی معمولی به صورت کدورت بشقابی شکل در زیر کپسول خلفی روی محور بینایی ظاهر میشود و با دانههای چندرنگ همراه است که ویژگی بارز آن است. اگرچه کدورت زیر کپسول خلفی در آبمروارید پیری نیز رخ میدهد، اما در صورت مشاهده آبمروارید زیر کپسول خلفی تا دهه ۴۰ سالگی، باید سابقه مصرف استروئید به طور فعال پرسیده شود. گاهی تشخیص آن از آبمروارید همراه با یووئیت دشوار میشود.
۳. علل و عوامل خطر
Section titled “۳. علل و عوامل خطر”خطر بر اساس راه مصرف
Section titled “خطر بر اساس راه مصرف”خطر عوارض چشمی ناشی از استروئیدها بسته به راه مصرف متفاوت است. مصرف سیستمیک بیشترین خطر را دارد و حتی مصرف موضعی نیز در صورت استفاده طولانی مدت میتواند منجر به بروز آن شود1).
- تجویز سیستمیک (خوراکی/وریدی): بالاترین خطر برای آبمروارید و گلوکوم. بروز با دوز کمتر از 10 میلیگرم در روز پردنیزولون نسبتاً نادر است. معمولاً در موارد مصرف طولانیمدت با دوز بالا بیش از یک سال رخ میدهد.
- قطرههای چشمی استروئیدی: خطر کمتر از تجویز سیستمیک است، اما استفاده طولانیمدت میتواند باعث آبمروارید زیرکپسولی خلفی و افزایش فشار چشم شود3).
- استروئید استنشاقی (درمان آسم): خطر آبمروارید زیرکپسولی خلفی وجود دارد8).
- استروئید بینی: بر اساس یک مرور سیستماتیک، خطر قابل توجهی برای آبمروارید یا افزایش فشار چشم وجود ندارد9).
- تزریق تریامسینولون داخل زجاجیه: در بیش از ۵۰٪ موارد باعث افزایش فشار چشم میشود که از این میان ۱ تا ۲٪ نیاز به مداخله جراحی دارند2)
عوامل خطر آب مروارید
Section titled “عوامل خطر آب مروارید”در دستورالعمل بالینی آب مروارید آکادمی چشمپزشکی آمریکا (Preferred Practice Pattern)، استفاده از استروئیدهای سیستمیک به عنوان یک عامل خطر برای آب مروارید زیرکپسولی خلفی ذکر شده است و مصرفکنندگان طولانیمدت کورتیکواستروئیدهای استنشاقی یا خوراکی در معرض خطر بالای ابتلا به آب مروارید هستند3).
- کودکان نسبت به بزرگسالان بیشتر مستعد ابتلا به آب مروارید استروئیدی هستند
- بیمارانی که به دلیل بیماریهای سیستمیک (کلاژنوز، SLE، آرتریت روماتوئید، سندرم نفروتیک، پس از پیوند کلیه) تحت درمان طولانیمدت سیستمیک قرار میگیرند، در معرض خطر بالاتری هستند
عوامل خطر گلوکوم
Section titled “عوامل خطر گلوکوم”- وجود گلوکوم زاویه باز اولیه
- سابقه افزایش فشار داخل چشم ناشی از مصرف استروئید در گذشته (پاسخدهنده به استروئید)
- دیابت نوع 1
- کودکان و سالمندان (واکنشپذیری بالا)
- استفاده طولانیمدت بیش از 3 ماه 2)
4. روشهای تشخیص و آزمایش
Section titled “4. روشهای تشخیص و آزمایش”تشخیص آب مروارید
Section titled “تشخیص آب مروارید”مشاهده عدسی با میکروسکوپ شکافدار (لامپ اسلیت) اساس تشخیص است.
- نکات مشاهده: وجود کدورت بشقابیشکل زیر کپسول خلفی و گرانولهای چندرنگ، قطر کدورت (بیش از ۲ میلیمتر باعث اختلال بینایی میشود)
- روش عبور نور (Transillumination): برای تشخیص کدورت زیرکپسول خلفی و وجود واکوئلها مفید است
- ارزیابی عملکرد بینایی: حتی با دید اصلاحشده خوب، ممکن است حساسیت کنتراست بهطور قابلتوجهی کاهش یابد که در این موارد زودهنگام نیاز به جراحی پیدا میشود
- طبقهبندی LOCS III: کدورت در چهار دسته هسته (NO/NC)، قشر (C) و زیرکپسول خلفی (PSC) ارزیابی میشود. در PSC، شدت کدورت زیرکپسول خلفی با روش عبور نور ارزیابی میگردد4)
مهمترین نکته در تشخیص، گرفتن شرح حال دقیق از مصرف استروئیدها است، از جمله راه مصرف (سیستمیک، قطره چشمی، استنشاقی، اسپری بینی)، دوز و مدت مصرف. در بیماران مبتلا به یووئیت که استروئید مصرف میکنند، افتراق از آب مروارید ناشی از یووئیت دشوار میشود. سابقه قرارگیری در معرض اشعه و ضربه به چشم نیز به عنوان عوامل خطر آب مروارید زیرکپسولی خلفی بررسی میشود3).
تشخیص گلوکوم
Section titled “تشخیص گلوکوم”- اندازهگیری فشار داخل چشم: اندازهگیری با تونومتر گلدمن استاندارد است
- معاینه زاویه: بررسی باز یا بسته بودن زاویه و ناهنجاریهای آن
- تست میدان بینایی: ارزیابی نقص میدان بینایی با استفاده از پریمتر استاتیک هامفری
- ارزیابی عصب بینایی: ارزیابی شکل دیسک و لایه فیبرهای عصبی شبکیه با OCT
حدت بینایی توانایی تشخیص نشانههای با کنتراست بالا (سیاه و سفید واضح) را اندازهگیری میکند، در حالی که حساسیت کنتراست توانایی تشخیص تفاوتهای نوری کم است. در آب مروارید زیرکپسولی خلفی، حتی اگر حدت بینایی نسبتاً خوب باشد، حساسیت کنتراست اغلب به طور قابل توجهی کاهش مییابد و باعث اختلال در فعالیتهای روزانه (مانند راه رفتن در مکانهای کم نور، رانندگی و غیره) میشود. اگر کاهش حساسیت کنتراست قابل توجه باشد، حتی با حدت بینایی خوب، ممکن است اندیکاسیون جراحی وجود داشته باشد.
5. روشهای درمانی استاندارد
Section titled “5. روشهای درمانی استاندارد”درمان آب مروارید استروئیدی
Section titled “درمان آب مروارید استروئیدی”مدیریت محافظهکارانه:
- درمان دارویی آب مروارید شواهد کافی برای اثربخشی ندارد و توصیه نمیشود3)
- برای کدورت مرکزی کوچک، میتوان با قطرههای گشادکننده مردمک به طور موقت بینایی را بهبود بخشید، اما باید مراقب بدتر شدن تابشخوردگی (glare) بود.
- کاهش دوز استروئید به حداقل مؤثر یا قطع آن (همراه با مدیریت بیماری زمینهای) بررسی شود.
اندیکاسیون جراحی:
- در مواردی که قطر کدورت زیرکپسول خلفی ۲ میلیمتر یا بیشتر باشد و اختلال عملکرد بینایی وجود داشته باشد، اغلب نیاز به جراحی است.
- در صورت کاهش قابل توجه حساسیت کنتراست، حتی با دید خوب، جراحی در نظر گرفته میشود
- از آنجایی که PSC به سرعت پیشرفت میکند، اغلب نیاز به جراحی زودهنگام وجود دارد
روش جراحی:
- فیکوامولسیفیکاسیون (phacoemulsification) + کاشت IOL روش اصلی است
- توجه حین عمل (مهم): در چشمهای با کدورت زیرکپسولی خلفی، کپسول خلفی ممکن است شکننده باشد و باید مراقب پارگی کپسول خلفی بود
- در موارد مبتلا به یووئیت، عمل جراحی در دوره نسبتاً آرام و در حین ادامه مصرف خوراکی استروئید انجام میشود. کارگذاری لنز داخل چشمی مشکلی ندارد
- در صورت احتمال نیاز به عمل فیلتراسیون برای گلوکوم ثانویه، ملتحمه فوقانی حفظ شده و عمل از طریق برش قرنیه انجام میشود
مراقبتهای پس از عمل:
- کنترل التهاب بیماری زمینهای (مانند یووئیت) مهم است
- در طول مصرف مداوم استروئید، خطر کاتاراکت ثانویه (PCO) نیز بالا است
درمان گلوکوم استروئیدی
Section titled “درمان گلوکوم استروئیدی”خط اول: کاهش یا قطع استروئید
- در صورت امکان، کاهش دوز یا قطع استروئیدها اولویت دارد. با این حال، ممکن است به دلیل مدیریت بیماری زمینهای، کاهش دوز دشوار باشد.
- تغییرات بافتی ممکن است غیرقابل برگشت باشند، بنابراین مداخله زودهنگام مهم است.
درمان کاهش فشار داخل چشم (مشابه گلوکوم زاویه باز اولیه):
- داروهای آنالوگ پروستاگلاندین، مسدودکنندههای بتا، مهارکنندههای کربنیک آنهیدراز (قطره و خوراکی)، و محرکهای گیرنده آلفا-۲ به ترتیب استفاده میشوند.
- در صورت عدم کنترل فشار چشم با قطره و داروهای خوراکی، جراحی لازم است2)
درمان جراحی:
- ترابکولوتومی: گزینهای برای گلوکوم استروئیدی است که با دارو فشار چشم به اندازه کافی کنترل نمیشود. مطالعات چندمرکزی نشان داده است که در کنترل فشار چشم در گلوکوم استروئیدی مؤثر است13)
- ترابکولوپلاستی انتخابی با لیزر: پاسخدهی خوبی دارد، اما در موارد همراه با یووئیت نباید انجام شود
- ترابکولکتومی (جراحی فیلتراسیون): در صورت ناکافی بودن جراحی برشی انجام میشود
در بسیاری موارد، با قطع یا کاهش دوز استروئید، فشار چشم کاهش مییابد. اما اگر استفاده طولانیمدت باعث تغییرات غیرقابل برگشت در بافت ترابکولار (تجمع ماتریکس خارج سلولی) شده باشد، ممکن است فشار چشم پس از قطع نیز بهبود نیابد و نیاز به داروهای کاهنده فشار چشم یا جراحی باشد. در مواردی که قطع استروئید به دلیل بیماری زمینهای دشوار است، چشمپزشک و پزشک معالج باید به صورت هماهنگ مدیریت کنند.
انتظار میرود که خود جراحی نتایج خوبی مشابه جراحی معمولی آب مروارید داشته باشد. با این حال، در طول مصرف مداوم استروئیدها، خطر آب مروارید ثانویه (PCO) بالا است و پیگیری منظم پس از جراحی ضروری است. PCO را میتوان با کپسولوتومی خلفی با لیزر Nd:YAG درمان کرد. از آنجایی که کپسول خلفی ممکن است شکننده باشد، تکنیک جراحی باید با دقت انجام شود تا از پارگی کپسول خلفی در حین عمل جلوگیری شود.
6. پاتوفیزیولوژی و مکانیسم دقیق بروز
Section titled “6. پاتوفیزیولوژی و مکانیسم دقیق بروز”مکانیسم آب مروارید استروئیدی
Section titled “مکانیسم آب مروارید استروئیدی”مکانیسم دقیق بروز آب مروارید استروئیدی به طور کامل شناخته نشده است، اما چندین مکانیسم گزارش شده است5)6)10).
- نظریه تشکیل حدواسط باز شیف (Schiff base intermediate): باز شیف بین گروه کتون C-20 استروئید و گروه هستهدوست پروتئین عدسی تشکیل میشود. سپس بازآرایی هینز (Heyns rearrangement) گروه هیدروکسیل C-21 رخ میدهد و یک افزوده آمینی پایدار تولید میشود. گفته میشود این افزوده فقط در آبمروارید ناشی از استروئید مشاهده میشود5)
- اختلال متابولیک و اختلال عملکرد غشا: اختلال در انتقال یون در سلولهای اپیتلیال عدسی
- آسیب اکسیداتیو: تخریب پروتئین عدسی (تجمع کریستالین) ناشی از تولید رادیکالهای آزاد
- مکانیسم از طریق گیرنده گلوکوکورتیکوئید: گیرنده گلوکوکورتیکوئید بر بیش از ۵۰۰۰ ژن تأثیر میگذارد و باعث ناهنجاری در مولکولهای چسبندگی سلولی میشود10)
- تشکیل adduct پروتئینی
- کاهش شفافیت سلولهای فیبر عدسی در ناحیه خلفی کپسول و تجمع کریستالین
- مهاجرت سلولهای آسیبدیده ناحیه استوای عدسی به سمت کپسول خلفی6)
آب مروارید زیرکپسولی خلفی به دلیل ایجاد در محور بینایی، نسبتاً زود باعث اختلال عملکرد بینایی میشود. اگر قطر کدورت ۱ میلیمتر یا بیشتر باشد، بر عملکرد بینایی تأثیر میگذارد؛ با قطر ۲ میلیمتر یا بیشتر، حتی اگر حدت بینایی اصلاحشده خوب باشد، حساسیت کنتراست به طور قابل توجهی کاهش مییابد؛ و با قطر ۳ میلیمتر یا بیشتر، اغلب حدت بینایی نیز کاهش مییابد.
مکانیسم گلوکوم استروئیدی
Section titled “مکانیسم گلوکوم استروئیدی”گلوکوکورتیکوئیدها با کاهش خروج زلالیه از اتاق قدامی، فشار داخل چشم را افزایش میدهند.
- افزایش تولید ماتریکس خارج سلولی در سلولهای ترابکولار: استروئیدها تجزیه ماتریکس خارج سلولی (مانند فیبرونکتین، لامینین و کلاژن) را در سلولهای ترابکولار مهار کرده و رسوب آن را تسریع میکنند. این امر باعث انسداد ساختار شبکه ترابکولار و اختلال در خروج زلالیه میشود.
- القای میوسیلین (myocilin): میوسیلین یک پروتئین 55 کیلودالتونی است که در سلولهای ترابکولار در مواجهه با استروئیدها القا میشود و در کاهش خروج زلالیه و افزایش فشار داخل چشم ناشی از استروئید نقش دارد2)
- تغییرات اسکلت سلولی: بازآرایی اسکلت سلولی اکتین باعث تغییرات مورفولوژیک در مسیر خروج زلالیه میشود
پاسخ فشار داخل چشم به استروئیدها در افراد مختلف متفاوت است و در افراد جوان، موارد با فشار بالای چشم، و مواردی که آسیب عصب بینایی شدید است، ممکن است نیاز به جراحی باشد11). در پاسخدهندگان به استروئید، صرف نظر از مسیر و مدت مصرف، بررسی منظم فشار چشم ضروری است12).
مکانیسم افزایش خطر عفونت
Section titled “مکانیسم افزایش خطر عفونت”گیرنده گلوکوکورتیکوئید رونویسی سیتوکینها و کموکاینها را مهار کرده و از مهاجرت و فعالسازی سلولهای ایمنی جلوگیری میکند. این امر باعث کاهش ایمنی موضعی در برابر قارچها، ویروسها و باکتریها میشود. به ویژه عفونتهای قارچی تحت سرکوب ایمنی ناشی از استروئیدها مستعد تشدید هستند7).
7. تحقیقات جدید و چشمانداز آینده
Section titled “7. تحقیقات جدید و چشمانداز آینده”ایمنی چشمی استروئیدهای بینی
Section titled “ایمنی چشمی استروئیدهای بینی”مرورهای سیستماتیک اخیر نشان دادهاند که استروئیدهای بینی ارتباط معنیداری با خطر آب مروارید و افزایش فشار داخل چشم ندارند9). با این حال، حتی استروئیدهایی مانند فلورومتولون و لوتپرادنول که «نفوذ داخل چشمی کمی» دارند، در صورت استفاده طولانیمدت ممکن است خطر افزایش فشار داخل چشم و آب مروارید را به همراه داشته باشند و نیاز به احتیاط دارند.
ایمپلنت رهش پایدار فلوسینولون استونید
Section titled “ایمپلنت رهش پایدار فلوسینولون استونید”تحقیقات در مورد دستگاه رهش پایدار فلوسینولون استونید داخل زجاجیهای در حال پیشرفت است و نشان داده شده که ممکن است برای مدیریت طولانیمدت یووئیت مفید باشد2). با این حال، عوارض جانبی موضعی (افزایش فشار چشم و آب مروارید) نسبت به استروئیدهای سیستمیک شایعتر است و نیاز به مدیریت فردی دارد.
شناسایی ژنتیکی پاسخدهندگان به استروئید
Section titled “شناسایی ژنتیکی پاسخدهندگان به استروئید”تصور میشود پاسخ فشار چشم به استروئید از نظر ژنتیکی تعیین میشود و شناسایی ژنهای مرتبط مانند ژن میوسیلین در حال پیشرفت است. انتظار میرود در آینده با استفاده از اطلاعات ژنتیکی، پزشکی فردیسازیشده برای شناسایی افراد پرخطر گلوکوم استروئیدی قبل از درمان محقق شود12).
بله، مراجعه منظم به چشمپزشک به شدت توصیه میشود. افزایش فشار چشم اغلب بدون علامت است و آب مروارید نیز در مراحل اولیه معمولاً بدون علامت میباشد. صرف نظر از راه مصرف (خوراکی، قطره چشمی، استنشاقی)، بیمارانی که از استروئید به مدت طولانی استفاده میکنند، حداقل سالی یک تا دو بار نیاز به ارزیابی چشمپزشکی (فشار چشم، عدسی، عصب بینایی) دارند. به ویژه بررسی فشار چشم در دو هفته تا یک ماه پس از شروع مصرف اهمیت دارد.
۸. منابع
Section titled “۸. منابع”-
McGhee CNJ, Dean S, Danesh-Meyer H. Locally administered ocular corticosteroids: benefits and risks. Drug Saf. 2002;25(1):33-55. PMID: 11820911. doi:10.2165/00002018-200225010-00004.
-
Okoye O, Okonkwo O. Inflammatory glaucoma. Community Eye Health. 2019;32(106):S1-S4.
-
Miller KM, Oetting TA, Tweeten JP, et al. Cataract in the Adult Eye Preferred Practice Pattern. Ophthalmology. 2022;129(1):P1-P126.
-
Chylack LT Jr, Wolfe JK, Singer DM, et al. The Lens Opacities Classification System III. Arch Ophthalmol. 1993;111(6):831-836. PMID: 8512486. doi:10.1001/archopht.1993.01090060119035.
-
Urban RC Jr, Cotlier E. Corticosteroid-induced cataracts. Surv Ophthalmol. 1986;31(2):102-110. PMID: 3541262. doi:10.1016/0039-6257(86)90077-9.
-
Jobling AI, Augusteyn RC. What causes steroid cataracts? A review of steroid-induced posterior subcapsular cataracts. Clin Exp Optom. 2002;85(2):61-75. PMID: 11952401. doi:10.1111/j.1444-0938.2002.tb03011.x.
-
Carnahan MC, Goldstein DA. Ocular complications of topical, peri-ocular, and systemic corticosteroids. Curr Opin Ophthalmol. 2000;11(6):478-483. PMID: 11141645.
-
Cumming RG, Mitchell P, Leeder SR. Use of inhaled corticosteroids and the risk of cataracts. N Engl J Med. 1997;337(1):8-14. PMID: 9203425. doi:10.1056/NEJM199707033370102.
-
Valenzuela CV, Liu JC, Vila PM, et al. Intranasal corticosteroids do not lead to ocular changes: a systematic review and meta-analysis. Laryngoscope. 2019;129(1):6-12. PMID: 30229924. PMCID: PMC6320292. doi:10.1002/lary.27209.
-
James ER. The etiology of steroid cataract. J Ocul Pharmacol Ther. 2007;23(5):403-420. PMID: 17900234. doi:10.1089/jop.2006.0067.
-
Sihota R, Konkal VL, Dada T, Agarwal HC, Singh R. Prospective, long-term evaluation of steroid-induced glaucoma. Eye (Lond). 2008;22(1):26-30. PMID: 16823461. doi:10.1038/sj.eye.6702474.
-
Phulke S, Kaushik S, Kaur S, Pandav SS. Steroid-induced glaucoma: an avoidable irreversible blindness. J Curr Glaucoma Pract. 2017;11(2):67-72. PMID: 28924342. PMCID: PMC5577123. doi:10.5005/jp-journals-10028-1226.
-
Japanese Steroid-Induced Glaucoma Multicenter Study Group. Success rates of trabeculotomy for steroid-induced glaucoma: a comparative, multicenter, retrospective cohort study. Am J Ophthalmol. 2011;151(6):1047-1056.e1. doi:10.1016/j.ajo.2010.11.028.
