Leve (Grado I–II)
Riesgo de elevación de la presión intraocular: Aproximadamente 13.5%.
Alteración visual: Permanece leve si el área pupilar está despejada.
Visualización del fondo de ojo: Generalmente posible.
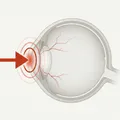
El hipema traumático es una condición en la que se acumulan glóbulos rojos en la cámara anterior (el espacio entre la córnea y el iris) después de un traumatismo cerrado. Una pequeña cantidad de sangrado que solo se puede ver con lámpara de hendidura se llama microhipema.
Cuando se aplica una fuerza contundente al ojo, la presión intraocular aumenta bruscamente y el limbo se estira. El humor acuoso se mueve hacia atrás y hacia el ángulo, dañando el iris y el cuerpo ciliar, lo que provoca sangrado. La parte más vulnerable es la unión delgada del iris con el cuerpo ciliar; un desgarro aquí (iridodiálisis) desplaza la pupila. Si se forma una hendidura en el cuerpo ciliar ligeramente hacia el lado escleral, se produce una recesión angular; si el cuerpo ciliar se desprende de la esclerótica más hacia el lado escleral, se produce una ciclodiálisis. Ambas condiciones son particularmente propensas al hipema.
Se clasifica según la cantidad de sangrado de la siguiente manera.
| Grado | Grado de sangrado |
|---|---|
| 0 | Microhipema |
| I | Menos de 1/3 de la cámara anterior |
| II | 1/3 a 1/2 de la cámara anterior |
| III | 1/2 a menos del llenado total de la cámara anterior |
| IV | Hifema total |
Entre el grado IV, cuando la cámara anterior está completamente llena de sangre roja brillante, se denomina hifema total (total hyphema). Cuando está llena de sangre rojo oscuro a negro, se denomina hifema en bola 8 (8-ball hyphema / black ball hyphema), lo que sugiere alteración de la circulación del humor acuoso e hipoxia.
Además del traumatismo, el hifema puede ocurrir espontáneamente después de cirugía intraocular (iatrogénico), debido a neovascularización del iris, tumores oculares, enfermedades sanguíneas (como leucemia, hemofilia) o uso de anticoagulantes. Consulte la sección “Causas y factores de riesgo” para más detalles.
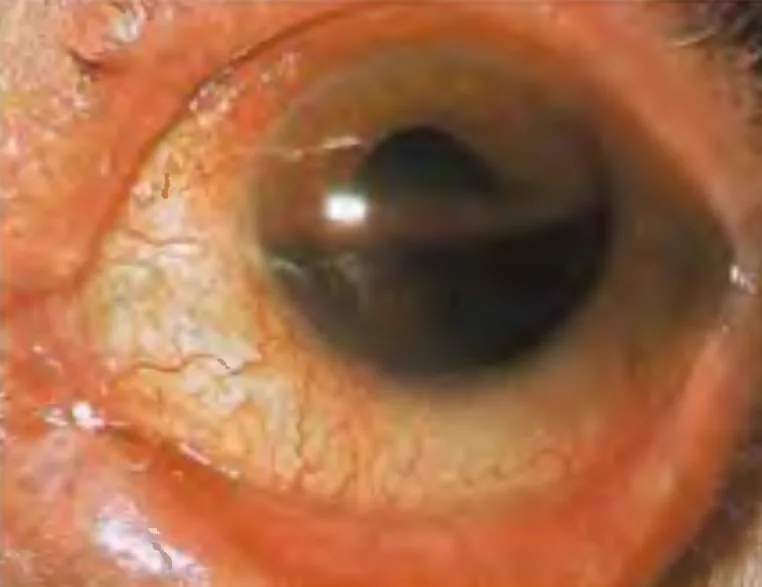
Los síntomas del hipema traumático varían según la cantidad de sangrado.
El hipema forma un nivel inferior (nivelación) y su color cambia de rojo a negro con el tiempo. La sangre coagulada tiene una apariencia más oscura. En posición erguida, la altura del nivel de sangre sirve como indicador de la cantidad de sangrado y es útil para monitorizar la absorción o el resangrado. Es importante registrar la altura desde el limbo corneal inferior en milímetros.
Leve (Grado I–II)
Riesgo de elevación de la presión intraocular: Aproximadamente 13.5%.
Alteración visual: Permanece leve si el área pupilar está despejada.
Visualización del fondo de ojo: Generalmente posible.
Grave (Grado III–IV)
Riesgo de elevación de la presión intraocular: Aumenta drásticamente al 27% en Grado III y al 52% en Grado IV.
Hipema en ocho: Alto riesgo de bloqueo pupilar y cierre angular secundario.
Visualización del fondo de ojo: A menudo imposible; se requiere examen ecográfico.
Las principales complicaciones son las siguientes:
Las siguientes complicaciones son importantes en niños:
El traumatismo contuso es la causa más común. Los ejemplos típicos incluyen pelotas, puños, accidentes de tráfico y lesiones laborales. La fuerza de compresión sobre el ojo causa ruptura de vasos sanguíneos en el iris, cuerpo ciliar y malla trabecular, lo que lleva a la acumulación de glóbulos rojos en la cámara anterior.
En el hifema sin antecedente de traumatismo, considere las siguientes causas.
La enfermedad de células falciformes es un factor de riesgo particularmente importante. En el ambiente hipóxico de la cámara anterior, los glóbulos rojos se falciformizan y se vuelven rígidos, dificultando su paso a través de la malla trabecular. Como resultado, incluso una pequeña cantidad de sangrado puede causar una elevación grave de la presión intraocular. Además, los glóbulos rojos falciformes dentro de los vasos pueden causar oclusión de la arteria central de la retina o neuropatía óptica isquémica. El rasgo falciforme también constituye un riesgo.
La cirugía de cataratas con warfarina continua aumenta los eventos hemorrágicos, pero la mayoría son hipemas autolimitados o hemorragias subconjuntivales, sin efectos adversos en la agudeza visual postoperatoria5). Sin embargo, la colaboración entre el médico de cabecera y el oftalmólogo es importante para la evaluación del riesgo individual.
El diagnóstico del hipema implica las siguientes exploraciones escalonadas. La anamnesis, la agudeza visual, el reflejo pupilar, la medición de la presión intraocular y la biomicroscopía con lámpara de hendidura son básicas. En caso de hipema masivo, también se debe comprobar el reflejo consensual del ojo contralateral.
| Prueba | Propósito principal |
|---|---|
| Microscopía con lámpara de hendidura | Clasificación de grado y seguimiento |
| Gonioscopia (1-2 semanas después de la lesión) | Recesión angular, sinequias anteriores periféricas |
| UBM / OCT de segmento anterior (UBM contraindicado en traumatismo ocular penetrante) | Evaluación estructural del cuerpo ciliar y el ángulo |
| Ecografía (modo B) | Evaluación del segmento posterior cuando el fondo de ojo no es visible |
| TC / RM (RM contraindicada para cuerpos extraños metálicos) | Evaluación de ruptura del globo ocular y cuerpos extraños intraoculares |
El principio básico del tratamiento es esperar la absorción espontánea con reposo. Se prohíbe el ejercicio intenso, se evita la posición supina y se mantiene al paciente en reposo con la cabecera de la cama elevada 30–45 grados en posición sentada o semincorporada. Se recomienda hospitalización para niños, casos en los que el nivel de hipema supere 1/3 a 1/2 de la cámara anterior, pacientes que no pueden seguir instrucciones y aquellos con enfermedad de células falciformes acompañada de presión intraocular elevada.
Para la presión intraocular elevada, agregue lo siguiente (solo 4, o 5+6, o una combinación de 4–6):
Los agentes antifibrinolíticos (ácido tranexámico) son útiles para reducir el riesgo de resangrado 4). Sin embargo, su efecto sobre el pronóstico visual no está claro 4).
Aproximadamente el 5% de los casos de hifema traumático requieren cirugía.
Las indicaciones para la cirugía son las siguientes:
| Grupo de pacientes | Criterios de indicación quirúrgica |
|---|---|
| Individuos sanos | PIO ≥50 mmHg durante 5 días, o ≥35 mmHg durante 7 días |
| Pacientes con enfermedad de células falciformes | PIO ≥25 mmHg durante más de 24 horas |
| Signos de tinción corneal por sangre | Indicado sin esperar los criterios anteriores |
| Hifema total en niños | Se considera la intervención temprana debido al riesgo de ambliopía por privación visual |
La cirugía de glaucoma (p. ej., cirugía filtrante) está indicada cuando la presión intraocular elevada persiste después del lavado de la cámara anterior. Si hay luxación o daño del cristalino, es necesaria la extracción del cristalino. Para el bloqueo pupilar, se debe considerar la iridotomía con láser.
En muchos casos, el manejo ambulatorio es posible con un seguimiento estrecho. Sin embargo, se recomienda la hospitalización en niños, casos con gran cantidad de sangrado (que exceda 1/3 a 1/2 de la cámara anterior), enfermedad de células falciformes con elevación de la presión intraocular, o cuando el paciente no puede cumplir con las restricciones de actividad.
Cuando se aplica una fuerza contundente al ojo, la presión intraocular aumenta bruscamente. El limbo corneal se estira y el humor acuoso se desplaza hacia la cámara posterior y el ángulo. Este cambio mecánico daña los vasos sanguíneos del iris y el cuerpo ciliar, causando sangrado en la cámara anterior.
Dependiendo de la gravedad de la lesión, se produce el siguiente daño estructural escalonado:
El resangrado ocurre de 3 a 7 días después de la lesión debido a la contracción y lisis del coágulo inicial 4). La incidencia se reporta entre 5 y 10% 4). El resangrado suele ser más abundante y grave que el sangrado inicial. Se observa elevación de la presión intraocular en más del 50% de los casos de resangrado.
Los factores de riesgo para el resangrado incluyen los siguientes:
La elevación de la presión intraocular asociada al hipema ocurre a través de múltiples mecanismos.
Cuando un hipema severo se acompaña de presión intraocular alta sostenida, la superficie posterior de la córnea se tiñe con sangre. Esto puede dejar deterioro visual incluso después de que el hipema se resuelva, y es necesario un lavado temprano de la cámara anterior.
Esta es una complicación crónica importante después de un traumatismo contuso. Se produce un desgarro entre los músculos circular y longitudinal del cuerpo ciliar, causando recesión del ángulo. En casos con recesión angular de 180 grados o más, el glaucoma se desarrolla a una alta tasa del 6–20% en 10 años. Dado que el inicio a menudo ocurre varios años o más después de la lesión, el seguimiento a largo plazo de la presión intraocular es esencial.
La incidencia general de resangrado es del 5–10% y a menudo ocurre de 3 a 7 días después de la lesión4). Dado que el resangrado tiende a ser más grave que la hemorragia inicial, es importante mantener reposo y someterse a una observación estrecha durante este período.
La complicación a largo plazo más importante es el glaucoma por recesión angular. En casos con recesión angular de 180 grados o más, el glaucoma se desarrolla en un 6–20% en 10 años. Dado que a menudo ocurre varios años o más después de la lesión, es esencial realizar exámenes regulares de la presión intraocular, el campo visual y el nervio óptico después del traumatismo.
Con la generalización de los fármacos de diana molecular, se han notificado hifemas espontáneos relacionados con fármacos.
Aldecoa et al. (2023) notificaron un hifema espontáneo en una mujer de 60 años que tomaba ibrutinib (inhibidor de BTK) 420 mg/día durante 4 meses para la leucemia linfocítica crónica 1). El hifema se resolvió completamente en 2 semanas tras la interrupción de ibrutinib y la administración tópica de corticosteroides. Se sugiere que ibrutinib reduce la adhesión plaquetaria al factor de von Willebrand e inhibe la agregación plaquetaria inducida por colágeno.
Chiang et al. (2022) notificaron un hifema espontáneo en un hombre de 37 años con leucemia mieloide aguda y neumonía grave por COVID-19 2). Además de trombocitopenia grave (6×10⁹/L), se estimó que la posición prona prolongada contribuyó al aumento de la presión venosa epiescleral.
Ison et al. (2022) notificaron un hifema espontáneo por microhemangiomas de iris (penachos de Cobb) en una mujer de 56 años con síndrome de Eisenmenger 3). Se consideró que la hipoxemia crónica (SpO₂ en reposo 78%) y la eritrocitosis secundaria (Hb 22.5 g/dL) indujeron la dilatación de los vasos del estroma del iris y contribuyeron a la formación de microhemangiomas. La hemorragia se resolvió con atropina y dexametasona tópicas.
Zhang et al. (Imágenes y Perspectivas) notificaron un hifema espontáneo y hemorragia de cámara posterior tras cirugía ICL (lente intraocular fáquica) 6). Una mujer de 23 años presentó pérdida súbita de visión sin traumatismo, frotamiento ocular ni uso de anticoagulantes. La ecografía UBM reveló la rotura de un quiste iridociliar asociado con los hápticos del ICL y hemorragia circundante. La hemorragia se resolvió con tratamiento conservador con tobramicina-dexametasona en gotas (4 veces al día) y gel de sulfato de atropina al 1% (2 veces al día) durante 17 días. Se demostró que la extracción urgente del ICL no siempre es necesaria.