Léger (Grade I–II)
Risque d’élévation de la pression intraoculaire : environ 13,5 %.
Troubles visuels : restent légers si la zone pupillaire est dégagée.
Visualisation du fond d’œil : souvent possible.
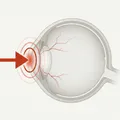
L’hyphema traumatique (traumatic hyphema) est une accumulation de globules rouges dans la chambre antérieure (l’espace entre la cornée et l’iris) après un traumatisme contondant. Un saignement minime visible uniquement au microscope à lampe à fente est appelé microhyphema.
Lorsqu’une force contondante est appliquée à l’œil, la pression intraoculaire augmente brusquement et le limbe cornéen s’étire. L’humeur aqueuse se déplace vers l’arrière et l’angle, endommageant l’iris et le corps ciliaire, provoquant un saignement. La partie la plus vulnérable est la fine zone d’attache de l’iris au corps ciliaire ; si elle se rompt (dialyse irienne), la pupille se déplace. Si une fissure se produit dans le corps ciliaire du côté scléral, il en résulte une récession de l’angle ; si le corps ciliaire se détache de la sclère plus loin, il s’agit d’une dialyse du corps ciliaire. Ces deux dernières conditions sont particulièrement sujettes à l’hyphema.
La classification selon la quantité de saignement est la suivante :
| Grade | Degré de saignement |
|---|---|
| 0 | Microhyphema |
| I | Moins d’un tiers de la chambre antérieure |
| II | Un tiers à la moitié de la chambre antérieure |
| III | De la moitié à moins que la chambre antérieure ne soit complètement remplie |
| IV | Hémorragie totale de la chambre antérieure |
Parmi les grades IV, l’état où la chambre antérieure est complètement remplie de sang rouge vif est appelé hémorragie totale de la chambre antérieure (total hyphema). L’état rempli de sang rouge foncé à noir est appelé hémorragie en huit (8-ball hyphema / black ball hyphema), ce qui suggère un trouble de la circulation de l’humeur aqueuse et une hypoxie.
Outre les traumatismes, elle peut survenir spontanément après une chirurgie intraoculaire (iatrogène), en raison de néovascularisation de l’iris, de tumeurs oculaires, de maladies du sang (leucémie, hémophilie, etc.) ou de l’utilisation d’anticoagulants. Voir la section « Causes et facteurs de risque » pour plus de détails.
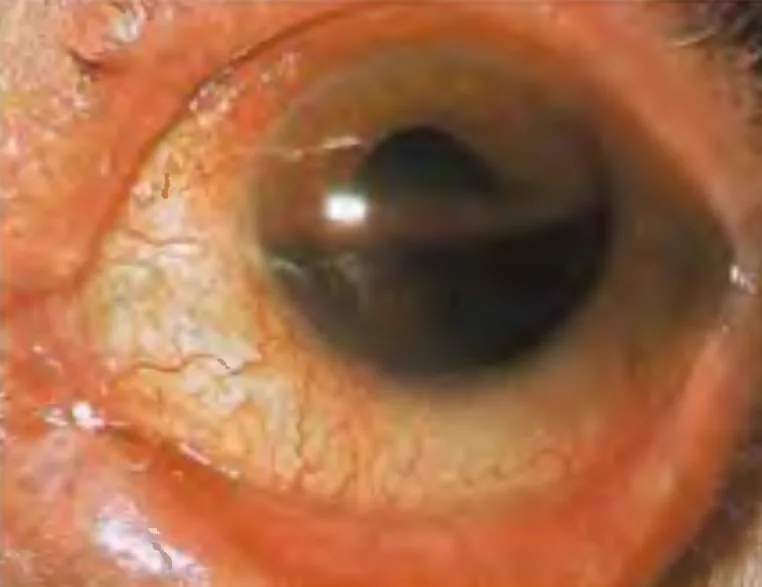
Les symptômes de l’hyphema traumatique varient en fonction de la quantité de saignement.
L’hyphema forme un niveau inférieur (formation d’un niveau liquide), et sa couleur varie du rouge au noir en fonction du temps écoulé. Le sang coagulé a un aspect plus foncé. La hauteur du niveau d’hyphema en position debout est un indicateur de la quantité de saignement et sert de référence pour le suivi de la résorption ou d’une récidive hémorragique. Il est important d’enregistrer la hauteur à partir du bord cornéen inférieur en millimètres.
Léger (Grade I–II)
Risque d’élévation de la pression intraoculaire : environ 13,5 %.
Troubles visuels : restent légers si la zone pupillaire est dégagée.
Visualisation du fond d’œil : souvent possible.
Sévère (Grade III–IV)
Risque d’élévation de la pression intraoculaire : augmente considérablement, 27 % pour le grade III et 52 % pour le grade IV.
Hyphema en eight-ball : risque élevé de bloc pupillaire ou de fermeture secondaire de l’angle.
Visualisation du fond d’œil : souvent impossible, nécessitant une échographie.
Les principales complications sont les suivantes.
Les complications spécifiques à l’enfant sont les suivantes :
Le traumatisme contondant est la cause la plus fréquente. Les exemples typiques sont les coups de ballon, les coups de poing, les accidents de la route et les accidents du travail. La force de compression sur l’œil provoque la rupture des vaisseaux de l’iris, du corps ciliaire et du trabéculum, entraînant une accumulation de globules rouges dans la chambre antérieure.
En l’absence de traumatisme, les causes suivantes doivent être envisagées.
La drépanocytose est un facteur de risque particulièrement important. Dans l’environnement hypoxique de la chambre antérieure, les globules rouges se falciforment, deviennent rigides et traversent difficilement le trabéculum. Ainsi, même une petite hémorragie peut provoquer une élévation sévère de la pression intraoculaire. De plus, les globules rouges falciformes intravasculaires peuvent entraîner une occlusion de l’artère centrale de la rétine ou une neuropathie optique ischémique. Même le trait drépanocytaire constitue un risque.
La chirurgie de la cataracte sous warfarine augmente les événements hémorragiques, mais la plupart sont des hyphemas ou des hémorragies sous-conjonctivales auto-limitées, sans effet néfaste sur l’acuité visuelle postopératoire5). Cependant, la collaboration entre le médecin traitant et l’ophtalmologiste est importante pour évaluer les risques individuels.
Le diagnostic de l’hyphema repose sur une série d’examens progressifs. L’anamnèse, l’examen de l’acuité visuelle, le réflexe pupillaire, la mesure de la pression intraoculaire et l’examen à la lampe à fente sont essentiels. En cas d’hyphema abondant, le réflexe pupillaire indirect de l’œil controlatéral est également vérifié.
| Examen | Objectif principal |
|---|---|
| Lampe à fente | Classification de grade et suivi |
| Gonioscopie (1 à 2 semaines après le traumatisme) | Récession de l’angle, synéchies antérieures |
| UBM / OCT du segment antérieur (UBM contre-indiqué en cas de plaie perforante) | Évaluation structurale du corps ciliaire et de l’angle |
| Échographie (mode B) | Évaluation du segment postérieur lorsque le fond d’œil n’est pas visible |
| CT / IRM (IRM contre-indiquée en cas de corps étranger métallique) | Évaluation de rupture du globe et de corps étranger intraoculaire |
Le principe de base du traitement est d’attendre la résorption spontanée par le repos. Il faut interdire les exercices intenses, éviter la position couchée sur le dos, et maintenir le repos en position assise ou avec la tête du lit surélevée de 30 à 45 degrés. Chez les enfants, en cas d’hyphema occupant plus d’un tiers à la moitié de la chambre antérieure, chez les patients incapables de suivre les instructions, ou en cas d’hypertension oculaire associée à une drépanocytose, une hospitalisation est souhaitable.
En cas d’élévation de la pression intraoculaire, ajouter ce qui suit (seul le 4, ou 5+6, ou une combinaison de 4 à 6).
Les antifibrinolytiques (acide tranexamique) sont utiles pour réduire le risque de resaignement 4). Cependant, leur impact sur le pronostic visuel n’est pas clair 4).
Environ 5 % des hyphémas traumatiques nécessitent une intervention chirurgicale.
Les indications chirurgicales sont les suivantes :
| Groupe de patients | Critères d’indication chirurgicale |
|---|---|
| Patients sains | Pression ≥ 50 mmHg pendant 5 jours, ou ≥ 35 mmHg pendant 7 jours |
| Patients drépanocytaires | Pression ≥ 25 mmHg pendant plus de 24 heures |
| Signes de teinture cornéenne par le sang | Indication sans attendre les critères ci-dessus |
| Hyphéma total chez l’enfant | Intervention précoce en raison du risque d’amblyopie par privation visuelle |
La chirurgie du glaucome (chirurgie filtrante, etc.) est indiquée en cas d’hypertension oculaire persistante après lavage de la chambre antérieure. En cas de luxation ou de lésion du cristallin, une extraction du cristallin est nécessaire. En cas de bloc pupillaire, envisager une iridotomie au laser.
Dans la plupart des cas, une prise en charge ambulatoire est possible sous réserve d’un suivi attentif. Cependant, chez l’enfant, en cas d’hémorragie abondante (plus d’1/3 à 1/2 de la chambre antérieure), d’hypertension oculaire associée à une drépanocytose, ou si le patient ne peut respecter le repos, une hospitalisation est préférable.
Lorsqu’une force contondante est appliquée au globe oculaire, la pression intraoculaire augmente brusquement. Il se produit un étirement du limbe cornéen, et l’humeur aqueuse se déplace vers l’arrière et l’angle. Ce changement mécanique endommage les vaisseaux de l’iris et du corps ciliaire, entraînant une hémorragie dans la chambre antérieure.
Selon la gravité de la lésion, une destruction structurelle progressive se produit.
Une récidive hémorragique survient 3 à 7 jours après le traumatisme en raison de la rétraction et de la lyse du caillot initial4). L’incidence est de 5 à 10 %4). La récidive est souvent plus abondante et plus grave que l’hémorragie initiale. Une hypertension oculaire est observée dans plus de 50 % des cas de récidive.
Les facteurs de risque de récidive hémorragique sont les suivants :
L’élévation de la pression intraoculaire associée à une hyphéma résulte de plusieurs mécanismes.
Lorsqu’une hyphéma sévère s’accompagne d’une hypertension oculaire persistante, la face postérieure de la cornée se teinte de sang. Cela peut laisser des séquelles visuelles même après la résorption de l’hyphéma, nécessitant un lavage précoce de la chambre antérieure.
C’est une complication chronique importante après un traumatisme contondant. Une rupture se produit entre les fibres circulaires et longitudinales du muscle ciliaire, entraînant une récession de l’angle. En particulier, les cas avec une récession de l’angle de 180 degrés ou plus développent un glaucome à un taux élevé de 6 à 20 % en 10 ans. Comme la survenue est souvent plusieurs années après le traumatisme, un suivi à long terme de la pression intraoculaire est indispensable.
Le taux de récidive hémorragique est globalement de 5 à 10 %, survenant souvent 3 à 7 jours après le traumatisme4). La récidive a tendance à être plus grave que l’hémorragie initiale, il est donc important de respecter le repos et de bénéficier d’une surveillance étroite pendant cette période.
La complication à long terme la plus importante est le glaucome par récession de l’angle. Chez les patients présentant une récession de l’angle de 180 degrés ou plus, un glaucome se développe dans 6 à 20 % des cas sur 10 ans. Comme il peut survenir plusieurs années après la blessure, il est essentiel de poursuivre des examens réguliers de la pression intraoculaire, du champ visuel et du nerf optique après un traumatisme.
Avec la généralisation des médicaments à cible moléculaire, des hémorragies spontanées de la chambre antérieure liées à des médicaments ont été rapportées.
Aldecoa et al. (2023) ont rapporté une hémorragie spontanée de la chambre antérieure chez une femme de 60 ans prenant de l’ibrutinib (inhibiteur de BTK) 420 mg/jour pendant 4 mois pour une leucémie lymphoïde chronique1). L’arrêt de l’ibrutinib et l’application locale de stéroïdes en collyre ont conduit à une résolution complète en 2 semaines. Il a été suggéré que l’ibrutinib réduit l’adhésion plaquettaire au facteur de von Willebrand et inhibe l’agrégation plaquettaire induite par le collagène.
Chiang et al. (2022) ont rapporté une hémorragie spontanée de la chambre antérieure chez un homme de 37 ans atteint de leucémie myéloïde aiguë et de pneumonie sévère à COVID-192). En plus d’une thrombocytopénie sévère (6×10⁹/L), une augmentation de la pression veineuse épisclérale due à un décubitus ventral prolongé a été estimée comme facteur contributif.
Ison et al. (2022) ont rapporté une hémorragie spontanée de la chambre antérieure provenant de microhémangiomes iriens (touffes de Cobb) chez une femme de 56 ans atteinte du syndrome d’Eisenmenger3). L’hypoxémie chronique (SpO₂ au repos 78 %) et la polyglobulie secondaire (Hb 22,5 g/dL) ont été considérées comme ayant induit une dilatation des vaisseaux stromaux iriens, contribuant à la formation de microhémangiomes. L’application locale d’atropine et de dexaméthasone a fait régresser l’hémorragie.
Zhang et al. (Pictures & Perspectives) ont rapporté une hémorragie spontanée des chambres antérieure et postérieure après implantation d’ICL (lentille intraoculaire phaque)6). Une femme de 23 ans a présenté une baisse soudaine de l’acuité visuelle sans traumatisme, frottement oculaire ni utilisation d’anticoagulants. L’examen UBM a confirmé la rupture d’un kyste iridociliaire lié aux haptiques de l’ICL et une hémorragie environnante. Un traitement conservateur de 17 jours avec des collyres de tobramycine et dexaméthasone (4 fois/jour) et du gel de sulfate d’atropine à 1 % (2 fois/jour) a entraîné la résolution de l’hémorragie. Il a été démontré que le retrait d’urgence de l’ICL n’est pas toujours nécessaire.