Lieve (Grado I–II)
Rischio di aumento della pressione intraoculare : circa il 13,5%.
Disturbo visivo : rimane lieve se l’area pupillare è libera.
Visualizzazione del fondo oculare : spesso possibile.
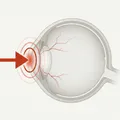
L’ipema traumatico (traumatic hyphema) è un accumulo di globuli rossi nella camera anteriore (lo spazio tra cornea e iride) dopo un trauma contusivo. Un sanguinamento minimo visibile solo al microscopio a lampada a fessura è chiamato microipema (microhyphema).
Quando una forza contusiva viene applicata all’occhio, la pressione intraoculare aumenta bruscamente e il limbus corneale si stira. L’umore acqueo si sposta posteriormente e nell’angolo, danneggiando l’iride e il corpo ciliare, provocando sanguinamento. La parte più vulnerabile è la sottile zona di attacco dell’iride al corpo ciliare; se si rompe (dialisi iridea), la pupilla si sposta. Se si forma una fessura nel corpo ciliare sul lato sclerale, si verifica una recessione angolare; se il corpo ciliare si stacca dalla sclera più oltre, si tratta di una dialisi del corpo ciliare. In queste due condizioni, l’ipema è particolarmente frequente.
La classificazione in base alla quantità di sanguinamento è la seguente:
| Grado | Entità del sanguinamento |
|---|---|
| 0 | Microipema |
| I | Meno di un terzo della camera anteriore |
| II | Da un terzo a metà della camera anteriore |
| III | Da metà a meno del completo riempimento della camera anteriore |
| IV | Emorragia totale della camera anteriore |
Tra i gradi IV, la condizione in cui la camera anteriore è completamente riempita di sangue rosso vivo è chiamata ipema totale (total hyphema). La condizione riempita di sangue rosso scuro-nero è chiamata ipema a palla da biliardo (8-ball hyphema / black ball hyphema) e suggerisce un disturbo della circolazione dell’umore acqueo e ipossia.
Oltre ai traumi, può verificarsi spontaneamente dopo chirurgia intraoculare (iatrogena), per neovascolarizzazione dell’iride, tumori oculari, malattie del sangue (leucemia, emofilia, ecc.) o uso di anticoagulanti. Per maggiori dettagli, vedere la sezione «Cause e fattori di rischio».
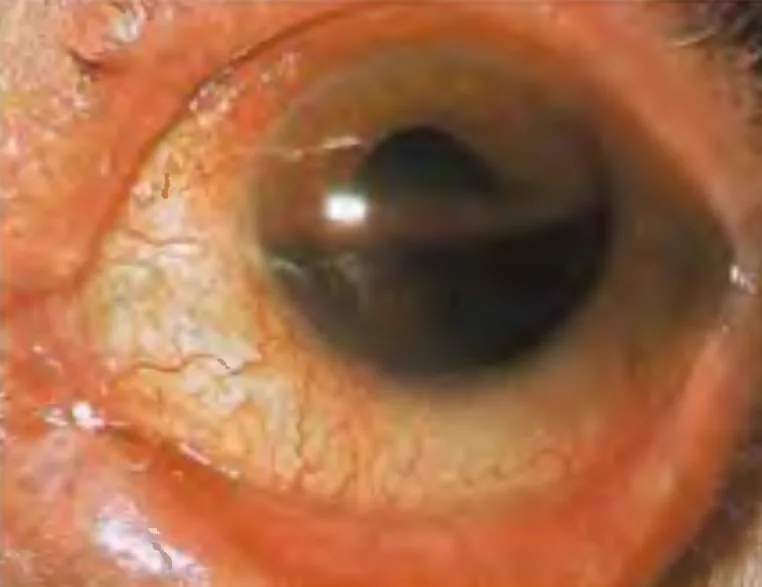
I sintomi dell’ipema traumatico variano in base alla quantità di sanguinamento.
L’ipema forma un livello inferiore (formazione di un livello liquido) e il colore varia dal rosso al nero con il passare del tempo. Il sangue coagulato ha un aspetto più scuro. L’altezza del livello dell’ipema in posizione eretta è un indicatore della quantità di sanguinamento e funge da riferimento per il successivo monitoraggio del riassorbimento o di una recidiva emorragica. È importante registrare l’altezza dal bordo corneale inferiore in millimetri.
Lieve (Grado I–II)
Rischio di aumento della pressione intraoculare : circa il 13,5%.
Disturbo visivo : rimane lieve se l’area pupillare è libera.
Visualizzazione del fondo oculare : spesso possibile.
Grave (Grado III–IV)
Rischio di aumento della pressione intraoculare : aumenta drasticamente, 27% per il grado III e 52% per il grado IV.
Ipema a palla da biliardo : alto rischio di blocco pupillare o chiusura secondaria dell’angolo.
Visualizzazione del fondo oculare : spesso impossibile, necessaria ecografia.
Le principali complicanze sono le seguenti.
Le complicanze specifiche dell’infanzia sono le seguenti:
Il trauma contusivo è la causa più comune. Esempi tipici sono colpi di palla, pugni, incidenti stradali e infortuni sul lavoro. La forza di compressione sull’occhio provoca la rottura dei vasi sanguigni dell’iride, del corpo ciliare e del trabecolato, con accumulo di globuli rossi nella camera anteriore.
In assenza di trauma, considerare le seguenti cause.
L’anemia falciforme è un fattore di rischio particolarmente importante. Nell’ambiente ipossico della camera anteriore, i globuli rossi si falcizzano, diventano rigidi e passano difficilmente attraverso il trabecolato. Di conseguenza, anche una piccola emorragia può causare un grave aumento della pressione intraoculare. Inoltre, i globuli rossi falcizzati intravascolari possono causare occlusione dell’arteria centrale della retina o neuropatia ottica ischemica. Anche il tratto falciforme (trait) costituisce un rischio.
L’intervento di cataratta in corso di terapia con warfarin aumenta gli eventi emorragici, ma la maggior parte sono ifemi auto-limitanti o emorragie sottocongiuntivali, senza effetti negativi sull’acuità visiva postoperatoria5). Tuttavia, per il rischio individuale è importante la collaborazione tra medico curante e oculista.
La diagnosi di ifema viene effettuata in modo graduale con i seguenti esami. Anamnesi, esame dell’acuità visiva, riflesso pupillare, tonometria e biomicroscopia con lampada a fessura sono fondamentali. In caso di ifema abbondante, si verifica anche il riflesso pupillare indiretto dell’occhio controlaterale.
| Esame | Scopo principale |
|---|---|
| Lampada a fessura | Classificazione del grado e follow-up |
| Gonioscopia (1-2 settimane dopo il trauma) | Recessione dell’angolo, sinechie anteriori |
| UBM / OCT del segmento anteriore (UBM controindicata nel trauma perforante) | Valutazione strutturale del corpo ciliare e dell’angolo |
| Ecografia (modalità B) | Valutazione del segmento posteriore quando il fondo oculare non è visualizzabile |
| TC / RM (RM controindicata in caso di corpo estraneo metallico) | Valutazione di rottura del bulbo e corpo estraneo intraoculare |
Il principio di base del trattamento è attendere il riassorbimento spontaneo con il riposo. È vietato l’esercizio fisico intenso, si evita la posizione supina e si mantiene il riposo in posizione seduta o con la testata del letto sollevata di 30–45 gradi. Nei bambini, in caso di ifema che occupa più di 1/3–1/2 della camera anteriore, in pazienti che non possono seguire le istruzioni, o in caso di aumento della pressione intraoculare associato ad anemia falciforme, è preferibile il ricovero ospedaliero.
In caso di aumento della pressione intraoculare, aggiungere quanto segue (solo 4, o 5+6, o una combinazione da 4 a 6).
Gli antifibrinolitici (acido tranexamico) sono utili per ridurre il rischio di risanguinamento 4). Tuttavia, l’impatto sulla prognosi visiva non è chiaro 4).
Circa il 5% degli ifemi traumatici richiede un intervento chirurgico.
Le indicazioni chirurgiche sono le seguenti:
| Gruppo di pazienti | Criteri di indicazione chirurgica |
|---|---|
| Pazienti sani | ≥ 50 mmHg per 5 giorni, o ≥ 35 mmHg per 7 giorni |
| Pazienti con anemia falciforme | ≥ 25 mmHg per più di 24 ore |
| Segni di colorazione corneale da sangue | Indicazione senza attendere i criteri sopra |
| Iperna totale nei bambini | Intervento precoce considerando il rischio di ambliopia da deprivazione visiva |
La chirurgia del glaucoma (chirurgia filtrante, ecc.) è indicata quando l’ipertensione oculare persiste dopo il lavaggio della camera anteriore. In caso di lussazione o danno del cristallino, è necessaria l’estrazione della lente. Per il blocco pupillare, considerare l’iridotomia laser.
Nella maggior parte dei casi, è possibile la gestione ambulatoriale a condizione di un attento follow-up. Tuttavia, nei bambini, in caso di emorragia abbondante (livello superiore a 1/3–1/2), in caso di anemia falciforme con aumento della pressione intraoculare, o se il paziente non può seguire le indicazioni di riposo, è preferibile il ricovero.
Quando una forza contundente viene applicata al globo oculare, la pressione nella camera anteriore aumenta bruscamente. Si verifica uno stiramento del limbo corneale e l’umore acqueo si sposta posteriormente e nell’angolo. Questo cambiamento meccanico danneggia i vasi dell’iride e del corpo ciliare, causando un’emorragia nella camera anteriore.
A seconda della gravità della lesione, si verifica una distruzione strutturale graduale.
Il risanguinamento si verifica 3-7 giorni dopo il trauma a causa della retrazione e lisi del coagulo iniziale4). L’incidenza è del 5-10%4). Il risanguinamento è spesso più abbondante e grave dell’emorragia iniziale. In oltre il 50% dei casi di risanguinamento si osserva un aumento della pressione intraoculare.
I fattori di rischio per il risanguinamento sono i seguenti:
L’aumento della pressione intraoculare associato a un ifema è causato da molteplici meccanismi.
In caso di ifema grave con ipertensione oculare persistente, la superficie posteriore della cornea si colora di sangue. Anche dopo la risoluzione dell’ifema, può persistere un deficit visivo, rendendo necessario un lavaggio precoce della camera anteriore.
È un’importante complicanza cronica dopo un trauma contusivo. Si verifica una lacerazione tra le fibre circolari e longitudinali del muscolo ciliare, con conseguente recessione dell’angolo. In particolare, nei casi con recessione dell’angolo di 180 gradi o più, il glaucoma si sviluppa in un’alta percentuale del 6-20% in 10 anni. Poiché l’esordio è spesso molti anni dopo il trauma, è indispensabile un follow-up a lungo termine della pressione intraoculare.
Il tasso di nuova emorragia è complessivamente del 5-10% e si verifica spesso 3-7 giorni dopo il trauma4). La nuova emorragia tende ad essere più grave dell’emorragia iniziale, quindi è importante mantenere il riposo e sottoporsi a uno stretto monitoraggio durante questo periodo.
La complicanza a lungo termine più importante è il glaucoma da recessione angolare. Nei casi con recessione angolare di 180 gradi o più, il glaucoma si sviluppa nel 6-20% dei casi in 10 anni. Poiché può manifestarsi anche molti anni dopo il trauma, è essenziale continuare regolari esami della pressione intraoculare, del campo visivo e del nervo ottico dopo la lesione.
Con la diffusione dei farmaci a bersaglio molecolare, sono state segnalate emorragie spontanee della camera anteriore correlate a farmaci.
Aldecoa et al. (2023) hanno riportato un’emorragia spontanea della camera anteriore in una donna di 60 anni che assumeva ibrutinib (inibitore di BTK) 420 mg/die per 4 mesi per leucemia linfatica cronica1). La sospensione di ibrutinib e l’applicazione locale di colliri steroidei hanno portato a una completa risoluzione in 2 settimane. È stato suggerito che l’ibrutinib riduca l’adesione piastrinica al fattore di von Willebrand e inibisca l’aggregazione piastrinica indotta dal collagene.
Chiang et al. (2022) hanno riportato un’emorragia spontanea della camera anteriore in un uomo di 37 anni con leucemia mieloide acuta e polmonite grave da COVID-192). Oltre a una grave trombocitopenia (6×10⁹/L), è stato ipotizzato che un aumento della pressione venosa episclerale dovuto alla prolungata posizione prona fosse un fattore contribuente.
Ison et al. (2022) hanno riportato un’emorragia spontanea della camera anteriore da microemangiomi dell’iride (ciuffi di Cobb) in una donna di 56 anni con sindrome di Eisenmenger3). L’ipossiemia cronica (SpO₂ a riposo 78%) e la policitemia secondaria (Hb 22,5 g/dL) sono state considerate come fattori che hanno indotto la dilatazione dei vasi stromali dell’iride e contribuito alla formazione di microemangiomi. L’applicazione locale di atropina e desametasone ha portato alla regressione dell’emorragia.
Zhang et al. (Pictures & Perspectives) hanno riportato un’emorragia spontanea delle camere anteriore e posteriore dopo impianto di ICL (lente intraoculare fachica)6). Una donna di 23 anni ha presentato un improvviso calo visivo senza trauma, sfregamento oculare o uso di anticoagulanti. L’esame UBM ha confermato la rottura di una cisti irido-ciliare associata agli aptici dell’ICL e un’emorragia circostante. Un trattamento conservativo di 17 giorni con colliri di tobramicina e desametasone (4 volte al giorno) e gel di atropina solfato all’1% (2 volte al giorno) ha portato alla risoluzione dell’emorragia. È stato dimostrato che la rimozione d’urgenza dell’ICL non è sempre necessaria.