Bloqueio Pupilar
Morfologia da íris: Abaulamento anterior da íris periférica (iris bombé)
Profundidade da câmara anterior: Especialmente rasa na periferia
PI: Ocluído ou não realizado
Miose farmacológica: Eficaz

O glaucoma maligno (malignant glaucoma) é uma condição de hipertensão ocular com câmara anterior muito rasa, tipicamente ocorrendo após cirurgia filtrante em olhos com glaucoma de ângulo fechado. Acredita-se que seja causado pela rotação anterior do corpo ciliar ou fluxo anormal de humor aquoso para a cavidade vítrea, deslocando o vítreo anteriormente e fechando o ângulo. Também é conhecido como síndrome de desvio do humor aquoso (aqueous misdirection syndrome), glaucoma de bloqueio ciliar (ciliary block glaucoma) e glaucoma de bloqueio direto do cristalino (direct lens block glaucoma), com vários termos sobrepostos. O código CID-10 é H40.8.
É um conceito de doença histórica relatado pela primeira vez por Von Graefe em 1869 como uma câmara anterior rasa refratária após cirurgia filtrante 3). Posteriormente, o conceito de que o humor aquoso é desviado para trás (em direção à cavidade vítrea) em vez da via anterior normal foi estabelecido, e o nome “aqueous misdirection” (desvio do humor aquoso) tornou-se amplamente utilizado. É mais frequentemente encontrado em olhos com glaucoma de ângulo fechado após cirurgia filtrante, mas é clinicamente importante que pode ocorrer após qualquer cirurgia intraocular, incluindo cirurgia de catarata.
Nas Diretrizes de Prática Clínica para Glaucoma (5ª edição), as seguintes quatro classificações são estabelecidas como mecanismos de elevação da pressão intraocular no glaucoma de ângulo fechado secundário 6).
O glaucoma maligno é classificado na terceira categoria acima, “deslocamento anterior de tecidos posteriores ao cristalino”. Na 5ª edição do EGS, corresponde ao “mecanismo de empurrão posterior” 5).
A incidência após cirurgia filtrante é relatada como 0,6-4% 5). Ocorre mais frequentemente em mulheres, geralmente unilateral. Ocorre mais frequentemente após cirurgia filtrante em olhos com glaucoma primário de ângulo fechado, mas pode ocorrer após qualquer cirurgia intraocular, incluindo cirurgia de catarata 5). Os fatores de risco incluem eixo ocular curto (<21 mm), hipermetropia alta (≥+6 D) e história de glaucoma primário de ângulo fechado 5). Raramente, casos idiopáticos sem história cirúrgica foram relatados. Sabe-se que a trabeculectomia em olhos com glaucoma de ângulo fechado tem uma probabilidade relativamente alta de causar glaucoma maligno com câmara anterior rasa e descolamento coroidal pós-operatório 6).
No bloqueio pupilar, a obstrução do fluxo do humor aquoso na borda pupilar faz com que a íris periférica se abaulamente para frente (íris em barril). Por outro lado, no desvio do humor aquoso, o humor aquoso se acumula na cavidade vítrea atrás do cristalino, tornando a câmara anterior rasa uniformemente, esta é a diferença. Medicamentos mióticos são eficazes para o bloqueio pupilar, mas são contraindicados no desvio do humor aquoso.
Nos casos de início agudo, os seguintes sintomas se manifestam.
Os sintomas são flutuantes e podem se manifestar semanas a anos após a cirurgia de catarata 3). No início, a pressão intraocular pode permanecer dentro da normalidade, atrasando o diagnóstico 5). Quando a pressão intraocular aumenta abruptamente, o quadro clínico se assemelha a um ataque agudo de glaucoma, com rápida deterioração visual.
O diagnóstico é feito pela combinação dos seguintes achados. Além do aumento da pressão intraocular, o padrão de alteração da profundidade da câmara anterior é o mais importante no diagnóstico diferencial.
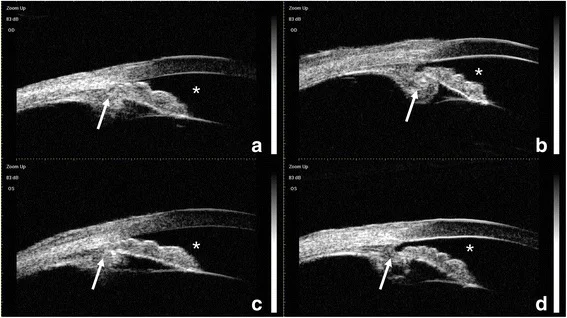
Na tomografia de coerência óptica do segmento anterior (AS-OCT), foi relatado que apresenta achados semelhantes a plateau iris (parte central da íris plana, mas ângulo fechado) devido ao deslocamento anterior do complexo CTR-IOL2). A biomicroscopia ultrassônica (UBM) pode confirmar diretamente o deslocamento anterior do complexo cápsula-IOL e a rotação anterior ou posição anormal do corpo ciliar4). A UBM tem alta resolução de 20-60 μm e pode delinear detalhadamente as estruturas do segmento anterior, como íris e corpo ciliar, portanto deve ser realizada ativamente em casos suspeitos de glaucoma maligno.
Os exames de UBM e OCT de segmento anterior são úteis para elucidar a fisiopatologia, especialmente avaliando o histórico cirúrgico e verificando se há anormalidade na posição do corpo ciliar.
O gatilho mais comum é a cirurgia intraocular5).
Quanto menor o olho, maior o risco5).
Quando ocorre em um olho, o risco de ocorrência no olho contralateral também aumenta3). O risco aumenta independentemente de história prévia de glaucoma, portanto o acompanhamento regular do olho contralateral é importante.
Os principais fatores de risco estão resumidos abaixo.
| Fator de Risco | Exemplo Específico |
|---|---|
| Morfologia Ocular | Eixo curto (<21 mm), hipermetropia alta (>+6 D), câmara anterior rasa |
| Cirurgia | Cirurgia filtrante, cirurgia de catarata, implante de CTR |
| Medicamentos | Topiramato, ISRS |
O topiramato aumenta a permeabilidade vascular da coroide e do corpo ciliar, causando edema e rotação anterior do corpo ciliar 1). Em olhos de alto risco, como microftalmia, pode desencadear desvio aquoso. ISRS também podem induzir oclusão angular em olhos com ângulo estreito através do efeito midriático.
O glaucoma maligno é um diagnóstico de exclusão, estabelecido somente após excluir sistematicamente bloqueio pupilar, hemorragia ou descolamento coroidal, hemorragia supracoroidal e outros mecanismos de oclusão angular 4). Não é uma doença que possa ser confirmada apenas por valores laboratoriais ou achados de imagem, mas sim avaliada de forma abrangente pela combinação da evolução clínica e múltiplos achados de exames.
Suspeite desta doença quando ocorrer câmara anterior extremamente rasa e pressão intraocular elevada no início do pós-operatório de glaucoma de ângulo fechado. O descolamento coroidal hemorrágico pode apresentar achados semelhantes à lâmpada de fenda, e ambos podem causar hipertensão, mas podem ser diferenciados pelo exame de fundo de olho. Nos casos idiopáticos, o diagnóstico é mais difícil devido à ausência de cirurgia prévia, e a confirmação da posição anormal do corpo ciliar por UBM é a chave para o diagnóstico.
Abaixo estão resumidos os pontos de diferenciação entre bloqueio pupilar e desvio aquoso.
Bloqueio Pupilar
Morfologia da íris: Abaulamento anterior da íris periférica (iris bombé)
Profundidade da câmara anterior: Especialmente rasa na periferia
PI: Ocluído ou não realizado
Miose farmacológica: Eficaz
Desvio do humor aquoso
Morfologia da íris: Deslocamento anterior total da íris
Profundidade da câmara anterior: Uniformemente rasa a ausente 5)
PI: Pérvio
Miose farmacológica: Contraindicada (piora)
Outros diagnósticos diferenciais incluem os seguintes. Todos podem causar câmara anterior rasa e hipertensão ocular, mas o mecanismo de início é diferente, portanto o plano de tratamento também difere.
A abordagem básica é gradual: terapia medicamentosa → laser → cirurgia. Primeiro, tenta-se reverter o bloqueio ciliar com medicamentos; se não houver resposta, avança-se para laser; se ainda ineficaz, para cirurgia. O objetivo final é criar um olho unicameral para prevenir recorrência.
Recomenda-se a combinação de três classes: anticolinérgicos (midriáticos e relaxantes ciliares), inibidores da produção de humor aquoso (colírios e orais) e agentes osmóticos (intravenosos) 5).
| Medicamento | Posologia | Mecanismo de Ação |
|---|---|---|
| Colírio de Atropina 1% | 1 a 3 vezes ao dia | Relaxamento ciliar e midríase |
| Colírio de Timolol 0,5% | 2 vezes ao dia | Inibição da produção de humor aquoso (betabloqueador) |
| Comprimidos de Diamox 250 mg | 2 comprimidos, 2 vezes ao dia após as refeições | Inibição da produção de humor aquoso (IAC oral) |
| Infusão de manitol | Administração intravenosa | Redução do volume vítreo |
A atropina aumenta a tensão da zônula ciliar para mover o cristalino para trás, ajudando o humor aquoso que foi para a cavidade vítrea a retornar para a frente. O ciclopentolato também pode ser usado como alternativa à atropina 5).
Colírios que suprimem a produção de humor aquoso (betabloqueadores e inibidores da anidrase carbônica) são usados em conjunto com infusão de agentes hiperosmóticos 6). Os agentes hiperosmóticos reduzem o volume vítreo, mas seu efeito terapêutico é temporário, sendo considerados um preparo pré-operatório 6).
A taxa de sucesso da terapia medicamentosa é de cerca de 50% (dentro de 5 dias), mas a taxa de recorrência é alta com medicamentos isolados 5). Mesmo que a câmara anterior se aprofunde e a pressão intraocular normalize com a terapia medicamentosa, a interrupção do colírio de atropina frequentemente leva à recorrência, portanto, pode ser necessário continuar o colírio de atropina como terapia de manutenção a longo prazo. A terapia medicamentosa é apenas uma abordagem inicial, e o tratamento curativo geralmente requer intervenção a laser ou cirúrgica.
Em olhos pseudofácicos, realiza-se capsulotomia posterior com laser Nd:YAG, em seguida desloca-se o foco para trás da cápsula posterior e aplicam-se 10 a 20 disparos com energia de 3 a 4 mJ para romper a membrana vítrea anterior. Ao criar uma passagem para o humor aquoso entre a cavidade vítrea e a câmara anterior, tenta-se aliviar o bloqueio. Se bem-sucedido, a profundidade da câmara anterior melhora e a pressão intraocular diminui imediatamente ou no dia seguinte.
Em olhos pseudofácicos ou afácicos, opta-se por laser YAG ou vitreotomia anterior cirúrgica ou capsulotomia 6) (nível de evidência 2C).
A fotocoagulação do corpo ciliar com laser de diodo pode ser considerada em qualquer estágio do tratamento 5). Causa necrose coagulativa e atrofia dos processos ciliares, podendo destruir a interface ciliar-vítrea e rotacionar o corpo ciliar para trás 3). No entanto, as condições de irradiação necessárias para destruir a interface ciliar-vítrea não foram estabelecidas.
Se o tratamento medicamentoso e a laser forem insuficientes, ou em casos de recorrência, realiza-se cirurgia. É importante realizar vitrectomia com vitreotomia anterior para resolver a condição patológica 6) (nível de evidência 2C).
A vitrectomia pars plana (PPV) é realizada 5). A extração do cristalino também pode ser realizada concomitantemente em alguns casos 6) (2C). Ao realizar a extração do cristalino, cria-se um olho unicameral, eliminando completamente o bloqueio entre as câmaras posterior e anterior para prevenir a recorrência.
Zonulo-hialoide-vitrectomia (iridectomia-zonulectomia-vitrectomia anterior) é eficaz 5). Aborda-se a câmara anterior através de uma iridectomia periférica, e as zônulas de Zinn ao redor da cápsula do cristalino e a membrana vítrea anterior são excisadas. Este procedimento cria uma via permanente entre a cavidade vítrea e a câmara anterior.
Na vitrectomia com vitreotomia anterior, a iridectomia pode ser necessária para tratar a membrana vítrea anterior na região mais periférica 6) (2C). Se a membrana vítrea anterior e as zônulas de Zinn não forem tratadas adequadamente, um bloqueio entre a cavidade vítrea e a câmara anterior pode persistir e levar à recorrência. Em olhos com cristalino natural, o cristalino também é removido simultaneamente para eliminar o contato entre os processos ciliares e o equador do cristalino, criando um olho unicameral.
Há relatos de que a combinação de remoção do CTR, vitrectomia anterior e fixação intraescleral da LIO foi eficaz 2).
O desvio aquoso é um glaucoma de ângulo fechado por mecanismo de empurrão posterior do cristalino. Os mióticos contraem o músculo ciliar, exacerbando a protrusão anterior do corpo ciliar e piorando o bloqueio ciliar, sendo portanto contraindicados 6). Em contraste, drogas cicloplégicas-midriáticas como atropina relaxam o músculo ciliar, aumentam a tensão das zônulas e movem o cristalino para trás, sendo eficazes para aliviar o bloqueio.
A ocorrência em um olho aumenta significativamente o risco no olho contralateral 3). O risco aumenta independentemente de história de glaucoma, portanto a avaliação regular da pressão intraocular e profundidade da câmara anterior no olho contralateral é importante.
O mecanismo exato do glaucoma maligno não é completamente compreendido, mas duas hipóteses principais foram propostas 5).
Teoria da Expansão Coroidal
Mecanismo principal: O aumento do volume da coroide gera resistência ao movimento do líquido de posterior para anterior 5)
Resultado: O humor aquoso acumula-se na cavidade vítrea, empurrando o diafragma íris-cristalino para frente
Teoria do bloqueio ciliar
Mecanismo principal: Contato anatômico anormal entre os processos ciliares, o equador do cristalino (ou LIO) e a membrana hialoide anterior
Resultado: Atua como uma válvula unidirecional, impedindo o fluxo anterior do humor aquoso, estabelecendo um “ciclo maligno”
A progressão da condição patológica pode ser entendida pela seguinte cascata. No olho normal, o humor aquoso produzido no corpo ciliar flui da câmara posterior através da pupila para a câmara anterior, saindo pela malha trabecular no ângulo. No glaucoma maligno, essa via é interrompida.
A instilação de atropina relaxa o músculo ciliar, aumenta a tensão das zônulas e desloca o cristalino para trás. Isso pode fazer com que o humor aquoso que foi para a cavidade vítrea retorne para a frente.
Por outro lado, mióticos como a pilocarpina contraem o músculo ciliar. Essa contração relaxa as zônulas e empurra o cristalino para frente, além de promover a protrusão anterior do corpo ciliar, agravando o bloqueio ciliar 6). Portanto, os mióticos são contraindicados no glaucoma maligno.
Em olhos pseudofácicos, o diâmetro horizontal do complexo LIO-saco é maior que o do cristalino natural, tornando-o mais propenso ao contato com os processos ciliares 4). Parte do humor aquoso produzido nos processos ciliares é secretada para trás (cavidade vítrea). Se a membrana hialoide anterior estiver intacta, o fluxo de líquido para frente é impedido, gerando um gradiente de pressão e aprofundamento da câmara anterior.
Mesmo em olhos com histórico de vitrectomia, foi relatado que a condição pode ocorrer se a membrana hialoide anterior permanecer 4). Em casos de recorrência com desvio miópico ≥3 D, a combinação de goniossinéquiálise, iridectomia e zonulo-hialoidectomia restaurou a refração e a pressão intraocular 4). Portanto, durante a vitrectomia, a membrana hialoide anterior deve ser completamente removida até a periferia mais extrema para prevenir recorrência.
O topiramato aumenta a permeabilidade dos vasos coroidianos ciliares, causando inchaço do corpo ciliar e coroide e rotação anterior do corpo ciliar 1). Na microftalmia, o comprometimento da drenagem das veias vorticosas devido à espessura escleral aumenta ainda mais o risco de efusão uveal 1).
A colocação do CTR causa expansão e espessamento do saco capsular, fazendo com que o complexo CTR-LIO entre em contato circunferencial com o corpo ciliar e a íris posterior 2). Isso comprime o espaço ciliar e aumenta a resistência ao movimento do humor aquoso de trás para frente. Como o grande diâmetro do complexo CTR-LIO limita parcialmente o deslocamento anterior, pode ocorrer oclusão angular em platô de íris com profundidade da câmara anterior preservada 2). Esse achado atípico difere da imagem clássica do glaucoma maligno de “câmara anterior uniformemente rasa”, tornando a avaliação detalhada da morfologia angular com AS-OCT a chave para o diagnóstico.
Chean et al. (2021) relataram um caso de desvio aquoso (aqueous misdirection) que se manifestou após cirurgia de catarata com surpresa miópica (myopic surprise) como único sinal inicial 3). A pressão intraocular permaneceu dentro da faixa normal por cerca de 3 anos após a cirurgia, atrasando o diagnóstico. Mesmo que a profundidade da câmara anterior pareça normal na biometria, erros de medição podem ocorrer em olhos com eixo curto, portanto, o desvio aquoso deve ser incluído no diagnóstico diferencial quando houver shift miópico.
Stephenson et al. (2023) relataram um caso de desvio aquoso com shift miópico ≥3 D em um olho com histórico de vitrectomia, cirurgia de catarata e implante de íris artificial 4). Eles mostraram que a condição pode ocorrer mesmo após vitrectomia se a membrana vítrea anterior permanecer, e a refração e a pressão intraocular foram recuperadas após goniosinequiólise + iridectomia + zonulo-hialoidectomia.
Goto et al. (2024) caracterizaram pela primeira vez o fechamento angular secundário devido ao deslocamento anterior do complexo CTR-IOL usando AS-OCT 2). Eles relataram uma imagem atípica semelhante a plateau iris com profundidade da câmara anterior preservada e mostraram a utilidade da AS-OCT na detecção de fechamento angular secundário após cirurgia de catarata e implante de CTR.
Uma abordagem escalonada foi proposta: terapia medicamentosa → laser Nd:YAG → ciclodiodo → cirurgia 3). O ciclodiodo pode causar coagulação necrótica e atrofia dos processos ciliares, potencialmente destruindo a interface ciliar-vítrea e rotacionando o corpo ciliar posteriormente. No entanto, as condições de irradiação necessárias para destruir a interface ciliar-vítrea não foram estabelecidas, e se medicamentos e laser forem insuficientes, a cirurgia para criar um olho unicameral continua sendo a opção de tratamento final 3).