Tắc đồng tử
Hình thái mống mắt: Phồng ra trước của mống mắt ngoại vi (iris bombé)
Độ sâu tiền phòng: Nông đặc biệt ở vùng ngoại vi
PI: Tắc hoặc chưa thực hiện
Thuốc co đồng tử: Có hiệu quả

Glôcôm ác tính (malignant glaucoma) là tình trạng tăng nhãn áp với tiền phòng rất nông, thường xảy ra sau phẫu thuật lọc ở mắt glôcôm góc đóng. Được cho là do thể mi xoay về phía trước hoặc dòng thủy dịch bất thường vào khoang dịch kính, đẩy dịch kính ra trước và đóng góc. Còn được gọi là hội chứng lệch hướng thủy dịch (aqueous misdirection syndrome), glôcôm block thể mi (ciliary block glaucoma) và glôcôm block thể thủy tinh trực tiếp (direct lens block glaucoma), với nhiều thuật ngữ chồng chéo. Mã ICD-10 là H40.8.
Đây là một khái niệm bệnh lý lịch sử được Von Graefe báo cáo lần đầu tiên vào năm 1869 như một tình trạng tiền phòng nông kháng trị sau phẫu thuật lọc 3). Sau đó, khái niệm thủy dịch bị dẫn lạc ra phía sau (về phía khoang dịch kính) thay vì đường đi phía trước bình thường đã được thiết lập, và tên gọi “aqueous misdirection” (dẫn lạc thủy dịch) được sử dụng rộng rãi. Thường gặp nhất ở mắt glôcôm góc đóng sau phẫu thuật lọc, nhưng quan trọng về mặt lâm sàng là nó có thể xảy ra sau bất kỳ phẫu thuật nội nhãn nào bao gồm phẫu thuật đục thủy tinh thể.
Trong Hướng dẫn Thực hành Lâm sàng Glôcôm (ấn bản thứ 5), bốn phân loại sau đây được xác định là cơ chế tăng nhãn áp trong glôcôm góc đóng thứ phát 6).
Glôcôm ác tính được phân loại vào loại thứ ba ở trên, “di chuyển ra trước của các mô phía sau thể thủy tinh”. Trong EGS ấn bản thứ 5, nó tương ứng với “cơ chế đẩy sau” 5).
Tỷ lệ mắc sau phẫu thuật lọc được báo cáo là 0,6-4% 5). Xảy ra thường xuyên hơn ở phụ nữ, thường một bên mắt. Thường gặp nhất sau phẫu thuật lọc ở mắt glôcôm góc đóng nguyên phát, nhưng có thể xảy ra sau bất kỳ phẫu thuật nội nhãn nào bao gồm phẫu thuật đục thủy tinh thể 5). Các yếu tố nguy cơ bao gồm trục nhãn cầu ngắn (<21 mm), viễn thị cao (≥+6 D), và tiền sử glôcôm góc đóng nguyên phát 5). Hiếm khi, các trường hợp vô căn không có tiền sử phẫu thuật đã được báo cáo. Phẫu thuật cắt bè ở mắt glôcôm góc đóng được biết là có khả năng tương đối cao gây glôcôm ác tính với tiền phòng nông và bong hắc mạc sau phẫu thuật 6).
Trong block đồng tử, sự cản trở dòng chảy thủy dịch ở bờ đồng tử làm cho mống mắt ngoại vi phồng ra trước (iris bombé). Mặt khác, trong dẫn lạc thủy dịch, thủy dịch tích tụ trong khoang dịch kính phía sau thể thủy tinh, làm cho tiền phòng nông đồng đều, đây là điểm khác biệt. Thuốc co đồng tử có hiệu quả đối với block đồng tử, nhưng chống chỉ định trong dẫn lạc thủy dịch.
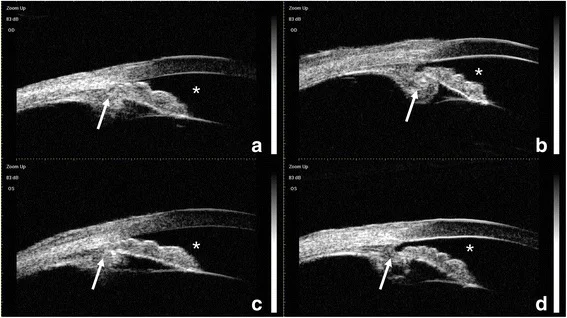
Trong trường hợp khởi phát cấp tính, các triệu chứng sau đây xuất hiện.
Các triệu chứng có tính dao động (fluctuant) và có thể xuất hiện vài tuần đến vài năm sau phẫu thuật đục thủy tinh thể 3). Giai đoạn đầu, áp lực nội nhãn có thể vẫn trong giới hạn bình thường, gây chậm trễ chẩn đoán 5). Khi áp lực nội nhãn tăng đột ngột, hình ảnh lâm sàng giống cơn glôcôm cấp, thị lực suy giảm nhanh chóng.
Chẩn đoán dựa trên sự kết hợp các dấu hiệu sau. Ngoài tăng áp lực nội nhãn, kiểu thay đổi độ sâu tiền phòng là quan trọng nhất trong chẩn đoán phân biệt.
Trên chụp cắt lớp quang học kết hợp vùng trước nhãn cầu (AS-OCT), đã được báo cáo cho thấy hình ảnh giống plateau iris (phần trung tâm mống mắt phẳng nhưng góc đóng) do di lệch ra trước của phức hợp CTR-IOL2). Kính hiển vi siêu âm sinh học (UBM) có thể trực tiếp xác nhận di lệch ra trước của phức hợp bao thể thủy tinh thể-IOL cũng như xoay ra trước hoặc bất thường vị trí của thể mi4). UBM có độ phân giải cao 20-60 μm và có thể mô tả chi tiết các cấu trúc vùng trước như mống mắt và thể mi, do đó cần được thực hiện tích cực trong các trường hợp nghi ngờ glôcôm ác tính.
Các xét nghiệm UBM và OCT vùng trước rất hữu ích để làm sáng tỏ cơ chế bệnh sinh, đặc biệt là đánh giá tiền sử phẫu thuật và kiểm tra xem có bất thường về vị trí của thể mi hay không.
Yếu tố kích hoạt phổ biến nhất là phẫu thuật nội nhãn5).
Nhãn cầu càng nhỏ thì nguy cơ càng cao5).
Nếu xảy ra ở một mắt, nguy cơ xảy ra ở mắt đối diện cũng tăng3). Nguy cơ tăng bất kể tiền sử glôcôm trước đó, do đó việc theo dõi định kỳ mắt đối diện là quan trọng.
Các yếu tố nguy cơ chính được tóm tắt dưới đây.
| Yếu tố nguy cơ | Ví dụ cụ thể |
|---|---|
| Hình thái nhãn cầu | Trục ngắn (<21 mm), viễn thị cao (>+6 D), tiền phòng nông |
| Phẫu thuật | Phẫu thuật lọc, phẫu thuật đục thủy tinh thể, đặt CTR |
| Thuốc | Topiramate, SSRI |
Topiramate làm tăng tính thấm mạch máu hắc mạc và thể mi, gây phù nề và xoay trước thể mi 1). Ở những mắt nguy cơ cao như mắt nhỏ, có thể kích hoạt lệch thủy dịch. SSRI cũng có thể gây tắc góc ở mắt góc hẹp thông qua tác dụng giãn đồng tử.
Glôcôm ác tính là chẩn đoán loại trừ, chỉ được xác định sau khi loại trừ một cách có hệ thống tắc đồng tử, xuất huyết hoặc bong hắc mạc, xuất huyết trên hắc mạc và các cơ chế tắc góc khác 4). Đây không phải là bệnh có thể xác định chỉ bằng các giá trị xét nghiệm hoặc hình ảnh cụ thể, mà được đánh giá toàn diện thông qua kết hợp diễn biến lâm sàng và nhiều kết quả xét nghiệm.
Nghi ngờ bệnh này khi có tiền phòng cực nông và nhãn áp cao sớm sau phẫu thuật glôcôm góc đóng. Bong hắc mạc xuất huyết có thể có biểu hiện tương tự trên sinh hiển vi, và cả hai đều có thể gây tăng nhãn áp, nhưng có thể phân biệt qua soi đáy mắt. Ở các trường hợp vô căn, chẩn đoán khó hơn do không có tiền sử phẫu thuật, và việc xác nhận vị trí bất thường của thể mi bằng UBM là chìa khóa chẩn đoán.
Dưới đây là tóm tắt các điểm phân biệt giữa tắc đồng tử và lệch thủy dịch.
Tắc đồng tử
Hình thái mống mắt: Phồng ra trước của mống mắt ngoại vi (iris bombé)
Độ sâu tiền phòng: Nông đặc biệt ở vùng ngoại vi
PI: Tắc hoặc chưa thực hiện
Thuốc co đồng tử: Có hiệu quả
Lạc hướng thủy dịch
Hình thái mống mắt: Mống mắt lệch ra trước toàn bộ
Độ sâu tiền phòng: Nông đều đến mất hoàn toàn 5)
PI: Thông thoáng
Thuốc co đồng tử: Chống chỉ định (làm nặng thêm)
Các bệnh cần chẩn đoán phân biệt khác bao gồm những bệnh sau. Tất cả đều có thể gây tiền phòng nông và nhãn áp cao, nhưng cơ chế khởi phát khác nhau nên phác đồ điều trị cũng khác nhau.
Cách tiếp cận cơ bản là từng bước: điều trị bằng thuốc → laser → phẫu thuật. Đầu tiên, cố gắng giải phóng block thể mi bằng thuốc; nếu không đáp ứng, chuyển sang laser; nếu vẫn không hiệu quả, chuyển sang phẫu thuật. Mục tiêu cuối cùng là tạo ra mắt một buồng (unicameral eye) để ngăn tái phát.
Khuyến cáo phối hợp ba nhóm thuốc: thuốc kháng cholinergic (làm giãn đồng tử và giãn thể mi), thuốc ức chế sản xuất thủy dịch (nhỏ mắt và uống), và thuốc thẩm thấu (tiêm tĩnh mạch) 5).
| Thuốc | Liều dùng | Cơ chế tác dụng |
|---|---|---|
| Thuốc nhỏ mắt Atropin 1% | 1–3 lần/ngày | Giãn thể mi và giãn đồng tử |
| Thuốc nhỏ mắt Timolol 0,5% | 2 lần/ngày | Ức chế sản xuất thủy dịch (chẹn beta) |
| Viên Diamox 250 mg | 2 viên, chia 2 lần sau ăn | Ức chế sản xuất thủy dịch (CAI đường uống) |
| Truyền mannitol | Đường tiêm tĩnh mạch | Giảm thể tích dịch kính |
Atropine làm tăng sức căng của dây chằng thể mi để di chuyển thủy tinh thể ra sau, giúp thủy dịch đã đi vào khoang dịch kính quay trở lại phía trước. Cyclopentolate cũng có thể được sử dụng thay thế atropine 5).
Thuốc nhỏ mắt ức chế sản xuất thủy dịch (thuốc chẹn beta và thuốc ức chế carbonic anhydrase) được sử dụng kết hợp với truyền tĩnh mạch các thuốc thẩm thấu cao 6). Các thuốc thẩm thấu cao làm giảm thể tích dịch kính, nhưng tác dụng điều trị chỉ là tạm thời, do đó được coi là bước chuẩn bị trước phẫu thuật 6).
Tỷ lệ thành công của điều trị bằng thuốc khoảng 50% (trong vòng 5 ngày), nhưng tỷ lệ tái phát cao khi chỉ dùng thuốc đơn thuần 5). Ngay cả khi tiền phòng sâu hơn và nhãn áp trở lại bình thường với điều trị bằng thuốc, việc ngừng nhỏ atropine thường dẫn đến tái phát, do đó có thể cần tiếp tục nhỏ atropine như liệu pháp duy trì lâu dài. Điều trị bằng thuốc chỉ là bước đầu, và điều trị triệt để thường cần can thiệp laser hoặc phẫu thuật.
Ở mắt đã đặt thủy tinh thể nhân tạo, thực hiện mở bao sau bằng laser Nd:YAG, sau đó dịch chuyển tiêu điểm ra sau bao sau và bắn 10-20 phát với năng lượng 3-4 mJ để phá vỡ màng dịch kính trước. Bằng cách tạo một đường dẫn thủy dịch giữa khoang dịch kính và tiền phòng, nhằm giải phóng sự tắc nghẽn. Nếu thành công, độ sâu tiền phòng được cải thiện và nhãn áp giảm ngay lập tức hoặc vào ngày hôm sau.
Ở mắt đã đặt thủy tinh thể nhân tạo hoặc mắt không có thủy tinh thể, lựa chọn laser YAG hoặc phẫu thuật cắt màng dịch kính trước hoặc mở bao 6) (mức độ bằng chứng 2C).
Quang đông thể mi bằng laser diode có thể được xem xét ở bất kỳ giai đoạn điều trị nào 5). Nó gây hoại tử đông và teo các mỏm thể mi, và có thể phá hủy mặt phân cách thể mi-dịch kính và xoay thể mi ra sau 3). Tuy nhiên, các điều kiện chiếu xạ cần thiết để phá hủy mặt phân cách thể mi-dịch kính vẫn chưa được thiết lập.
Nếu điều trị bằng thuốc và laser không đủ hiệu quả, hoặc trong trường hợp tái phát, tiến hành phẫu thuật. Điều quan trọng là thực hiện cắt dịch kính kèm cắt màng dịch kính trước để giải quyết tình trạng bệnh lý 6) (mức độ bằng chứng 2C).
Phẫu thuật cắt dịch kính qua thể mi (PPV) được thực hiện 5). Trong một số trường hợp, có thể kết hợp lấy thủy tinh thể 6) (2C). Việc lấy thủy tinh thể tạo ra mắt một buồng (unicameral eye), loại bỏ hoàn toàn sự tắc nghẽn giữa hậu phòng và tiền phòng để ngăn tái phát.
Phẫu thuật cắt dây Zinn-màng hyaloid-dịch kính (zonulo-hyaloido-vitrectomy) có hiệu quả 5). Tiếp cận từ tiền phòng qua vùng cắt mống mắt ngoại vi, cắt bỏ dây Zinn quanh bao thủy tinh thể và màng dịch kính trước. Phẫu thuật này tạo ra một đường thông vĩnh viễn giữa khoang dịch kính và tiền phòng.
Trong cắt dịch kính kèm mở màng dịch kính trước, có thể cần cắt mống mắt để xử lý màng dịch kính trước ở vùng ngoại vi nhất 6) (2C). Nếu không xử lý đầy đủ màng dịch kính trước và dây Zinn, sự tắc nghẽn giữa khoang dịch kính và tiền phòng có thể tồn tại và dẫn đến tái phát. Ở mắt còn thủy tinh thể, thủy tinh thể cũng được lấy ra cùng lúc để loại bỏ sự tiếp xúc giữa mỏm thể mi và xích đạo thủy tinh thể, tạo ra mắt một buồng.
Có báo cáo cho thấy sự kết hợp giữa loại bỏ CTR, cắt dịch kính trước và cố định IOL trong củng mạc có hiệu quả 2).
Lệch dòng thủy dịch là glôcôm góc đóng do cơ chế đẩy thủy tinh thể ra phía sau. Thuốc co đồng tử làm co cơ thể mi, làm trầm trọng thêm sự nhô ra phía trước của thể mi và làm nặng thêm block thể mi, do đó chống chỉ định 6). Ngược lại, thuốc liệt điều tiết-giãn đồng tử như atropine làm giãn cơ thể mi, tăng căng dây Zinn và di chuyển thủy tinh thể ra sau, có hiệu quả trong việc giải phóng block.
Xảy ra ở một mắt làm tăng đáng kể nguy cơ ở mắt đối diện 3). Nguy cơ tăng lên bất kể tiền sử glôcôm, do đó việc đánh giá định kỳ nhãn áp và độ sâu tiền phòng ở mắt đối diện là rất quan trọng.
Cơ chế chính xác của glôcôm ác tính chưa được hiểu đầy đủ, nhưng hai giả thuyết chính đã được đề xuất 5).
Thuyết giãn nở hắc mạc
Cơ chế chính: Sự gia tăng thể tích hắc mạc tạo ra sức cản đối với sự di chuyển của dịch từ sau ra trước 5)
Kết quả: Thủy dịch tích tụ trong khoang dịch kính, đẩy mống mắt-thể thủy tinh ra phía trước
Thuyết tắc nghẽn thể mi
Cơ chế chính: Tiếp xúc giải phẫu bất thường giữa các mỏm thể mi, xích đạo thể thủy tinh (hoặc IOL) và màng hyaloid trước
Kết quả: Hoạt động như một van một chiều, cản trở dòng chảy thủy dịch ra phía trước, thiết lập một “vòng xoắn ác tính”
Sự tiến triển của tình trạng bệnh lý có thể được hiểu qua thác sau. Ở mắt bình thường, thủy dịch được sản xuất tại thể mi chảy từ hậu phòng qua đồng tử vào tiền phòng, sau đó thoát ra qua bè củng giác mạc ở góc. Trong glôcôm ác tính, đường dẫn này bị phá vỡ.
Nhỏ atropine làm giãn cơ thể mi, tăng sức căng dây chằng Zinn và di chuyển thủy tinh thể ra phía sau. Điều này có thể khiến thủy dịch đã đi vào khoang dịch kính quay trở lại phía trước.
Mặt khác, các thuốc co đồng tử như pilocarpine làm co cơ thể mi. Sự co này làm giãn dây chằng Zinn và đẩy thủy tinh thể ra phía trước, đồng thời thúc đẩy sự nhô ra phía trước của thể mi, làm trầm trọng thêm block thể mi 6). Do đó, thuốc co đồng tử chống chỉ định trong glôcôm ác tính.
Ở mắt giả thể thủy tinh, đường kính ngang của phức hợp IOL-bao lớn hơn thủy tinh thể tự nhiên, dễ tiếp xúc với các mỏm thể mi 4). Một phần thủy dịch được sản xuất tại mỏm thể mi được tiết ra phía sau (khoang dịch kính). Nếu màng hyaloid trước còn nguyên vẹn, dòng chảy dịch ra phía trước bị cản trở, tạo ra chênh lệch áp suất và làm tiền phòng nông.
Ngay cả ở những mắt đã từng cắt dịch kính, đã có báo cáo về khả năng khởi phát nếu màng hyaloid trước còn sót lại 4). Trong trường hợp tái phát với độ cận thị dịch chuyển ≥3 D, sự kết hợp giữa goniosynechialysis (bóc tách dính góc), cắt mống mắt và zonulo-hyaloidectomy đã phục hồi khúc xạ và nhãn áp 4). Vì vậy, khi cắt dịch kính, cần loại bỏ hoàn toàn màng hyaloid trước đến tận vùng ngoại vi nhất để ngăn ngừa tái phát.
Topiramate làm tăng tính thấm của mạch máu hắc mạc-thể mi, gây phù nề thể mi và hắc mạc, đồng thời xoay thể mi ra phía trước 1). Trong bệnh nhãn cầu nhỏ, rối loạn dẫn lưu tĩnh mạch xoáy do củng mạc dày làm tăng thêm nguy cơ tràn dịch màng bồ đào 1).
Đặt CTR làm giãn nở và dày lên bao thủy tinh thể, khiến phức hợp CTR-IOL tiếp xúc toàn bộ chu vi với thể mi và mống mắt sau 2). Điều này chèn ép khoang thể mi và tăng sức cản đối với sự di chuyển của thủy dịch từ sau ra trước. Do đường kính lớn của phức hợp CTR-IOL hạn chế một phần sự lệch ra trước, có thể xảy ra tắc góc dạng plateau iris trong khi độ sâu tiền phòng vẫn được duy trì 2). Dấu hiệu không điển hình này khác với hình ảnh kinh điển của glôcôm ác tính là “tiền phòng nông đồng nhất”, do đó đánh giá chi tiết hình thái góc bằng AS-OCT là chìa khóa chẩn đoán.
Chean và cộng sự (2021) báo cáo một trường hợp lệch thủy dịch (aqueous misdirection) xuất hiện sau phẫu thuật đục thủy tinh thể với biểu hiện cận thị bất ngờ (myopic surprise) là dấu hiệu ban đầu duy nhất 3). Áp lực nội nhãn vẫn trong giới hạn bình thường khoảng 3 năm sau phẫu thuật, dẫn đến chẩn đoán chậm trễ. Ngay cả khi độ sâu tiền phòng có vẻ bình thường trên đo sinh trắc, sai số đo có thể xảy ra ở mắt có trục ngắn, do đó cần đưa lệch thủy dịch vào chẩn đoán phân biệt khi phát hiện dịch chuyển cận thị.
Stephenson và cộng sự (2023) báo cáo một trường hợp lệch thủy dịch với dịch chuyển cận thị ≥3 D ở mắt đã từng phẫu thuật cắt dịch kính, đục thủy tinh thể và đặt mống mắt nhân tạo 4). Họ chỉ ra rằng tình trạng này có thể xảy ra ngay cả sau cắt dịch kính nếu màng dịch kính trước còn sót lại, và khúc xạ cũng như áp lực nội nhãn đã phục hồi sau phẫu thuật goniosynechialysis + cắt mống mắt + zonulo-hyaloidectomy.
Goto và cộng sự (2024) lần đầu tiên mô tả đặc điểm của glôcôm góc đóng thứ phát do di lệch ra trước của phức hợp CTR-IOL bằng AS-OCT 2). Họ báo cáo hình ảnh không điển hình giống plateau iris với độ sâu tiền phòng được bảo tồn, và cho thấy tính hữu ích của AS-OCT trong phát hiện glôcôm góc đóng thứ phát sau phẫu thuật đục thủy tinh thể và đặt CTR.
Một phương pháp tiếp cận theo từng bước đã được đề xuất: điều trị bằng thuốc → laser Nd:YAG → cyclodiode → phẫu thuật 3). Cyclodiode có thể gây đông máu hoại tử và teo các mỏm thể mi, có khả năng phá hủy mặt phân cách thể mi-dịch kính và xoay thể mi ra sau. Tuy nhiên, các điều kiện chiếu xạ cần thiết để phá hủy mặt phân cách thể mi-dịch kính vẫn chưa được thiết lập, và nếu thuốc và laser không đủ hiệu quả, phẫu thuật tạo mắt một buồng (unicameral eye) vẫn là lựa chọn điều trị cuối cùng 3).