黏膜類天皰瘡(MMP)整體概觀
標靶器官:口腔、眼表、鼻咽、喉、食道、生殖器等全身具有複層扁平上皮的黏膜。
皮膚病變:多不伴隨。糜爛和疤痕比水皰更突出。
好發年齡:60~80歲。女性居多。
全身併發症:食道狹窄導致的吞嚥困難、喉狹窄可影響生命預後2)。

眼黏膜類天皰瘡(ocular mucous membrane pemphigoid,簡稱OCP)是一種由針對黏膜上皮基底膜黏附成分的自體抗體引起的慢性進行性自體免疫水皰性疾病,可導致結膜等部位的瘢痕形成。黏膜類天皰瘡(mucous membrane pemphigoid,MMP)是一組可侵犯口腔、眼表面、鼻咽、喉、食道、外陰等多個黏膜的全身性疾病,其中具有眼部病變者稱為眼類天皰瘡或眼瘢痕性類天皰瘡。無皮膚病變的病例並不少見。
在眼科領域,OCP被視為伴有角膜上皮幹細胞缺乏的瘢痕性角結膜上皮病的代表性疾病,其病程呈階段性進展,從慢性結膜炎發展為眼瞼球黏連,最終導致角膜角化。
本病為罕見疾病。英國的一項監測研究報告瘢痕性結膜炎的年發生率約為每百萬人1.3例,OCP的盛行率估計約為1/1萬至1/5萬5)。好發於60~80歲的老年人,男女比例約為1:2,女性多見5)。黏膜病變最常見於口腔(約85%),其次為眼(約65%),約50%的OCP患者合併口腔或皮膚等眼外病變2)。
通常以雙眼慢性結膜炎的形式潛行性發病,病程常持續數年至十餘年。發病初期僅有非特異性結炎症狀,因此常被長期當作過敏性結膜炎、慢性結膜炎或乾眼症治療。以本病為前提進行詳細的問診和裂隙燈顯微鏡檢查,對於早期診斷和改善視功能預後至關重要。
黏膜類天皰瘡(MMP)整體概觀
標靶器官:口腔、眼表、鼻咽、喉、食道、生殖器等全身具有複層扁平上皮的黏膜。
皮膚病變:多不伴隨。糜爛和疤痕比水皰更突出。
好發年齡:60~80歲。女性居多。
全身併發症:食道狹窄導致的吞嚥困難、喉狹窄可影響生命預後2)。
眼黏膜類天皰瘡(OCP)特徵
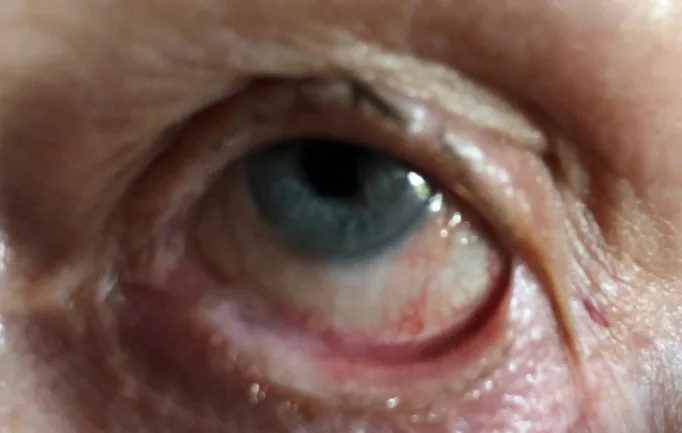
初期主要表現為慢性結膜充血、乾燥感、異物感、灼熱感、流淚。這些症狀對常規乾眼治療有抵抗性,長期持續是懷疑本病的契機1)。進展期可出現瞼球沾黏導致的眼球運動障礙和眼瞼閉合不全、睫毛亂生引起的角膜刺激症狀,以及角膜混濁和結膜上皮侵入導致的視力下降。
本病的進展是潛行性的,可能長期無症狀,有些病例以視力下降為契機首次被發現2)。
評估進展程度廣泛使用Foster分類(改良Tauber-Foster分類)。從I期慢性結膜炎開始,II期下穹窿縮短,III期瞼球沾黏和角膜血管侵入,IV期眼表面角化,逐步進展2)。
| 病期 | 主要所見 |
|---|---|
| I期 | 慢性結膜炎、Rose bengal陽性(黏蛋白障礙)、結膜上皮下纖維化 |
| II期 | 下穹窿縮短(A~D:以25%為單位評估進展程度) |
| III期 | 瞼球沾黏、角膜血管侵入、睫毛亂生、淚液分泌減少 |
| IV期 | 眼表面角化、眼瞼沾黏、重度乾燥、角膜皮膚樣變化 |
早期,在眼瞼結膜上觀察到線狀或斑狀的白色腱樣組織疤痕。隨著病程進展,出現結膜穹窿縮短、Vogt角膜輪部柵欄(POV)消失、角膜內結膜上皮侵入、淚管阻塞、結膜杯狀細胞消失、瞼板腺消失導致的嚴重乾眼。急性惡化時可能發生廣泛的持續性上皮缺損。
組織學上可見結膜間質纖維化、杯狀細胞完全消失和鱗狀上皮化生1)。杯狀細胞的消失意味著結膜黏蛋白分泌功能喪失,淚膜穩定性顯著受損。此外,瞼板腺破壞導致脂質層也喪失,淚液蒸發加劇,形成嚴重的蒸發過強型乾眼。
作為全身黏膜併發症,需要評估引起剝脫性牙齦炎和水疱性病變的口腔病變、引起吞嚥困難的食道病變、以及引起聲音沙啞和呼吸困難的喉頭/氣管病變。喉頭狹窄是需要氣道管理的生命預後決定因素,對於有呼吸道症狀的患者,需要與耳鼻喉科緊急協作2)。食道狹窄導致吞嚥困難和營養不良,需由腸胃科進行內視鏡評估並根據需要考慮氣球擴張術。皮膚病變常表現為紅斑或萎縮性變化而非水疱,尤其好發於頭部、臉部和頸部。
眼黏膜類天疱瘡由自體免疫機轉引起(詳見第6節)。發病風險因素包括高齡、女性和其他自體免疫疾病史。尚未確定明確的誘因,但感染和藥物暴露可能參與免疫耐受的破壞。國外研究報告了與HLA-DQB1*0301的關聯,提示遺傳易感性的作用。
臨床上,需要與表現為疤痕性結膜炎的其他疾病進行鑑別。以下列出的疾病病理和治療均不同,因此初診時需要縮小病因範圍。
需鑑別的自體免疫/發炎性疾病
需鑑別的外源性疾病
雙眼角膜結膜上皮慢性炎症緩慢進展為瘢痕化,強烈提示OCP。尤其是老年女性出現倒睫或眼瞼內翻時,應仔細評估結膜囊縮短和瞼球黏連的情況。
問診時詳細詢問眼外傷、眼部感染史以及過去和現在的眼藥水、口服藥使用史。此外,對口腔、鼻咽、喉、食道、皮膚的黏膜病變進行全身性回顧,必要時與皮膚科、耳鼻喉科、腸胃科、風濕科協作 2)。
確診的支柱是結膜活檢。從下方球結膜取標本,同時進行福馬林固定標本的組織病理學檢查和Michel液固定的直接免疫螢光法(DIF)5)。
OCP的DIF陽性結果是結膜上皮基底膜帶IgG、IgA、IgM、補體C3的線狀沉積 5)。但DIF假陰性並不少見。原因包括疾病靜止期、末期基底膜完全消失、取材部位不當、免疫反應的局部變異。臨床高度懷疑OCP時,即使DIF陰性也不能排除疾病,多次活檢(包括對側眼再活檢)可提高敏感性 4,5)。
| 疾病 | 鑑別關鍵 |
|---|---|
| 眼黏膜類天疱瘡(OCP) | 雙眼性、緩慢進展;DIF顯示基底膜帶線狀沉積;抗BP180/層黏連蛋白332抗體陽性 |
| 史蒂文斯-強森症候群 | 藥物反應引起的急性發作;有全身發燒、皮疹病史 |
| 藥物誘導的假性OCP | 長期使用抗青光眼眼藥水等上皮毒性藥物。停用致病藥物後改善 7) |
| 慢性GVHD | 有造血幹細胞移植史。但重度沾黏病例需注意與OCP合併存在 4) |
| 類肉瘤病 | 即使ACE/溶菌酶正常,仍需鑑別;免疫螢光陰性有助於排除OCP 3) |
DIF檢查的敏感性並非完美,有多種因素可導致偽陰性。主要原因包括:疾病的靜止期、基底膜在終末期完全消失的病例、檢體取自活動性低的區域,以及免疫沉積的局部分布不均。也有報告稱左右眼結果不同5)。當臨床發現強烈提示OCP時,透過對側眼或其他部位重複活檢等多次檢查可提高敏感性4)。檢測血清抗BP180抗體、抗層黏連蛋白332抗體也有助於診斷。
治療目標是阻止進行性瘢痕形成、預防和矯正角膜及眼瞼併發症,以及緩解症狀。本病是全身性自體免疫疾病,單用局部治療無法控制病情進展。治療核心是全身免疫抑制治療,強烈建議與皮膚科、風濕科協作2)。
根據病情活動和炎症程度逐步選擇藥物。所有方案均需監測副作用並定期進行血液檢查2,5)。
全身治療:階梯式選擇
局部治療和手術治療
症狀治療:低濃度類固醇眼藥水抗炎、無防腐劑人工淚液管理乾眼、拔除睫毛減輕角膜刺激。
眼瞼球黏連重建:炎症控制後進行黏連鬆解,羊膜移植或口腔黏膜移植重建2)。
合併青光眼:基本措施是改用無防腐劑眼藥水。也有微創青光眼手術(如XEN凝膠支架)的病例報告6)。
末期:用於角膜上皮重建的培養黏膜上皮移植,重度病例的角膜義體(Boston KPro type 2、OOKP)
許多藥物對該疾病不在健保給付範圍內,因此在開始治療前需向患者充分說明並考慮倫理問題。注意口服環孢素和環磷酰胺同樣不在該疾病的健保給付範圍內。氨苯砜可能誘發紅血球溶血和高鐵血紅蛋白血症,因此給藥前應檢測葡萄糖-6-磷酸脫氫酶(G6PD)活性以排除缺乏症。開始給藥後應定期評估血常規、肝功能和腎功能,並逐漸增加劑量。嗎替麥考酚酯耐受性相對較好,適合長期使用,但需考慮伺機性感染風險並進行感染篩查。環磷酰胺是用于重症病例的強效免疫抑制劑,但伴有骨髓抑制、出血性膀胱炎和長期致癌風險,因此需要管理總劑量。利妥昔單抗作為抗CD20單克隆抗體,被定位為難治性OCP的救援治療,給藥前評估B型肝炎病毒再活化風險非常重要2)。
局部治療作為全身治療的輔助對症治療非常重要。低濃度類固醇眼藥水可減輕眼表炎症,不含防腐劑的人工淚液可管理乾眼症。淚點栓塞術等手術介入可能加速疤痕形成,因此需謹慎判斷。
手術治療僅在炎症完全控制的情況下進行。活動性炎症下的手術會導致疤痕化、粘連和角化的快速進展2)。
在重症OCP等雙眼進行性疾病中,自體角膜緣幹細胞移植(CLAu、CLET、SLET)的適應症有限。由於許多病例為雙眼性且無健康供體眼,因此會考慮異體移植或培養黏膜上皮移植9)。自體角膜緣幹細胞移植的系統性回顧(主要針對單眼化學外傷等)分析了1,023隻眼,報告解剖成功率為69%,功能成功率為60%,但在OCP等雙眼自體免疫疾病中,它不太可能成為首選9)。
在活動性炎症狀態下進行手術是導致瞼球粘連和角膜角化迅速進展的重大危險因素。計劃手術時,應從手術當天開始聯合全身免疫抑制治療(如類固醇、環孢素、環磷酰胺等)以徹底抑制炎症,術中盡量減少眼表的物理損傷,術後繼續免疫抑制。如果術前消炎不充分就進行手術,術後粘連和角化迅速進展的風險很高。術式選擇、全身管理以及與皮膚科、風濕科的協作極為重要2)。
OCP是一種以產生針對半橋粒相關基底膜成分的自體抗體為特徵的II型(細胞毒型)自體免疫疾病5)。
當自體抗體與結膜上皮基底膜結合時,補體系統被激活,發炎細胞被募集。急性期以嗜酸性粒細胞和中性粒細胞為主,慢性期則以淋巴細胞浸潤為主5)。釋放的細胞因子和蛋白酶激活結膜上皮下的纖維母細胞,促進膠原等細胞外基質的過度產生,導致結膜纖維化和疤痕形成。轉化生長因子-β(TGF-β)、介白素-4(IL-4)、IL-5、IL-13等Th2型細胞因子在病變部位表現上調,被認為是纖維化的主要驅動因素。基質金屬蛋白酶-9(MMP-9)與組織抑制劑(TIMP)之間的平衡被打破,導致結膜組織重塑失控,這也是該病理的特徵之一。
結膜疤痕化的階段性進展對應於Foster分類。持續的慢性發炎導致結膜下纖維化(I期)、結膜穹窿縮短(II期)、眼瞼球粘連(III期),最終角膜緣的Vogt柵欄(POV)消失8)。由於角膜上皮幹細胞存在於POV中,POV的消失意味著角膜上皮正常再生的失敗。角膜上皮幹細胞耗竭導致結膜上皮侵入角膜表面(結膜化),進而出現角膜混濁、血管化,最終出現皮膚樣角化(IV期)8)。
造血幹細胞移植後的慢性眼移植物抗宿主病(oGVHD)通常表現為眼表慢性發炎、乾眼和輕度結膜纖維化,但當出現嚴重且快速進展的疤痕化和眼瞼球粘連時,應考慮合併OCP的可能性4)。儘管oGVHD和OCP的臨床表現相似,但治療策略不同,因此通過結膜活檢和DIF進行鑑別非常重要4)。
角膜緣存在負責角膜上皮再生的幹細胞,可觀察到Vogt柵欄(POV)。在OCP中,慢性發炎和疤痕化累及角膜緣,導致POV和幹細胞喪失。幹細胞耗竭後,結膜上皮侵入角膜表面(結膜化),正常的角膜上皮再生變得不可能。結果導致角膜混濁、血管化和角化,造成嚴重的視力障礙8)。這種情況是眼黏膜類天皰瘡、Stevens-Johnson症候群和化學傷後常見的嚴重眼表疾病的最終表現。
病例系列研究顯示,利妥昔單抗和IVIG對難治性OCP有效,並正成為對傳統免疫抑制治療耐藥病例的治療選擇2)。利妥昔單抗給藥可清除自體抗體產生B細胞,已有獲得臨床緩解的病例報告。IVIG兼具抗炎和免疫調節作用,被定位為重症或耐藥病例的聯合治療。JAK抑制劑等新型免疫調節藥物的可能性也在討論中,其作為口服藥物便於門診管理,未來臨床應用的期待很高。
在角膜上皮重建領域,培養角膜上皮片移植和自體口腔黏膜上皮片移植已進入臨床應用,作為先進醫療技術正在不斷完善。自體角膜上皮片使用健康眼的角膜上皮細胞製備,但在雙眼受累的OCP中無法使用,因此選擇使用眼庫提供的角膜製備的異體角膜上皮片,或使用患者自身口腔黏膜細胞製備的自體口腔黏膜上皮片。自體口腔黏膜無排斥反應風險,可期待長期眼表面穩定化。作為載體材料,羊膜、纖維蛋白膠、溫度響應性培養皿、聚偏氟乙烯(PVDF)膜等已被開發,手術方式的選擇範圍正在擴大8)。
對於合併青光眼的病例,由於結膜瘢痕化導致傳統濾過手術困難,已有使用XEN凝膠支架進行微創青光眼手術(MIGS)的成功病例報告。在控制眼表面炎症後,通過ab interno法植入支架,術後1年無需使用滴眼液即可控制眼壓並實現炎症消退的病例已被展示,作為重度眼表面疾病合併青光眼的新方法備受關注6)。未來期待通過多中心聯合研究積累長期結果,以及利用生物標誌物評估治療反應性。