粘膜類天疱瘡(MMP)全体像
標的臓器:口腔・眼表面・鼻咽頭・喉頭・食道・生殖器など全身の重層扁平上皮を持つ粘膜
皮膚病変:伴わないことが多い。水疱よりもびらん・瘢痕が前面に出る
好発年齢:60〜80歳代。女性優位
全身合併症:食道狭窄による嚥下障害、喉頭狭窄は生命予後を左右する2)

眼粘膜類天疱瘡(ocular mucous membrane pemphigoid、以下OCP)は、結膜を含む粘膜上皮基底膜の接着成分に対する自己抗体により、慢性・進行性の瘢痕化が生じる自己免疫性水疱性疾患である。粘膜類天疱瘡(mucous membrane pemphigoid、MMP)は口腔、眼表面、鼻咽頭、喉頭、食道、外陰部など複数の粘膜を侵す全身疾患群であり、眼病変を有する一群を眼類天疱瘡、または眼瘢痕性類天疱瘡(ocular cicatricial pemphigoid)とよぶ。皮膚病変を伴わない症例も珍しくない。
眼科領域では、OCPは角膜上皮幹細胞疲弊を伴う瘢痕性角結膜上皮症の代表的疾患として位置づけられ、慢性結膜炎から瞼球癒着、さらに角膜の角化に至る段階的な病期進行をたどる。
本疾患は稀少疾患である。英国の監視調査では瘢痕性結膜炎の年間罹患率は100万人あたり約1.3人と報告され、OCPの有病率はおおむね1万〜5万人に1人と見積もられている5)。60〜80歳代の高齢者に好発し、男女比は約1:2と女性に多い5)。粘膜病変の頻度は口腔が最も多く約85%、眼が約65%とされ、OCP患者の約50%で口腔や皮膚など眼外病変を合併する2)。
両眼性の慢性結膜炎として潜行性に発症し、病悩期間は数年から十数年に及ぶことも珍しくない。発症初期には非特異的な結膜炎症状のみのため、アレルギー性結膜炎、慢性結膜炎、ドライアイとして長期間治療されるケースも多い。本疾患を念頭に置いた丁寧な問診と細隙灯顕微鏡所見の評価が、早期診断と視機能予後の改善にとって極めて重要である。
粘膜類天疱瘡(MMP)全体像
標的臓器:口腔・眼表面・鼻咽頭・喉頭・食道・生殖器など全身の重層扁平上皮を持つ粘膜
皮膚病変:伴わないことが多い。水疱よりもびらん・瘢痕が前面に出る
好発年齢:60〜80歳代。女性優位
全身合併症:食道狭窄による嚥下障害、喉頭狭窄は生命予後を左右する2)
眼粘膜類天疱瘡(OCP)特徴
粘膜類天疱瘡(MMP)は口腔・眼・鼻咽頭・喉頭・食道・外陰部など複数の粘膜を侵す自己免疫性水疱性疾患の総称である。このうち眼病変を有するものを眼類天疱瘡(眼瘢痕性類天疱瘡、OCP)とよぶ。OCPは眼病変のみの場合と、口腔や皮膚など眼外病変を合併する場合があり、約50%の症例で眼外病変を伴う2)。皮膚病変が目立たないことも珍しくないため、眼科医が最初に診断にたどり着くケースも多い。
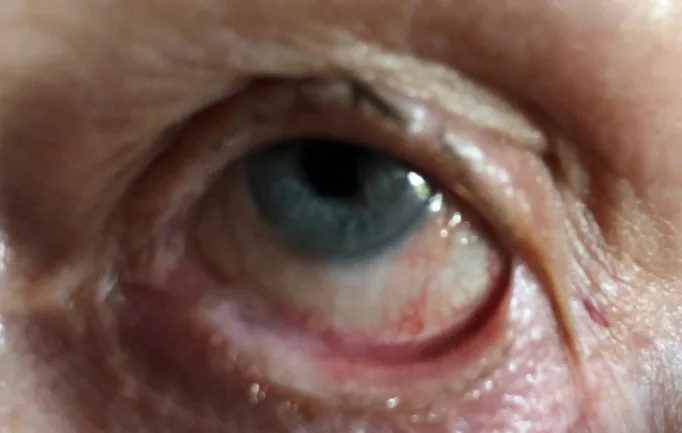
初期には慢性の結膜充血、乾燥感、異物感、灼熱感、流涙が主訴となる。これらは通常のドライアイ治療に抵抗性を示し、長期化することで本疾患を疑う契機となる1)。進行例では瞼球癒着による眼球運動障害や開瞼不全、睫毛乱生による角膜刺激症状、さらに角膜混濁や結膜上皮侵入による視力低下が加わる。
本疾患の進行は潜行性であり、長期間無症状のまま経過し、視力低下をきっかけに初めて発見される例もある2)。
進行度の評価にはFoster分類(修正Tauber-Foster分類)が広く用いられる。I期の慢性結膜炎から始まり、II期で下穹窿部の短縮、III期で瞼球癒着と角膜血管侵入、IV期で眼表面の角化へと段階的に進む2)。
| 病期 | 主要所見 |
|---|---|
| I期 | 慢性結膜炎、Rose bengal陽性(ムチン障害)、結膜上皮下線維化 |
| II期 | 下穹窿部短縮(A〜D:25%刻みで進行度を評価) |
| III期 | 瞼球癒着、角膜への血管侵入、睫毛乱生、涙液分泌減少 |
| IV期 | 眼表面の角化、眼瞼癒着、重度乾燥、角膜の皮膚様変化 |
初期には瞼結膜に線状・斑状の白色腱様組織として瘢痕が観察される。病期が進むと結膜囊の短縮、Vogtの角膜輪部柵(palisades of Vogt、POV)の消失、角膜内への結膜上皮侵入、涙導管閉塞、結膜杯細胞消失、マイボーム腺消失による重度のドライアイが出現する。急性増悪時には広範な遷延性上皮欠損を生じうる。
組織学的には結膜間質の線維化、杯細胞の完全消失、扁平上皮化生を認める1)。杯細胞の消失は結膜のムチン分泌機能の喪失を意味し、涙液層の安定性が著しく損なわれる。また、マイボーム腺の破壊により脂質層も失われ、涙液の蒸発が亢進して重度の蒸発亢進型ドライアイが完成する。
全身の粘膜合併症として、剥離性歯肉炎や水疱性病変を生じる口腔病変、嚥下困難をきたす食道病変、嗄声や呼吸困難を生じる喉頭・気管病変を評価する必要がある。喉頭狭窄は気道確保を要する生命予後規定因子であり、呼吸器症状を訴える患者では耳鼻咽喉科との緊急連携が求められる2)。食道狭窄は嚥下困難と栄養不良の原因となり、消化器内科による内視鏡評価と必要に応じたバルーン拡張術が検討される。皮膚病変は水疱よりも瘢痕性紅斑や萎縮性変化として現れることが多く、特に頭部・顔面・頸部に好発する傾向がある。
眼粘膜類天疱瘡は自己免疫機序によって発症する(病態の詳細はセクション6)。発症のリスク因子として、加齢、女性、他の自己免疫疾患の既往が挙げられる。明確な発症誘因は同定されていないが、感染症や薬剤曝露が免疫寛容の破綻に関与する可能性が議論されている。HLA-DQB1*0301との関連が海外研究で報告されており、遺伝的素因の寄与が示唆されている。
臨床では、瘢痕性結膜炎を呈する他疾患との鑑別が重要である。以下に列挙する疾患は病態も治療も異なるため、初診時に原因を絞り込む必要がある。
鑑別すべき自己免疫・炎症性疾患
スティーブンス・ジョンソン症候群/中毒性表皮壊死症:薬剤反応に伴う急性粘膜皮膚障害。発熱・全身皮疹の既往で鑑別
移植片対宿主病(GVHD):造血幹細胞移植後に発症。重度・進行性の癒着形成例ではOCPの合併を考慮4)
サルコイドーシス:非乾酪性肉芽腫形成性の結膜炎で瘢痕化しうる。OCPの模倣疾患として報告がある3)
扁平苔癬・線状IgA水疱性皮膚症:皮膚科的評価を要する
鑑別すべき外因性疾患
両眼性に角結膜上皮の慢性炎症が緩徐に瘢痕化として進行する所見はOCPの強い示唆となる。とくに高齢者、なかでも女性で睫毛乱生や内反症を認める場合には、結膜囊の短縮や瞼球癒着の有無を注意深く評価する。
問診では眼外傷、眼感染症、過去および現在の点眼薬・内服薬の使用歴を詳細に聴取する。加えて、口腔・鼻咽頭・喉頭・食道・皮膚の粘膜病変について全身のレビューを行い、必要に応じて皮膚科・耳鼻咽喉科・消化器内科・リウマチ科との連携を図る2)。
確定診断の柱は結膜生検である。下方球結膜から検体を採取し、ホルマリン固定標本による組織病理学的検査と、ミシェル液固定による直接免疫蛍光法(direct immunofluorescence、DIF)を同時に施行する5)。
OCPのDIF陽性所見は、結膜上皮基底膜帯へのIgG、IgA、IgM、補体C3の線状沈着である5)。ただしDIFには偽陰性が少なくない。疾患の静止期、終末期における基底膜の完全消失、検体採取部位の不適切さ、免疫反応の局所的ばらつきが原因となる。臨床的にOCPが強く疑われる症例ではDIFが陰性であっても疾患を除外せず、対側眼からの再生検を含む複数回の生検で感度向上が期待できる4,5)。
| 疾患 | 鑑別の鍵 |
|---|---|
| 眼粘膜類天疱瘡(OCP) | 両眼性・緩徐進行、DIFで基底膜帯線状沈着、抗BP180/ラミニン332抗体陽性 |
| スティーブンス・ジョンソン症候群 | 薬剤反応による急性発症、全身発熱・発疹の既往 |
| 薬剤誘発性偽OCP | 抗緑内障点眼薬など上皮毒性薬剤の長期使用歴。原因薬剤中止で改善7) |
| 慢性GVHD | 造血幹細胞移植歴。ただし重度癒着例ではOCPとの合併に注意4) |
| サルコイドーシス | ACE・リゾチーム正常でも鑑別に残り、免疫蛍光陰性がOCP除外に有用3) |
DIF検査は感度が完全ではなく、偽陰性を生じる要因が複数ある。疾患の静止期、基底膜が終末期にかけて完全に消失してしまった症例、検体採取部位が活動性の低い領域であった場合、そして免疫沈着の局所的な分布のばらつきなどが主な原因である。左右眼で結果が異なる例も報告されている5)。臨床所見がOCPを強く示唆する場合には、対側眼や別部位からの再生検を含めた複数回の検査で感度が向上する4)。血清抗BP180抗体、抗ラミニン332抗体の検出も診断補助として有用である。
治療目標は進行性瘢痕化の停止、角膜・眼瞼合併症の予防と矯正、および症状緩和である。本疾患は全身性の自己免疫疾患であり、局所療法単独では進行を制御できない。治療の主軸は全身免疫抑制療法であり、皮膚科・リウマチ科との連携が強く推奨される2)。
病勢や炎症活動性に応じて薬剤を段階的に選択する。いずれも副作用モニタリングと定期的な血液検査が不可欠である2,5)。
全身療法:段階的選択
軽度〜中等度:ダプソン(ジアミノジフェニルスルホン)50〜200mg/日が第一選択。G6PD欠損症の除外と貧血・メトヘモグロビン血症のモニタリングが必須5)
ダプソン無効・中等度:ミコフェノール酸モフェチル1〜3g/日、アザチオプリン1〜2mg/kg/日、メトトレキサート7.5〜25mg/週へのステップアップ2)
重度・急性増悪:シクロホスファミド1〜2mg/kg/日とプレドニゾロン短期大量療法の併用5)
難治例:リツキシマブ(抗CD20モノクローナル抗体)、免疫グロブリン静注療法(IVIG)2)
局所療法と外科的治療
対症療法:低濃度ステロイド点眼で消炎、防腐剤無添加人工涙液でドライアイ管理、睫毛抜去で角膜刺激を軽減
瞼球癒着の再建:炎症鎮静後に癒着解除、羊膜移植または口腔粘膜移植で再建2)
緑内障合併例:防腐剤フリー点眼への変更が基本。低侵襲緑内障手術(XENゲルステント等)の症例報告もある6)
終末期:角膜上皮再建目的の培養粘膜上皮移植、重度例に対する角膜プロテーゼ(Boston KPro type 2、OOKP)
薬剤の多くは本疾患に対して保険適用外であり、導入前に患者への十分な説明と倫理的配慮が求められる。シクロスポリンやシクロホスファミドの内服も同様に本疾患に対する効能・効果としては保険適用外であることに注意する。ダプソンは赤血球の溶血とメトヘモグロビン血症を誘発しうるため、投与前にグルコース-6-リン酸脱水素酵素(G6PD)活性を測定し、欠損症を除外する。投与開始後は定期的な血算・肝機能・腎機能評価を行い、投与量を漸増する。ミコフェノール酸モフェチルは比較的忍容性が高く長期使用に向くが、日和見感染症のリスクを考慮して感染症スクリーニングを行う。シクロホスファミドは重症例に対する強力な免疫抑制薬であるが、骨髄抑制、出血性膀胱炎、長期的には発癌リスクを伴うため、総投与量を管理する必要がある。リツキシマブは抗CD20モノクローナル抗体として難治性OCPに対する救済療法に位置づけられ、投与前のB型肝炎ウイルス再活性化リスク評価が重要である2)。
局所治療は全身療法に付随する対症療法として重要である。低濃度ステロイド点眼により眼表面の炎症を和らげ、防腐剤無添加の人工涙液でドライアイを管理する。涙点閉鎖術などの手術的介入は瘢痕化を加速させるおそれがあるため慎重に判断する。
外科的治療は炎症が完全にコントロールされた状態でのみ施行する。活動性炎症下での手術は瘢痕化・癒着・角化の急激な進行を招く2)。
重症OCPのような両眼性の進行性疾患では、自家輪部幹細胞移植(CLAu、CLET、SLET)の適応は限定的である。両眼性で健常な提供眼を持たない症例が多く、他家移植や培養粘膜上皮移植が検討される9)。自家輪部幹細胞移植の系統的レビューでは片眼性の化学外傷等を主な適応として1,023眼の解析で解剖学的成功率69%、機能的成功率60%と報告されているが、OCPのような両眼性自己免疫疾患では第一選択とはなりにくい9)。
OCPはヘミデスモソーム関連基底膜成分に対する自己抗体の産生を特徴とするII型(細胞傷害型)自己免疫疾患である5)。
自己抗体が結膜上皮基底膜に結合すると、補体系が活性化されて炎症細胞が動員される。急性期には好酸球と好中球が炎症の主体となり、慢性期にはリンパ球浸潤が優位となる5)。放出されたサイトカインとプロテアーゼが結膜上皮下の線維芽細胞を活性化し、コラーゲンなどの細胞外マトリックスの過剰産生を促すことで結膜の線維化と瘢痕化が進行する。トランスフォーミング増殖因子β(TGF-β)、インターロイキン-4(IL-4)、IL-5、IL-13などのTh2系サイトカインが病変部で発現亢進しており、線維化の主要なドライバーとされる。マトリックスメタロプロテアーゼ(MMP-9)と組織インヒビター(TIMP)のバランスが崩れ、結膜組織のリモデリングが制御不能に進む点も病態の特徴である。
結膜瘢痕化の段階的進行はFoster分類に対応する。慢性炎症が持続すると結膜下線維化(I期)、結膜囊短縮(II期)、瞼球癒着(III期)と進み、最終的には角膜輪部のPalisades of Vogt(POV)が消失する8)。POVには角膜上皮幹細胞が存在するため、POV消失は角膜上皮の正常再生の破綻を意味する。角膜上皮幹細胞が枯渇すると結膜上皮が角膜表面に侵入する「結膜化」が生じ、角膜混濁、血管侵入、そして最終的には皮膚様の角化(IV期)へと至る8)。
造血幹細胞移植後の慢性眼GVHD(oGVHD)は、眼表面の慢性炎症とドライアイ、軽度の結膜線維化を呈することが一般的であるが、重度かつ急速進行性の瘢痕化・瞼球癒着をきたす場合にはOCPの合併を考慮する必要がある4)。oGVHDとOCPは臨床像が類似するが、治療戦略が異なるため、結膜生検とDIFによる鑑別が重要である4)。
角膜輪部には角膜上皮の再生を担う幹細胞が存在し、Vogtの角膜輪部柵(POV)として観察できる。OCPでは慢性炎症と瘢痕化が輪部に及び、POVと幹細胞が失われる。幹細胞が枯渇すると結膜上皮が角膜表面に進入する「結膜化」が起こり、正常な角膜上皮の再生が不可能となる。結果として角膜混濁、血管侵入、角化が生じ、高度の視力障害に至る8)。この状態は眼粘膜類天疱瘡、スティーブンス・ジョンソン症候群、化学外傷後に共通してみられる重症眼表面疾患の最終像である。
難治性OCPに対するリツキシマブやIVIGの有効性が症例集積で示されており、従来免疫抑制療法に抵抗性を示す症例に対する治療選択肢として確立されつつある2)。リツキシマブ投与により自己抗体産生B細胞が除去され、臨床的寛解が得られる症例が報告されている。IVIGは抗炎症作用と免疫調節作用を併せ持ち、重症例や他剤抵抗例の併用療法として位置づけられる。JAK阻害薬など新しい免疫調節薬の可能性も議論されており、経口剤として外来管理しやすい点で今後の臨床応用が期待される。
角膜上皮再建の領域では、培養角膜上皮シート移植、自家口腔粘膜上皮シート移植が臨床応用されており、先進医療としての整備が進んでいる。自家角膜上皮シートは健側眼の角膜上皮細胞を用いて作製するが、両眼罹患のOCPでは使用できないため、アイバンクから提供された角膜を用いる他家角膜上皮シートや、患者自身の口腔粘膜細胞から作製する自家口腔粘膜上皮シートが選択される。自家口腔粘膜は拒絶反応のリスクがなく長期の眼表面安定化が期待できる。キャリア材料としての羊膜、フィブリン糊、温度応答性培養皿、ポリフッ化ビニリデン(PVDF)膜などが開発され、術式の選択肢は広がっている8)。
緑内障合併例に対しては、結膜の瘢痕化により従来型濾過手術が困難なため、XENゲルステントによる低侵襲緑内障手術(MIGS)の成功例が報告されている。眼表面の炎症をコントロールしたうえでab interno法により挿入し、術後1年で点眼薬なしでの眼圧管理と炎症鎮静を達成した症例が示されており、重度眼表面疾患合併緑内障への新しいアプローチとして注目される6)。今後は多施設共同研究による長期成績の蓄積と、バイオマーカーを用いた治療反応性の評価が期待される領域である。