Salzmann结节状角膜变性(SND)是一种非炎症性角膜 变性,在Bowman膜上形成青灰色上皮下结节1) 。
患病率约为每2,420人中有1人,发病年龄呈双峰分布,高峰在50多岁和80多岁1) 。
女性多见(72-88%),双侧受累占58-80%1) 。
常继发于慢性眼表疾病,如慢性睑缘炎、睑板腺功能障碍 和干眼症 ,背景包括角膜疱疹 、春季角结膜炎 、沙眼 、麻疹后等炎症性眼表疾病。
早期常无症状,但当结节累及角膜 中央时,会导致不规则散光 和视力 下降。
治疗从保守治疗(人工泪液、眼睑卫生、低浓度类固醇 )到手术治疗(结节切除、浅层角膜 切除术、PTK 、角膜上皮 清创术)逐步进行1) 4) 。
Salzmann结节状角膜变性(SND)是一种进行性、非炎症性角膜 变性疾病,特征是在Bowman层 上的上皮下区域形成灰白色至蓝灰色结节1) 9) 。1925年由奥地利眼科医生Maximilian Salzmann首次报道,此后被归类为“Salzmann结节变性”1) 。结节由透明样物质和纤维组织构成,随着进展可累及角膜 中央,引起不规则散光 和视力 障碍1) 10) 。
患病率估计约为每2,420人中有1人,是一种罕见疾病1) 。发病年龄呈双峰分布,高峰在50多岁和80多岁1) 。Farjo等人的回顾性研究(93例)显示,男性平均发病年龄约为69岁,女性约为52岁6) 。性别比例中女性占72-88%,双侧受累占58-80%,多数病例双眼均形成结节1) 。
结节好发于角膜 中周边部,常沿角膜缘 呈弧形排列1) 。可为单发或多发,进展病例中可见8个以上结节1) 。Maharana等人的全面综述指出,SND的发病率随年龄增长而增加,且相当数量的病例无症状而被忽视9) 。Paranjpe等人基于Bascom Palmer眼科研究所经验的管理策略综述也认为,SND虽被视为罕见病,但在白内障 术前筛查或角膜 屈光 手术术前评估中仍有一定频率遇到7) 。
许多SND是继发于慢性眼表疾病的获得性变性。经典已知的背景疾病如下。
这些慢性眼表炎症和机械刺激被认为会诱导Bowman层 和上皮基底膜的破坏,从而触发结节形成1) 。
Q
是否可能只发生在单眼?
A
双侧病例占报告的58%至67%,但单眼发病的病例也占30%至40%。当原发病为MGD 或干眼症 等双眼共有的疾病时,多为双眼性;而外伤或单侧LASIK 术后则倾向于单眼性。
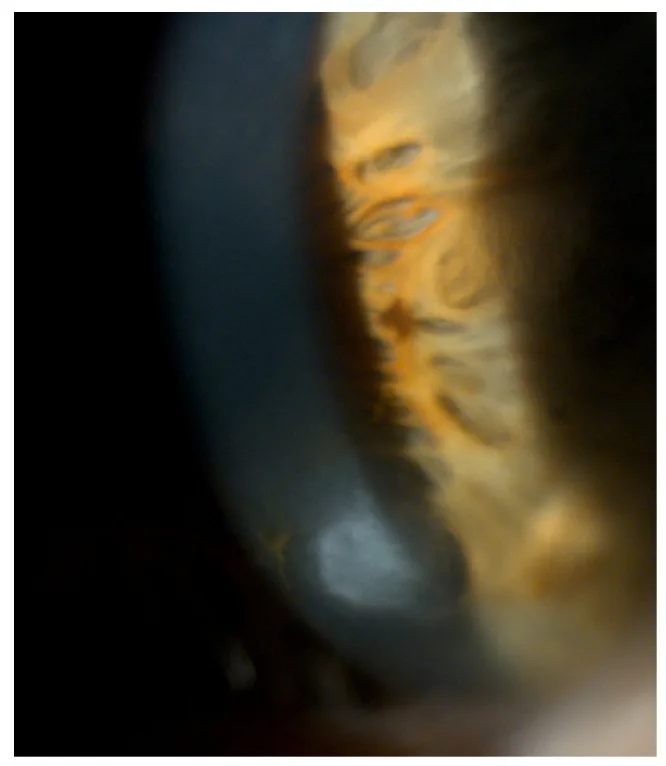
Salzmann结节变性的裂隙灯照片 Roszkowska AM, Azzaro C, Calderone A, et al. Salzmann Nodular Degeneration in Ocular and Systemic Diseases. Journal of Clinical Medicine. 2024 Aug 20; 13(4900):$2. Figure 1. PM
CI D: PMC11355337. License: CC BY.
裂隙灯 显示从
角膜 周边向前隆起的青白色结节。直观地展示了Salzmann结节的立体感和浅表性病变。
无症状 :当结节局限于周边部时,常无自觉症状1) 。不少病例在体检或白内障 术前检查中偶然发现1) 7) 。视力 下降角膜 中央或表面不平导致不规则散光 时,会引起视力 下降1) 。超高分辨率OCT 可测量结节上的上皮变薄和角膜 表面隆起11) 。异物感 :由于结节隆起和结节上的上皮变薄,眨眼时会出现异物感。眩光(glare)和畏光 :由角膜 表面不平引起的光散射所致1) 。流泪和复发性糜烂 :结节上的上皮不稳定,可能导致复发性角膜糜烂 和流泪1) 。
上皮下结节 :角膜上皮 下可见青灰色至灰白色的隆起性结节1) 。直径通常为1-3毫米,单发或多发1) 3) 。结节分布 :好发于角膜 中周边部,常沿角膜缘 呈弧形排列1) 。部分病例在下象限呈火焰状分布1) 。上皮变薄 :结节上的角膜上皮 变薄1) 10) 。角膜 表面不平角膜地形图 可检测到结节引起的表面隆起和结节间的平坦化1) 7) 。继发性改变 :由于继发性变性,常合并基础疾病引起的角膜 混浊、结膜 瘢痕、角膜 表层血管和角膜缘 异常。角膜缘干细胞 衰竭角膜缘 功能不全,结节可能形成于结膜 侵入的前端。广泛结膜 侵入时需要眼表面重建。
组织学上,特征为Bowman层 断裂和消失,以及其上沉积的透明样物质、纤维组织和胶原增生10) 。结节内部细胞成分少,由不规则排列的胶原纤维和基底膜样物质构成1) 10) 。
大多数SND继发于慢性眼表疾病或机械刺激,作为获得性变性发病。主要风险因素如下1) 7) 8) 。
慢性睑缘炎/睑板腺功能障碍 (MGD ) :最常见的相关眼表疾病1) 7) 。泪膜不稳定和慢性炎症促进Bowman层 变性。干眼症 1) 。长期佩戴隐形眼镜 :Hamada等人报告有隐形眼镜佩戴史的病例比例很高8) 。长期佩戴导致的慢性机械刺激和缺氧与之相关。泡性角结膜炎 1) 。翼状胬肉 Bowman层 破裂和基质成纤维细胞活化,已有共存病例报告2) 。春季角结膜炎 、沙眼 、麻疹后角膜 炎角膜 屈光 手术后IK 或PRK后发病已有报告;Roszkowska的综述中,5名21-48岁年轻女性在LASIK 后发生双侧SND1) 。倾向于发生在瓣缘。白内障 手术后角膜 切口愈合不全部位形成结节;透明角膜 切口位置与SND结节形成位置密切相关1) 。角膜 外伤2) 。
近年来,与全身疾病合并的报告不断积累1) 。多数为双眼性;当发现原因不明的双眼SND时,建议查找潜在的全身疾病。
结缔组织疾病/皮肤疾病
埃勒斯-丹洛斯综合征 :共享结缔组织脆弱性;有LASIK 术后双侧SND复发的报告1) 。
网状色素性皮肤病 :一种常染色体显性遗传 的皮肤色素异常症,伴有广泛角膜 结节1) 。
炎症性/综合征性/内分泌疾病
克罗恩病 :消化道慢性炎症,有病例报告SND复发与疾病活动相关1) 。
歌舞伎综合征 角膜 中周边部SND1) 。
卡塔格内综合征 :伴有纤毛运动障碍,有病例报告下方角膜 出现火焰状SND1) 。
甲状腺眼病 :有研究指出通过眼表慢性炎症相关联1) 。
部分家族性病例报告为常染色体显性遗传 模式,并且在SND患者中检测到TGFBI基因突变,该基因已知是角膜营养不良 的致病基因1) 。但大多数SND是获得性继发性变性,遗传不是主要原因。
Q
佩戴隐形眼镜是否相关?
A
长期佩戴隐形眼镜会引起慢性机械刺激和泪膜不稳定,并多次被报道为SND的危险因素。佩戴者,尤其是长时间佩戴者,建议定期进行眼科检查以评估角膜 表面。
SND的诊断主要基于裂隙灯显微镜检查 的临床诊断。影像学检查有助于评估病变的范围和深度,以及评估对白内障 手术等手术计划的影响1) 7) 。
检查方法 主要发现 意义 裂隙灯 显微镜上皮下蓝灰色结节,中周边部分布 确诊基础1) 2) 角膜地形图 表面不规则、不规则散光 、结节上方平坦化 对IOL度数计算 的影响评估1) 7) 眼前节OCT (AS-OCT ) 上皮下高反射沉积物 深度评估与手术方式选择1) 11) 活体共聚焦显微镜 (IVCM) 不规则纤维结构、角膜基质 细胞消失 病理状态评估1) 12)
裂隙灯显微镜检查 角膜 中央区,以及背景是否存在睑缘炎或MGD 1) 2) 。角膜地形图 (Placido盘式)散光 1) 。结节上方角膜 平坦化,结节间陡峭化,呈现特征性模式。角膜 形态变化会影响白内障 手术时的IOL度数计算 ,因此术前评估很重要1) 。眼前节OCT (AS-OCT ) :将结节显示为上皮下的高反射沉积物,可无创评估其与Bowman膜的关系及深度1) 11) 。超高分辨率OCT 可详细测量结节的内部结构和厚度11) 。术前通过AS-OCT 掌握结节和混浊的深度,有助于判断表层切除术、PTK 或更深层手术是否足够。活体共聚焦显微镜 (IVCM) :可在细胞水平观察结节内部微结构,特征性表现为不规则纤维结构、角膜基质 细胞消失以及上皮下神经丛密度降低1) 12) 。结节上方的上皮细胞呈现CK19阳性的短暂扩增细胞特性,提示上皮分化异常1) 12) 。
需要与表现为上皮下结节的其他疾病进行鉴别1) 2) 。
带状角膜变性 角膜缘 和病变之间留有透明带(limbal clear zone)。与SND的主要区别在于对EDTA螯合治疗有反应。球形角膜 变性(气候性滴状角膜 病变/球状变性)角膜 暴露部位多发黄色至琥珀色颗粒状沉积。已知与紫外线、干燥环境暴露有关。疱疹性角膜基质炎 :可表现为结节状炎性病变,但通过角膜 知觉减退、混浊、炎症表现和视力 下降的急性病程进行鉴别2) 。泡性角结膜炎 角膜缘 或周边角膜 形成伴有血管的圆形小结节,作为对结核或金黄色葡萄球菌的迟发型超敏反应而发病2) 。角膜上皮 内瘤变(OSSN )角膜缘 附近的上皮性肿块,特征为新生血管 和胶冻样隆起。细胞学检查或活检有助于鉴别。边缘性角膜溃疡 /卡他性溃疡 :与睑缘炎相关的周边角膜 浸润和溃疡,通过病变过程和炎症表现进行鉴别。中心周围肥厚性上皮下角膜 变性(PHS CD) :一种罕见的变性,表现为旁中心区上皮下混浊,不同之处在于混浊呈带状而非结节状。
Kuan等人的病例系列中,报告了3例表现为角膜 结节的病例,最终诊断分别为疱疹性角膜基质炎 、泡性角结膜炎 和SND2) 。角膜 结节的鉴别需结合详细病史(既往眼病、外伤、隐形眼镜佩戴史、屈光 手术史)、裂隙灯 检查(结节位置、颜色、有无血管、角膜 知觉)以及AS-OCT 深度评估2) 。发病时间过程也很重要:SND在数月至数年内缓慢进展,而感染性或炎性结节在相对较短时间内发病和进展2) 。
根据结节的位置、大小、症状严重程度以及对视功能的影响,逐步选择治疗方案1) 4) 7) 。无症状或局限于周边的SND通常只需观察1) 。
对于无症状或轻症病例,保守治疗是基础。由于控制潜在的慢性眼表疾病直接关系到预防复发,因此原发病的管理是首要任务1) 7) 。
人工泪液/透明质酸滴眼液 :频繁使用以稳定泪膜和保护角膜上皮 。首选不含防腐剂的制剂。眼睑卫生 :通过热敷和眼睑清洁来管理睑缘炎和睑板腺功能障碍 。低浓度类固醇 滴眼液 :用于控制慢性炎症。长期使用时需注意眼压 和白内障 。环孢素 滴眼液1) 。治疗性软性角膜 接触镜 :用于复发性糜烂或表面不规则引起的严重异物感,临时使用 1) 。泪点塞 :对合并严重干眼症 的病例有效 1) 。热敷和强脉冲光(IPL) :对于以睑板腺功能障碍 为背景的病例,IPL 已被报道作为辅助疗法 1) 。
如果保守治疗症状无改善,或结节累及瞳孔 区导致视力 下降,则考虑手术治疗。
根据结节的深度分层选择手术方式。AAO 的《角膜水肿 和混浊优选实践模式》也推荐了针对 SND 等上皮下纤维化的管理,包括上皮清创术(ED)、浅层角膜 切除术(SK)和 PTK 三个阶段 4) 。
结节切除 / 浅层角膜切除术
方法 :用镊子夹住结节,在 Bowman 膜水平钝性剥离并切除 1) 4) 。有时使用角膜 刀(如高尔夫刀)将异常上皮和结节一并剥离。
成功率 :仅行浅层角膜 切除术即可使约 90% 的病例获得视力 改善 1) 。术后角膜 变平可能导致散光 和屈光 度改变。
联合羊膜移植 :浅层角膜 切除术后辅助羊膜移植可促进伤口愈合和预防角膜 混浊,被认为有效 1) 。
治疗性准分子激光角膜切除术(PTK)
方法 :使用准分子激光均匀切除包括结节在内的表层组织 1) 4) 。适用于深层混浊或浅层切除后平滑化不足的病例。
优点 :可获得均匀平滑的角膜 表面,提高术后光学质量4) 。
联合MMC :联合使用丝裂霉素C(MMC)可抑制术后角膜 混浊(haze)1) 4) 。
术前评估 :通过眼前节OCT 了解结节和深层混浊的厚度,确定切除深度11) 。
在结节切除和PTK 中,对于Bowman层 下仍有混浊残留的病例,PTK 平滑化特别有效。手术方式的选择需通过眼前节OCT 掌握病变深度。
重症病例,即伴有广泛结节分布和角膜缘干细胞 缺乏并出现结膜 侵入的病例,需要切除异常结膜 上皮并进行眼表面重建。可选择角膜缘 移植或角膜上皮 成形术,术后需长期维持治疗,包括局部类固醇 滴眼液抑制排斥反应、治疗性隐形眼镜佩戴、抗炎治疗、免疫抑制和表层上皮保护。进一步进展至深层实质混浊的病例,可能需要板层角膜移植 (DALK )或穿透性角膜移植 (PKP ),但频率不高1) 。
手术治疗后的复发是SND治疗的重要课题。Farjo等人对93例病例的回顾性研究显示,平均随访61个月,约22%出现复发6) 。韩国的Yoon和Park也在Jpn J Ophthalmol上报告了双眼复发性SND病例,表明双侧病例和合并全身疾病的病例复发倾向较高5) 。
预防复发的关键在于对背景慢性眼表面疾病的持续管理1) 5) 7) 。控制睑缘炎、MGD 、干眼症 ,平息炎症性疾病,纠正隐形眼镜佩戴,管理全身疾病活动性等,被认为有助于降低术后复发率。Paranjpe等人在管理策略综述中指出,结节位置越深,切除越困难,复发风险越高,此时采用表层切除联合PTK 以确保角膜 表面平滑,并联合MMC抑制混浊和纤维化复发的多步骤方法是有用的7) 。Maharana等人的综述也强调,术后持续保守治疗(人工泪液、类固醇 、眼睑卫生)对于抑制复发至关重要9) 。
对于SND患者,应根据结节周围上皮不稳定的情况提供生活指导。建议避免用力揉眼、长时间佩戴隐形眼镜以及暴露于灰尘或干燥环境。即使症状轻微,也应继续使用抗炎滴眼液和人工泪液,并定期进行裂隙灯显微镜检查 和角膜地形图检查 以监测病情。当计划进行白内障 手术时,由于结节会影响手术计划,建议先治疗SND以稳定角膜 形态,然后再计算IOL 度数1) 7) 。
Q
手术后是否会复发?
A
手术治疗后的复发是一个重要问题,平均约5年的随访中,约22%的病例报告复发。双侧病例和有全身性疾病背景的病例复发倾向更高。耐心管理背景眼表疾病如睑缘炎、MGD 和干眼症 对于预防复发最为重要。
SND的病理被理解为始于Bowman层 和上皮基底膜破裂的一系列纤维化过程1) 10) 。
Bowman层 破裂Bowman层 和上皮基底膜出现微小撕裂1) 10) 。角膜基质 细胞迁移角膜基质 细胞通过破裂区域迁移到上皮下区域1) 。分化为肌成纤维细胞 :迁移的角膜 细胞分化为肌成纤维细胞1) 10) 。纤维性细胞外基质沉积 :肌成纤维细胞产生并沉积以透明化胶原为主的纤维性ECM,形成结节1) 10) 。
只要背景慢性眼表炎症或机械刺激持续存在,这一过程就会重复,导致结节数量和大小增加。
SND的结节形成被认为与基质金属蛋白酶-2(MMP-2)、血小板衍生生长因子(PDGF)和转化生长因子β1(TGF-β1)这三种因子密切相关1) 。
MMP-2 :降解上皮基底膜的主要成分IV型胶原,促进PDGF和TGF-β1向基质内迁移1) 。PDGF :促进角膜基质 细胞的迁移和增殖1) 。TGF-β1 :诱导角膜基质 细胞向肌成纤维细胞分化,增强纤维性ECM的产生1) 。上皮来源的酶 :结节上皮表现出高增殖活性,高表达α-烯醇化酶等酶类1) 。
结节上的角膜上皮 中可见CK19阳性的短暂扩增细胞,而完全分化上皮细胞的标志物CK3/12和干细胞标志物ABCG2的表达降低1) 12) 。也就是说,结节上的上皮处于既非干细胞也非完全分化细胞的中间状态,提示上皮自身的分化异常可能参与结节形成1) 12) 。
组织学上,结节内部细胞成分稀少,由不规则排列的胶原纤维、透明样物质和基底膜样物质构成10) 。Bowman层 部分消失,其上沉积的纤维组织将上皮抬起,形成隆起的结节。
当SND的背景存在慢性睑缘炎、MGD 或干眼时,泪膜不稳定和炎症细胞因子的持续存在形成恶性循环,促进结节形成。如果原发疾病不消除,Bowman层 的破坏和肌成纤维细胞的激活可能反复发生。因此,仅切除结节而原发疾病持续存在时容易复发。治疗策略上,必须同时进行保守治疗控制原发疾病和手术切除结节1) 7) 9) 。
结节上上皮细胞处于中间分化状态的发现支持这样一种观点:SND不仅仅是基质纤维化,而是上皮、Bowman层 和基质三者稳态破坏的结果1) 12) 。正常角膜 中,来自角膜缘 的上皮干细胞来源的细胞规则地分化和向中央迁移,但在SND结节上,这一分化过程被认为部分停滞,导致短暂扩增细胞局部积聚。这种上皮变化可能为促进下方Bowman层 破坏和基质纤维化提供了基础。
在一些家族性SND病例中,已报道常染色体显性遗传 模式,并且在部分SND患者中检测到已知导致角膜营养不良 的TGFBI基因突变1) 。随着基因组分析的进展,SND的遗传易感性与发病机制之间的关系有望进一步阐明。
近年来,已报道SND与多种全身疾病相关,如埃勒斯-丹洛斯综合征、克罗恩病、歌舞伎综合征 、卡塔格纳综合征、网状色素性皮肤病和甲状腺眼病1) 。这些关联可能基于共同的炎症通路或结缔组织脆弱性,提供了将SND重新视为“全身炎症状态在眼表面的表现”而非“眼局部变性”的视角。
圆锥角膜 与SND并发的病例报告正在积累3) 。圆锥角膜 和SND均涉及Bowman层 破裂和角膜基质 细胞活化,有研究指出它们可能具有共同的危险因素,如眼表炎症和机械刺激(揉眼、佩戴隐形眼镜)3) 。对于年轻患者出现双侧SND时,建议使用Pentacam或前段OCT 积极评估是否合并圆锥角膜 。
使用超高分辨率前段OCT 和谱域OCT 对结节深度和内部结构进行定量评估正在进展中11) ,提高了手术方式选择的精确性。通过客观测量结节厚度、边界和背景基质的状况,正在建立判断标准,以确定单纯表层切除术是否足够、是否需要PTK 或联合MMC。此外,使用IVCM对上皮分化异常和神经丛变化进行定量评估,可能应用于病理的早期检测和治疗效果评估12) 。未来,结合全身疾病和炎症生物标志物 的测量,有望实现SND的风险分层和个体化治疗。
Q
是否存在遗传因素?
A
在一些家族中已报道常染色体显性遗传 模式,并且在部分SND患者中检测到TGFBI基因突变。然而,大多数SND是继发于慢性眼表疾病的获得性变性,遗传因素罕见。仅在早发或强烈家族史的情况下才考虑遗传背景检查。
Roszkowska AM, Azzaro C, Calderone A, Spinella R, Schiano-Lomoriello D, Mencucci R, Wylegala A. Salzmann Nodular Degeneration in Ocular and Systemic Diseases. J Clin Med. 2024;13(16):4900. doi:10.3390/jcm13164900
Kuan HC, Cheng EYI, Yong MH, Wan Abdul Halim WH, Othman O. Corneal Nodules and Possible Pathologies: A Case Series. Cureus. 2021;13(12):e20822. doi:10.7759/cureus.20822
Das D, Lomi N, Sasi A, Kumari N, Muraleekrishna M, Tandon R. Layers of Rarity: An Unusual Concurrence of Keratoconus, Salzmann’s Nodular Degeneration, Ptosis, and Congenital Retinal Macrovessel. Cureus. 2025;17(9):e92115. doi:10.7759/cureus.92115
American Academy of Ophthalmology Cornea/External Disease Panel. Corneal Edema and Opacification Preferred Practice Pattern. Ophthalmology. 2024.
Yoon KC, Park YG. Recurrent Salzmann’s nodular degeneration. Jpn J Ophthalmol. 2003;47(4):401-404. doi:10.1016/S0021-5155(03)00044-3.
Farjo AA, Halperin GI, Syed N, Sutphin JE, Wagoner MD. Salzmann’s nodular corneal degeneration clinical characteristics and surgical outcomes. Cornea. 2006;25(1):11-15. doi:10.1097/01.ico.0000167879.88815.6b
Paranjpe V, Galor A, Monsalve P, Dubovy SR, Karp CL. Salzmann nodular degeneration: prevalence, impact, and management strategies. Clin Ophthalmol. 2019;13:1305-1314. doi:10.2147/OPTH.S166280
Hamada S, Darrad K, McDonnell PJ. Salzmann’s nodular corneal degeneration (SNCD): Clinical findings, risk factors, prognosis and the role of previous contact lens wear. Cont Lens Anterior Eye. 2011;34(4):173-178. doi:10.1016/j.clae.2011.02.004
Maharana PK, Sharma N, Das S, Agarwal T, Sen S, Prakash G, Vajpayee RB. Salzmann’s Nodular Degeneration. Ocul Surf. 2016;14(1):20-30. doi:10.1016/j.jtos.2015.08.006
Stone DU, Astley RA, Shaver RP , Chodosh J. Histopathology of Salzmann nodular corneal degeneration. Cornea. 2008;27(2):148-151. doi:10.1097/ICO.0b013e31815a50fb
Hurmeric V, Yoo SH, Karp CL, Galor A, Vajzovic L, Wang J, Dubovy SR, Forster RK. In vivo morphologic characteristics of Salzmann nodular degeneration with ultra-high-resolution optical coherence tomography. Am J Ophthalmol. 2011;151(2):248-256.e2. doi:10.1016/j.ajo.2010.08.013
Roszkowska AM, Spinella R, Aragona P. Morphologic and confocal investigation on Salzmann nodular degeneration of the cornea. Invest Ophthalmol Vis Sci. 2011;52(8):5910-5919. doi:10.1167/iovs.11-7789.