眼部局部原因

带状角膜变性
一目了然的要点
Section titled “一目了然的要点”1. 什么是带状角膜变性?
Section titled “1. 什么是带状角膜变性?”带状角膜变性(Calcific Band Keratopathy: CBK)是一种慢性角膜变性疾病,其特征是以钙羟基磷灰石为主的无机磷酸盐和碳酸盐沉积在上皮下、鲍曼层和前基质中1)。本症首次描述由Dixon于1948年提出,此后被广泛认为是继发于慢性眼病和全身代谢异常的变性1, 7)。沉积物主体是钙结晶,但可能伴有非结晶性磷酸盐、碳酸盐或弹性纤维变性胶原等混合物质,此时对螯合剂的反应较差1)。
本症的特征是在水平睑裂区形成带状灰白色混浊,混浊与角膜缘之间留有透明带。进展通常缓慢;混浊局限于角膜周边时无症状,但累及瞳孔区时会导致视力障碍、畏光,以及因上皮糜烂引起的疼痛和异物感4)。如果原发病控制不佳,治疗后可能复发8)。
在成人中,常继发于长期慢性葡萄膜炎、硅油填充眼或难治性青光眼。在儿童中,常见于幼年特发性关节炎(JIA)相关慢性虹膜睫状体炎的晚期并发症,常在症状轻微的“白色葡萄膜炎”病程中与并发性白内障和虹膜后粘连一同被发现6)。全身背景包括甲状旁腺功能亢进、慢性肾衰竭和结节病等代谢性和炎症性疾病。鉴于这种多样性,带状角膜变性应被理解为一种“以钙沉积为临床特征的综合征”,而非单一疾病7)。
典型发病年龄取决于基础疾病:JIA相关性慢性虹膜睫状体炎多见于学龄期至青春期;硅油填充病例多见于术后数月至数年;高钙血症病例多见于中老年以后。可双眼或单眼发病,但伴有全身性疾病时倾向于双眼发病10)。
EDTA螯合治疗后的复发率约为17.8%1)。在葡萄膜炎或角膜疱疹等基础疾病持续存在的病例中复发率较高1, 8)。地形图引导的PRK联合治疗性激光角膜切除术可通过改善表面平滑度和泪膜稳定性来降低复发率1)。
2. 主要症状与临床所见
Section titled “2. 主要症状与临床所见”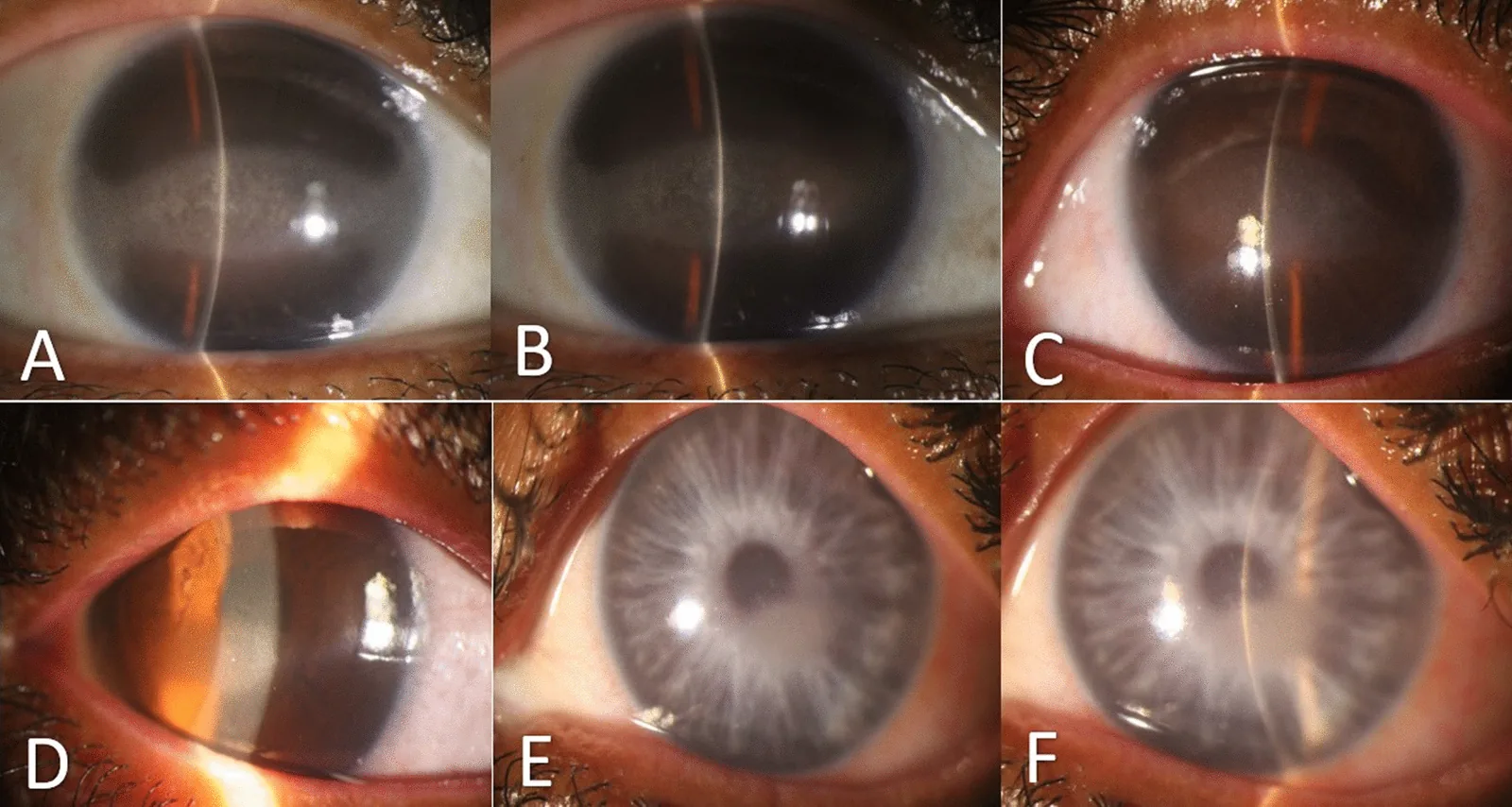
轻症多无症状。病变覆盖瞳孔区时出现视力障碍、畏光、异物感4)。钙结晶引起的光散射导致眩光和对比敏感度下降1)。伴有上皮糜烂或上皮缺损的进展期病例可出现剧烈疼痛和流泪。视力下降的自觉通常在沉积物达到瞳孔区中央时才变得明显,日常活动中的眩光、雾视和夜间视力下降可能是前驱症状。单眼病例可能通过与对侧眼比较而被发现。反复发作的角膜糜烂病例以晨起时剧烈疼痛和流泪为特征。
混浊始于水平方向(3点和9点方向)的睑裂部角膜周边部。角膜缘与沉积物之间存在1-2mm宽的透明带(角膜缘透明区),是本病的形态学特征。混浊逐渐向中央进展并融合成带状。混浊中散在瑞士奶酪样透明小孔,对应于角膜神经穿过Bowman层的部位。进展期病例可伴有上皮不规则、反复性上皮缺损和前部基质混浊7)。
影像学检查:共焦显微镜下沉积物呈高亮度的厚积云状,沉积物内可见声影。眼前节光学相干断层扫描(AS-OCT)可将沉积层显示为高反射信号,定量评估其深度和厚度,有病例报告确认沉积层厚度约150μm1)。角膜地形图可通过角膜形态不规则指数(CMI)定量评估不规则程度1)。
沉积物的分布模式是推断病理状态的线索。在伴有慢性葡萄膜炎的病例中,常表现为从3点和9点方向的睑裂区向心性进展的典型模式,而在JIA相关病例中,也可能遇到透明带变得模糊、进展至中央部的重症病例6)。职业性汞蒸气暴露病例可能在角膜中央附近出现不规则沉积,病史采集是鉴别诊断的关键1)。进展期病例可观察到因角膜表面不规则导致的泪膜破裂时间缩短和上皮微小缺损,裂隙灯下荧光素染色呈现点状角膜上皮病变样染色模式。有复发性角膜上皮糜烂病史的病例,推测其背景存在鲍曼层断裂7)。
3. 原因与风险因素
Section titled “3. 原因与风险因素”带状角膜变性继发于多种眼部局部疾病和全身性疾病。临床上常见的原因包括慢性眼内炎症性疾病、高钙血症、玻璃体手术后硅油填充。原因可能单独存在,也可能多重叠加,例如长期葡萄膜炎病例中,炎症、继发性青光眼使用含磷酸盐的类固醇滴眼液以及高钙血症三者可能同时参与。
全身性原因
原发性甲状旁腺功能亢进症:通过高钙血症介导的代表性全身性原因
慢性肾衰竭/透析患者:血清钙磷乘积升高导致的转移性钙化,引起结膜和角膜钙化5, 10)
结节病、维生素D中毒:肉芽肿性疾病引起的高钙血症为背景
职业性暴露:有汞蒸气或铬酸钙蒸气暴露的病例报告1)
含磷酸盐的类固醇滴眼液:长期使用可能导致沉淀物沉积在角膜上。
钙沉积的确切机制尚未完全阐明,但组织pH升高和泪液蒸发增强被认为是主要因素。在睑裂区,泪液暴露于大气中,二氧化碳释放,导致泪液pH升高,钙盐溶解度降低。泪液蒸发量在睑裂较宽的部位更大,睑裂区比睑缘部在常温下更容易干燥,这支持了沉积物分布与睑裂一致的原因。干眼症通过增加泪液蒸发和组织渗透压而成为加重因素,眼表环境的慢性不稳定与本病的进展有关5)。在慢性肾功能衰竭病例中,除了血清钙磷乘积升高外,还推测存在转移性钙化的机制,即通过来自角膜缘血管的血流携带的钙盐沉积在上皮下5, 10)。
风险因素总结如表所示。在多种因素并存的情况下,发病前的潜伏期往往较短。在幼年特发性关节炎相关的慢性虹膜睫状体炎中,带状角膜病变可能在诊断数年后才显现,因此定期进行眼前段筛查很重要6)。儿童病例通常难以主诉自觉症状,因此最好在视力下降或异物感出现之前通过定期检查早期发现。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”带状灰白色混浊、瑞士奶酪样外观以及混浊与角膜缘之间的透明带这三联征是特征性临床表现,可通过裂隙灯显微镜检查进行诊断4)。裂隙灯彻照法可使沉积物呈现为阴影,便于直观评估沉积的范围和密度。AS-OCT可用于评估沉积物的深度和厚度以及向前部基质的延伸,是治疗选择的重要指标1)。角膜地形图用于定量评估角膜形态不规则程度,可客观追踪治疗前后CMI的变化1)。共聚焦显微镜下沉积物表现为高反射结构,同时可评估基底下神经丛的损伤程度,有助于理解伴有复发性上皮糜烂的病例的病理生理。超声生物显微镜(UBM)是评估角膜前部至角膜缘结构的有用辅助检查。
对于原因不明的带状角膜变性,尤其是年轻患者或双眼病例,全身性病因检查非常重要。
| 检查项目 | 目的 |
|---|---|
| 血清钙、磷、校正钙、完整甲状旁腺激素 | 评估高钙血症和甲状旁腺功能亢进5, 10) |
| 肾功能(尿素氮、肌酐、估算肾小球滤过率) | 判断是否存在慢性肾衰竭 |
| 血清尿酸 | 评估痛风和代谢异常 |
| 血管紧张素转换酶水平、胸部影像 | 排除结节病 |
| 血沉、C反应蛋白、抗核抗体、HLA-B27 | 评估全身炎症性疾病和胶原病 |
Vogt角膜缘带是与年龄相关的角膜周边部细微钙盐沉积,常见于健康个体,是一种无症状的年龄相关变化4)。它发生在角膜缘附近,不向睑裂中央进展,以此与带状角膜变性区分。球形变性(气候性滴状角膜病变)是透明样物质的上皮下沉积,形态与本病相似,但沉积物性质不同,常见于强烈紫外线暴露地区的户外工作者,特征为金色至黄褐色的油滴状小球。继发性角膜淀粉样变性也会在睑裂区产生白色沉积,需要鉴别,通过刚果红染色阳性和偏振光下的双折射来诊断。胶样滴状角膜营养不良是一种青少年发病的上皮淀粉样变性,表现为桑葚状或带状混浊,外观相似,因此需要注意。
5. 标准治疗
Section titled “5. 标准治疗”如果没有视力障碍或症状,原则上进行观察4)。出现症状时开始积极治疗。治疗方法大致分为三类:用针头局部去除、药物螯合和准分子激光角膜切削。
用针头局部去除钙质
Section titled “用针头局部去除钙质”当钙沉积局部突出或呈板状时,有一种简单的方法是用27号针头将沉积物翻转去除。然而,沉积物正下方的基质通常较薄,切入深层基质可能导致医源性瘢痕,因此需要谨慎。
EDTA螯合疗法
Section titled “EDTA螯合疗法”这是最广泛使用的治疗方法4, 7, 8)。机械去除角膜上皮后,用浸有乙二胺四乙酸(EDTA)溶液的棉签涂抹钙沉积物,并用高尔夫刀等器械刮除沉积物。标准浓度为0.4–1% EDTA溶液或0.05 mol/L EDTA-Na,最后用足量磷酸盐缓冲液或生理盐水冲洗。2004年报道的一项长期随访研究表明,虽然EDTA螯合可改善平均视力,但在基础疾病持续存在的病例中复发率很高8)。对于幼年特发性关节炎相关慢性虹膜睫状体炎并发症的带状角膜变性,可使用EDTA或稀盐酸处理以及准分子激光治疗6)。
传统的Na2EDTA在美国FDA撤回批准后变得难以获得且昂贵,因此提出了使用K2EDTA采血管的替代制备方法3)。从K2EDTA涂层采血管内壁制备的简便方法已在多项报告中证实安全有效2, 3)。
K2EDTA(采血管来源)
特点:从紫色帽采血管内壁的K2EDTA涂层溶解制备的简便方法3)
优点:价格低廉(每100管36–47美元,低于Na2EDTA平均117美元)且易于获得3)
有效性:多个临床病例已证实其钙去除效果与Na2EDTA相当2, 3)
安全性:尚未报告对角膜内皮的负面影响或延迟愈合。与白内障手术或角膜内皮移植同时进行也是安全的2)
治疗性激光角膜切除术/PRK(准分子激光)
| K2EDTA制备方法 | 浓度 | 制备时间 |
|---|---|---|
| 方法1(5瓶转移法) | 65 mg/mL3) | 189秒3) |
| 方法2(1瓶振荡法) | 35 mg/mL3) | 38秒3) |
| 方法3(棉签溶解法) | 52mg/mL3) | 83秒3) |
标准Na2EDTA的配制浓度为30~40mg/mL,方法3可在短时间内达到更高浓度,因此在浓度、配制时间和简便性之间达到最佳平衡,被推荐使用3)。
治疗性激光角膜切除术(PTK)联合PRK
Section titled “治疗性激光角膜切除术(PTK)联合PRK”自1993年O’Brart等人的长期随访研究以来,使用准分子激光的治疗性激光角膜切除术(phototherapeutic keratectomy: PTK)已被确立为去除深层沉积物和混合型物质的有效治疗方法9)。近年来,通过地形图引导的经上皮PRK与PTK相结合的个体化手术,可以同时实现沉积物去除和不规则散光矫正1)。在一例汞蒸气暴露导致的带状角膜变性病例(63岁男性)中,EDTA无效后实施了地形图引导的PRK+PTK联合手术,右眼裸眼视力(UCVA)从20/100提高到20/20,左眼从20/200提高到20/631)。角膜形态不规则指数(CMI)也显著改善,右眼从15μm降至3μm,左眼从21μm降至11μm1)。
术后管理在EDTA螯合和PTK/PRK中是共通的:佩戴治疗性软性隐形眼镜,并给予抗菌眼药水和低剂量类固醇眼药水,以促进快速上皮再生。术后早期的疼痛管理和感染预防至关重要。通常上皮化需要5~7天,在此期间随访评估上皮缺损面积、前房炎症情况以及隐形眼镜的佩戴状态。对于有慢性葡萄膜炎背景的病例,术前应充分抗炎,术后继续抗炎治疗以降低复发风险6, 8)。
视力预后取决于基础疾病的控制和沉积物的深度。对于仅表层的沉积物,单独EDTA螯合即可获得良好的视力改善,但对于延伸至前部基质的深层沉积物,需要联合PTK,术后可能仍残留不规则散光1, 9)。对于遗留严重角膜瘢痕或合并内皮功能低下的病例,最终可能选择板层角膜移植(DALK)或穿透性角膜移植(PKP)7)。
从采血管中提取K2EDTA用于治疗带状角膜病变的方法,已在多项报告中确认其安全性和有效性2, 3)。未见对角膜内皮的不良影响或延迟愈合的报道3)。与白内障手术或角膜内皮移植同时进行手术也可安全实施2)。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”本病的本质是羟基磷灰石钙沉积于角膜上皮基底膜、鲍曼层和前基质1, 4)。沉积物可能包含无定形磷酸盐、碳酸盐和弹性纤维变性胶原等混合物质,混合物质的存在可能导致对EDTA螯合治疗反应不佳1, 7)。
沉积沿睑裂呈带状分布的原因,主要认为是泪液pH升高和蒸发增强所致。在睑裂区,泪液暴露于空气,二氧化碳释放,导致局部pH升高,从而降低钙盐(尤其是磷酸钙、碳酸钙)的溶解度,促进沉积。泪液层蒸发增强、干眼、高渗透压等眼表应激也促进沉积5)。
当钙沉积严重时,鲍曼层受损和断裂,导致其上方的角膜上皮粘附异常。这一机制导致复发性角膜上皮糜烂和慢性疼痛7)。在慢性葡萄膜炎中,房水中的炎症细胞因子和增加的钙离子从角膜后表面渗透,通过慢性角膜内皮和基质应激促进沉积6)。
慢性肾功能衰竭中的带状角膜病变涉及转移性钙化和慢性全身性炎症两方面5, 10)。当血清钙磷乘积升高时,钙盐通过来自角膜缘血管的血流更容易沉积于上皮下组织。透析患者常合并甲状旁腺功能亢进(继发性或三发性),钙代谢异常成为角膜病变的背景10)。血清钙磷乘积持续超过70 mg²/dL²时,角膜和结膜钙化的风险明显升高,透析管理中矿物质代谢的矫正是预防本病的基础10)。
在分子水平上,有研究指出炎症细胞因子和碱性磷酸酶活性的局部升高可能促进钙化的成核。慢性葡萄膜炎的房水中含有高浓度的炎症细胞因子,这些因子被认为通过从角膜后表面扩散到基质参与沉积物的形成6, 7)。干眼症导致的泪液渗透压升高、睑裂区的慢性机械刺激以及长期使用含有磷酸盐缓冲液的眼药水(如某些类固醇眼药水)也被报道为危险因素,为减少医源性发病,需要关注制剂选择5)。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”地形图引导的经上皮PRK联合治疗性激光角膜切除术已被报道为EDTA无效病例的有效治疗选择1)。通过光线追踪算法,可以综合矫正眼前节和眼后节的像差,在最小化基质消耗的同时优化视觉质量。术后6个月,角膜透明度和视力改善得以维持1)。
使用K2EDTA采血管的制备方法简化也在推进中,与传统Na2EDTA相比,可实现更低成本和更快速的治疗2, 3)。近年来,有报道通过透明角膜切口同时进行白内障手术和角膜内皮移植,扩大了视力恢复策略的灵活性2)。
未来的挑战包括优化结合EDTA、PTK、羊膜移植和地形图引导PRK的个体化治疗,以及建立与基础疾病治疗(慢性葡萄膜炎的分子靶向治疗、甲状旁腺功能亢进的外科治疗、透析患者的磷代谢管理)联动的复发预防策略6, 8)。
随着生物制剂(阿达木单抗、英夫利西单抗等)用于幼年特发性关节炎相关葡萄膜炎,眼内炎症的控制比以前更加稳定,这可能长期抑制带状角膜变性的新发和复发6)。事实上,日本已有病例报告在引入生物制剂后安全进行白内障手术和EDTA螯合治疗,并获得良好的视力改善6)。在基础疾病得到控制的状态下进行手术干预是决定长期预后的最重要因素。
影像诊断的进步也备受关注。通过结合AS-OCT对沉积层的三维评估、Scheimpflug成像的角膜密度分析以及地形图指标的时序比较,有望实现治疗适应症和激光照射方案的精细化1)。此外,基于基础疾病进行复发风险分层的生物标志物(泪液炎症细胞因子、血清钙磷乘积)的临床应用也是未来的课题。在诊疗的各个阶段确保多学科协作(风湿免疫科、肾内科、内分泌科)是抑制复发和保护视功能的关键。
8. 参考文献
Section titled “8. 参考文献”- Passidomo F, Addabbo G, Pignatelli F, Niro A, Buonamassa R. Combined Topography-Guided Trans-Epithelial PRK and PTK for Treatment of Calcific Band Keratopathy Unresponsive to EDTA Chelation Therapy. Int Med Case Rep J. 2025;18:187-194.
- Abusayf MM, Tobaigy MF. Blood tubes potassium ethylenediaminetetraacetic acid in comparison to calcium disodium ethylenediaminetetraacetic acid and disodium ethylenediaminetetraacetic acid for calcific band keratopathy. Saudi J Ophthalmol. 2025;39:407-409.
- Narvaez J, Chang M, Ing J, De Chance D, Narvaez JJ. Simplified, Readily Available Method for the Treatment of Band Keratopathy With Ethylenediaminetetraacetic Acid. Cornea. 2021;40:1360-1362.
- American Academy of Ophthalmology Corneal/External Disease PPP Panel. Corneal Edema and Opacification Preferred Practice Pattern. Ophthalmology. 2024.
- Markoulli M, Ahmad S, Engel L, et al. TFOS Lifestyle: Impact of the natural, built, and social environments on the ocular surface. Ocul Surf. 2023;29:226-271.
- 日本眼科学会ぶどう膜炎標準診療ガイドライン策定委員会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635-696.
- Jhanji V, Rapuano CJ, Vajpayee RB. Corneal calcific band keratopathy. Curr Opin Ophthalmol. 2011;22(4):283-289.
- Najjar DM, Cohen EJ, Rapuano CJ, Laibson PR. EDTA chelation for calcific band keratopathy: results and long-term follow-up. Am J Ophthalmol. 2004;137(6):1056-1064.
- O’Brart DP, Gartry DS, Lohmann CP, Patmore AL, Kerr Muir MG, Marshall J. Treatment of band keratopathy by excimer laser phototherapeutic keratectomy: surgical techniques and long term follow up. Br J Ophthalmol. 1993;77(11):702-708.
- Porter R, Crombie AL. Corneal and conjunctival calcification in chronic renal failure. Br J Ophthalmol. 1973;57(5):339-343.
