眼部局部原因
慢性葡萄膜炎:最常見的眼部局部原因之一,持續性眼內炎症促進鈣沉積2, 7)
幼年特發性關節炎相關性慢性虹膜睫狀體炎:常伴有併發性白內障和虹膜後粘連,帶狀角膜變性發生率高,是晚期的主要併發症6)
續發性青光眼:長期青光眼病例,特別是角膜內皮功能下降的病例可能續發2)
角膜基質炎:慢性皰疹性角膜基質炎或間質性角膜炎為基礎
矽油填充後:玻璃體手術後長期留置誘發角膜變性
角膜暴露:兔眼或顏面神經麻痺導致的持續性乾燥參與

帶狀角膜變性(Calcific Band Keratopathy: CBK)是一種慢性角膜變性疾病,特徵是以鈣羥基磷灰石為主的無機磷酸鹽和碳酸鹽沉積在上皮下、鮑曼層和前基質中1)。本症首次描述由Dixon於1948年提出,此後被廣泛認為是繼發於慢性眼病和全身代謝異常的變性1, 7)。沉積物主體是鈣結晶,但可能伴有非結晶性磷酸鹽、碳酸鹽或彈性纖維變性膠原等混合物質,此時對螯合劑的反應較差1)。
本症的特徵是在水平眼裂區形成帶狀灰白色混濁,混濁與角膜緣之間留有透明帶。進展通常緩慢;混濁局限於角膜周邊時無症狀,但累及瞳孔區時會導致視力障礙、畏光,以及因上皮糜爛引起的疼痛和異物感4)。如果原發病控制不佳,治療後可能復發8)。
在成人中,常繼發於長期慢性葡萄膜炎、矽油填充眼或難治性青光眼。在兒童中,常見於幼年型特發性關節炎(JIA)相關慢性虹膜睫狀體炎的晚期併發症,常在症狀輕微的「白色葡萄膜炎」病程中與併發性白內障和虹膜後粘連一同被發現6)。全身背景包括副甲狀腺功能亢進、慢性腎衰竭和結節病等代謝性和炎症性疾病。鑑於這種多樣性,帶狀角膜變性應被理解為一種「以鈣沉積為臨床特徵的症候群」,而非單一疾病7)。
典型發病年齡取決於基礎疾病:JIA相關慢性虹膜睫狀體炎多見於學齡期至青春期;矽油填充病例多見於術後數月至數年;高鈣血症病例多見於中老年以後。可雙眼或單眼發病,但伴有全身性疾病時傾向於雙眼發病10)。
EDTA螯合治療後的復發率約為17.8%1)。在葡萄膜炎或角膜皰疹等基礎疾病持續存在的病例中復發率較高1, 8)。地形圖引導的PRK聯合治療性雷射角膜切除術可通過改善表面平滑度和淚膜穩定性來降低復發率1)。
輕症多無症狀。病變覆蓋瞳孔區時出現視力障礙、畏光、異物感4)。鈣結晶引起的光散射導致眩光和對比敏感度下降1)。伴有上皮糜爛或上皮缺損的進展期病例可出現劇烈疼痛和流淚。視力下降的自覺通常在沉積物達到瞳孔區中央時才變得明顯,日常活動中的眩光、霧視和夜間視力下降可能是前驅症狀。單眼病例可能通過與對側眼比較而被發現。反覆發作的角膜糜爛病例以晨起時劇烈疼痛和流淚為特徵。
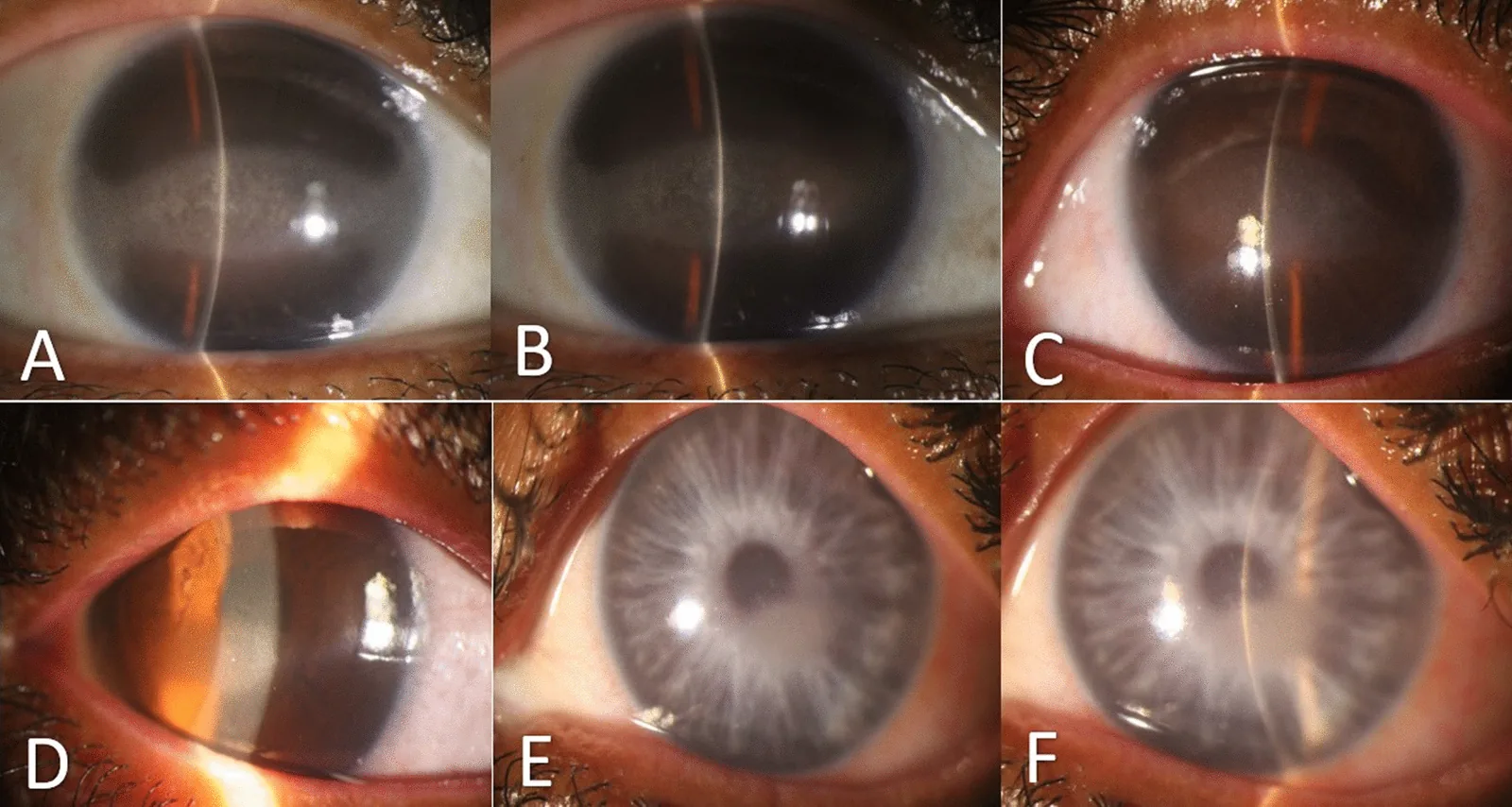
混濁始於水平方向(3點和9點方向)的瞼裂部角膜周邊部。角膜緣與沉積物之間存在1-2mm寬的透明帶(角膜緣透明區),是本病的形態學特徵。混濁逐漸向中央進展並融合成帶狀。混濁中散在瑞士起司樣透明小孔,對應於角膜神經穿過Bowman層的部位。進展期病例可伴有上皮不規則、反覆性上皮缺損和前部基質混濁7)。
影像學檢查:共焦顯微鏡下沉積物呈高亮度的厚積雲狀,沉積物內可見音影。前段光學同調斷層掃描(AS-OCT)可將沉積層顯示為高反射訊號,定量評估其深度和厚度,有病例報告確認沉積層厚度約150μm1)。角膜地形圖可通過角膜形態不規則指數(CMI)定量評估不規則程度1)。
沉積物的分布模式是推斷病理狀態的線索。在伴有慢性葡萄膜炎的病例中,常表現為從3點和9點方向的眼瞼裂區向心性進展的典型模式,而在JIA相關病例中,也可能遇到透明帶變得模糊、進展至中央部的重症病例6)。職業性汞蒸氣暴露病例可能在角膜中央附近出現不規則沉積,病史詢問是鑑別診斷的關鍵1)。進展期病例可觀察到因角膜表面不規則導致的淚膜破裂時間縮短和上皮微小缺損,裂隙燈下螢光素染色呈現點狀角膜上皮病變樣染色模式。有復發性角膜上皮糜爛病史的病例,推測其背景存在鮑曼層斷裂7)。
帶狀角膜變性繼發於多種眼部局部疾病和全身性疾病。臨床上常見的原因包括慢性眼內炎症性疾病、高鈣血症、玻璃體手術後矽油填充。原因可能單獨存在,也可能多重疊加,例如長期葡萄膜炎病例中,炎症、續發性青光眼使用含磷酸鹽的類固醇眼藥水以及高鈣血症三者可能同時參與。
眼部局部原因
慢性葡萄膜炎:最常見的眼部局部原因之一,持續性眼內炎症促進鈣沉積2, 7)
幼年特發性關節炎相關性慢性虹膜睫狀體炎:常伴有併發性白內障和虹膜後粘連,帶狀角膜變性發生率高,是晚期的主要併發症6)
續發性青光眼:長期青光眼病例,特別是角膜內皮功能下降的病例可能續發2)
角膜基質炎:慢性皰疹性角膜基質炎或間質性角膜炎為基礎
矽油填充後:玻璃體手術後長期留置誘發角膜變性
角膜暴露:兔眼或顏面神經麻痺導致的持續性乾燥參與
全身性原因
原發性副甲狀腺功能亢進症:通過高鈣血症介導的代表性全身性原因
慢性腎衰竭/透析患者:血清鈣磷乘積升高導致的轉移性鈣化,引起結膜和角膜鈣化5, 10)
結節病、維生素D中毒:肉芽腫性疾病引起的高鈣血症為背景
職業性暴露:有汞蒸氣或鉻酸鈣蒸氣暴露的病例報告1)
含磷酸鹽的類固醇眼藥水:長期使用可能導致沉澱物沉積在角膜上。
鈣沉積的確切機制尚未完全闡明,但組織pH升高和淚液蒸發增強被認為是主要因素。在眼瞼裂區,淚液暴露於大氣中,二氧化碳釋放,導致淚液pH升高,鈣鹽溶解度降低。淚液蒸發量在眼瞼裂較寬的部位更大,眼瞼裂區比眼瞼邊緣在常溫下更容易乾燥,這支持了沉積物分佈與眼瞼裂一致的原因。乾眼症通過增加淚液蒸發和組織滲透壓而成為加重因素,眼表環境的慢性不穩定與本病的進展有關5)。在慢性腎功能衰竭病例中,除了血清鈣磷乘積升高外,還推測存在轉移性鈣化的機制,即通過來自角膜緣血管的血流攜帶的鈣鹽沉積在上皮下5, 10)。
風險因素總結如表所示。在多種因素並存的情況下,發病前的潛伏期往往較短。在幼年特發性關節炎相關的慢性虹膜睫狀體炎中,帶狀角膜病變可能在診斷數年後才顯現,因此定期進行眼前段篩查很重要6)。兒童病例通常難以主訴自覺症狀,因此最好在視力下降或異物感出現之前通過定期檢查早期發現。
帶狀灰白色混濁、瑞士起司樣外觀以及混濁與角膜緣之間的透明帶這三聯徵是特徵性臨床表現,可通過裂隙燈顯微鏡檢查進行診斷4)。裂隙燈徹照法可使沉積物呈現為陰影,便於直觀評估沉積的範圍和密度。AS-OCT可用於評估沉積物的深度和厚度以及向前部基質的延伸,是治療選擇的重要指標1)。角膜地形圖用於定量評估角膜形態不規則程度,可客觀追蹤治療前後CMI的變化1)。共聚焦顯微鏡下沉積物表現為高反射結構,同時可評估基底下神經叢的損傷程度,有助於理解伴有復發性上皮糜爛的病例的病理生理。超音波生物顯微鏡(UBM)是評估角膜前部至角膜緣結構的有用輔助檢查。
對於原因不明的帶狀角膜變性,尤其是年輕患者或雙眼病例,全身性病因檢查非常重要。
| 檢查項目 | 目的 |
|---|---|
| 血清鈣、磷、校正鈣、完整副甲狀腺激素 | 評估高鈣血症和副甲狀腺功能亢進5, 10) |
| 腎功能(尿素氮、肌酸酐、估算腎絲球過濾率) | 判斷是否存在慢性腎衰竭 |
| 血清尿酸 | 評估痛風和代謝異常 |
| 血管收縮素轉化酶濃度、胸部影像 | 排除類肉瘤病 |
| 紅血球沉降速率、C反應蛋白、抗核抗體、HLA-B27 | 評估全身性發炎疾病和膠原病 |
Vogt角膜緣帶是與年齡相關的角膜周邊部細微鈣鹽沉積,常見於健康個體,是一種無症狀的年齡相關變化4)。它發生在角膜緣附近,不向眼瞼裂中央進展,以此與帶狀角膜變性區分。球形變性(氣候性滴狀角膜病變)是透明樣物質的上皮下沉積,形態與本病相似,但沉積物性質不同,常見於強烈紫外線暴露地區的戶外工作者,特徵為金色至黃褐色的油滴狀小球。繼發性角膜澱粉樣變性也會在眼瞼裂區產生白色沉積,需要鑑別,通過剛果紅染色陽性和偏振光下的雙折射來診斷。膠樣滴狀角膜營養不良是一種青少年發病的上皮澱粉樣變性,表現為桑葚狀或帶狀混濁,外觀相似,因此需要注意。
如果沒有視力障礙或症狀,原則上進行觀察4)。出現症狀時開始積極治療。治療方法大致分為三類:用針頭局部去除、藥物螯合和準分子雷射角膜切削。
當鈣沉積局部突出或呈板狀時,有一種簡單的方法是用27號針頭將沉積物翻轉去除。然而,沉積物正下方的基質通常較薄,切入深層基質可能導致醫源性疤痕,因此需要謹慎。
這是最廣泛使用的治療方法4, 7, 8)。機械去除角膜上皮後,用浸有乙二胺四乙酸(EDTA)溶液的棉籤塗抹鈣沉積物,並用高爾夫刀等器械刮除沉積物。標準濃度為0.4–1% EDTA溶液或0.05 mol/L EDTA-Na,最後用足量磷酸鹽緩衝液或生理鹽水沖洗。2004年報導的一項長期追蹤研究表明,雖然EDTA螯合可改善平均視力,但在基礎疾病持續存在的病例中復發率很高8)。對於幼年特發性關節炎相關慢性虹膜睫狀體炎併發症的帶狀角膜變性,可使用EDTA或稀鹽酸處理以及準分子雷射治療6)。
傳統的Na2EDTA在美國FDA撤回批准後變得難以獲得且昂貴,因此提出了使用K2EDTA採血管的替代製備方法3)。從K2EDTA塗層採血管內壁製備的簡便方法已在多項報告中證實安全有效2, 3)。
K2EDTA(採血管來源)
特點:從紫色帽採血管內壁的K2EDTA塗層溶解製備的簡便方法3)
優點:價格低廉(每100管36–47美元,低於Na2EDTA平均117美元)且易於獲得3)
有效性:多個臨床病例已證實其鈣去除效果與Na2EDTA相當2, 3)
安全性:尚未報告對角膜內皮的不良影響或延遲癒合。與白內障手術或角膜內皮移植同時進行也是安全的2)
治療性雷射角膜切除術/PRK(準分子雷射)
| K2EDTA製備方法 | 濃度 | 製備時間 |
|---|---|---|
| 方法1(5瓶轉移法) | 65 mg/mL3) | 189秒3) |
| 方法2(1瓶振盪法) | 35 mg/mL3) | 38秒3) |
| 方法3(棉籤溶解法) | 52mg/mL3) | 83秒3) |
標準Na2EDTA的配製濃度為30~40mg/mL,方法3可在短時間內達到更高濃度,因此在濃度、配製時間和簡便性之間達到最佳平衡,被推薦使用3)。
自1993年O’Brart等人的長期追蹤研究以來,使用準分子雷射的治療性雷射角膜切除術(phototherapeutic keratectomy: PTK)已被確立為去除深層沉積物和混合型物質的有效治療方法9)。近年來,透過地形圖引導的經上皮PRK與PTK相結合的個別化手術,可以同時實現沉積物去除和不規則散光矯正1)。在一例汞蒸氣暴露導致的帶狀角膜變性病例(63歲男性)中,EDTA無效後實施了地形圖引導的PRK+PTK聯合手術,右眼裸眼視力(UCVA)從20/100提高到20/20,左眼從20/200提高到20/631)。角膜形態不規則指數(CMI)也顯著改善,右眼從15μm降至3μm,左眼從21μm降至11μm1)。
術後管理在EDTA螯合和PTK/PRK中是共通的:佩戴治療性軟性隱形眼鏡,並給予抗菌眼藥水和低劑量類固醇眼藥水,以促進快速上皮再生。術後早期的疼痛管理和感染預防至關重要。通常上皮化需要5~7天,在此期間追蹤評估上皮缺損面積、前房炎症情況以及隱形眼鏡的佩戴狀態。對於有慢性葡萄膜炎背景的病例,術前應充分抗炎,術後繼續抗炎治療以降低復發風險6, 8)。
視力預後取決於基礎疾病的控制和沉積物的深度。對於僅表層的沉積物,單獨EDTA螯合即可獲得良好的視力改善,但對於延伸至前部基質的深層沉積物,需要聯合PTK,術後可能仍殘留不規則散光1, 9)。對於遺留嚴重角膜疤痕或合併內皮功能低下的病例,最終可能選擇板層角膜移植(DALK)或穿透性角膜移植(PKP)7)。
從採血管中提取K2EDTA用於治療帶狀角膜病變的方法,已在多項報告中確認其安全性與有效性2, 3)。未見對角膜內皮的不良影響或延遲癒合的報告3)。與白內障手術或角膜內皮移植同時進行手術也可安全執行2)。
本病的本質是羥基磷灰石鈣沉積於角膜上皮基底膜、鮑曼層和前基質1, 4)。沉積物可能包含無定形磷酸鹽、碳酸鹽和彈性纖維變性膠原等混合物質,混合物質的存在可能導致對EDTA螯合治療反應不佳1, 7)。
沉積沿瞼裂呈帶狀分佈的原因,主要認為是淚液pH升高和蒸發增強所致。在瞼裂區,淚液暴露於空氣,二氧化碳釋放,導致局部pH升高,從而降低鈣鹽(尤其是磷酸鈣、碳酸鈣)的溶解度,促進沉積。淚液層蒸發增強、乾眼、高滲透壓等眼表應激也促進沉積5)。
當鈣沉積嚴重時,鮑曼層受損和斷裂,導致其上方的角膜上皮粘附異常。這一機制導致復發性角膜上皮糜爛和慢性疼痛7)。在慢性葡萄膜炎中,房水中的發炎細胞因子和增加的鈣離子從角膜後表面滲透,通過慢性角膜內皮和基質應激促進沉積6)。
慢性腎功能衰竭中的帶狀角膜病變涉及轉移性鈣化和慢性全身性發炎兩方面5, 10)。當血清鈣磷乘積升高時,鈣鹽通過來自角膜緣血管的血流更容易沉積於上皮下組織。透析患者常合併副甲狀腺功能亢進(繼發性或三發性),鈣代謝異常成為角膜病變的背景10)。血清鈣磷乘積持續超過70 mg²/dL²時,角膜和結膜鈣化的風險明顯升高,透析管理中礦物質代謝的矯正是預防本病的基礎10)。
在分子層級,有研究指出發炎性細胞激素和鹼性磷酸酶活性的局部升高可能促進鈣化的成核。慢性葡萄膜炎的房水中含有高濃度的發炎性細胞激素,這些激素被認為透過從角膜後表面擴散到基質參與沉積物的形成6, 7)。乾眼症導致的淚液滲透壓升高、眼瞼裂區的慢性機械刺激以及長期使用含有磷酸鹽緩衝液的眼藥水(如某些類固醇眼藥水)也被報導為危險因子,為減少醫源性發生,需要關注製劑選擇5)。
地形圖引導的經上皮PRK聯合治療性雷射角膜切除術已被報導為EDTA無效病例的有效治療選擇1)。透過光線追蹤演算法,可以綜合矯正眼前節和眼後節的像差,在最小化基質消耗的同時最佳化視覺品質。術後6個月,角膜透明度和視力改善得以維持1)。
使用K2EDTA採血管的製備方法簡化也在進展中,與傳統Na2EDTA相比,可實現更低成本和更快速的治療2, 3)。近年來,有報導透過透明角膜切口同時進行白內障手術和角膜內皮移植,擴大了視力恢復策略的靈活性2)。
未來的挑戰包括最佳化結合EDTA、PTK、羊膜移植和地形圖引導PRK的個別化治療,以及建立與基礎疾病治療(慢性葡萄膜炎的分子標靶治療、甲狀腺功能亢進的外科治療、透析患者的磷代謝管理)聯動的復發預防策略6, 8)。
隨著生物製劑(阿達木單抗、英夫利西單抗等)用於幼年特發性關節炎相關葡萄膜炎,眼內發炎的控制比以前更加穩定,這可能長期抑制帶狀角膜變性的新發和復發6)。事實上,日本已有病例報告在引入生物製劑後安全進行白內障手術和EDTA螯合治療,並獲得良好的視力改善6)。在基礎疾病得到控制的狀態下進行手術干預是決定長期預後的最重要因素。
影像診斷的進步也備受關注。透過結合AS-OCT對沉積層的三維評估、Scheimpflug成像的角膜密度分析以及地形圖指標的時序比較,有望實現治療適應症和雷射照射方案的精細化1)。此外,基於基礎疾病進行復發風險分層的生物標誌物(淚液發炎性細胞因子、血清鈣磷乘積)的臨床應用也是未來的課題。在診療的各個階段確保多學科協作(風濕免疫科、腎臟內科、內分泌科)是抑制復發和保護視功能的關鍵。