ความผิดปกติแต่กำเนิดของส่วนหน้าของตา (ASD A) เป็นกลุ่มของโรคแต่กำเนิดที่เกี่ยวข้องกับการสร้างกระจกตา ม่านตา และเลนส์ตา
มีมากกว่า 50 ยีนที่เกี่ยวข้อง และมีลักษณะที่หลากหลายทั้งในด้านฟีโนไทป์และจีโนไทป์ (heterozygous)
โรคต้อหินทุติยภูมิ จากการพัฒนาทางเดินระบายน้ำอารมณ์ขันไม่สมบูรณ์เป็นภาวะแทรกซ้อนหลักที่พบบ่อย จำเป็นต้องควบคุมความดันลูกตา ตั้งแต่ระยะแรก
มีหน่วยโรคที่แตกต่างกันตามฟีโนไทป์ เช่น วงแหวนเอ็มบริโอหลัง, กลุ่มอาการแอ็กเซนเฟลด์-รีเกอร์, ความผิดปกติของปีเตอร์ส, และภาวะไม่มีม่านตา
ในกรณีที่มีต้อหิน ร่วมด้วย นอกจากการรักษาด้วยยาแล้ว การผ่าตัดมุมลูกตา (การผ่าตัดเปิดมุมลูกตาและการผ่าตัดเปิดช่องระบายน้ำ) เป็นพื้นฐาน
ความผิดปกติของการเคลื่อนที่และการแยกตัวของเซลล์ประสาทคริสต้าเป็นพื้นฐานทางเอ็มบริโอวิทยาที่พบบ่อยในโรคหลายชนิด
ยังคงไม่ทราบยีนที่เป็นสาเหตุใน 40–75% ของผู้ป่วย ซึ่งจำเป็นต้องมีการวิจัยทางพันธุกรรมอย่างต่อเนื่อง
ความผิดปกติของการพัฒนาส่วนหน้าของตา (Anterior Segment Developmental Anomalies; ASD A) เป็นคำรวมสำหรับความผิดปกติของการพัฒนาที่เกี่ยวข้องกับส่วนหน้าของตา ได้แก่ กระจกตา (cornea) ม่านตา (iris) เลนส์แก้วตา (lens) และช่องหน้าตา (anterior chamber) เรียกอีกอย่างว่า “ภาวะการสร้างส่วนหน้าผิดปกติ (Anterior Segment Dysgenesis; ASD )”
ASD A ประกอบด้วยโรคหลักดังต่อไปนี้
วงแหวนหลังเอ็มบริโอ (Posterior embryotoxon: PE) กลุ่มอาการแอ็กเซนเฟลด์-รีเกอร์ (Axenfeld-Rieger syndrome: ARS) ปีเตอร์สอะโนมาลี (Peters anomaly) / ปีเตอร์สพลัสซินโดรม (Peters Plus syndrome) โรคต้อหินแต่กำเนิด ปฐมภูมิ (Primary congenital glaucoma: PCG)ภาวะไม่มีม่านตา (Aniridia) โรคเสื่อมของเยื่อบุผนังกระจกตา ที่ถ่ายทอดทางพันธุกรรมแต่กำเนิด (CHED ) โรคเสื่อมของกระจกตา ชนิดพหุสัณฐานส่วนหลัง (PPM D) กระจกตา คล้ายตาขาว (Sclerocornea)กระจกตาโตแต่กำเนิด (Megalocornea)กลุ่มอาการเยื่อบุผนังกระจกตา -ม่านตา (ICE syndrome) กลุ่มอาการม่านตา และมุมตาพัฒนาผิดปกติ กลุ่มอาการม่านตา คว่ำแต่กำเนิด โรคกระจกตา ทรงกรวยด้านหลัง (Posterior keratoconus)
โรคเหล่านี้มีความหลากหลายทั้งในด้านฟีโนไทป์และจีโนไทป์ โดยพบว่ามียีนมากกว่า 50 ชนิดที่เกี่ยวข้อง ความรู้ทางพันธุกรรมยังคงขยายตัวอย่างต่อเนื่องจากการวิเคราะห์เอ็กโซมและจีโนมทั้งหมด แต่ยังคงไม่สามารถระบุยีนที่เป็นสาเหตุได้ใน 40–75% ของผู้ป่วย กรณีที่ไม่สามารถจำแนกเป็นฟีโนไทป์เฉพาะได้จะถูกบันทึกเป็น “ASD ที่ไม่สามารถจำแนกประเภท (unclassified ASD )” 1)
อารมณ์ขันที่เป็นน้ำ (aqueous humor) ที่ผลิตจากซิลิอารีบอดี ของม่านตา จะถูกระบายออกผ่าน trabecular meshwork ไปยังคลองชเลมม์ (Schlemm’s canal) และทางเดินระบายออกทางยูเวียสเคลอรัล (uveoscleral outflow) ใน ASD A กระบวนการนี้มักเกิดความผิดปกติ ทำให้ต้อหินทุติยภูมิ (secondary glaucoma) เป็นภาวะแทรกซ้อนที่สำคัญร่วมกัน
กรณีที่มีเฉพาะ posterior embryotoxon โดยไม่มีอาการทางระบบ จะถูกแยกออกจาก ARS ตามรายงานฉันทามติครั้งที่ 9 ของสมาคมต้อหิน โลก 1)
โรคต้อหินจากพัฒนาการ (developmental glaucoma) ถูกนิยามในแนวทางเวชปฏิบัติโรคต้อหิน ของญี่ปุ่นว่าเป็น “โรคต้อหิน ที่เกิดจากความผิดปกติของพัฒนาการของทางระบายอารมณ์ขันน้ำ” แบ่งตามระยะเวลาที่เกิดเป็นชนิดเริ่มต้นเร็ว (ตรงกับโรคต้อหินแต่กำเนิด ปฐมภูมิ) และชนิดเริ่มต้นช้า ความถี่ของโรคต้อหินจากพัฒนาการ ชนิดเริ่มต้นเร็วในญี่ปุ่นพบได้น้อยมาก คือ 1 ใน 100,000 คน ร้อยละ 75 เป็นสองตา และร้อยละ 65 ของผู้ป่วยเป็นเพศชาย ร้อยละ 80 ของผู้ป่วยเกิดอาการภายในปีแรกของชีวิต
Q
ความผิดปกติของพัฒนาการส่วนหน้าของตา (ASDA) มักได้รับการวินิจฉัยเมื่ออายุเท่าใด?
A
ขึ้นอยู่กับโรค โรคต้อหินแต่กำเนิด ปฐมภูมิมักเกิดอาการภายในปีแรกของชีวิต กลุ่มอาการแอ็กเซนเฟลด์-รีเกอร์และปีเตอร์สแอบนอร์มอลลิตี้มักได้รับการวินิจฉัยตั้งแต่แรกเกิด โรคต้อหินจากพัฒนาการ ชนิดเริ่มต้นช้าอาจเกิดอาการช้าถึงช่วงอายุ 10-20 ปี การตรวจพบและการรักษาตั้งแต่เนิ่นๆ มีความสำคัญในทุกกรณี
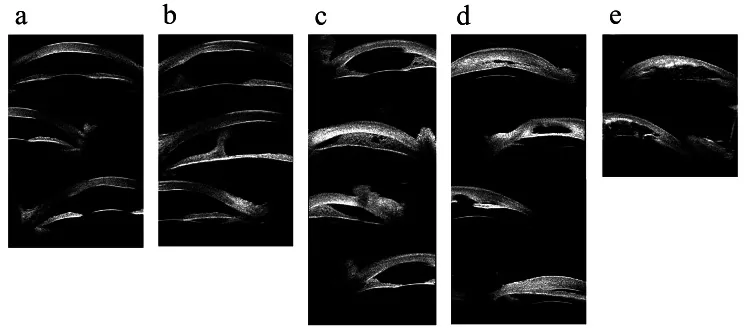
ภาพจากกล้องจุลทรรศน์อัลตราซาวนด์ชีวภาพของความผิดปกติของส่วนหน้าของตา Hong J, et al. Classifications of anterior segment structure of congenital corneal opacity in infants and toddlers by ultrasound biomicroscopy and slit-lamp microscopic photographs: an observational study. BMC Ophthalmol. 2024. Figure 1. PM
CI D: PMC10804776. License: CC BY.
(a) กระจกตา ขุ่นมัว (b) กระจกตา ขุ่นมัวร่วมกับการยึดติดด้านหน้าส่วนกลาง (c) การยึดติดของม่านตา กับกระจกตา ส่วนปลายน้อยกว่า 180 องศา (d) การยึดติดของม่านตา กับกระจกตา ส่วนปลายมากกว่า 180 องศา (e) กระจกตา ขุ่นมัวร่วมกับความผิดปกติของม่านตา และเลนส์แก้วตา จากภาพกล้องจุลทรรศน์อัลตราซาวนด์ชีวภาพ ซึ่งสอดคล้องกับการยึดติดของส่วนหน้าของตาและกระจกตา ขุ่นมัวที่กล่าวถึงในหัวข้อ “2. อาการหลักและผลการตรวจทางคลินิก”
ในวัยทารกและเด็กเล็ก อาการต่อไปนี้ที่เกิดจากความดันลูกตา สูงมักพบเป็นอาการเริ่มแรก
น้ำตาไหล (การหลั่งน้ำตามากเกินไป) : เกิดจากการระคายเคืองจากภาวะบวมน้ำที่เยื่อบุกระจกตา อันเนื่องมาจากความดันลูกตา สูงกลัวแสง (ไวต่อแสง ) : อาการที่สะท้อนถึงการระคายเคืองของกระจกตา การกระตุกของเปลือกตา : เกิดขึ้นจากกลไกเดียวกับน้ำตาไหลและกลัวแสง
ในเด็กโตและผู้ใหญ่ อาจมีอาการตามัวหรือสายตาเลือนรางตั้งแต่อายุยังน้อยในกรณีที่เริ่มมีอาการช้า หากความดันลูกตา สูงมาก อาจมีอาการปวดตา หรือปวดศีรษะ ในภาวะไม่มีม่านตา อาจมีอาการไวต่อแสง (ตาบอดกลางวัน)
ตาโต (เส้นผ่านศูนย์กลางกระจกตา เพิ่มขึ้น) หรือกระจกตา ขุ่นมัว มักเป็นสาเหตุให้ผู้ปกครองสังเกตพบและนำผู้ป่วยมาพบแพทย์
ASD A แสดงอาการทางคลินิกที่จำเพาะต่อแต่ละโรค อาการหลักของโรคที่เป็นตัวแทนแสดงไว้ด้านล่าง
วงแหวนหลังเอ็มบริโอ・ARS
วงแหวนหลังเอ็มบริโอ (PE) : เส้นของชวาลเบอ (Schwalbe’s line) ที่เคลื่อนไปข้างหน้าและหนาตัวขึ้น ตรวจพบด้วยกล้องจุลทรรศน์ชนิดกรีดเป็นเส้นสีขาวเทาเป็นวงกลมร่วมศูนย์กลางด้านในของลิมบัส กระจกตา
ความผิดปกติแบบแอ็กเซนเฟลด์ : วงแหวนหลังเอ็มบริโอร่วมกับการยึดเกาะของเนื้อเยื่อม่านตา ส่วนปลายเป็นเส้น
ความผิดปกติแบบรีเกอร์ : นอกเหนือจากข้างต้น ยังมีม่านตา ผิดรูปเนื่องจากเนื้อเยื่อม่านตา ชั้นกลางเจริญไม่สมบูรณ์ ทำให้รูม่านตา เบี่ยงเบน เยื่อบุผิวม่านตา พลิกกลับ และมีรูม่านตา ปลอมหลายรู เป็นลักษณะการถ่ายทอดทางพันธุกรรมแบบออโตโซมิดีเด่น พบต้อหิน ร่วมด้วยร้อยละ 50-60
ความผิดปกติของปีเตอร์ส
ความขุ่นของกระจกตา ส่วนกลาง : เป็นลักษณะที่จำเป็นสำหรับการวินิจฉัย สะท้อนถึงความบกพร่องของเซลล์เยื่อบุผนังกระจกตา ชั้นเดสเซเมต และเนื้อกระจกตา
ชนิดที่ 1 : มีเพียงความบกพร่องของชั้นหลังกระจกตา และความขุ่นของกระจกตา
ชนิดที่ 2 : ร่วมกับการยึดติดของม่านตา
ชนิดที่ 3 : มีการเคลื่อนไปข้างหน้าของเลนส์แก้วตา หรือต้อกระจก ประมาณ 80% เป็นทั้งสองข้าง พบต้อหิน ร่วมด้วย 50-70%
ภาวะไม่มีม่านตา
ภาวะม่านตา พัฒนาน้อย : ส่วนใหญ่เป็นการขาดหายของส่วนหลังของม่านตา อาจพบภาวะจอประสาทตา ส่วนกลางพัฒนาน้อย เส้นประสาทตา พัฒนาน้อย และต้อหิน ร่วมด้วย
โรคกระจกตา ที่เกี่ยวข้องกับภาวะไม่มีม่านตา (AAK) : มีรายงานอัตราการเกิด 20-80% หรือมากกว่า เป็นภาวะกระจกตา ขุ่นแบบลุกลามจากภาวะเซลล์ต้นกำเนิดบริเวณขอบกระจกตา ล้มเหลว (LSCD ) ซึ่งจะลุกลามไปตลอดชีวิต 2)
กลุ่มอาการ WAGR : เกิดจากการกลายพันธุ์ของยีน PAX6 และ WT1 ที่อยู่ติดกัน ประกอบด้วยเนื้องอกวิลม์ส, ภาวะไม่มีม่านตา , ความผิดปกติของระบบสืบพันธุ์และทางเดินปัสสาวะ, และภาวะพัฒนาการทางสติปัญญาล่าช้า 3)
ชนิดความผิดปกติของกระจกตา
กระจกตา โตผิดปกติ (Megalocornea)กระจกตา ตั้งแต่ 13 มม. ขึ้นไป (ในทารกแรกเกิดตั้งแต่ 12 มม. ขึ้นไป) โดยปกติความดันลูกตา และความหนาแน่นของเซลล์เยื่อบุผิวยังปกติ มักถ่ายทอดทางพันธุกรรมแบบ X-linked recessive
กระจกตา กลายเป็นตาขาว (Sclerocornea)ตาขาว ทึบแสงรุกล้ำเข้าไปในกระจกตา ส่วนรอบ ขอบเขตระหว่างตาขาว และกระจกตา ไม่ชัดเจน และมีเส้นเลือดเจริญเข้าไป
CHED กระจกตา แบบสมมาตรทั้งสองข้างปรากฏตั้งแต่แรกเกิดถึงอายุ 1-2 ปี ไม่มีความดันลูกตา สูงร่วมด้วย ถ่ายทอดทางพันธุกรรมแบบ autosomal recessive
อาการที่เพิ่มขึ้นเมื่อมีภาวะต้อหินทุติยภูมิ ร่วมแสดงดังต่อไปนี้
ความดันลูกตา สูงความดันลูกตา สูง (ประมาณ 30-50 mmHg)เส้นผ่านศูนย์กลางกระจกตา เพิ่มขึ้น (ตาวัว) : เกิดจากการยืดขยายของเยื่อหุ้มลูกตา หากเกิน 12.0 มม. ทันทีหลังคลอด ให้สงสัยต้อหิน แต่กำเนิดเส้น Haab : ความขุ่นเป็นเส้นถาวรที่เหลืออยู่บริเวณที่เยื่อเดสเซเมต์แตกการขยายของรอยบุ๋มจานประสาทตา : ในทารกและเด็กเล็ก หากอัตราส่วน C/D มากกว่า 0.3 ให้สงสัยโรคต้อหิน ความแตกต่างระหว่างตาทั้งสองข้างมากกว่า 0.2 ก็เป็นสิ่งที่ทำให้สงสัย
Q
กลุ่มอาการแอ็กเซนเฟลด์-รีเกอร์ทำให้เกิดต้อหินในผู้ป่วยกี่เปอร์เซ็นต์?
A
ต้อหิน เกิดขึ้นใน 50-60% (รายงานบางฉบับระบุ 50-75%) ซึ่งมีความถี่สูง 3) มีรูปแบบการถ่ายทอดทางพันธุกรรมแบบออโตโซมเด่น ผู้ที่มีอาการทางระบบ (ความผิดปกติของฟัน กระดูกใบหน้า ต่อมใต้สมอง ฯลฯ) เรียกว่ากลุ่มอาการรีเกอร์ แนะนำให้ตรวจคัดกรองต้อหิน ในญาติ
สาเหตุหลักของ ASD A คือความผิดปกติทางพันธุกรรม ซึ่งเกี่ยวข้องกับยีนและรูปแบบการถ่ายทอดทางพันธุกรรมที่แตกต่างกันในแต่ละโรค ยีนที่ก่อให้เกิดโรคหลักแสดงไว้ด้านล่าง
โรค ยีนก่อโรคหลัก รูปแบบการถ่ายทอดทางพันธุกรรม ARS PITX2 (4q25), FOXC1 (6p25) ถ่ายทอดทางพันธุกรรมแบบเด่นบนออโตโซม ปีเตอร์สอะนอมอลี PAX6, PITX2, CYP1B1 ประปราย, เด่น, ด้อย ต้อหิน แต่กำเนิดปฐมภูมิCYP1B1 (GLC3A), LTBP2 (GLC3C) ถ่ายทอดแบบออโตโซมอลรีเซสซีฟ ภาวะไม่มีม่านตา PAX6 (โครโมโซมที่ 11) ถ่ายทอดแบบออโตโซมอลโดมิแนนต์ CHED SLC4A11, ZEB 1 ถ่ายทอดทางพันธุกรรมแบบด้อยในออโตโซม กระจกตาโตแต่กำเนิด CHRDL1 ถ่ายทอดทางพันธุกรรมแบบด้อยบนโครโมโซม X
นอกจากนี้ ยังมีรายงานโรคต้อหิน ในเด็กที่เกี่ยวข้องกับความผิดปกติของยีน เช่น PAX6, PITX2, FOXC1 ความสัมพันธ์ระหว่างจีโนไทป์และฟีโนไทป์มีความหลากหลาย แม้ในครอบครัวเดียวกันที่มีความผิดปกติของยีนเดียวกัน ฟีโนไทป์อาจแตกต่างกันได้
โรคต้อหิน ในเด็กชนิดเริ่มต้นเร็ว (primary congenital glaucoma) ส่วนใหญ่เป็นแบบประปราย แต่ประมาณ 10% มีรูปแบบการถ่ายทอดทางพันธุกรรมแบบออโตโซมัลด้อย นอกจากนี้ยังมีทฤษฎีว่าอาจเกิดจากหลายปัจจัยร่วมกัน
เซลล์นิวรัลครีสต์ (neural crest cells) มีบทบาทสำคัญในการสร้างส่วนหน้าของดวงตา เซลล์ trabecular meshwork มีต้นกำเนิดจากนิวรัลครีสต์ ส่วนเนื้อเยื่อเกี่ยวพันรอบคลองชเลมม์ มีต้นกำเนิดจากเซลล์บุผนังหลอดเลือด จุดที่เนื้อเยื่อทั้งสองชนิดซึ่งมีต้นกำเนิดต่างกันมาบรรจบกันเป็นจุดที่มีความต้านทานต่อการไหลของอารมณ์ขันน้ำมากที่สุด กลุ่มอาการ Axenfeld-Rieger , Peters anomaly, และ congenital iris ectropion syndrome ล้วนเป็นความผิดปกติแต่กำเนิดที่เกิดจากการเคลื่อนย้ายที่ผิดปกติของเซลล์นิวรัลครีสต์
การศึกษาในเกาหลีใต้ขนาดใหญ่พบว่าการเพิ่มขึ้นของการสัมผัส PM2.5 (ฝุ่นละอองขนาดเล็ก) ของมารดาในช่วง 3 เดือนก่อนปฏิสนธิและในช่วงไตรมาสที่ 1 และ 2 ของการตั้งครรภ์สัมพันธ์กับความเสี่ยงที่เพิ่มขึ้นของ ASD A ในบุตร
ในโรคที่ถ่ายทอดทางพันธุกรรมแบบออโตโซมัลเด่น เช่น ARS และ aniridia การตรวจตา (รวมถึงการวัดความดันตาและการตรวจมุมตา ) ของญาติที่ป่วยมีประโยชน์ ในกรณี aniridia ที่เกิดขึ้นเป็นครั้งแรกในครอบครัว แนะนำให้เด็กได้รับการตรวจคัดกรอง Wilms tumor โดยกุมารแพทย์จนถึงอายุ 6 ปี ควรพิจารณาปรึกษาแพทย์ผู้เชี่ยวชาญด้านพันธุกรรมด้วย
การวินิจฉัย ASD A ส่วนใหญ่ทำทางคลินิก ในเด็กอายุต่ำกว่า 5 ปี มักต้องทำการตรวจภายใต้การดมยาสลบหรือการสะกดจิต
การตรวจด้วยกล้องจุลทรรศน์ชนิดกรีดแสง (Slit-lamp microscopy)กระจกตา การมีหรือไม่มีเส้น Haab ความลึกของช่องหน้าม่านตา ความผิดปกติของม่านตา (วงแหวนตัวอ่อนส่วนหลัง การยึดเกาะของม่านตา กับเส้น Schwalbe) และความผิดปกติของเลนส์ตา ตรวจสอบการมีวงแหวนตัวอ่อนส่วนหลัง ความผิดปกติของม่านตา (ARS) และต้อกระจก (ความผิดปกติของ Peters)การวัดความดันลูกตา เครื่องวัดความดันลูกตาแบบรีบาวด์ (iCare) หรือเครื่องวัดความดันลูกตา แบบพกพา (Tonopen) มีประโยชน์ ควรระวังว่าความดันลูกตา ลดลงภายใต้การดมยาสลบ ค่าที่วัดได้จากเครื่องวัดต่างชนิดกันไม่สามารถใช้แทนกันได้การวัดเส้นผ่านศูนย์กลางกระจกตา : วัดเส้นผ่านศูนย์กลางแนวนอนและแนวตั้งด้วยคาลิปเปอร์ ค่าปกติในทารกแรกเกิดคือ 9.5–10.5 มม. หากเกิน 12.0 มม. ทันทีหลังคลอด ให้สงสัยโรคต้อหินแต่กำเนิด การตรวจมุมลูกตา : ใช้โคมไฟกรีดแบบมือถือและ gonioscope ชนิดตรง เช่น Koelee lens ประเมินการเกาะสูงของม่านตา การเกาะของม่านตา ที่เส้น Schwalbe (ARS) และความกว้างของ trabecular meshworkการตรวจอวัยวะภายในลูกตา : สังเกตการบุ๋มของหัวประสาทตา ในทารกและเด็กเล็ก หาก C/D ratio ≥ 0.3 ให้สงสัยโรคต้อหิน การลดลงของความบุ๋มหัวประสาทตาหลังจากลดความดันลูกตา เป็นสัญญาณของการควบคุมความดันที่ดีกล้องจุลทรรศน์อัลตราซาวนด์ชีวภาพ (UBM ) : มีประโยชน์ในกรณีที่มองเห็นมุมตาได้ยากเนื่องจากกระจกตา ขุ่น ช่วยประเมินความผิดปกติของมุมตาและพยากรณ์ผลการผ่าตัดสร้างทางระบายน้ำOCT ส่วนหน้าของตา (AS-OCT )กระจกตา แบบไม่รุกรานได้ แต่ไม่สามารถใช้แทนการตรวจ gonioscopy ในการวินิจฉัย 3) การตรวจลานสายตา โรคเส้นประสาทตา จากต้อหิน ในเด็ก ในเด็กอายุต่ำกว่า 5 ปี แม้ผู้ตรวจที่มีความชำนาญก็ทำได้ยาก การตรวจลานสายตา แบบพลวัตทำได้ง่ายกว่า
ตามแนวทางเวชปฏิบัติโรคต้อหิน ฉบับที่ 4 ของสมาคมโรคต้อหิน แห่งญี่ปุ่น การวินิจฉัยโรคต้อหิน ในเด็กจะพิจารณาเมื่อมีข้อต่อไปนี้อย่างน้อย 2 ข้อ
ความดันลูกตา > 21 มิลลิเมตรปรอทการเพิ่มขึ้นของอัตราส่วน C/D ที่ดำเนินไป ความแตกต่างของอัตราส่วน C/D ระหว่างตาข้างซ้ายและขวา ≥ 0.2 การบางลงของขอบประสาทตา
ลักษณะของกระจกตา : เส้น Haab หรือในทารกแรกเกิดเส้นผ่านศูนย์กลางกระจกตา ตั้งแต่ 11 มิลลิเมตรขึ้นไป ในเด็กอายุต่ำกว่า 1 ปีตั้งแต่ 12 มิลลิเมตรขึ้นไป และในทุกอายุตั้งแต่ 13 มิลลิเมตรขึ้นไป
การลุกลามของสายตาสั้น เนื่องจากการยืดตัวของความยาวแกนลูกตา ที่เกินกว่าการพัฒนาปกติ
ข้อบกพร่องของลานสายตาที่สามารถทำซ้ำได้ซึ่งสอดคล้องกับโรคเส้นประสาทตา จากต้อหิน
การแยกโรคจากภาวะที่มีความขุ่นของกระจกตา และการขยายขนาดเส้นผ่านศูนย์กลางกระจกตา แสดงดังต่อไปนี้
กระจกตา โต (Megalocornea)ความดันลูกตา สูง ไม่มีตุ่มรับภาพขยาย ไม่มีเส้น Haab มุมลูกตาปกติกระจกตา กลายเป็นตาขาว (Sclerocornea)ตาขาว ทึบแสงและเส้นเลือดงอกเข้าไปCHED กระจกตา บวมทั้งสองข้างเท่ากัน ไม่มีความดันลูกตา สูงโรคกระจกตา เสื่อมแบบพหุสัณฐานส่วนหลัง (Posterior polymorphous corneal dystrophy) : ไม่มีเส้นผ่านศูนย์กลางกระจกตา เพิ่มขึ้น การตรวจเยื่อบุผิวกระจกตา มีประโยชน์ในการวินิจฉัยการบาดเจ็บจากการคลอดด้วยคีม : ความขุ่นเป็นเส้นตรงแนวตั้งหรือแนวเฉียงในตาข้างเดียวโรคเมตาบอลิก เช่น โรคเมือกโพลีแซ็กคาไรด์สะสม โรคซิสตินูเรีย : การประเมินอาการทั่วร่างกายมีความสำคัญในการวินิจฉัยแยกโรค
กลุ่มโรคที่รวมอยู่ใน ASD (ความผิดปกติของ Axenfeld-Rieger, ความผิดปกติของ Peters, ภาวะไม่มีม่านตา , โรคจอประสาทตา เสื่อมชนิดหลังหลายรูปแบบ, ตาเล็ก, กระจกตา เล็ก เป็นต้น) จำเป็นต้องพิจารณาร่วมกันในการวินิจฉัยแยกโรค 3)
Q
ภาวะ posterior embryotoxon เพียงอย่างเดียวสามารถเกิดร่วมกับโรคต้อหินได้หรือไม่?
A
กรณีที่มี posterior embryotoxon เพียงอย่างเดียว (ไม่มีอาการทางระบบ) จะแตกต่างจาก ARS แต่ก็เป็นหนึ่งในอาการร่วมของ ARS ได้ posterior embryotoxon สามารถพบได้ในตาปกติ และไม่ได้บ่งชี้ถึงความเสี่ยงต่อโรคต้อหิน เสมอไป อย่างไรก็ตาม หากพบร่วมกับโรคอื่น เช่น Alagille syndrome จำเป็นต้องติดตามความดันลูกตา
การรักษาโรคต้อหิน ที่เกิดจาก ASD A เป็นไปตามแนวทางการรักษาโรคต้อหินแต่กำเนิด ปฐมภูมิ (PCG)
การรักษาด้วยยา เป็นการรักษาเสริมเพื่อลดความดันลูกตา ในระยะสั้นก่อนการผ่าตัดและควบคุมความดันลูกตา หลังผ่าตัด การเลือกใช้ยาโดยทั่วไปเหมือนกับโรคต้อหินมุมเปิด ในผู้ใหญ่ อย่างไรก็ตาม ต้องระวังการใช้ยา beta-blocker ในผู้ป่วยโรคหอบหืดหรือหัวใจเต้นช้า และมีรายงานภาวะหยุดหายใจในทารกแรกเกิด สามารถใช้ acetazolamide รับประทาน (5-10 มก./กก. ทุก 6-8 ชั่วโมง) ได้
โรคต้อหินแต่กำเนิด ชนิดเริ่มต้นโดยทั่วไปจำเป็นต้องการผ่าตัดรักษา การรักษาด้วยยาเป็นเพียงการเสริม
การผ่าตัดเปิดมุมลูกตา (goniotomy) : เหมาะสำหรับการผ่าตัดครั้งแรกในผู้ป่วยที่กระจกตา ขุ่นเล็กน้อย ข้อดีคือไม่กระทบต่อเยื่อบุตา ใช้เลนส์ Barkan หรือ Swan-Jacob และใช้มีดผ่าตัดมุมลูกตาขูดผิวของ trabecular meshworkการผ่าตัดเปิดช่อง trabecular meshwork (trabeculotomy) : สามารถทำได้ไม่ว่ากระจกตา จะขุ่นหรือไม่ก็ตาม ใช้เป็นการผ่าตัดเพิ่มเติมเมื่อการผ่าตัดเปิดมุมตา (goniotomy) ได้ผลไม่เพียงพอการผ่าตัด trabeculectomy และการผ่าตัดใส่ท่อระบายน้ำ (tube shunt) : เป็นทางเลือกเมื่อการผ่าตัดมุมตาไม่ได้ผล ใน ARS หากมุมตาเปิดและไม่มีการปิดคลุม trabecular meshwork จากการยึดติดของม่านตา ส่วนปลายมากเกินไป จะเลือกผ่าตัดมุมตา แต่อัตราความสำเร็จต่ำกว่า PCG ในกรณีที่ผ่าตัดมุมตาไม่ได้ผล การผ่าตัด trabeculectomy หรือการผ่าตัดใส่ท่อระบายน้ำแบบมีแผ่นรองอาจเป็นทางเลือกแรก 4)
ในปีเตอร์สอะนอมอลี (Peters anomaly) ให้การรักษาตามแนวทางเดียวกับ PCG แต่สัดส่วนของผู้ป่วยที่ได้ความดันลูกตา ที่ดีหลังผ่าตัดมีเพียงประมาณ 1 ใน 3 ของผู้ที่ได้รับการผ่าตัด และมักมีพยากรณ์โรคไม่ดี เนื่องจากมีความผิดปกติของกระจกตา ร่วมด้วย จึงมักยากที่จะได้การมองเห็น ที่ใช้งานได้จริง 4)
โรคต้อหิน ที่เกิดร่วมกับภาวะไม่มีม่านตา (aniridia) ก็รักษาตามแนวทางเดียวกับ PCG 4)
ปีเตอร์ส อนอร์มอลลิตี้ (Peters anomaly) : ในรายที่ไม่รุนแรง ภาวะกระจกตา ขุ่นมักจะค่อยๆ ลดลงเอง หากความดันลูกตา ปกติก็มักจะดีขึ้นบ้าง และเนื่องจากผลการผ่าตัดปลูกถ่ายกระจกตา ไม่ดี จึงมักไม่ทำการปลูกถ่ายกระจกตา ในเด็กเล็ก ผู้ป่วยจำนวนมากดื้อต่อการรักษาด้วยยาโรคต้อหิน และแม้จะผ่าตัดสร้างทางระบายน้ำออกใหม่ก็ยังควบคุมได้ยาก มีพยากรณ์โรคไม่ดี
CHED กระจกตา ล้มเหลว การปลูกถ่ายกระจกตา (รวมถึงการปลูกถ่ายชั้นบุผนังกระจกตา ) อาจเป็นข้อบ่งชี้
กระจกตา คล้ายตาขาว (Sclerocornea)ASD อื่นๆ ในรายที่รุนแรงอาจเป็นข้อบ่งชี้ในการปลูกถ่ายกระจกตา
อาการกลัวแสง และเมื่อยล้าทางตาโรคกระจกตา ที่เกี่ยวข้องกับภาวะไม่มีม่านตา (AAK) : สำหรับภาวะกระจกตา ขุ่นที่ลุกลาม อาจพิจารณาการปลูกถ่ายเซลล์ต้นกำเนิดบริเวณลิมบัส ของกระจกตา การตรวจคัดกรองเนื้องอกวิลมส์ : หากพบภาวะไม่มีม่านตา ชนิดประปราย ควรส่งต่อผู้ป่วยไปยังกุมารแพทย์ และแนะนำให้ตรวจคัดกรองจนถึงอายุ 6 ปี 4)
แม้ความดันลูกตา จะลดลงแล้ว แต่มักยังจำเป็นต้องรักษาภาวะตามัว เนื่องจากภาวะสายตายาว ต่างกัน สายตาเอียง ไม่สม่ำเสมอ กระจกตา ขุ่นมัว หรือเส้น Haab อาจเป็นสาเหตุของภาวะตามัว จึงควรตรวจวัดสายตาและค่าสายตาควบคู่ไปกับการวัดความดันลูกตา อย่างต่อเนื่อง การลุกลามของสายตาสั้น และการยืดตัวของความยาวแกนตา อาจบ่งชี้ถึงการลุกลามของโรคต้อหิน จึงจำเป็นต้องวัดเป็นระยะ
การสร้างส่วนหน้าของดวงตาปกติเป็นไปตามโปรแกรมการพัฒนาที่ซับซ้อน จุดเริ่มต้นของการพัฒนาอวัยวะรับภาพคือการสร้างร่องตา (optic sulcus) บนแผ่นประสาทในช่วงต้นสัปดาห์ที่ 3 ของการตั้งครรภ์ ตุ่นตา (optic vesicle) ก่อตัวขึ้นในช่วงปลายสัปดาห์ที่ 3 และถ้วยตา (optic cup) ก่อตัวขึ้นในสัปดาห์ที่ 4 การปิดของรอยแยกของตาเริ่มขึ้นประมาณสัปดาห์ที่ 6 และเสร็จสมบูรณ์ในสัปดาห์ที่ 7 เนื้อเยื่อมีเซนไคม์ที่ปกคลุมด้านหน้าของเลนส์ตาแยกตัวออกเพื่อสร้างช่องหน้าม่านตา
เซลล์คริสตานิวรัล (neural crest cells) หลุดออกจากแนวประสาท (neural crest) และผ่านกระบวนการเปลี่ยนจากเยื่อบุผิวเป็นมีเซนไคม์ (epithelial-mesenchymal transition) เพื่อย้ายไปยังตำแหน่งต่างๆ ภายในดวงตา เซลล์ trabecular meshwork มีต้นกำเนิดจากคริสตานิวรัล ส่วนเนื้อเยื่อเกี่ยวพันรอบคลองชเลมม์ (Schlemm’s canal) มีต้นกำเนิดจากเซลล์บุผนังหลอดเลือด ความแตกต่างของต้นกำเนิดนี้ก่อให้เกิดบริเวณที่มีความต้านทานต่อการไหลของอารมณ์ขันน้ำ (aqueous humor) มากที่สุด
PAX6 : “ตัวควบคุมหลัก” ในการพัฒนาของดวงตา อยู่บนโครโมโซมที่ 11 เกี่ยวข้องกับภาวะไม่มีม่านตา (aniridia), ปีเตอร์สแอนอมาลี (Peters anomaly), และกลุ่มอาการเอ็กโทรเปียนยูเวียแต่กำเนิด (congenital ectropion uveae syndrome)PITX2 : ปัจจัยการถอดรหัส อยู่บนโครโมโซมที่ 4 (4q25) เกี่ยวข้องกับทั้งอาการทางตาและการได้ยินใน ARSFOXC1 : ปัจจัยการถอดรหัส อยู่บนโครโมโซมที่ 6 (6p25) เกี่ยวข้องกับ ARS และเช่นเดียวกับ PITX2 สัมพันธ์กับทั้งอาการทางตาและการได้ยินCYP1B1 : เอนไซม์ในตระกูลไซโตโครม P450 (ตำแหน่ง GLC3A) เกี่ยวข้องกับโรคต้อหินแต่กำเนิด ปฐมภูมิ ความผิดปกติของปีเตอร์ส และกระจกตา คล้ายตาขาว CHRDL1 : เกี่ยวข้องกับการพัฒนาของเนื้อกระจกตา และเยื่อบุผนังกระจกตา เป็นยีนที่ทำให้เกิดโรคกระจกตา โตแบบเชื่อมโยงกับโครโมโซม XB3GLCT : ยีนที่ทำให้เกิดกลุ่มอาการปีเตอร์ส พลัส เกี่ยวข้องกับความบกพร่องในการเติมน้ำตาล ถ่ายทอดทางพันธุกรรมแบบออโตโซมอลด้อย
โรคต้อหินทุติยภูมิ ใน ASD A เกิดจากกลไกหลักคือความผิดปกติของทางระบายน้ำอารมณ์ขัน โดยมีปัจจัยหลายอย่างร่วมกันดังนี้
ความยังไม่สมบูรณ์ของ trabecular meshwork: เนื้อเยื่อเกี่ยวพันรอบคลอง Schlemm หนาผิดปกติ และมีการสะสมของ extracellular matrix มากเกินไป
การยึดเกาะของเลนส์ปรับตา (ciliary body) กับบริเวณ trabecular meshwork: การหดตัวของกล้ามเนื้อเลนส์ปรับตาดึง scleral spur ไปข้างหน้า ทำให้กดทับคลอง Schlemm และ trabecular meshwork
การยึดเกาะของโคนม่านตา ในตำแหน่งสูง: โคนม่านตา อยู่ในตำแหน่งของ trabecular meshwork ขัดขวางการไหลออกของอารมณ์ขัน
การสร้างคลองชเลมม์ น้อยหรือไม่มีเลย
ICE syndrome มีสาเหตุการเกิดโรคที่แตกต่างจาก ASD A อื่น มีการเสนอทฤษฎีไวรัสที่เกี่ยวข้องกับเชื้อ herpes simplex virus (HS V) ในการทำให้เซลล์เยื่อบุผนังกระจกตา เสื่อม แต่ยังไม่ได้รับการยืนยัน โรคนี้เกิดขึ้นภายหลังในผู้ใหญ่ตอนกลาง (พบในผู้หญิงบ่อยกว่าเล็กน้อย) และมักเป็นข้างเดียว ซึ่งแตกต่างจาก ASD A อื่น
ผู้ป่วยภาวะไม่มีม่านตา มีแนวโน้มที่จะเกิดความขุ่นของกระจกตา ที่ดำเนินไปตลอดชีวิต กลไกหลักคิดว่าเกิดจากภาวะพร่องเซลล์ต้นกำเนิดลิมบัส (limbal stem cell deficiency; LSCD ) การศึกษาหลายชิ้นที่ยืนยันการกลายพันธุ์ของ PAX6 ได้บันทึกการเปลี่ยนแปลงที่ดำเนินไปนี้ อัตราการเกิดรายงานอยู่ที่ 20–80% หรือมากกว่า มักเกิดขึ้นแบบสมมาตรแต่ไม่เสมอไป 2)
เนื้อหาต่อไปนี้อยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิกเท่านั้น และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับการพัฒนาทางการแพทย์ในอนาคต
การวิเคราะห์เอ็กโซมและการวิเคราะห์จีโนมทั้งหมดกำลังเร่งระบุยีนที่เกี่ยวข้องใหม่ ยังคงมีผู้ป่วย 40-75% ที่ไม่สามารถระบุยีนก่อโรคได้ และการวิเคราะห์ “กรณีที่ไม่ทราบสาเหตุ” ที่เหลืออยู่เป็นประเด็นสำคัญในอนาคต การอธิบายความสัมพันธ์ระหว่างจีโนไทป์และฟีโนไทป์ทางคลินิกคาดว่าจะนำไปสู่การประยุกต์ใช้ในการแพทย์เฉพาะบุคคล
ในผู้ป่วยที่มีการกลายพันธุ์ของ FOXC1 และ PITX2 อายุที่เริ่มเป็นโรคต้อหิน และลักษณะทางคลินิกมีความหลากหลาย แม้ว่าจีโนไทป์อาจสัมพันธ์กับความหลากหลายของฟีโนไทป์ แต่การกลายพันธุ์ของยีนเดียวกันก็สามารถแสดงโรคในรูปแบบที่แตกต่างกัน ทำให้การวินิจฉัยและการพยากรณ์โรคเป็นเรื่องยาก 1)
อุบัติการณ์ของโรคกระจกตา ในภาวะไม่มีม่านตา แต่กำเนิด (AAK) รายงานว่าอยู่ที่ 20–80% หรือมากกว่า และการศึกษาหลายชิ้นที่ยืนยันการกลายพันธุ์ของ PAX6 ได้บันทึกการลุกลามของความขุ่นของกระจกตา ตลอดชีวิต การวิจัยเกี่ยวกับการปลูกถ่ายเซลล์ต้นกำเนิดบริเวณลิมบัส ของกระจกตา ที่มุ่งเป้าไปที่ LCSD กำลังก้าวหน้า แต่ในปัจจุบันยังอยู่ในขั้นตอนการวิจัยและยังไม่ได้รับการยอมรับให้เป็นการรักษามาตรฐาน 2)
การศึกษาทางระบาดวิทยาแสดงให้เห็นถึงความสัมพันธ์ระหว่างการสัมผัสมลพิษทางอากาศ (PM2.5) ก่อนและระหว่างตั้งครรภ์กับความเสี่ยงของ ASD A ซึ่งกำลังมีการสำรวจการประยุกต์ใช้ในด้านสาธารณสุขจากมุมมองของเวชศาสตร์ป้องกันสิ่งแวดล้อม ซึ่งอาจนำไปสู่กลยุทธ์การป้องกันในอนาคต
การประยุกต์ใช้เลเซอร์ไมโครพัลส์และอุปกรณ์ผ่าตัดต้อหิน รุกรานน้อยที่สุด (MIGS ) ในเด็ก ASD A อยู่ในขั้นตอนการวิจัย ข้อมูลผลลัพธ์ระยะยาวมีจำกัด และยังไม่มีการกำหนดประสิทธิภาพและความปลอดภัยที่เทียบเท่ากับต้อหิน ในผู้ใหญ่
Knight LSW, Ruddle JB, Taranath DA, et al. Childhood and Early Onset Glaucoma Classification and Genetic Profile in a Large Australasian Disease Registry. Ophthalmology. 2021;128(11):1549-1560. doi:10.1016/j.ophtha.2021.04.016.
Hu JCW, Trief D. A narrative review of limbal stem cell deficiency & severe ocular surface disease. Ann Eye Sci. 2023;8:13. doi:10.21037/aes-22-35. https://aes.amegroups.org/article/view/7385/html
European Glaucoma Society. Terminology and guidelines for glaucoma, 6th Edition. Br J Ophthalmol. 2025;109(Suppl 1):1-225. doi:10.1136/bjophthalmol-2025-egsguidelines.
日本緑内障学会緑内障診療ガイドライン作成委員会. 緑内障診療ガイドライン第5版.