ภาวะไม่มีม่านตา เป็นภาวะแต่กำเนิดที่ม่านตา ขาดหายไปทั้งหมดหรือบางส่วน โดยมีความชุกประมาณ 1 ใน 64,000 ถึง 96,000 คน และเป็นโรคหายากที่กำหนด
ประมาณ 2 ใน 3 ของทั้งหมดเป็นกรรมพันธุ์แบบออโตโซมอลโดมิแนนต์ (ยีน PAX6) และประมาณ 30% ของผู้ป่วยที่เกิดขึ้นเองมีความเสี่ยงต่อกลุ่มอาการ WAGR ที่มีเนื้องอกวิลมส์ร่วมด้วย
ภาวะจอประสาทตา ส่วนกลางเจริญไม่เต็มที่พบได้เกือบทุกกรณีและเป็นปัจจัยจำกัดการมองเห็น ที่สำคัญที่สุด ปัจจุบันยังไม่มีการรักษาที่ได้ผล
มีภาวะแทรกซ้อนสูง ได้แก่ ต้อกระจก (ประมาณ 80%) ต้อหิน (50-75%) และภาวะขอบกระจกตา เสื่อม ส่งผลให้การมองเห็น บกพร่องแบบซับซ้อน
ตามการจำแนกความรุนแรง (ระดับ I-IV) ระดับ III ขึ้นไปมีสิทธิ์ได้รับเงินอุดหนุนค่ารักษาพยาบาล
การรักษาต้อหิน เป็นแบบขั้นบันได เริ่มด้วยการใช้ยา และดำเนินการผ่าตัดใส่ท่อระบายน้ำยาวในกรณีที่ดื้อต่อการรักษา
การดูแลผู้มีความบกพร่องทางการมองเห็น (การแก้ไขสายตา แว่นกันแสง คอนแทคเลนส์ที่มีม่านตาเทียม ฯลฯ) มีความจำเป็นต่อการรักษาการทำงานของการมองเห็น และปรับปรุงคุณภาพชีวิต
ภาวะไม่มีม่านตา (aniridia) คือภาวะที่ม่านตา ขาดหายไปทั้งหมดหรือบางส่วนเนื่องจากปัจจัยแต่กำเนิด แม้จะเรียกว่า “ไม่มีม่านตา ” แต่โดยทั่วไปแล้วยังคงมีโคนม่านตา หลงเหลืออยู่บริเวณมุมของช่องหน้าลูกตา ส่วนปลายสุด
ในปี 2017 โรคนี้ได้รับการยอมรับว่าเป็นโรคหายากที่ถูกกำหนดตามกฎหมายโรคหายากของกระทรวงสาธารณสุข แรงงาน และสวัสดิการ 1) ผู้ป่วยที่ได้รับการวินิจฉัยว่าเป็นโรคหายากที่ถูกกำหนดและมีความรุนแรงของโรคระดับ III ขึ้นไปจะมีสิทธิ์ได้รับเงินอุดหนุนค่ารักษาพยาบาล โดยมีวงเงินสูงสุดที่ต้องจ่ายเองตามรายได้ 2) .
รายการ เนื้อหา ความชุก 1 ใน 64,000–96,000 คน1) ความแตกต่างทางเพศ ไม่มี1) เป็นทั้งสองตา 60–90%1) รูปแบบการถ่ายทอดทางพันธุกรรม (ในครอบครัว) ประมาณ 2/3 ของทั้งหมด (ถ่ายทอดแบบออโตโซมเด่น) ประปราย ประมาณ 1/3 ของทั้งหมด เนื้องอกวิลมส์ร่วม (กรณีประปราย) ประมาณ 30% (กลุ่มอาการ WAGR) 3)
การศึกษาทางระบาดวิทยาในสวีเดนและนอร์เวย์รายงานความชุกประมาณ 1 ใน 90,000 คน 3) การประเมินทางจักษุวิทยาอย่างละเอียดใน 43 รายที่มีการกลายพันธุ์ของยีน PAX6 แสดงให้เห็นว่าระดับความผิดปกติของม่านตา ขึ้นอยู่กับชนิดของการกลายพันธุ์ 3) .
Q
ภาวะไม่มีม่านตาถ่ายทอดทางพันธุกรรมหรือไม่?
A
ประมาณสองในสามของกรณีเป็นแบบ autosomal dominant โดยมีโอกาสถ่ายทอดจากพ่อแม่ที่ป่วยไปยังบุตร 50% ส่วนที่เหลืออีกหนึ่งในสามเป็นแบบ sporadic โดยไม่มีประวัติครอบครัว ในกรณี sporadic มีความเสี่ยงต่อกลุ่มอาการ WAGR ซึ่งรวมถึงเนื้องอก Wilms (เนื้องอกไต) ดังนั้นจึงแนะนำให้ตรวจทางพันธุกรรมของยีน PAX6 และ WT1.
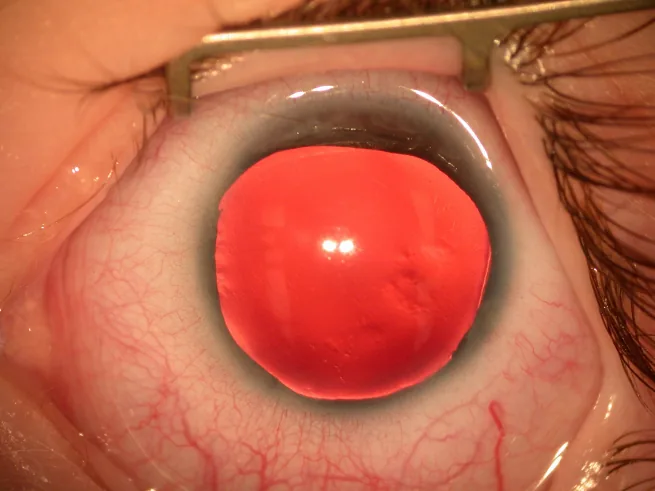
ภาพถ่ายส่วนหน้าของตาในภาวะไม่มีม่านตา ม่านตาเกือบหายไป เห็นบริเวณรูม่านตาขนาดใหญ่ชัดเจน Law SK, et al. Asymmetric phenotype of Axenfeld-Rieger anomaly and aniridia associated with a novel PITX2 mutation. Mol Vis. 2011. Figure 2. PM
CI D: PMC3102021. License: CC BY.
ภาพถ่ายด้วยกล้องจุลทรรศน์ชนิดกรีดของส่วนหน้าแสดงให้เห็นม่านตา เกือบหายไป เหลือเพียงม่านตา บางๆ ที่บริเวณรอบนอกเท่านั้น นี่แสดงผลการตรวจทางคลินิกที่พบได้ทั่วไปในภาวะไม่มีม่านตา เหมาะสำหรับอธิบายอาการหลักและผลการตรวจทางคลินิก.
เนื่องจากม่านตา ขาดหายหรือไม่สมบูรณ์ รูม่านตา จึงไม่ทำงานและไม่สามารถควบคุมปริมาณแสงที่เข้าสู่ดวงตาได้ ดังนั้นผู้ป่วยจึงมีอาการกลัวแสง อย่างรุนแรง นอกจากนี้ การจ้องมองที่ไม่ดีเนื่องจากภาวะจอประสาทตา ส่วนกลางเจริญไม่เต็มที่ มักเป็นสาเหตุหลักของอาการตาสั่นในแนวราบที่ปรากฏตั้งแต่ช่วงต้นของชีวิต
กลัวแสง : ม่านตา ไม่สามารถควบคุมแสงได้ → แสงจ้ามากตาสั่น (ตาสั่นในแนวราบ) : การจ้องมองไม่ดีเนื่องจากจอประสาทตา ส่วนกลางเจริญไม่เต็มที่ ปรากฏตั้งแต่ช่วงต้นของชีวิตการมองเห็น ลดลงจอประสาทตา ส่วนกลางเจริญไม่เต็มที่ ต้อกระจก ต้อหิน และภาวะพร่องเซลล์ต้นกำเนิดลิมบัส (LSCD )
ภาวะแทรกซ้อนแต่กำเนิด (ตั้งแต่แรกเกิด)
ความผิดปกติของม่านตา : มีระดับความรุนแรงตั้งแต่ฝ่อบางส่วนจนถึงไม่มีเลย
ภาวะโพรงจอประสาทตา ส่วนกลางเจริญไม่เต็มที่ : พบได้เกือบทุกกรณี ไม่มีรอยบุ๋มจอตา และเม็ดสีจอประสาทตา ส่วนกลางไม่ชัดเจน เป็นปัจจัยจำกัดการมองเห็น ที่สำคัญที่สุด
ตาแกว่ง : ส่วนใหญ่เป็นการแกว่งในแนวราบ เกิดจากภาวะโพรงจอประสาทตา ส่วนกลางเจริญไม่เต็มที่
ตาเหล่
ภาวะแทรกซ้อนที่เกิดขึ้นภายหลัง (เกิดขึ้นเมื่อโตขึ้น)
ต้อกระจก
ต้อหิน
ภาวะพร่องเซลล์ต้นกำเนิดลิมบัส (LSCD ) : มักปกติในวัยเด็ก แต่เมื่อโตขึ้น จะเกิดความขุ่นของสโตรมาคอร์เนียและหลอดเลือดพานนัสที่ลุกลาม
ภาวะแทรกซ้อน ความถี่และระยะเวลา ผลกระทบต่อการทำงานของการมองเห็น ภาวะจอประสาทตา ส่วนกลางเจริญไม่เต็มที่ เกือบทุกกรณี (แต่กำเนิด) ปัจจัยจำกัดการมองเห็น ที่สำคัญที่สุด ไม่มีการรักษาที่ได้ผล ต้อกระจก ประมาณ 80% (ภายหลัง) 1) การมองเห็น ลดลงและอาการกลัวแสง แย่ลงต้อหิน 50–75% (ที่เกิดขึ้นภายหลัง) 1) ความบกพร่องของลานสายตา ที่ไม่สามารถฟื้นคืนได้หากดำเนินไปภาวะพร่องเซลล์ต้นกำเนิดลิมบัส เริ่มและดำเนินหลังการเจริญเติบโต 3) ความขุ่นของสโตรมาคอร์เนีย → การมองเห็น ลดลงอย่างรุนแรง อาตา แต่กำเนิด (เกือบทุกกรณี) การจ้องมองไม่ดี ตาเหล่ แต่กำเนิดถึงวัยทารก ความเสี่ยงต่อภาวะตาขี้เกียจ
ยีน PAX6 มีการแสดงออกในเนื้อเยื่อตา รวมถึงระบบประสาทส่วนกลาง เกาะเล็กแลงเกอร์ฮานส์ในตับอ่อน และเยื่อบุรับกลิ่น ภาวะเจริญน้อยของเนื้อเยื่อเหล่านี้อาจทำให้เกิดภาวะแทรกซ้อนนอกตาที่หลากหลาย 1) .
ภาวะไม่มีคอร์ปัส คาโลซัม, โรคลมชัก, ความผิดปกติของการทำงานของสมองระดับสูง
ภาวะเสียการได้กลิ่น
ภาวะไม่ทนต่อกลูโคส
กลุ่มอาการ WAGR (ประมาณ 30% ของผู้ป่วยที่เกิดแบบประปราย): เนื้องอกวิล์มส์, ภาวะไม่มีม่านตา , ความผิดปกติของระบบสืบพันธุ์และทางเดินปัสสาวะ, ภาวะปัญญาอ่อน3)
Q
ในภาวะไม่มีม่านตา สามารถมองเห็นได้มากน้อยเพียงใด?
A
การพยากรณ์โรคทางการมองเห็น โดยทั่วไปไม่ดี มักอยู่ที่ประมาณ 0.1 อย่างไรก็ตาม มีความแตกต่างระหว่างบุคคลตั้งแต่ 0.1 ถึง 0.7 ขึ้นอยู่กับระดับของภาวะจุดรับภาพเจริญไม่เต็มที่และการมีภาวะแทรกซ้อน ปัจจุบันภาวะจุดรับภาพเจริญไม่เต็มที่ยังไม่มีวิธีการรักษาที่ได้ผล และเป็นปัจจัยจำกัดการมองเห็น ที่สำคัญที่สุด คุณภาพชีวิตประจำวันสามารถดีขึ้นได้ด้วยการแก้ไขค่าสายตาที่เหมาะสมและการดูแลผู้มีสายตาเลือนราง
สาเหตุของภาวะไม่มีม่านตา คือการสูญเสียการทำงานของอัลลีลหนึ่ง (haploinsufficiency) ของยีน PAX6 ซึ่งอยู่บนแขนสั้นของโครโมโซมคู่ที่ 11 (11p13) เกิดจากปริมาณยีนที่ทำงานได้ลดลงครึ่งหนึ่ง ความผิดปกติของอัลลีลทั้งสองเชื่อว่าทำให้ทารกในครรภ์เสียชีวิต 1) .
PAX6 เป็นยีนควบคุมหลักของปัจจัยถอดรหัสที่ควบคุมการเปลี่ยนแปลงของอวัยวะในช่วงตัวอ่อน และประสานงานปัจจัยถอดรหัสต่างๆ ความผิดปกติของ PAX6 ทำให้เกิดความผิดปกติแต่กำเนิดต่างๆ ทั่วทั้งดวงตา (ไม่มีม่านตา , ความผิดปกติของปีเตอร์ส, จุดรับภาพเจริญไม่เต็มที่ ฯลฯ)
ประเภทของการกลายพันธุ์ของยีนมักเป็นแบบ premature truncated codon (PTC) เช่น nonsense และ frameshift และยังมีการรายงานการกลายพันธุ์แบบ missense ด้วย 1) การวิเคราะห์ลำดับดีเอ็นเอในภาวะ aniridia แบบแยกเดี่ยวตรวจพบการกลายพันธุ์ของ PAX6 ในประมาณ 85% ของผู้ป่วย 2) .
ยีน PAX6 อยู่ติดกับยีน WT1 ซึ่งเป็นยีนต้านเนื้องอกบนโครโมโซม 11p13 ในผู้ป่วยประปราย การขาดหายของยีนที่อยู่ติดกันอาจทำให้เกิดกลุ่มอาการ WAGR ซึ่งประกอบด้วยเนื้องอกวิลมส์, aniridia, ความผิดปกติของระบบสืบพันธุ์และทางเดินปัสสาวะ, และภาวะปัญญาอ่อน 3) ประมาณ 30% ของผู้ป่วยประปรายเกิดเนื้องอกวิลมส์ทั้งสองข้างก่อนอายุ 5 ปี.
หากการกลายพันธุ์ PAX6 เป็นบวกโดยไม่มีการขาดหายของ WT1 สามารถสันนิษฐานได้ว่าไม่มีกลุ่มอาการ WAGR 2) .
การตรวจทางพันธุกรรมประกอบด้วยการหาลำดับดีเอ็นเอร่วมกับการตรวจหาความผิดปกติของโครงสร้างจีโนมด้วย MLPA/CMA 2) .
ในกรณีที่สงสัยกลุ่มอาการ WAGR แบบประปราย แนะนำให้ตรวจทางพันธุกรรม 2)
Q
ฉันควรตรวจยีนสำหรับภาวะไม่มีม่านตาหรือไม่?
A
การตรวจยีน PAX6 จำเป็นเพื่อยืนยันการวินิจฉัยที่แน่ชัด และโดยเฉพาะในกรณีประปราย แนะนำให้ตรวจยีน PAX6 และ WT1 เพื่อประเมินความเสี่ยงของเนื้องอกวิลมส์ ควรตรวจโดยใช้การหาลำดับดีเอ็นเอร่วมกับ MLPA/CMA ภายใต้การให้คำปรึกษาทางพันธุกรรม ที่เหมาะสม
เกณฑ์การวินิจฉัยภาวะไม่มีม่านตา และการจำแนกประเภทตามความรุนแรง 1) แสดงไว้ด้านล่าง
หมวดหมู่การวินิจฉัย ชุดเกณฑ์การวินิจฉัย แน่นอน เข้าเกณฑ์ข้อใดข้อหนึ่งของ A + B1 + E และไม่เข้าเกณฑ์ C น่าจะเป็น (1) เข้าเกณฑ์ข้อใดข้อหนึ่งของ A + B1 + F และไม่เข้าเกณฑ์ C น่าจะเป็น (2) เข้าเกณฑ์ข้อใดข้อหนึ่งของ A + B1 + B2 และไม่เข้าเกณฑ์ C น่าจะเป็น (3) เข้าเกณฑ์ข้อใดข้อหนึ่งของ A + B1 + B3 และไม่เข้าเกณฑ์ C เป็นไปได้ เข้าเกณฑ์ข้อใดข้อหนึ่งของ A + B1 และไม่สามารถแยก C ออกได้ทั้งหมด
ก. อาการ
ความบกพร่องทางการมองเห็น ทั้งสองข้าง (การมองเห็น ลดลงจากภาวะจอประสาทตา ส่วนกลางเจริญไม่เต็มที่ ต้อกระจก ต้อหิน หรือภาวะขอบกระจกตา เสื่อม)
อาการกลัวแสง (ขึ้นอยู่กับระดับของความบกพร่องของม่านตา )
ข. ผลการตรวจ
การตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด พบความผิดปกติของม่านตา ตั้งแต่ฝ่อบางส่วนจนถึงไม่มีม่านตา โดยสมบูรณ์ (60-90% เป็นทั้งสองข้าง)การตรวจอวัยวะภายในลูกตาและ OCT พบภาวะจอประสาทตา ส่วนกลางเจริญไม่เต็มที่ (รอยบุ๋มจอตา เม็ดสีจอประสาทตา ส่วนกลาง และบริเวณไร้หลอดเลือดที่รอยบุ๋มจอตา ไม่ชัดเจน)
การตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด (slit-lamp) พบภาวะพร่องเซลล์ต้นกำเนิดบริเวณลิมบัส (limbal stem cell deficiency) หรือกระจกตา ขุ่น หรือรอยโรคที่กระจกตา อื่นๆการตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด พบต้อกระจก (เกิดในประมาณ 80% ของผู้ป่วย)การตรวจด้วยคลื่นเสียงความถี่สูง, MRI หรือ CT พบภาวะลูกตาเล็ก (microphthalmos)
ภาวะตากระตุก (nystagmus)
การวัดความดันลูกตา ฯลฯ พบต้อหิน (เกิดใน 50-75% ของผู้ป่วย)
ค. การวินิจฉัยแยกโรค (โรคที่ควรตัดออก)
ฝ่อของม่านตา จากการติดเชื้อไวรัสในวงศ์ Herpesviridae มาก่อน
ความบกพร่องของม่านตา หลังการบาดเจ็บหรือการผ่าตัดภายในลูกตา
รอยแยกของม่านตา แต่กำเนิดที่เกี่ยวข้องกับการปิดรอยแยกของแก้วนำแสงไม่สมบูรณ์
ความผิดปกติของรีเกอร์
กลุ่มอาการเยื่อบุผิวม่านตา และกระจกตา
ง. ภาวะแทรกซ้อนนอกตาที่เกี่ยวข้องกับการกลายพันธุ์ของยีน PAX6 (การไม่มีคอร์ปัสคัลโลซัม, โรคลมชัก ฯลฯ)
E. การกลายพันธุ์ของยีน PAX6 ที่ก่อโรค หรือการขาดหายของบริเวณ 11p13 (การตรวจทางพันธุศาสตร์)
F. การเกิดในครอบครัว (ถ่ายทอดทางพันธุกรรมแบบออโตโซมเด่นใน 2/3 ของผู้ป่วย)
การตรวจ วัตถุประสงค์และเนื้อหา การตรวจด้วยกล้องจุลทรรศน์ชนิดร่องกราด การประเมินระดับความผิดปกติของม่านตา (พื้นฐานการวินิจฉัย) การตรวจอวัยวะภายในลูกตาและ OCT การประเมินภาวะจอประสาทตา ส่วนกลางเจริญไม่เต็มที่ (การหายไปของรอยบุ๋มจอตา และเม็ดสีจอประสาทตา ส่วนกลางไม่ชัดเจน) การตรวจมุมตา (gonioscopy)การประเมินความผิดปกติของมุมตาและการยึดเกาะของรากม่านตา ที่เหลือกับ trabecular meshwork การวัดความดันลูกตา (เป็นประจำ)การคัดกรองโรคต้อหิน ดำเนินการเป็นประจำตั้งแต่วัยรุ่น การตรวจอัลตราซาวนด์ช่องท้อง การคัดกรองเนื้องอกวิล์มส์ (ผู้ป่วยประปราย ทุกสองสามเดือน โดยเฉพาะจนถึงอายุ 5 ปี) การตรวจทางพันธุกรรม การระบุการกลายพันธุ์ของยีน PAX6 หรือการขาดหายของบริเวณ 11p13 (จำเป็นสำหรับการวินิจฉัยที่แน่นอน)
ในเด็ก อาจต้องตรวจภายใต้การดมยาสลบ
ในผู้ป่วยประปรายประมาณ 30% พบเนื้องอกวิลมส์ร่วมด้วย เนื่องจากมีแนวโน้มเกิดสองข้างเร็วก่อนอายุ 5 ปี การตรวจอัลตราซาวนด์ช่องท้องเป็นระยะทุกสองสามเดือนจึงจำเป็น แนะนำให้ติดตามต่อเนื่องแม้หลังจากอายุ 5 ปีแล้ว
Q
การวินิจฉัยภาวะไม่มีม่านตาทำได้อย่างไร?
A
พื้นฐานคือการยืนยันความผิดปกติของม่านตา ด้วยการตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด และประเมินภาวะจอประสาทตา ส่วนกลางเจริญไม่เต็มที่ด้วย OCT การตรวจยีน PAX6 สามารถวินิจฉัยได้แน่ชัด และในผู้ป่วยประปรายจะค้นหายีน WT1 ร่วมด้วย สิ่งสำคัญคือการแยกจากภาวะม่านตา ฝ่อจากเริม ม่านตา ขาดหลังบาดเจ็บ ม่านตาผิดปกติแต่กำเนิด กลุ่มอาการรีเกอร์ และกลุ่มอาการไอซ์
ความผิดปกติของม่านตา จอประสาทตา ส่วนกลางเจริญไม่เต็มที่ ตาเล็ก และตากระตุก ไม่สามารถแก้ไขได้ในปัจจุบัน การสังเกตอาการจึงเป็นพื้นฐาน เป้าหมายการรักษาคือโรคกระจกตา ต้อกระจก ต้อหิน กลัวแสง และสายตาเลือนราง 2) .
CQ เป้าหมายการรักษา คำแนะนำ CQ1 ความขุ่นของสโตรมาที่กระจกตา → การปลูกถ่ายกระจกตา แนะนำอย่างอ่อน ไม่ให้ทำCQ2 ภาวะพร่องเซลล์ต้นกำเนิดเยื่อบุกระจกตา → การผ่าตัด แนะนำอย่างอ่อน ให้ดำเนินการCQ3 ต้อกระจก → การผ่าตัดแนะนำอย่างอ่อน ให้ดำเนินการCQ4 ความดันลูกตา สูง/ต้อหิน → การรักษาแนะนำอย่างยิ่ง ให้ดำเนินการCQ5 การดูแลผู้มีสายตาเลือนราง แนะนำอย่างยิ่ง ให้ดำเนินการCQ6 กลัวแสง → การรักษา แนะนำอย่างยิ่งให้ดำเนินการ
ความขุ่นของกระจกตา (CQ1) : แนะนำอย่างอ่อนให้ไม่ทำการปลูกถ่ายกระจกตา 2) การปรับปรุงการมองเห็น ที่ได้จากการปลูกถ่ายกระจกตา มีจำกัดเนื่องจากภาวะแทรกซ้อนของภาวะไม่มีม่านตา ในระยะยาว การพยากรณ์โรคทางสายตามักไม่ดีเนื่องจากโรคต้อหิน แย่ลงและความล้มเหลวของ graft เมื่อเวลาผ่านไป การปลูกถ่ายกระจกตา แบบเต็มชั้นสำหรับความขุ่นของกระจกตา มักไม่นำไปสู่การปรับปรุงการมองเห็น และต้องระวังอัตราการปฏิเสธที่สูง ในกรณีรุนแรง ควรพิจารณาความสมดุลระหว่างประโยชน์และโทษอย่างรอบคอบก่อนตัดสินใจทำการรักษา
โรคพร่องสเต็มเซลล์เยื่อบุกระจกตา (LSCD , CQ2) : แนะนำให้รักษาด้วยการผ่าตัดอย่างอ่อน2) โดยเฉพาะอย่างยิ่ง การสร้างพื้นผิวตาขึ้นใหม่ สามารถคาดหวังได้ในระดับหนึ่งผ่านการปลูกถ่ายขอบกระจกตาจากผู้บริจาค (KLAL ) หรือการปลูกถ่ายเยื่อบุช่องปากที่เพาะเลี้ยง (COMET)3) หากมีต้อกระจก ตาขุ่นร่วมด้วย การปลูกถ่ายกระจกตา ร่วมมักมีประโยชน์ในการปรับปรุงการมองเห็น 2) .
แนะนำให้ผ่าตัดต้อกระจก อย่างอ่อน 2) ต้อกระจก เกิดขึ้นในผู้ป่วย 50-85% เมื่ออายุ 20 ปี และวางแผนการผ่าตัดตามความรุนแรงของความขุ่นและอาการกลัวแสง
ความยากในการผ่าตัดสูงเนื่องจากความเปราะบางของแคปซูลเลนส์และเส้นใยซินน์
ระวังความเสี่ยงของโรคต้อหิน ที่แย่ลงหลังผ่าตัด กลุ่มอาการพังผืดด้านหน้า และโรคกระจกตาพุพอง 2)
การใส่เลนส์แก้วตาเทียม (IOL ) ต้องมีข้อบ่งชี้อย่างระมัดระวัง 3)
ไม่แนะนำให้ใส่ม่านตาเทียม พร้อมกับการผ่าตัดต้อกระจก เพราะอาจกระตุ้นให้เกิดโรคต้อหิน
ดำเนินการหลังจากอธิบายความเสี่ยงที่เกี่ยวข้องกับการผ่าตัดอย่างเพียงพอ
แนะนำให้รักษาโรคต้อหิน อย่างยิ่ง2) โดยใช้แนวทางแบบเป็นขั้นตอนดังนี้
การรักษาด้วยยา : ลดความดันลูกตา ด้วยยาหยอดตาหรือยารับประทาน โดยคำนึงถึงผลข้างเคียงและผลต่อร่างกายในเด็กการผ่าตัดสร้างทางระบายน้ำใหม่ : การผ่าตัดโกนิโอโตมีหรือทราเบคิวโลโตมี (พิจารณาเมื่อการรักษาด้วยยาไม่ได้ผล)การผ่าตัดกรอง น้ำการผ่าตัดทราเบคิวเลกโตมี การผ่าตัดปลูกถ่ายท่อระบายน้ำต้อหิน : การผ่าตัดท่อยาว (ต้องได้รับการรับรองจากสถานพยาบาล)การจี้ทำลายซิลิอารีบอดี ้ : ทางเลือกสุดท้ายเมื่อการรักษาอื่นไม่ได้ผล
มักดื้อต่อการรักษาด้วยยา และการผ่าตัดท่อระบายน้ำอาจเป็นทางเลือกที่ดี4) เนื่องจากความเสียหายของลานสายตาในต้อหิน ไม่สามารถฟื้นคืนได้ การควบคุมความดันลูกตา ตั้งแต่เนิ่นๆ จึงเป็นกุญแจสำคัญในการรักษาการทำงานของการมองเห็น
Q
รักษาต้อหินในภาวะไม่มีม่านตาอย่างไร?
A
ขั้นแรกให้การรักษาด้วยยาหยอดตาและยารับประทาน แต่มักดื้อยา หากผลไม่เพียงพอ ให้พิจารณาผ่าตัดสร้างทางระบายน้ำใหม่ (goniotomy หรือ trabeculotomy) จากนั้นจึงดำเนินการผ่าตัด trabeculectomy หรือผ่าตัดท่อยาว (ผ่าตัดปลูกถ่ายท่อระบายน้ำต้อหิน ) การผ่าตัดท่อยาวต้องได้รับการรับรองจากสถานพยาบาล การจี้ทำลายซิลิอารีบอดี ้เป็นทางเลือกสุดท้ายเมื่อการรักษาอื่นไม่ได้ผล การติดตามความดันลูกตา เป็นประจำเป็นสิ่งจำเป็น
แนะนำอย่างยิ่งให้ดูแลผู้มีสายตาเลือนรางและรักษาอาการกลัวแสง 2) .
แก้ไขค่าสายตา : แก้ไขค่าสายตาผิดปกติด้วยแว่นตาเพื่อส่งเสริมพัฒนาการทางการมองเห็น ให้มากที่สุด (พื้นฐาน)แว่นตาป้องกันแสง : มีประสิทธิภาพในการลดอาการกลัวแสง กำหนดใช้ในกรณีกลัวแสงรุนแรงคอนแทคเลนส์ที่มีม่านตาเทียม : มีประโยชน์ทั้งในการปรับปรุงอาการกลัวแสง และรูปลักษณ์ใช้อุปกรณ์ช่วยการมองเห็น เช่น แว่นขยาย แว่นตาสำหรับผู้มีสายตาเลือนราง และเครื่องอ่านขยาย
ผู้ป่วยภาวะไม่มีม่านตา ส่วนใหญ่สามารถเรียนในโรงเรียนปกติได้ แต่ต้องการการสนับสนุนทางการเรียนรู้ เช่น หนังสือเรียนขยายใหญ่ นอกจากนี้ยังสามารถใช้ประโยชน์จากการเรียนบางส่วนในชั้นเรียนสำหรับผู้บกพร่องทางการเห็น การให้คำปรึกษาด้านการเลี้ยงดูและการศึกษาที่โรงเรียนคนตาบอดหรือโรงเรียนสนับสนุนทางการเห็นพิเศษ เนื่องจากสามารถขอรับการช่วยเหลือค่าใช้จ่ายทางการแพทย์ในฐานะโรคหายากที่กำหนดได้ โปรดปรึกษาแพทย์ผู้ดูแลหรือที่ปรึกษาทางการแพทย์
ยีน PAX6 เป็นยีนควบคุมหลักที่ถอดรหัสปัจจัยการถอดรหัสซึ่งควบคุมการเปลี่ยนแปลงของอวัยวะในระยะตัวอ่อน ยีนนี้แสดงออกตั้งแต่ระยะแรกของดวงตาและประสานปัจจัยการถอดรหัสต่างๆ การสูญเสียการทำงานของอัลลีลหนึ่งของ PAX6 (haploinsufficiency) ทำให้เกิดความผิดปกติแต่กำเนิดทั่วทั้งดวงตา (ภาวะไม่มีม่านตา , ความผิดปกติของปีเตอร์ส, ภาวะจอประสาทตา พัฒนาน้อย เป็นต้น)
การกลายพันธุ์ของ PAX6 ส่วนใหญ่เป็นชนิด PTC เช่น nonsense และ frameshift และยังมีการรายงานการกลายพันธุ์แบบ missense ด้วย 1) การศึกษาเกี่ยวกับความสัมพันธ์ระหว่างจีโนไทป์และฟีโนไทป์แสดงให้เห็นว่าความรุนแรงของอาการทางจักษุวิทยาแตกต่างกันไปตามชนิดของการกลายพันธุ์ 3) .
PAX6 ยังแสดงออกนอกดวงตาในระบบประสาทส่วนกลาง เกาะแลงเกอร์ฮานส์ของตับอ่อน และเยื่อบุรับกลิ่น ดังนั้นอาจเกิดภาวะแทรกซ้อนนอกดวงตาเนื่องจากการพัฒนาน้อยของเนื้อเยื่อเหล่านี้ (ภาวะไม่มีคอร์ปัส คัลโลซัม, โรคลมชัก, ภาวะไม่รู้กลิ่น, ภาวะไม่ทนต่อกลูโคส) 1) .
มีสองเส้นทางที่คิดว่าเกี่ยวข้องกับกลไกการเกิดโรคต้อหิน ที่มาพร้อมกับภาวะไม่มีม่านตา
พยาธิสภาพแบบมุมเปิด : ความต้านทานการไหลของอารมณ์ขันใน trabecular meshwork เพิ่มขึ้นพยาธิสภาพแบบมุมปิด : โคนม่านตา ที่เหลืออยู่บริเวณรอบนอกสุดยึดติดกับ trabecular meshwork ทำให้เกิดพยาธิสภาพแบบต้อหินมุมปิด
ต้อหิน พบได้น้อยในวัยทารก โดยมักจะค่อยๆ พัฒนาในวัยรุ่นเมื่อโตขึ้น อาจเกิดจากความผิดปกติของมุมที่ทำให้เกิดภาวะมุมเปิด หรือจากมุมปิดที่ทำให้เกิดต้อหิน
ทางพยาธิวิทยาพบความผิดปกติของเซลล์ต้นกำเนิดเยื่อบุกระจกตา ทำให้เกิดความผิดปกติของเยื่อบุผิวและเยื่อโบว์แมน และเกิดพานนัสที่มีหลอดเลือดมาก จากภาวะเจริญผิดปกติของ Palisades of Vogt ดำเนินไปสู่การบุกรุกของเนื้อเยื่อเยื่อบุตา และการกลายเป็นเคราติน 1)
กระจกตา ในภาวะไม่มีม่านตา หนากว่าคนปกติ ในวัยเด็กตอนต้นกระจกตา มักปกติ แต่เมื่อโตขึ้นจะเกิดความขุ่นของสโตรมากระจกตา และ LSCD ทำให้การมองเห็น ลดลง ในการศึกษาในโรงพยาบาลเดียวเป็นเวลา 14 ปี (738 ตา) ภาวะไม่มีม่านตา เป็นสาเหตุที่พบบ่อยที่สุดของ LSCD คิดเป็น 30.9% 6)
การพยากรณ์การมองเห็น โดยทั่วไปไม่ดี มักอยู่ที่ประมาณ 0.1
ภาวะเจริญผิดปกติของจอประสาทตา ส่วนกลางไม่มีวิธีการรักษาที่ได้ผลและเป็นปัจจัยจำกัดการมองเห็น ที่สำคัญที่สุด
ความเสียหายของลานสายตาจากต้อหิน ไม่สามารถฟื้นคืนได้ ดังนั้นการควบคุมความดันลูกตา ตั้งแต่เนิ่นๆ จึงสำคัญ
ในกรณีที่เกิดเป็นครั้งคราว ควรระวังการเกิดเนื้องอกวิลมส์ก่อนอายุ 5 ปี และตรวจอัลตราซาวนด์ช่องท้องเป็นประจำ
การศึกษาเกี่ยวกับการพยากรณ์โรคระยะยาวรายงานว่าการพยากรณ์โรคทางสายตาโดยทั่วไปไม่ดี แต่มีความแตกต่างกันในแต่ละบุคคลขึ้นอยู่กับชนิดและความรุนแรงของภาวะแทรกซ้อน5) .
เนื้อหาต่อไปนี้รวมถึงการรักษาที่ยังอยู่ในขั้นตอนการวิจัยหรือดำเนินการเฉพาะในบางสถานที่เท่านั้น ไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป การตัดสินใจแผนการรักษาต้องขึ้นอยู่กับดุลยพินิจของจักษุแพทย์ผู้เชี่ยวชาญ
ด้วยการแพร่หลายของการหาลำดับรุ่นถัดไป (NGS) อัตราการตรวจพบการกลายพันธุ์ของ PAX6 ใน isolated aniridia อยู่ที่ประมาณ 85% 2) โครโมโซมไมโครอาร์เรย์ (CMA) มีความไวสูงกว่าการตรวจโครโมโซมแบบดั้งเดิมในการตรวจหาการขาดหายขนาดเล็กของ 11p13 ซึ่งช่วยเพิ่มความแม่นยำในการวินิจฉัยกลุ่มอาการ WAGR 2) .
ผลลัพธ์ระยะยาวของการปลูกถ่ายเยื่อบุช่องปากที่เพาะเลี้ยง (COMET) กำลังสะสมมากขึ้น 2) สำหรับกระจกตา เทียม Boston type I การมองเห็น ดีขึ้นในระยะสั้น (17-28.7 เดือน) 65-93% แต่ลดลงเหลือ 43.5% ที่ 4.5 ปีตามรายงาน 2) .
HumanOptics CustomFlex ArtificialIris เป็นอุปกรณ์ม่านตาเทียม ซิลิโคนที่สั่งทำเฉพาะบุคคล ซึ่งถือว่ามีประโยชน์ในการลดอาการกลัวแสง และปรับปรุงรูปลักษณ์ แต่ยังไม่ได้รับการอนุมัติในญี่ปุ่น ณ ปี 2024 การบำบัดแบบมุ่งเป้าระดับโมเลกุลที่กำหนดเป้าหมาย PAX6 haploinsufficiency ยังอยู่ในขั้นตอนการวิจัยและยังไม่ถึงการประยุกต์ใช้ทางคลินิก 3) .
大家義則, 川崎諭, 西田希, 木下茂, 外園千恵, 大橋裕一, 他. 無虹彩症の診断基準および重症度分類. 日眼会誌. 2020;124:83-88.
厚生労働科学研究費補助金難治性疾患政策研究事業「角膜難病の標準的診断法および治療法の確立を目指した調査研究」研究班. 無虹彩症の診療ガイドライン. 日眼会誌. 2021;125:38-73.
Moosajee M, Hingorani M, Moore AT. PAX6-Related Aniridia. GeneReviews®. University of Washington, Seattle. https://www.ncbi.nlm.nih.gov/books/n/gene/aniridia/
American Academy of Ophthalmology. Diagnosis and Management of Aniridia. EyeNet Magazine. 2014. https://www.aao.org/eyenet/article/diagnosis-management-of-aniridia
Japanese Ophthalmological Society. Clinical practice guideline for aniridia. Jpn J Ophthalmol. 2026. doi:10.1007/s10384-025-01296-y. https://link.springer.com/article/10.1007/s10384-025-01296-y
Hu JCW, Weissbart SB. Limbal stem cell deficiency and severe ocular surface disease: a review. Ann Eye Sci. 2023;8:35.