先天性併發症(出生時即有)

無虹彩症(Aniridia)
1. 什麼是無虹膜症
Section titled “1. 什麼是無虹膜症”無虹膜症(aniridia)是一種因先天因素導致虹膜完全或部分缺失的狀態。雖然稱為「無虹膜」,但隅角最周邊區域常殘留虹膜根部。
2017年,根據日本厚生勞動省的難病法,被認定為指定難病1)。被診斷為指定難病且重症度分類為Ⅲ度以上的患者,可享受醫療費補助,並根據收入設定個人負擔上限2)。
| 項目 | 內容 |
|---|---|
| 盛行率 | 每6.4萬至9.6萬人中有1人1) |
| 性別差異 | 無1) |
| 雙眼性 | 60–90%1) |
| 遺傳方式(家族性) | 約佔全體病例的2/3(體染色體顯性遺傳) |
| 散發性 | 約佔全體病例的1/3 |
| 合併Wilms腫瘤(散發病例) | 約30%(WAGR症候群)3) |
瑞典和挪威的流行病學研究報告盛行率約為每90,000人中有1人3)。對43例PAX6基因突變患者的詳細眼科評估顯示,虹膜發育不良的程度因突變類型而異3)。
約三分之二的病例為體染色體顯性遺傳,患病父母有50%的機率遺傳給子女。其餘三分之一為散發性,無家族史。散發性病例有發生WAGR症候群(包括Wilms腫瘤,即腎腫瘤)的風險,因此建議進行PAX6和WT1基因的遺傳學檢測。
2. 主要症狀和臨床所見
Section titled “2. 主要症狀和臨床所見”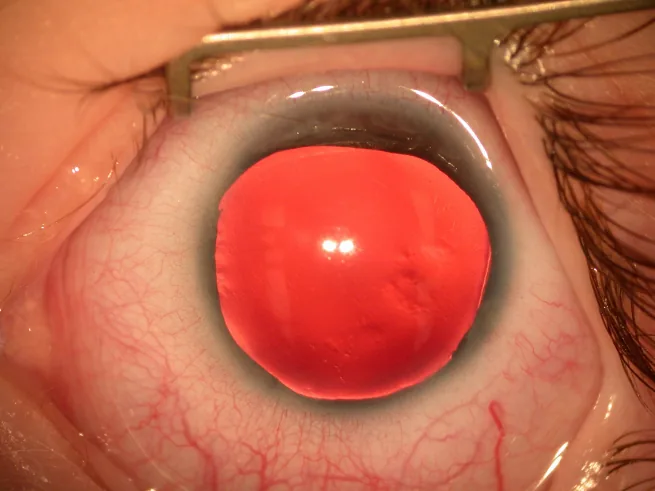
因為虹膜缺損或不完整,瞳孔無法正常運作,不能調節進入眼球的光量。因此患者會主訴嚴重的畏光。此外,因黃斑發育不良導致的固視不良,常成為出生後早期出現的水平眼震的主訴原因。
後天性併發症(隨成長而出現)
眼併發症頻率總結
Section titled “眼併發症頻率總結”| 併發症 | 頻率/時期 | 對視功能的影響 |
|---|---|---|
| 黃斑發育不全 | 幾乎全部(先天性) | 視力的最大限制因素。無有效治療方法。 |
| 白內障 | 約80%(後天性)1) | 視力下降和畏光加重 |
| 青光眼 | 50–75%(後天性)1) | 進展會導致不可逆的視野缺損 |
| 角膜輪部幹細胞缺乏症 | 生長後發病並進展3) | 角膜實質混濁→嚴重視力下降 |
| 眼球震顫 | 先天性(幾乎所有病例) | 固視不良 |
| 斜視 | 先天性至嬰兒期 | 弱視風險 |
PAX6基因不僅在眼組織中表現,也在中樞神經系統、胰臟蘭氏小島和嗅上皮中表現。這些組織的發育不全可能導致多種眼外併發症1)。
- 胼胝體缺損、癲癇、高階腦功能障礙
- 嗅覺缺失症
- 葡萄糖不耐受
- WAGR症候群(約30%的散發病例):Wilms腫瘤、無虹膜、泌尿生殖器異常、智能障礙3)
視力預後通常不佳,多為0.1左右。但根據黃斑部發育不全的程度及有無併發症,個體差異可從0.1到0.7。黃斑部發育不全目前尚無有效治療方法,是視力的最大限制因素。透過適當的屈光矯正及低視力復健,可改善日常生活品質。
3. 原因與風險因素
Section titled “3. 原因與風險因素”病因:PAX6基因單套缺失
Section titled “病因:PAX6基因單套缺失”無虹彩症的原因為位於第11號染色體短臂(11p13)上的PAX6基因一個對偶基因功能喪失(單套缺失)。功能性基因劑量減半導致發病。兩個對偶基因皆異常時,可能導致胚胎致死1)。
PAX6是胚胎期器官分化的主控轉錄因子基因,調控多種轉錄因子。PAX6異常會導致眼球整體的多種先天異常(如無虹彩、彼得斯異常、黃斑部發育不全等)。
基因突變的類型多為無義突變、框架位移突變等提前終止密碼子(PTC)型突變,也有錯義突變的報告1)。在孤立性無虹膜的定序分析中,約85%可檢測到PAX6突變2)。
WAGR症候群(散發病例的注意事項)
Section titled “WAGR症候群(散發病例的注意事項)”PAX6基因與抑癌基因WT1在11p13染色體上相鄰。散發病例中,相鄰基因缺失可能導致WAGR症候群,表現為Wilms腫瘤、無虹膜、泌尿生殖系統異常和智能障礙3)。約30%的散發病例在5歲前早期雙側發生Wilms腫瘤。
遺傳諮詢要點
Section titled “遺傳諮詢要點”- PAX6突變陽性且無WT1缺失→可推斷無WAGR症候群的可能性2)
- 遺傳學檢測應結合DNA定序和MLPA/CMA檢測基因組結構異常2)
- 對於疑似WAGR症候群的散發病例,建議進行基因檢測2)
PAX6基因檢測對於確診是必要的,尤其是在散發病例中,建議進行PAX6和WT1基因檢測以評估Wilms腫瘤風險。檢測應結合DNA定序和MLPA/CMA,並在適當的遺傳諮詢下進行。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”診斷標準(厚生勞動省指定罕見疾病 2020)
Section titled “診斷標準(厚生勞動省指定罕見疾病 2020)”無虹彩症的診斷標準和嚴重程度分類1)以及類別分類如下所示。
| 診斷類別 | 診斷標準的組合 |
|---|---|
| 確診 | 符合A任一項 + B1 + E,並排除C |
| 可能(1) | 符合A任一項 + B1 + F,並排除C |
| 可能(2) | 符合A任一項+B1+B2,並排除C |
| 可能(3) | 符合A任一項+B1+B3,並排除C |
| 疑似 | 符合A任一項+B1,但無法完全排除C |
A. 症狀
B. 檢查所見
- 裂隙燈顯微鏡檢查顯示不同程度的虹膜發育異常,從部分虹膜萎縮到完全虹膜缺損(60-90%為雙眼性)
- 眼底檢查和OCT檢查顯示黃斑發育不良(中心凹凹陷、黃斑色素、中心凹無血管區不明顯)
- 裂隙燈顯微鏡檢查發現角膜輪部疲乏症及角膜混濁等角膜病變
- 裂隙燈顯微鏡檢查發現白內障(約80%合併)
- 超音波檢查、MRI、CT發現小眼球
- 眼球震顫
- 眼壓檢查等發現青光眼(50~75%合併)
C. 鑑別診斷(應排除的疾病)
D. PAX6基因突變相關的眼外併發症(如胼胝體缺失、癲癇等)
E. PAX6基因的致病性基因突變或11p13區域的缺失(遺傳學檢查)
F. 家族內發病(體染色體顯性遺傳佔2/3)
標準檢查方法
Section titled “標準檢查方法”| 檢查 | 目的/內容 |
|---|---|
| 裂隙燈顯微鏡檢查 | 虹膜發育異常的嚴重程度評估(診斷基礎) |
| 眼底檢查和OCT | 評估黃斑發育不良(中心凹消失、黃斑色素不明顯) |
| 隅角鏡檢查 | 評估隅角發育不全及殘留虹膜根部與小梁網的粘連 |
| 眼壓測量(定期) | 青光眼篩查。從青春期開始定期進行。 |
| 腹部超音波檢查 | Wilms腫瘤篩檢(散發病例,每數月一次,尤其至5歲) |
| 基因檢測 | 鑑定PAX6基因突變或11p13缺失(確診所需) |
兒童可能需要在全身麻醉下進行檢查。
5. 標準治療方法
Section titled “5. 標準治療方法”治療總體方針
Section titled “治療總體方針”虹膜發育異常、黃斑發育不良、小眼球、眼球震顫目前無法干預,以觀察為主。治療對象為角膜病變、白內障、青光眼、畏光、低視力2)。
CQ建議列表(無虹膜症診療指引 2021)
Section titled “CQ建議列表(無虹膜症診療指引 2021)”| CQ | 治療對象 | 建議 |
|---|---|---|
| CQ1 | 角膜實質混濁→角膜移植 | 弱建議不執行 |
| CQ2 | 角膜上皮幹細胞缺乏症→手術 | 弱推薦執行 |
| CQ3 | 白內障→手術 | 弱推薦執行 |
| CQ4 | 高眼壓/青光眼→治療 | 強烈建議執行 |
| CQ5 | 低視力照護 | 強烈建議執行 |
| CQ6 | 畏光→治療 | 強烈建議實施 |
角膜病變的治療
Section titled “角膜病變的治療”角膜基質混濁(CQ1):弱建議不進行角膜移植2)。由於無虹膜症的併發症,角膜移植帶來的視力改善有限。長期而言,因青光眼惡化及移植片逐年功能衰竭,視力預後往往不佳。全層角膜移植治療角膜混濁常無法改善視力,且需注意排斥反應率高。重症病例應在充分權衡利弊後決定是否施行。
角膜緣幹細胞缺乏症(LSCD,CQ2):弱建議手術治療2)。具體而言,異體角膜緣移植(KLAL)或培養口腔黏膜上皮移植(COMET)可望實現一定程度的眼表重建3)。合併角膜基質混濁時,聯合角膜移植常有助於提高視力2)。
白內障的治療(CQ3)
Section titled “白內障的治療(CQ3)”弱推薦進行白內障手術2)。20歲前50~85%的患者會出現白內障,根據混濁和畏光程度計劃手術。
在充分說明手術相關風險後進行。
青光眼的治療(CQ4)
Section titled “青光眼的治療(CQ4)”強烈建議青光眼治療2)。採取以下逐步方法。
- 藥物治療:注意副作用,考慮對兒童的全身影響,透過眼藥水或口服藥物降低眼壓。
- 流出道重建術:隅角切開術或小樑切開術(藥物治療無效時考慮)。
- 濾過手術:小樑切除術。
- 青光眼植入手術:長管手術(需機構認證)
- 睫狀體光凝固術:其他治療無效時的最後手段
許多病例對藥物治療有抗藥性,管分流手術可能是個好選擇4)。青光眼導致的視野缺損是不可逆的,因此早期眼壓控制是維持視功能的關鍵。
首先進行點眼及口服藥物治療,但多數病例有抗藥性。效果不佳時考慮流出道重建術(隅角切開術或小樑切開術),然後進展到小樑切除術或長管手術(青光眼植入手術)。長管手術需要機構認證。睫狀體光凝固術是其他治療無效時的最後手段。定期監測眼壓至關重要。
低視力照護與畏光對策(CQ5和CQ6)
Section titled “低視力照護與畏光對策(CQ5和CQ6)”強烈建議低視力照護和畏光治療2)。
- 屈光矯正:用眼鏡矯正屈光不正,盡可能促進視覺發育(基本)
- 遮光眼鏡:有效減輕畏光。嚴重畏光時處方
- 帶人工虹膜的SCL:在改善畏光和外觀方面均有用
- 使用放大鏡、弱視眼鏡、放大閱讀器等視覺輔助器具
6. 病理生理學與詳細發病機制
Section titled “6. 病理生理學與詳細發病機制”PAX6基因與眼形成
Section titled “PAX6基因與眼形成”PAX6基因是編碼胚胎期器官分化轉錄因子的主控基因。它在早期眼球中表現,並調控多種轉錄因子。PAX6的一個等位基因功能喪失(單倍劑量不足)會導致整個眼球的先天異常(無虹膜、彼得斯異常、黃斑發育不良等)。
PAX6突變多為無義突變和框架位移突變等PTC類型,也有錯義突變的報導1)。關於基因型與表現型相關性的研究顯示,突變類型不同,眼科表現的嚴重程度也不同3)。
PAX6不僅在眼中表現,還在中樞神經系統、胰臟蘭氏小島和嗅上皮中表現,這些組織的發育不良可能導致眼外併發症(胼胝體缺失、癲癇、嗅覺喪失、葡萄糖不耐受)1)。
青光眼的發病機轉
Section titled “青光眼的發病機轉”無虹膜症伴隨青光眼的發病機轉有兩種路徑。
- 開放隅角型病態:小樑網房水流出阻力增加
- 閉塞隅角型病態:最周邊殘留的虹膜根部與小樑網粘連,導致一種閉塞隅角青光眼
嬰兒期很少出現青光眼,隨著成長在青春期進行性發病。可能因隅角發育異常呈開放狀態,或因隅角關閉而出現青光眼。
角膜輪部幹細胞缺乏症(LSCD)的病理生理
Section titled “角膜輪部幹細胞缺乏症(LSCD)的病理生理”病理學上,角膜上皮幹細胞功能異常,導致上皮和Bowman膜異常,形成富含血管的角膜血管翳。Vogt柵欄發育不全,進而發展為結膜組織侵入和角化1)。
無虹膜症的角膜比健康人厚。幼年時角膜通常正常,但隨著成長,出現角膜實質混濁和LSCD,導致視力下降。在一項為期14年的單中心研究(738眼)中,無虹膜症佔LSCD病因的30.9%,為最常見原因6)。
- 視力預後通常不良,多為0.1左右
- 黃斑發育不全無有效治療方法,是最大的視力限制因素
- 青光眼導致的視野損害不可逆,早期眼壓管理至關重要
- 對於散發病例,需注意5歲前早期發生Wilms腫瘤,並定期進行腹部超音波檢查。
關於長期預後的研究報告顯示,視力預後通常不佳,但根據併發症的類型與嚴重程度存在個體差異5)。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”遺傳學檢查的進展
Section titled “遺傳學檢查的進展”隨著次世代定序(NGS)的普及,孤立性無虹膜症中PAX6突變的檢出率約為85% 2)。染色體微陣列(CMA)在檢測11p13微缺失方面比傳統染色體檢查更敏感,有助於提高WAGR症候群的診斷準確性 2)。
培養口腔黏膜上皮移植(COMET)的長期結果正在累積中 2)。對於Boston I型人工角膜,短期(17–28.7個月)內65–93%的病例視力改善,但根據報告,4.5年時降至43.5% 2)。
人工虹膜裝置與基因治療展望
Section titled “人工虹膜裝置與基因治療展望”HumanOptics CustomFlex ArtificialIris是一種客製化矽膠人工虹膜裝置,有助於減輕畏光和改善外觀,但截至2024年,在日本尚未核准。針對PAX6單套不足的分子標靶治療目前處於研究階段,尚未進入臨床應用 3)。
8. 參考文獻
Section titled “8. 參考文獻”- 大家義則, 川崎諭, 西田希, 木下茂, 外園千恵, 大橋裕一, 他. 無虹彩症の診断基準および重症度分類. 日眼会誌. 2020;124:83-88.
- 厚生労働科学研究費補助金難治性疾患政策研究事業「角膜難病の標準的診断法および治療法の確立を目指した調査研究」研究班. 無虹彩症の診療ガイドライン. 日眼会誌. 2021;125:38-73.
- Moosajee M, Hingorani M, Moore AT. PAX6-Related Aniridia. GeneReviews®. University of Washington, Seattle. https://www.ncbi.nlm.nih.gov/books/n/gene/aniridia/
- American Academy of Ophthalmology. Diagnosis and Management of Aniridia. EyeNet Magazine. 2014. https://www.aao.org/eyenet/article/diagnosis-management-of-aniridia
- Japanese Ophthalmological Society. Clinical practice guideline for aniridia. Jpn J Ophthalmol. 2026. doi:10.1007/s10384-025-01296-y. https://link.springer.com/article/10.1007/s10384-025-01296-y
- Hu JCW, Weissbart SB. Limbal stem cell deficiency and severe ocular surface disease: a review. Ann Eye Sci. 2023;8:35.
