คำจำกัดความ : การปลูกถ่ายเนื้อเยื่อลิมบัส จากผู้บริจาค (KLAL ) เป็นการปลูกถ่ายเซลล์ต้นกำเนิดผิวตา (OSST) ชนิดหนึ่งสำหรับภาวะขาดเซลล์ต้นกำเนิดลิมบัส (LSCD ) โดยปลูกถ่ายเนื้อเยื่อลิมบัส จากผู้บริจาคที่เสียชีวิตพร้อมกับตัวรองรับกระจกตา -ตาขาว
ข้อบ่งชี้ : เลือกใช้ในกรณี LSCD สองตาที่ไม่มีผู้บริจาคมีชีวิต หรือ LSCD ข้างเดียวเมื่อตาข้างดีไม่เหมาะสมเป็นผู้บริจาค นอกจากนี้ยังมีประโยชน์สำหรับ LSCD ที่ไม่มีการเกี่ยวข้องกับเยื่อบุตา เช่น ภาวะไม่มีม่านตา
การผ่าตัด : หลังจากกรีดเยื่อบุตา 360° และนำพานนัสออก วางเนื้อเยื่อรูปพระจันทร์เสี้ยวที่เตรียมจากลิมบัส กระจกตา -ตาขาว ของผู้บริจาคลงในบริเวณลิมบัส
การกดภูมิคุ้มกัน : การกดภูมิคุ้มกันทั่วร่างกาย (ทาโครลิมัส + ไมโคฟีโนเลต โมเฟทิล + เพรดนิโซน) เป็นสิ่งจำเป็นสำหรับการอยู่รอดของกราฟต์ในระยะยาว
ผลลัพธ์ : ภายใต้การกดภูมิคุ้มกันที่เหมาะสม ผิวตาที่คงที่สามารถทำได้ใน 73-77% ของดวงตา
การปลูกถ่ายเนื้อเยื่อลิมบัส จากผู้บริจาค (KLAL ) เป็นการปลูกถ่ายเซลล์ต้นกำเนิดผิวตา (OSST) ชนิดหนึ่งเพื่อรักษาภาวะขาดเซลล์ต้นกำเนิดลิมบัส (LSCD ) โดยปลูกถ่ายเนื้อเยื่อลิมบัส จากผู้บริจาคที่ติดอยู่กับตัวรองรับกระจกตา -ตาขาว จากผู้บริจาคที่เสียชีวิต เพื่อฟื้นฟูสมดุลของเยื่อบุกระจกตา
ใน LSCD เซลล์ต้นกำเนิดเยื่อบุกระจกตา ถูกทำลาย และเยื่อบุกระจกตา ถูกแทนที่ด้วยเยื่อบุตา 1) การกลายเป็นเยื่อบุตา นี้ทำให้กระจกตา สูญเสียความใส ส่งผลให้การมองเห็น ลดลง เกิดแผลเป็น และเส้นเลือดใหม่ 1) การปลูกถ่ายกระจกตา เพียงอย่างเดียวไม่ได้ผลสำหรับ LSCD และการแตกของผิวตาซ้ำๆ และความผิดปกติของการหายของเยื่อบุทำให้กราฟต์ล้มเหลว 2)
KLAL มีข้อบ่งชี้ในกรณีต่อไปนี้: LSCD สองตาที่ไม่มีผู้บริจาคมีชีวิต; LSCD ข้างเดียวเมื่อตาข้างดีไม่เหมาะสมเป็นผู้บริจาค; LSCD ที่มีการเกี่ยวข้องกับเยื่อบุตา เล็กน้อย เช่น ภาวะไม่มีม่านตา หรือ LSCD ที่เกี่ยวข้องกับคอนแทคเลนส์
ในอดีต Thoft รายงานการปลูกถ่ายเยื่อบุกระจกตา ในปี 1984 ในปี 1990 Turgeon และ Thoft รายงานเทคนิคที่ปรับปรุงรวมถึงเนื้อเยื่อลิมบัส ซึ่งเป็น KLAL ครั้งแรกที่บันทึกไว้
Q
ความแตกต่างระหว่าง KLAL และการปลูกถ่ายอัตโนมัติคืออะไร?
A
การปลูกถ่ายอัตโนมัติ (CLAu, SLET ) นำเนื้อเยื่อลิมบัส จากตาข้างดีสำหรับ LSCD ข้างเดียว โดยมีข้อดีคือไม่ต้องกดภูมิคุ้มกัน ในขณะที่ KLAL ใช้เนื้อเยื่อจากผู้บริจาคที่เสียชีวิต จึงต้องกดภูมิคุ้มกันทั่วร่างกาย แต่สามารถทำได้ใน LSCD สองตาหรือเมื่อตาข้างดีไม่เหมาะสมเป็นผู้บริจาค ในการทบทวนอย่างเป็นระบบ อัตราความสำเร็จทางกายวิภาคของ CLAu แบบอัตโนมัติคือ 81% และ SLET 78% 2)
ภาพการปลูกถ่ายเนื้อเยื่อลิมบัสจากผู้บริจาค Yhu Fhei Lee, Dayna Wei Wei Yong, Ray Manotosh A Review of Contact Lens-Induced Limbal Stem Cell Deficiency 2023 Dec 5 Biology (Basel). 2023 Dec 5; 12(12):1490 Figure 3. PM
CI D: PMC10740976. License: CC BY.
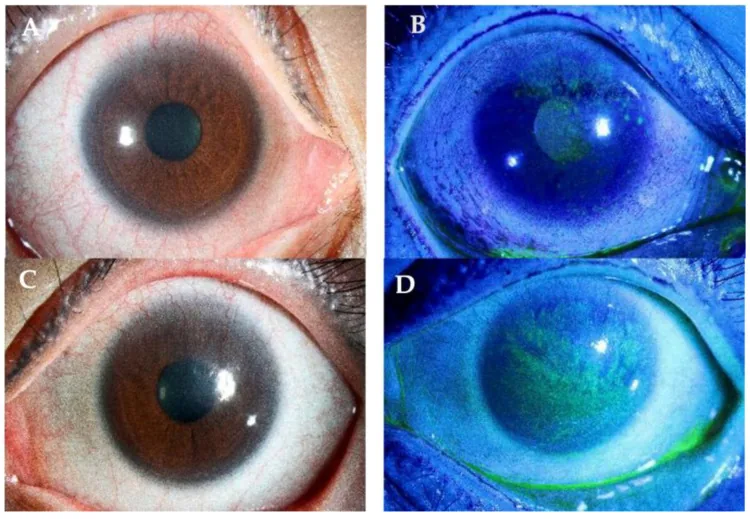
A และ C แสดงเส้นเลือดใหม่จากลิมบัส เข้าสู่กระจกตา ภายใต้การย้อมฟลูออเรสซีน B และ D แสดงพานนัสและความขุ่นผิวที่ลามไปถึงแกนการมองเห็น แสดงถึงขอบเขตของความเสียหายของเซลล์ต้นกำเนิดลิมบัส
ผู้ป่วย LSCD มีอาการหลักคือการมองเห็น ลดลง สาเหตุมาจากการสูญเสียความใสของกระจกตา เนื่องจากการกลายเป็นเยื่อบุตา และแผลเป็น หากมีข้อบกพร่องของเยื่อบุกระจกตา อย่างต่อเนื่อง จะมีอาการปวดตา นอกจากนี้ยังพบอาการกลัวแสง และน้ำตาไหล
ภาพทางคลินิกของ LSCD แตกต่างกันไปตามความรุนแรง1) .
ความรุนแรงของ LSCD อาการแสดงทางคลินิก เล็กน้อย โรคเยื่อบุผิวแบบเกลียว ปานกลาง เส้นเลือดใหม่ที่ผิวและพานนัส รุนแรง การกลายเป็นเยื่อบุตา รอบด้านทั้งหมด
ใน LSCD เล็กน้อย การย้อมฟลูออเรสซีน แสดงโรคเยื่อบุผิวแบบเกลียว (whorl-like)1) ในระดับปานกลาง จะมีเส้นเลือดใหม่ที่กระจกตา ผิวและพานนัสบริเวณรอบนอก1) ในระดับรุนแรง การกลายเป็นเยื่อบุตา รอบด้านทั้งหมดจะแทนที่กระจกตา ทั้งหมดด้วยเยื่อบุตา 1) .
ในการจำแนกความรุนแรงของ LSCD ตามการให้คะแนนทางคลินิก แบ่งเป็น เล็กน้อย (2-4 คะแนน) ปานกลาง (5-7 คะแนน) และรุนแรง (8-10 คะแนน)1) ความหนาแน่นของเซลล์เยื่อบุฐานคือ 9,252 เซลล์/ตร.มม. ในตากลุ่มควบคุม ในขณะที่ตา LSCD รุนแรงลดลงเหลือ 2,821 เซลล์/ตร.มม.1) .
LSCD เกิดจากความเสียหายต่อเซลล์ต้นกำเนิดลิมบัส สาเหตุที่พบบ่อยที่สุดคือภาวะไม่มีม่านตา (30.9%) รองลงมาคือแผลไหม้จากสารเคมี (20.6%) คอนแทคเลนส์ (16.8%) และ SJS (10.4%) 1) ในกรณีที่เป็นข้างเดียว แผลไหม้จากสารเคมี พบได้บ่อยที่สุด 1) .
ประเภทสาเหตุ โรคที่เป็นตัวแทน บาดเจ็บ แผลไหม้จากสารเคมี การใช้คอนแทคเลนส์ภูมิคุ้มกัน SJS , เพมฟิกอยด์เยื่อเมือก, GVHDพันธุกรรม ภาวะไม่มีม่านตา
การผ่าตัดต้อหิน เป็นปัจจัยเสี่ยงของ LSCD 1) การบาดเจ็บทางกลโดยตรงจากการตัดเนื้อเยื่อโพรงลูกตาหรือการผ่าตัดแบ่งน้ำอารมณ์สามารถทำลายเซลล์ต้นกำเนิดลิมบัส 1) การใช้ยาต้านเมตาบอไลต์ (ไมโตมัยซิน C, 5-FU) ก็ส่งผลต่อสภาพแวดล้อมจุลภาคของลิมบัส 1) มีรายงานว่าผู้ป่วย LSCD 35% มีต้อหิน หรือความดันลูกตา สูง 1) .
ในแผลไหม้จากสารเคมี เซลล์ต้นกำเนิดเยื่อบุกระจกตา ที่อยู่ในลิมบัส กระจกตา -เยื่อบุตา จะถูกทำลาย การหายไปของรั้ว Vogt สะท้อนถึงระดับความเสียหายของเซลล์ต้นกำเนิดเยื่อบุกระจกตา
หากได้รับบาดเจ็บทางตาจากสารเคมี ให้ล้างตาทันทีด้วยน้ำประปาปริมาณมากอย่างน้อย 10 นาที เวลาจากการบาดเจ็บจนถึงการล้างตาและปริมาณน้ำที่ใช้ล้างเป็นตัวกำหนดพยากรณ์โรค การใช้คอนแทคเลนส์มากเกินไปก็เป็นสาเหตุของ LSCD ดังนั้นควรไปพบจักษุแพทย์เป็นประจำและใช้คอนแทคเลนส์อย่างเหมาะสม
การวินิจฉัย LSCD ขึ้นอยู่กับการรวมกันของอาการทางคลินิกและการตรวจภาพ 1) .
การตรวจทางคลินิก
การตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด (Slit-lamp)1) การย้อมด้วยฟลูออเรสซีน ใช้ประเมินขอบเขตของ epitheliopathy แบบเกลียวหรือการเปลี่ยนเป็นเยื่อบุตา (conjunctivalization)1)
การตรวจเซลล์วิทยาแบบประทับ (Impression cytology) : เก็บเยื่อบุผิวผิวตาด้วยแผ่นกรองเซลลูโลสอะซิเตต1) การมีเซลล์กุณโฑ (goblet cells) บ่งชี้ถึงการเปลี่ยนเป็นเยื่อบุตา 1) ถือเป็นเกณฑ์หนึ่งในการวินิจฉัย LSCD แต่คุณภาพของตัวอย่างมีความแปรปรวน1)
การตรวจทางภาพ
กล้องจุลทรรศน์คอนโฟคอล ในสิ่งมีชีวิต (In vivo confocal microscopy)กระจกตา และเยื่อบุตา 1) เยื่อบุผิวกระจกตา ประกอบด้วยเซลล์แบนรูปหลายเหลี่ยมขนาดใหญ่ ในขณะที่เยื่อบุผิวตาเป็นรูปทรงลูกบาศก์มีไซโทพลาซึมสะท้อนแสงสูง1)
OCT ส่วนหน้าตา (AS-OCT )1) สามารถประเมินขอบเขตการเปลี่ยนเป็นเยื่อบุตา ของกระจกตา และการเปลี่ยนแปลงความหนาของเยื่อบุผิว
ทำภายใต้การดมยาสลบหรือการฉีดยาชา retrobulbar ทำการผ่าเยื่อบุตา บริเวณลิมบัส 360 องศา และนำเยื่อ fibrovascular pannus และเยื่อบุผิวผิดปกติออกจากผิวกระจกตา ตัดกระจกตา ส่วนกลางจากขอบกระจกตา -ตาขาว ของผู้บริจาคสองชิ้น และเตรียมเนื้อเยื่อลิมบัส รูปพระจันทร์เสี้ยวสี่ชิ้น ครึ่งหลังของแต่ละชิ้นถูกเอาออกโดยการผ่า lamellar และโดยปกติจะวางสามชิ้นรอบกระจกตา ของผู้รับ ยึดด้วยไหมไนลอน 10-0 และกาวเนื้อเยื่อ
เกณฑ์การเลือกเนื้อเยื่อผู้บริจาครวมถึง: ผู้บริจาคอายุน้อยต่ำกว่า 60 ปี ลดเวลาจากการเสียชีวิตถึงการเก็บรักษาให้สั้นที่สุด และการปลูกถ่ายภายใน 5 วันหลังเสียชีวิต
การกดภูมิคุ้มกันทั่วร่างกายเป็นสิ่งจำเป็นสำหรับการอยู่รอดของ graft ในระยะยาวหลัง KLAL ในโปรโตคอล Cincinnati OSSTP ให้ tacrolimus ชนิดรับประทาน 4 มก. วันละสองครั้ง และ MMF 1 กรัม วันละสองครั้ง เริ่ม 1-2 สัปดาห์ก่อนผ่าตัด หลังผ่าตัดเพิ่ม prednisone ชนิดรับประทาน 1 มก./กก./วัน และลดขนาดลงใน 1-3 เดือน ในผู้ป่วยที่มีผิวตาคงที่ ให้ลด tacrolimus อย่างค่อยเป็นค่อยไปหลังผ่าตัด 12-18 เดือน และ MMF หลัง 3 ปี
ผลลัพธ์ของ KLAL
ผิวตาที่คงที่ : บรรลุได้ใน 73-77% ของกรณีภายใต้การกดภูมิคุ้มกันสามชนิดที่เหมาะสม รายงานในการติดตามผลเฉลี่ย 4.5-4.7 ปี
การจำแนกความล้มเหลวของกราฟต์ : ความล้มเหลวปฐมภูมิ (เยื่อบุผิวไม่สมบูรณ์ภายใน 1 สัปดาห์หลังผ่าตัด), ความล้มเหลวบางส่วน (เยื่อบุตา หรือเนื้อเยื่อเกี่ยวพันปนกับเยื่อบุผิวปกติ), ความล้มเหลวทั้งหมด (LSCD กลับเป็นซ้ำรอบด้าน), ความล้มเหลวระยะหลัง (เนื่องจากการปฏิเสธเรื้อรัง)
ปัจจัยเสี่ยงต่อความล้มเหลว : การกลายเป็นเคราติน, ตาแห้ง , หนังตาติดลูกตา , การอักเสบเรื้อรัง, ประวัติการปฏิเสธก่อนหน้านี้
เปรียบเทียบเทคนิค LSCT แบบใช้เซลล์ตนเอง
CLAu (การปลูกถ่ายลิมบัส และเยื่อบุตา ตนเอง) : อัตราความสำเร็จทางกายวิภาค 81%, ทางการทำงาน 74.4%2) รายงานครั้งแรกโดย Kenyon และ Tseng ในปี 19892)
SLET (การปลูกถ่ายเยื่อบุลิมบัส แบบง่าย)2) ผลลัพธ์เทียบเท่ากับ CLAu2)
CLET (การปลูกถ่ายเยื่อบุลิมบัส ที่เพาะเลี้ยง) : อัตราความสำเร็จทางกายวิภาค 61.4%, ทางการทำงาน 53% ซึ่งด้อยกว่า CLAu และ SLET 2)
ภาวะแทรกซ้อนที่สำคัญที่สุดของ KLAL คือปฏิกิริยาการปฏิเสธทางภูมิคุ้มกัน การปฏิเสธเฉียบพลันแสดงออกเป็นอาการบวมและแดงของกราฟต์ เยื่อบุตา แดง และปวดตา การปฏิเสธเรื้อรังจะรุนแรงน้อยกว่า แสดงออกเป็นเยื่อบุตา หรือเนื้อเยื่อเกี่ยวพันค่อยๆ เกิดขึ้นและกราฟต์บางลง ในตาที่มีประวัติการปฏิเสธ อัตราการคงตัวลดลงเหลือ 39% การรักษาโดยการเสริมการกดภูมิคุ้มกันเฉพาะที่และทั่วร่างกาย ข้อห้ามสัมพัทธ์ของ KLAL ได้แก่ SJS , เพมฟิกอยด์เยื่อเมือกชนิดมีแผลเป็น และ LSCD ชนิดมีแผลเป็นจากการบาดเจ็บสารเคมีรุนแรง
Q
ต้องกดภูมิคุ้มกันนานเท่าใด?
A
โดยทั่วไปการกดภูมิคุ้มกันทั่วร่างกายจะลดลงทีละน้อย: ทาโครลิมัสหลังจาก 12-18 เดือนหลังผ่าตัด, MMF หลังจาก 3 ปี หากผิวตาคงที่และไม่มีประวัติการปฏิเสธ อาจหยุดยาได้ในที่สุด อย่างไรก็ตาม หากมีประวัติการปฏิเสธ ต้องให้การกดภูมิคุ้มกันขนาดต่ำต่อไปอย่างไม่มีกำหนด แนะนำให้ประสานงานกับผู้เชี่ยวชาญด้านการปลูกถ่ายอวัยวะ
Q
การมองเห็นดีขึ้นหลัง KLAL หรือไม่?
A
เป้าหมายหลักของ KLAL คือการสร้างผิวตาที่คงที่ ไม่ใช่การปรับปรุงการมองเห็น โดยตรง อย่างไรก็ตาม หลังจากผิวกระจกตา คงที่แล้ว สามารถเพิ่มการปลูกถ่ายกระจกตา เพื่อการมองเห็น (PKP หรือ DALK ) เพื่อปรับปรุงการมองเห็น ในกรณีที่ทำ KLAL ตามด้วย DMAK + allo-SLET มีรายงานการปรับปรุงค่าสายตาที่แก้ไขแล้วจาก 20/200 เป็น 20/403)
เซลล์ต้นกำเนิดลิมบัส อยู่ใน Palisades of Vogt ที่ชั้นเบซอลของลิมบัส 1) เซลล์ต้นกำเนิดเหล่านี้เคลื่อนที่เข้าสู่ศูนย์กลาง ก่อนอื่นจะแยกตัวเป็นเซลล์เยื่อบุผิวเบซอล จากนั้นเพิ่มจำนวนและเคลื่อนที่ไปยังผิวและหลุดลอก1) ลิมบัส ยังทำหน้าที่เป็นเกราะป้องกันการบุกรุกของเยื่อบุตา เข้าสู่กระจกตา 1)
ใน LSCD ความเสียหายต่อเซลล์ต้นกำเนิดลิมบัส ทำให้เยื่อบุกระจกตา ถูกแทนที่ด้วยเยื่อบุตา ทำให้กระจกตา สูญเสียความใส หากเหลือเซลล์ต้นกำเนิดลิมบัส เพียง 7% ก็สามารถสร้างเยื่อบุกระจกตา ขึ้นใหม่ได้ด้วยเทคนิคการผ่าตัดสมัยใหม่1)
ในโรคตาที่เรื้อรัง การทำงานร่วมกันของไซโตไคน์ที่ก่อให้เกิดการอักเสบและเพมฟิกอยด์ของเยื่อเมือกจะเปลี่ยนแปลงสภาพแวดล้อมจุลภาคของเซลล์ต้นกำเนิดลิมบัส 1) ใน LSCD ที่เกิดร่วมกับโรคกระจกตาพุพอง ในตาที่ไม่มีเส้นเลือดใหม่ที่กระจกตา การสร้างเยื่อบุผิวใช้เวลาประมาณ 6 วัน ในขณะที่ตาที่มีเส้นเลือดใหม่ต้องใช้เวลาประมาณ 29 วัน 1)
เยื่อบุกระจกตา และเยื่อบุตา ต่างกันทางสัณฐานวิทยา 1) เยื่อบุกระจกตา ปกติประกอบด้วยเซลล์แบนรูปหลายเหลี่ยมขนาดใหญ่ ชั้นฐานมีไซโทพลาสซึมสะท้อนแสงต่ำและขอบเขตชัดเจน 1) เยื่อบุตา รูปทรงลูกบาศก์ มีไซโทพลาสซึมสะท้อนแสงสูงกว่าและมีเซลล์กุณโฑ 1) ไซโตเคราติน 3 จำเพาะต่อเยื่อบุกระจกตา ในขณะที่ไซโตเคราติน 19 จำเพาะต่อเยื่อบุตา 1)
เพื่อเป็นการกู้ชีพหลังจาก KLAL ล้มเหลว มีรายงานการใช้การปลูกถ่ายกระจกตา ชั้นหน้าด้วยเยื่อเดสเซเมตที่กำจัดเซลล์ออก (DMAK) ร่วมกับการปลูกถ่ายเยื่อบุลิมบัส แบบอัลโลจีนิกอย่างง่าย (allo-SLET ) 3) เยื่อเดสเซเมตทนทานต่อการย่อยสลายได้ดีกว่าเมื่อเทียบกับเยื่อหุ้มน้ำคร่ำของมนุษย์ (HAM) โดยสามารถทนต่อการแช่ในคอลลาจีเนสความเข้มข้นสูงนานกว่า 24 ชั่วโมง ในขณะที่ HAM ถูกย่อยสลายภายใน 30 นาที 3)
เซลล์ต้นกำเนิดลิมบัส ที่เพาะเลี้ยงบนเยื่อเดสเซเมตแสดงการแสดงออกของเครื่องหมายเซลล์ต้นกำเนิด (ABCG2, p63) ได้ดีกว่าเมื่อเทียบกับที่เพาะเลี้ยงบน HAM 3) ในกรณี LSCD ที่เกี่ยวข้องกับกลุ่มอาการต่อมไร้ท่อหลายต่อมชนิดภูมิต้านตนเองซึ่งเกิดการปฏิเสธ KLAL หลังจากทำ DMAK + allo-SLET การมองเห็นที่แก้ไขแล้ว ดีขึ้นจาก 20/200 เป็น 20/40 และไม่มีการกลับเป็นซ้ำของข้อบกพร่องของเยื่อบุผิวนาน 1.5 ปี 3)
เยื่อเดสเซเมตมีข้อดีในด้านความโปร่งใส ความทนทาน และการเป็นวัสดุรองรับการเพาะเลี้ยงเซลล์ต้นกำเนิดลิมบัส จึงมีแนวโน้มเป็นวิธีการกู้ชีพหลังจาก KLAL ล้มเหลว อย่างไรก็ตาม ประสิทธิภาพในระยะยาวและการตอบสนองทางภูมิคุ้มกันยังต้องศึกษาเพิ่มเติม 3)
มีความก้าวหน้าในการวินิจฉัย LSCD เช่นกัน 1) ด้วยความแม่นยำที่เพิ่มขึ้นของกล้องจุลทรรศน์คอนโฟคอล ในร่างกายและ AS-OCT การประเมินความรุนแรงของ LSCD อย่างเป็นกลางและการติดตามผลการรักษากำลังดีขึ้น 1) ในภาวะไม่มีม่านตา ความก้าวหน้าในการวิเคราะห์ทางพันธุกรรมอาจมีส่วนช่วยในการพยากรณ์โรคและการจัดการ 1)
Hu JCW, Trief D. A narrative review of limbal stem cell deficiency & severe ocular surface disease. Ann Eye Sci. 2023;8:13.
Vazirani J, Nair D, Shanbhag S, et al. Autologous limbal stem cell transplantation for unilateral limbal stem cell deficiency: a systematic review. Br J Ophthalmol. 2021;105(2):247-252.
Cheung AY, Reinisch CB, Hou JH. Decellularized Descemet Membrane Anterior Keratoplasty With Allogeneic Simple Limbal Epithelial Transplantation for Partial Limbal Stem Cell Deficiency Following Partial Keratolimbal Allograft Failure. Cornea. 2025;44(1):108-112.
ถาม AI เกี่ยวกับบทความนี้
คัดลอกข้อความบทความแล้ววางในผู้ช่วย AI ที่คุณต้องการใช้
เปิดผู้ช่วย AI ด้านล่าง แล้ววางข้อความที่คัดลอกลงในช่องแชต