导致高频率I-CNV的疾病

葡萄膜炎相关的脉络膜新生血管(炎症性脉络膜新生血管)
1. 什么是炎症性脉络膜新生血管(I-CNV)?
Section titled “1. 什么是炎症性脉络膜新生血管(I-CNV)?”脉络膜新生血管(CNV)是一种源自脉络膜的新生血管好发于黄斑部的疾病。新生血管在视网膜色素上皮(RPE)下(1型/经典型)或RPE上(2型/隐匿型)增殖。在脉络膜炎或特发性病例中,炎症起重要作用,CNV被认为是RPE-Bruch膜-脉络膜毛细血管层损伤后的反应性改变或伤口愈合过程。
炎症性脉络膜新生血管(I-CNV)是由脉络膜视网膜炎症引起的后葡萄膜炎的严重并发症。它可发生于感染性和非感染性葡萄膜炎1)。I-CNV被认为是继AMD和病理性近视之后CNV的第三大原因1)。
后葡萄膜炎患者中CNV发生率为2.7%,全葡萄膜炎患者中为0.8%,高于前部和中间部葡萄膜炎(0.1%)1)。特发性葡萄膜炎中13-20%出现CNV并发症3)。I-CNV大多表现为2型(经典型)CNV,突破Bruch膜后形成于RPE下(1型)或RPE上(2型)1)。
感染性疾病中的I-CNV
弓形虫脉络膜视网膜炎:0.3%~19%
眼组织胞浆菌病:5%~17.4%
眼结核:罕见病例报告
念珠菌脉络膜视网膜炎:罕见(患病率未知)
风疹视网膜病变:罕见病例报告
弓蛔虫病:罕见病例报告
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”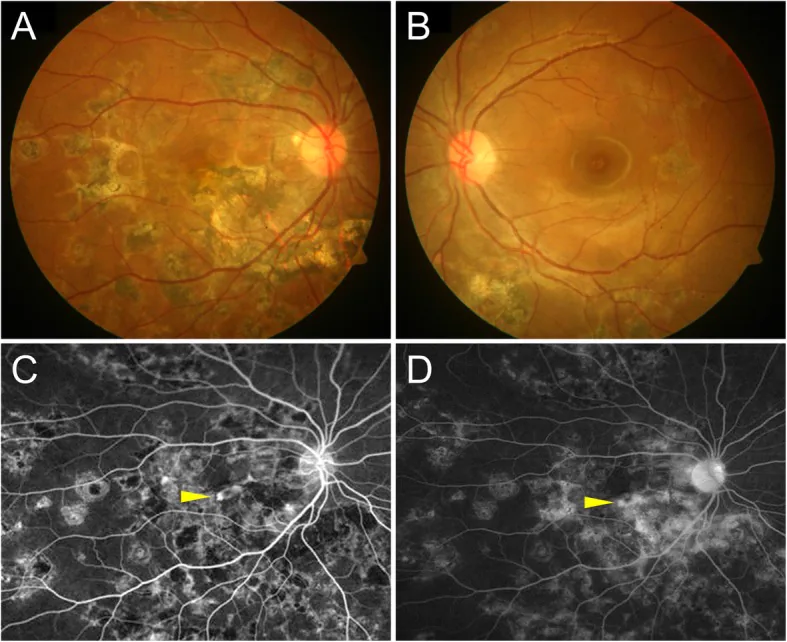
I-CNV的典型初发症状是视力急剧下降和出现视物变形1)。
- 无痛性视力下降和暗点
- 视物变形症:直线看起来扭曲
- 闪光感:伴有活动性葡萄膜炎时
- 中心暗点:在进展期出现1)
位于中心凹外的活动性病变可能无症状,并可能因炎性病变、瘢痕、色素沉着或视网膜内外液体积聚而被漏诊1)。
眼底检查可见黄斑周围有黄白色视网膜下病变。
- 视网膜色素上皮下CNV(经典型):表现为橙红色隆起病灶
- 视网膜色素上皮上CNV(隐匿型):表现为灰白色斑块,伴有边缘性视网膜下出血和视网膜脱离
- I-CNV的黄斑内分布:中心凹下60%、中心凹旁35%、视乳头周围5%
- 纤维血管性瘢痕(既往CNV活动的痕迹)可能残留
CNV消退后,视网膜色素上皮-脉络膜毛细血管层可形成萎缩病灶。视网膜色素上皮上CNV在视网膜下形成纤维组织,可能导致永久性视力下降、中心暗点和视物变形。
3. 病因与危险因素
Section titled “3. 病因与危险因素”病理生理:两种机制1)
活化的炎性细胞分泌细胞毒性酶,降解Bruch膜。释放的促血管生成细胞因子(IL-6、IL-8、TNF-α)促进VEGF表达和CNV生长2)。在葡萄膜炎中,TNF-α、IL-6和IL-1等细胞因子损伤RPE,进一步放大VEGF表达,促进I-CNV形成3)。
根据葡萄膜炎诊疗指南(2019年),在PIC、多灶性脉络膜炎、结节病、原田病、匍行性脉络膜炎等后葡萄膜炎中,需注意CNV的合并,推荐炎症控制与抗VEGF疗法联合使用3)。
风险因素5):
| 风险因素 | 内容 |
|---|---|
| 视网膜下新生血管的存在 | I-CNV发病风险增加3倍以上 |
| 活动性炎症 | 与非活动期相比,CNV风险显著增高 |
| 前房炎症2级以上 | 与I-CNV显著相关 |
| 对侧眼CNV病史 | CNV发病风险增加数倍 |
| 单侧葡萄膜炎 | CNV风险高于双侧 |
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”I-CNV的诊断较为困难,建议采用多模态影像诊断1)。
荧光素眼底血管造影(FA):大多数I-CNV表现为经典型(2型)CNV。CNV病变显示早期等荧光至强荧光,晚期有荧光渗漏。然而,活动性炎症病变也呈现类似的FA表现,因此单独使用FA进行诊断存在局限性1)。特征性表现为早期边界清晰的强荧光(经典型)或晚期弥漫性色素渗漏(隐匿型)。
吲哚青绿血管造影(ICGA):能比FA更详细地评估脉络膜血管结构。I-CNV早期即显示强荧光,可与活动性炎症灶(早期弱荧光)鉴别1)。ICGA对于鉴别视网膜色素上皮下CNV至关重要,在多灶性脉络膜炎中,有助于评估脉络膜毛细血管板无灌注范围及CNV发生风险1)。
光学相干断层扫描(OCT):可无创、快速地检查黄斑部断面,评估CNV与中心凹的位置关系、CNV位于RPE上方还是下方,以及伴随的视网膜脱离、RPE脱离和囊样黄斑水肿的状态。
- “干草叉征(pitchfork sign)”:从I-CNV向外层视网膜呈指状延伸的高反射病变。这是多灶性脉络膜炎/PIC、眼内结核、急性梅毒性后极多形性脉络膜视网膜炎中报告的I-CNV特征性OCT表现1)
- “海绵征(sponge sign)”:I-CNV下方的脉络膜厚度增加(治疗后降低)。用于鉴别炎症性与近视性CNV的辅助征象1)
- 中心视网膜厚度可作为I-CNV活动性的客观指标1)
OCT血管造影(OCTA):可无创显示CNV的血管结构。与单独FA相比,在区分CNV和炎性病变方面具有更高的准确性,尤其有助于识别1型新生血管网络8)。
自发荧光眼底摄影(FAF):活动性I-CNV显示正常荧光或高自发荧光。低自发荧光区域与光感受器和RPE丧失相关,有助于检测周边I-CNV1)。
5. 标准治疗方法
Section titled “5. 标准治疗方法”及时治疗I-CNV可防止不可逆的视力丧失。治疗需要结合两种方法。
方法1:基础葡萄膜炎的管理
Section titled “方法1:基础葡萄膜炎的管理”首先排除感染性疾病(如弓形虫病、结核、汉塞巴尔通体等),并进行适当的抗感染治疗。排除后对基础葡萄膜炎的治疗:
- 短期:全身糖皮质激素治疗(泼尼松龙 0.5–1 mg/kg/天)
- 复发性、慢性或进行性疾病(如多灶性脉络膜炎、原田病、匍行性脉络膜炎):为减少类固醇用量而使用免疫抑制治疗
- 如果炎症持续存在:后部Tenon囊下糖皮质激素注射(曲安奈德)也是一种选择
方法2:中心凹CNV的抗VEGF药物玻璃体内注射
Section titled “方法2:中心凹CNV的抗VEGF药物玻璃体内注射”无论病因如何,对于中心凹CNV,均进行抗VEGF药物的玻璃体内注射。由于VEGF与CNV的发生发展密切相关,抑制VEGF的药物有助于促进CNV消退、防止出血和渗出。
| 药物 | 概述 | 对炎症性CNV的适用 |
|---|---|---|
| 阿柏西普(艾力雅) | VEGF-A/VEGF-B/PlGF抑制 | 医保不覆盖(AMD和近视性黄斑病变已覆盖) |
| 雷珠单抗(Lucentis) | 抗VEGF-A单克隆抗体片段 | 医保不覆盖(AMD和近视性黄斑病变已覆盖) |
| 贝伐珠单抗(Avastin) | 抗VEGF-A全长单克隆抗体 | 医保不覆盖(超说明书使用),用于炎症性CNV |
阿柏西普和雷珠单抗的保险适用范围仅限于年龄相关性黄斑变性和近视性黄斑病变。对于炎症性CNV,贝伐珠单抗(1.25 mg/0.05 mL玻璃体内注射)可超说明书使用3)。
抗炎治疗与抗VEGF药物联合使用可使80%的患者改善,15%的患者稳定4)。PIC患者单独使用抗VEGF药物治疗的复发率为50%,表明需要对基础葡萄膜炎进行全身治疗7)。
导入期(每月注射,持续3个月)与按需给药(PRN)的比较显示,设置导入期并不能带来更好的预后1)。随机对照试验已证实抗VEGF药物(雷珠单抗0.5 mg玻璃体内注射)对改善I-CNV的视力和消退新生血管有效6)。
中心凹外CNV的激光光凝术
Section titled “中心凹外CNV的激光光凝术”对于中心凹外CNV,采用热激光进行光凝治疗。光凝可直接闭塞CNV,但照射部位会造成永久性视网膜损伤,因此需仔细评估与中心凹的距离以决定适应症。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”I-CNV的病理生理学与AMD、病理性近视等CNV相似,但特点是增加了炎症因子1)。
慢性炎症、氧化应激和缺血等因素参与,CNV作为对RPE-Bruch膜-脉络膜毛细血管板损伤的反应性变化或伤口愈合过程而发生。
分子机制:
- VEGF表达增加促进新生血管增殖(与AMD和近视性CNV相同)
- CNV的血管外成分中存在表达CXCR4的成纤维细胞和白细胞
- RPE细胞产生TNF-α、IL-1、IL-2、IL-6和IL-10,作为炎症成分发挥作用1)
- 与血管生成抑制因子(血管抑素、内皮抑素、PEDF)之间的失衡是触发因素1)
在葡萄膜炎中,TNF-α、IL-6、IL-1等细胞因子由炎症细胞分泌,损伤RPE并进一步放大VEGF的表达3)。这些细胞因子与VEGF的相互作用促进了I-CNV的形成。
I-CNV与AMD相关CNV的区别: 免疫组织化学研究报道,I-CNV血管网的CXCR4染色模式与AMD相关CNV不同,提示毛细血管在膜形成中可能扮演不同角色9)。
部分“特发性”CNV可能作为后葡萄膜炎的前驱症状出现1)。新生血管常从炎症病灶边缘(炎症后萎缩性脉络膜视网膜瘢痕的边缘)生长。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”OCTA提高诊断准确性:
OCTA在I-CNV的诊断和随访中发挥着重要作用。与单独使用FA/ICGA相比,OCTA的优势证据正在积累,即使FA/ICGA结果不确定,OCTA也被证明对于识别1型新生血管网络至关重要8)。OCTA也可作为活动性CNV的监测指标,能够定量评估治疗后新生血管的消退情况8)。
“海绵征”的临床意义:
OCT上I-CNV下方的脉络膜厚度增加(治疗后下降的“海绵征”)作为监测I-CNV活动性的新辅助指标而受到关注。它也可能用于区分炎症性CNV和近视性CNV1)。
抗VEGF治疗的长期结果:
针对各种原因的后部葡萄膜炎,抗VEGF治疗(1-5次注射)后,logMAR视力改善约0.3个单位的中长期数据已积累4)。PIC患者单独使用抗VEGF药物治疗的复发率为50%,基础疾病的管理决定长期预后7)。
治疗并延长(T&E)方案:
在AMD和近视性CNV中确立的T&E方案(逐步延长治疗间隔)正在被研究应用于I-CNV。它可能在减少治疗负担的同时维持视力,但需要积累针对炎症性CNV的证据。
Faricimab(抗VEGF-A/Ang-2双重抑制剂):
同时抑制VEGF-A和血管生成素-2(Ang-2)的faricimab已获批用于AMD和糖尿病黄斑水肿,其对炎症性CNV的应用正处于研究阶段。由于Ang-2参与血管新生和炎症,预计对I-CNV有特异性效果。
多模态方法标准化:
I-CNV的诊断采用包括FAF、OCTA和近红外自发荧光成像的多模态方法很有前景,尤其是FAF在检测和监测周边I-CNV方面非常有用1)。
8. 参考文献
Section titled “8. 参考文献”- Karska-Basta I, Pociej-Marciak W, Zuber-Laskawiec K, et al. Diagnostic challenges in inflammatory choroidal neovascularization. Medicina. 2024;60(3):465.
- Cheung CMG, Arnold JJ, Holz FG, et al. Myopic choroidal neovascularization: review, guidance, and consensus statement on management. Ophthalmology. 2017;124(11):1690-1711.
- 日本眼科学会ぶどう膜炎診療ガイドライン作成委員会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635-696.
- D’Souza Y, Balasubramaniam S, Nair U. Anti-VEGF treatment for inflammatory choroidal neovascularization: a comprehensive review. Surv Ophthalmol. 2023;68(3):435-461.
- Baxter SL, Pistilli M, Pujari SS, et al. Risk of choroidal neovascularization among the uveitides. Am J Ophthalmol. 2013;156(3):468-477.e2.
- Rouvas A, Petrou P, Douvali M, et al. Intravitreal ranibizumab for the treatment of inflammatory choroidal neovascularization. Retina. 2011;31(5):871-879.
- Amer R, Lois N. Punctate inner choroidopathy. Surv Ophthalmol. 2011;56(1):36-53.
- Astroz P, Miere A, Mrejen S, et al. Optical coherence tomography angiography to distinguish choroidal neovascularization from macular inflammatory lesions in multifocal choroiditis. Retina. 2018;38(2):299-309.
- Neri P, Lettieri M, Fortuna C, et al. Inflammatory choroidal neovascularization. Middle East Afr J Ophthalmol. 2009;16(4):245-251.
