โรคที่ทำให้เกิด I-CNV บ่อย

เยื่อหุ้มคอรอยด์สร้างเส้นเลือดใหม่จากการอักเสบ (Inflammatory Choroidal Neovascularization)
1. ภาวะหลอดเลือดใหม่ในคอรอยด์จากการอักเสบ (I-CNV) คืออะไร
หัวข้อที่มีชื่อว่า “1. ภาวะหลอดเลือดใหม่ในคอรอยด์จากการอักเสบ (I-CNV) คืออะไร”ภาวะหลอดเลือดใหม่ในคอรอยด์ (choroidal neovascularization; CNV) คือโรคที่เกิดจากหลอดเลือดใหม่ที่มาจากคอรอยด์ มักเกิดบริเวณจอประสาทตาส่วนกลาง (macula) หลอดเลือดใหม่เหล่านี้เจริญเติบโตใต้ชั้น retinal pigment epithelium (RPE) (ชนิดที่ 1/Classic) หรือเหนือชั้น RPE (ชนิดที่ 2/Occult) ในกรณีที่เกิดจากคอรอยด์อักเสบหรือไม่ทราบสาเหตุ การอักเสบมีบทบาทสำคัญ และ CNV ถือเป็นปฏิกิริยาตอบสนองต่อความเสียหายของชั้น RPE-Bruch’s membrane-choriocapillaris หรือเป็นกระบวนการสมานแผล
หลอดเลือดใหม่ผิดปกติในคอรอยด์จากสาเหตุการอักเสบ (I-CNV) เป็นภาวะแทรกซ้อนรุนแรงของม่านตาอักเสบส่วนหลังที่เกิดจากการอักเสบของคอรอยด์และจอประสาทตา สามารถเกิดได้ทั้งจากม่านตาอักเสบที่ติดเชื้อและไม่ติดเชื้อ1) I-CNV เป็นสาเหตุอันดับสามของ CNV รองจาก AMD และสายตาสั้นทางพยาธิวิทยา1)
ในผู้ป่วยม่านตาอักเสบส่วนหลังพบ CNV ร้อยละ 2.7 ในผู้ป่วยม่านตาอักเสบทั้งส่วนหน้าและส่วนหลังพบร้อยละ 0.8 ซึ่งสูงกว่าม่านตาอักเสบส่วนหน้าและส่วนกลาง (ร้อยละ 0.1)1) ในม่านตาอักเสบที่ไม่ทราบสาเหตุพบ CNV เป็นภาวะแทรกซ้อนร้อยละ 13–203) I-CNV ส่วนใหญ่เป็นชนิดที่ 2 (คลาสสิก) ซึ่งเกิดการทะลุผ่าน Bruch’s membrane และก่อตัวใต้ RPE (ชนิดที่ 1) หรือเหนือ RPE (ชนิดที่ 2)1)
I-CNV ในโรคติดเชื้อ
จอประสาทตาอักเสบจากท็อกโซพลาสมา : 0.3–19%
โรคฮิสโทพลาสโมซิสที่ตา : 5–17.4%
วัณโรคตา: รายงานผู้ป่วยที่พบได้ยาก
จอประสาทตาอักเสบจากเชื้อแคนดิดา: พบได้ยาก (ไม่ทราบความชุกที่แน่ชัด)
จอประสาทตาจากโรคหัดเยอรมัน: รายงานผู้ป่วยที่พบได้ยาก
โรคท็อกโซคารา: รายงานผู้ป่วยที่พบได้ยาก
2. อาการหลักและผลการตรวจทางคลินิก
หัวข้อที่มีชื่อว่า “2. อาการหลักและผลการตรวจทางคลินิก”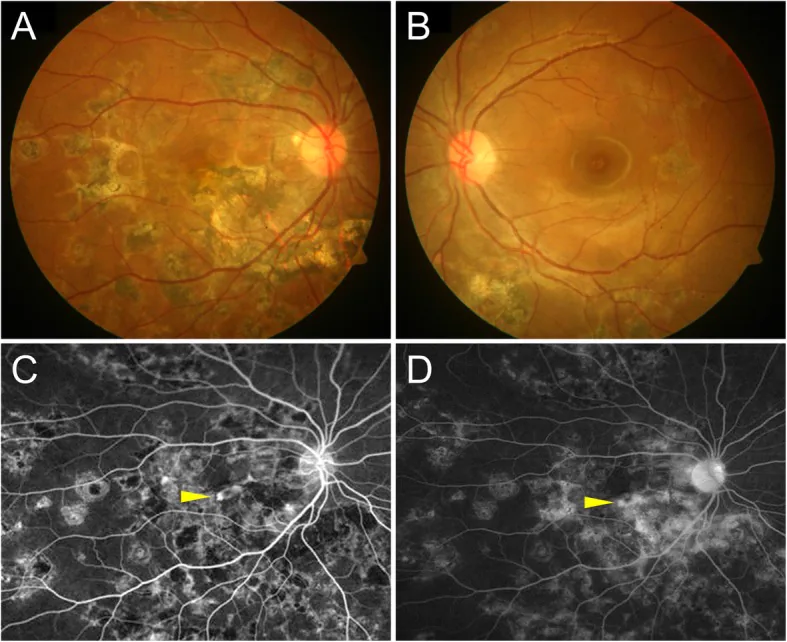
อาการที่ผู้ป่วยรับรู้
หัวข้อที่มีชื่อว่า “อาการที่ผู้ป่วยรับรู้”อาการเริ่มแรกโดยทั่วไปของ I-CNV คือการมองเห็นแย่ลงอย่างรวดเร็วและการมองเห็นผิดรูป (metamorphopsia) 1)
- การมองเห็นลดลงโดยไม่เจ็บปวดและจุดบอด (scotoma)
- การมองเห็นผิดรูป (metamorphopsia): เห็นเส้นตรงบิดเบี้ยว
- การเห็นแสงวาบ (photopsia): เมื่อมีม่านตาอักเสบชนิด active uveitis ร่วมด้วย
- จุดบอดกลาง: เกิดขึ้นในกรณีที่ลุกลาม 1)
รอยโรคที่ทำงานอยู่นอกโฟเวียอาจไม่มีอาการ และอาจถูกมองข้ามเนื่องจากรอยโรคอักเสบ แผลเป็น การสะสมของเม็ดสี หรือการสะสมของของเหลวในและนอกจอประสาทตา 1)
อาการทางคลินิก
หัวข้อที่มีชื่อว่า “อาการทางคลินิก”การตรวจอวัยวะภายในลูกตาพบรอยโรคใต้จอประสาทตาสีขาวเหลืองรอบบริเวณจอประสาทตา
- CNV ใต้เยื่อบุจอประสาทตา (ชนิด Classic): แสดงเป็นรอยโรคยกตัวสีส้มแดง
- CNV เหนือเยื่อบุจอประสาทตา (ชนิด Occult): พบเป็นรอยสีเทาขาว ร่วมกับเลือดออกใต้จอประสาทตาและจอประสาทตาลอกแบบมีขอบ
- การกระจายของ I-CNV ในจอประสาทตาส่วนกลาง: ใต้รอยบุ๋มจอประสาทตา (subfoveal) 60%, ใกล้รอยบุ๋มจอประสาทตา (juxtafoveal) 35%, รอบหัวประสาทตา (peripapillary) 5%
- รอยแผลเป็นจากเส้นใยหลอดเลือด (ร่องรอยของกิจกรรม CNV ในอดีต) ยังคงอยู่
แม้ CNV จะแห้งแล้ว ยังเกิดรอยฝ่อของชั้น retinal pigment epithelium-choriocapillaris ได้ สำหรับ CNV เหนือ RPE จะเกิดเนื้อเยื่อพังผืดใต้จอประสาทตา ทำให้สายตาเสื่อม จุดบอดกลาง และภาพบิดเบี้ยวอาจคงอยู่ถาวร
3. สาเหตุและปัจจัยเสี่ยง
หัวข้อที่มีชื่อว่า “3. สาเหตุและปัจจัยเสี่ยง”พยาธิสรีรวิทยา: 2 กลไก1)
- การบาดเจ็บจากการอักเสบ: การอักเสบทำลาย RPE-เยื่อบรูช → การทำลายสิ่งกีดขวางเลือด-จอประสาทตาชั้นนอก → การเจริญของเส้นเลือดใหม่จากคอรอยด์
- ภาวะขาดเลือด/ขาดออกซิเจน: การไหลเวียนบกพร่องจากการอักเสบ → การไล่ระดับออกซิเจนต่ำในจอประสาทตาและคอรอยด์ → ส่งเสริมการสร้าง CNV
เมื่อเซลล์อักเสบถูกกระตุ้น จะหลั่งเอนไซม์ที่ทำลายเซลล์เพื่อย่อยสลายเยื่อบรูช ไซโตไคน์ที่ส่งเสริมการสร้างเส้นเลือดใหม่ (IL-6, IL-8, TNF-α) ที่ถูกปล่อยออกมาจะกระตุ้นการแสดงออกของ VEGF และส่งเสริมการเจริญของ CNV2) ในม่านตาอักเสบ ไซโตไคน์เช่น TNF-α, IL-6, IL-1 จะทำลาย RPE และเพิ่มการแสดงออกของ VEGF มากขึ้นไปอีก ส่งเสริมการสร้าง I-CNV3)
ตามแนวทางเวชปฏิบัติสำหรับโรคม่านตาอักเสบ (ปี 2019) ในกรณีของ posterior uveitis เช่น PIC, multifocal choroiditis, sarcoidosis, Vogt-Koyanagi-Harada disease, และ serpiginous choroiditis จำเป็นต้องระวังการเกิด CNV ร่วมด้วย และแนะนำให้ใช้การควบคุมการอักเสบร่วมกับการรักษาด้วย anti-VEGF 3)
ปัจจัยเสี่ยง5):
| ปัจจัยเสี่ยง | รายละเอียด |
|---|---|
| การมีอยู่ของหลอดเลือดใหม่ในชั้นจอประสาทตา | ความเสี่ยงในการเกิด I-CNV เพิ่มขึ้นมากกว่า 3 เท่า |
| การอักเสบที่ยังดำเนินอยู่ | ความเสี่ยงของ CNV สูงกว่าช่วงที่ไม่มีการอักเสบอย่างมีนัยสำคัญ |
| การอักเสบในช่องหน้าม่านตาระดับ 2+ | ความสัมพันธ์ที่มีนัยสำคัญกับ I-CNV |
| ประวัติ CNV ในตาข้างตรงข้าม | ความเสี่ยงในการเกิด CNV สูงขึ้นหลายเท่า |
| ยูเวียอักเสบข้างเดียว | มีความเสี่ยงต่อ CNV สูงกว่าการเกิดสองข้าง |
4. วิธีการวินิจฉัยและการตรวจ
หัวข้อที่มีชื่อว่า “4. วิธีการวินิจฉัยและการตรวจ”การวินิจฉัย I-CNV เป็นเรื่องยาก และแนะนำให้ใช้การวินิจฉัยด้วยภาพหลายรูปแบบ (multimodal imaging) 1)
การตรวจหลอดเลือดด้วยฟลูออเรสซีน (FA) : I-CNV ส่วนใหญ่จะปรากฏเป็น CNV แบบคลาสสิก (ชนิดที่ 2) รอยโรค CNV จะแสดงการเรืองแสงเท่ากับหรือมากกว่าปกติในระยะแรก และมีการรั่วของฟลูออเรสซีนในระยะหลัง อย่างไรก็ตาม รอยโรคอักเสบที่ยังทำงานอยู่ก็ให้ผล FA ที่คล้ายกัน ดังนั้นการวินิจฉัยด้วย FA เพียงอย่างเดียวจึงมีข้อจำกัด 1) ลักษณะเฉพาะคือการเรืองแสงมากเกินไปที่มีขอบเขตชัดเจนในระยะแรก (ชนิดคลาสสิก) หรือการรั่วของสีแบบกระจายในระยะหลัง (ชนิดอ็อคคัลท์)
การตรวจหลอดเลือดด้วยอินโดไซยานีนกรีน (ICGA) : สามารถประเมินโครงสร้างหลอดเลือดคอรอยด์ได้ละเอียดกว่า FA I-CNV จะแสดงการเรืองแสงมากเกินไปตั้งแต่ระยะแรก และสามารถแยกความแตกต่างจากรอยโรคอักเสบที่ยังทำงานอยู่ (ซึ่งมีการเรืองแสงน้อยในระยะแรก) ได้ 1) ICGA เป็นสิ่งจำเป็นในการแยกความแตกต่างของ CNV ใต้ชั้นจอประสาทตา และในกรณีของ choroiditis หลายจุด (multifocal choroiditis) มีประโยชน์ในการประเมินบริเวณที่ไม่มีการไหลเวียนของหลอดเลือดฝอยคอรอยด์และการประเมินความเสี่ยงในการเกิด CNV 1)
เครื่องตรวจการเชื่อมโยงแสง (OCT) : สามารถตรวจสอบภาพตัดขวางของจอประสาทตาส่วนกลางได้อย่างรวดเร็วและไม่รุกราน ช่วยประเมินความสัมพันธ์ระหว่าง CNV กับรอยบุ๋มจอตา ว่า CNV อยู่เหนือหรือใต้ RPE รวมถึงประเมินภาวะจอตาลอก RPE ลอก และจอตาบวมน้ำแบบถุงน้ำที่เกิดขึ้นร่วม
- “สัญญาณคราด (pitchfork sign)” : รอยโรคสะท้อนแสงสูงที่ยื่นจาก I-CNV ไปยังชั้นจอตาชั้นนอกคล้ายนิ้วมือ เป็นลักษณะ OCT ที่จำเพาะต่อ I-CNV ที่รายงานใน multifocal choroiditis/PIC, วัณโรคในตา, และ acute syphilitic posterior polymorphous chorioretinitis 1)
- “สัญญาณฟองน้ำ (sponge sign)” : ความหนาของคอรอยด์ที่เพิ่มขึ้นใต้ I-CNV (ลดลงหลังการรักษ) เป็นลักษณะช่วยแยก CNV อักเสบจาก CNV สายตาสั้น 1)
- ความหนาจอตาส่วนกลางเป็นตัวชี้วัดภาวะกิจกรรมของ I-CNV ที่เป็นกลางและมีประโยชน์ 1)
OCT angiography (OCTA): สามารถมองเห็นโครงสร้างหลอดเลือดของ CNV ได้โดยไม่ต้องรุกราน มีความแม่นยำสูงกว่า FA เพียงอย่างเดียวในการแยก CNV ออกจากรอยโรคอักเสบ และมีประโยชน์โดยเฉพาะในการระบุเครือข่ายหลอดเลือด新生ชนิดที่ 1 8)
การถ่ายภาพอัตโนมัติของจอประสาทตา (FAF): ใน I-CNV ที่มีการเคลื่อนไหว จะแสดงการเรืองแสงปกติหรือการเรืองแสงมากเกินไป บริเวณที่เรืองแสงน้อยสัมพันธ์กับการสูญเสียเซลล์รับแสงและ RPE และมีประโยชน์ในการตรวจหา I-CNV ที่บริเวณรอบนอก 1)
5. วิธีการรักษามาตรฐาน
หัวข้อที่มีชื่อว่า “5. วิธีการรักษามาตรฐาน”การรักษา I-CNV อย่างรวดเร็วช่วยป้องกันการสูญเสียการมองเห็นที่ไม่สามารถฟื้นคืนได้ การรักษาจำเป็นต้องใช้สองแนวทางร่วมกัน
แนวทางที่ 1: การจัดการโรคม่านตาอักเสบที่เป็นสาเหตุพื้นฐาน
หัวข้อที่มีชื่อว่า “แนวทางที่ 1: การจัดการโรคม่านตาอักเสบที่เป็นสาเหตุพื้นฐาน”ต้องแยกโรคติดเชื้อ (เช่น ทอกโซพลาสมา วัณโรค บาร์โตเนลลา เฮนเซเล) ออกก่อน แล้วให้การรักษาด้วยยาต้านการติดเชื้อที่เหมาะสม หลังจากแยกโรคแล้ว การรักษาโรคม่านตาอักเสบพื้นฐาน:
- ระยะสั้น: การรักษาด้วยสเตียรอยด์ทั่วร่างกาย (prednisolone 0.5-1 มก./กก./วัน)
- โรคที่กลับเป็นซ้ำ เรื้อรัง หรือลุกลาม (multifocal choroiditis, Harada disease, serpiginous choroiditis): การรักษาด้วยยากดภูมิคุ้มกันเพื่อลดขนาดสเตียรอยด์
- หากยังมีการอักเสบหลงเหลือ: การฉีดสเตียรอยด์ใต้ Tenon capsule ด้านหลัง (triamcinolone) เป็นทางเลือกหนึ่ง
แนวทางที่ 2: การฉีดยา anti-VEGF เข้าแก้วตาเพื่อรักษา CNV ที่จอประสาทตาส่วนกลาง
หัวข้อที่มีชื่อว่า “แนวทางที่ 2: การฉีดยา anti-VEGF เข้าแก้วตาเพื่อรักษา CNV ที่จอประสาทตาส่วนกลาง”โดยไม่คำนึงถึงโรคที่เป็นสาเหตุ สำหรับ CNV ที่จอประสาทตาส่วนกลาง (foveal CNV) ให้ฉีดยา VEGF inhibitor เข้าไปในน้ำวุ้นตา เนื่องจาก VEGF มีส่วนเกี่ยวข้องอย่างใกล้ชิดกับการเกิดและการเจริญเติบโตของ CNV ยาที่ยับยั้ง VEGF จึงมีประโยชน์ในการทำให้ CNV หดตัวและป้องกันการรั่วซึมของเลือดและของเหลว
| ยา | ภาพรวม | การประยุกต์ใช้กับ CNV ที่เกิดจากการอักเสบ |
|---|---|---|
| อะฟลิเบอร์เซปต์ (Eylea) | ยับยั้ง VEGF-A/VEGF-B/PlGF | ไม่ครอบคลุมโดยประกัน (ครอบคลุมสำหรับ AMD และจอประสาทตาเสื่อมจากสายตาสั้น) |
| รานิบิซูแมบ (Lucentis) | ชิ้นส่วนโมโนโคลนอลแอนติบอดีที่ต้าน VEGF-A | ไม่ครอบคลุมโดยประกัน (ครอบคลุมสำหรับ AMD และจอประสาทตาเสื่อมจากสายตาสั้น) |
| เบวาซิซูแมบ (อาวาสติน) | แอนติบอดีโมโนโคลนอลแบบเต็มความยาวต่อต้าน VEGF-A | นอกเหนือข้อบ่งชี้ (off-label) ใช้สำหรับ CNV อักเสบ |
การครอบคลุมของประกันสำหรับอะฟลิเบอร์เซปต์และรานิบิซูแมบจำกัดเฉพาะโรคจอประสาทตาเสื่อมตามอายุและโรคจอประสาทตาเหตุสายตาสั้น สำหรับ CNV อักเสบ จะใช้เบวาซิซูแมบ (1.25 มก./0.05 มล. ฉีดเข้าน้ำวุ้นตา) แบบนอกเหนือข้อบ่งชี้3)
การรักษาด้วยยาต้านการอักเสบร่วมกับยาต้าน VEGF ช่วยให้ผู้ป่วย 80% ดีขึ้น และ 15% มีอาการคงที่4) การรักษาด้วยยาต้าน VEGF เพียงอย่างเดียวในผู้ป่วย PIC รายงานอัตราการกลับเป็นซ้ำ 50% ซึ่งบ่งชี้ถึงความจำเป็นในการรักษาทั่วร่างกายสำหรับม่านตาอักเสบพื้นฐาน7)
การเปรียบเทียบระหว่างระยะเริ่มต้น (ฉีดทุกเดือนเป็นเวลา 3 เดือน) และการให้ยาเมื่อจำเป็น (PRN) พบว่าการมีระยะเริ่มต้นไม่ได้ให้ผลลัพธ์ที่ดีกว่า1) การทดลองแบบสุ่มที่มีกลุ่มควบคุมยืนยันว่ายาต้าน VEGF (ranibizumab 0.5 มก. ฉีดเข้าแก้วตา) มีประสิทธิภาพในการฟื้นฟูการมองเห็นและทำให้หลอดเลือดใหม่ใน I-CNV หดตัว6)
การจี้ด้วยเลเซอร์สำหรับ CNV นอกโฟเวีย
หัวข้อที่มีชื่อว่า “การจี้ด้วยเลเซอร์สำหรับ CNV นอกโฟเวีย”สำหรับ CNV นอกโฟเวีย จะทำการจี้ด้วยเลเซอร์ความร้อนเพื่ออุดตัน CNV โดยตรง แต่บริเวณที่ถูกจี้จะเกิดความเสียหายต่อจอประสาทตาอย่างถาวร ดังนั้นจึงต้องประเมินระยะห่างจากโฟเวียอย่างรอบคอบเพื่อตัดสินใจในการรักษา
6. พยาธิสรีรวิทยาและกลไกการเกิดโรคโดยละเอียด
หัวข้อที่มีชื่อว่า “6. พยาธิสรีรวิทยาและกลไกการเกิดโรคโดยละเอียด”พยาธิสรีรวิทยาของ I-CNV คล้ายคลึงกับ CNV ใน AMD และสายตาสั้นทางพยาธิวิทยา แต่มีลักษณะเด่นคือการมีปัจจัยการอักเสบร่วมด้วย1)
การอักเสบเรื้อรัง ความเครียดออกซิเดชัน และภาวะขาดเลือดมีส่วนเกี่ยวข้อง โดย CNV เกิดขึ้นจากการเปลี่ยนแปลงปฏิกิริยาหรือกระบวนการสมานแผลต่อความเสียหายของ RPE-เยื่อบรูค-แผ่นเส้นเลือดฝอยคอรอยด์
กลไกระดับโมเลกุล:
- การเพิ่มขึ้นของการแสดงออกของ VEGF ส่งเสริมการเจริญของเส้นเลือดใหม่ (ร่วมกับ CNV ใน AMD และสายตาสั้น)
- ในส่วนประกอบนอกหลอดเลือดของ CNV มีไฟโบรบลาสต์และเม็ดเลือดขาวที่แสดง CXCR4 อยู่
- เซลล์ RPE ผลิต TNF-α, IL-1, IL-2, IL-6, IL-10 และทำหน้าที่เป็นส่วนประกอบของการอักเสบ1)
- ความไม่สมดุลกับปัจจัยยับยั้งการสร้างหลอดเลือดใหม่ (แองจิโอสแตติน เอนโดสแตติน PEDF) เป็นตัวกระตุ้น1)
ในม่านตาอักเสบ ไซโตไคน์ เช่น TNF-α, IL-6, IL-1 ถูกหลั่งจากเซลล์อักเสบ ทำให้ RPE เสียหายและเพิ่มการแสดงออกของ VEGF มากขึ้น3) ปฏิสัมพันธ์ระหว่างไซโตไคน์เหล่านี้กับ VEGF ส่งเสริมการเกิด I-CNV
ความแตกต่างระหว่าง I-CNV และ CNV ที่เกี่ยวข้องกับ AMD: การศึกษาทางอิมมูโนฮิสโตเคมีรายงานว่ารูปแบบการย้อม CXCR4 ของโครงข่ายหลอดเลือดใน I-CNV แตกต่างจาก CNV ที่เกี่ยวข้องกับ AMD ซึ่งบ่งชี้ว่าเส้นเลือดฝอยอาจมีบทบาทที่แตกต่างกันในการสร้างเยื่อ9)
CNV “ไม่ทราบสาเหตุ” บางชนิดอาจปรากฏเป็นอาการนำของยูเวียอักเสบส่วนหลัง1) หลอดเลือดใหม่มักเจริญจากขอบของรอยโรคอักเสบ (ขอบของแผลเป็นจอประสาทตาคอรอยด์ฝ่อหลังการอักเสบ)
7. งานวิจัยล่าสุดและแนวโน้มในอนาคต
หัวข้อที่มีชื่อว่า “7. งานวิจัยล่าสุดและแนวโน้มในอนาคต”การปรับปรุงความแม่นยำในการวินิจฉัยด้วย OCTA:
OCTA มีบทบาทสำคัญในการวินิจฉัยและติดตาม I-CNV ข้อได้เปรียบของ OCTA เมื่อเทียบกับ FA และ ICGA เพียงอย่างเดียวกำลังถูกสะสมมากขึ้น และแสดงให้เห็นว่า OCTA มีความจำเป็นในการระบุเครือข่ายหลอดเลือดใหม่ชนิดที่ 1 แม้ว่าผล FA และ ICGA จะไม่ชัดเจนก็ตาม8) OCTA ยังมีประโยชน์เป็นตัวบ่งชี้ในการติดตาม CNV ที่ยังทำงานอยู่ และสามารถประเมินการหดตัวของหลอดเลือดใหม่หลังการรักษาในเชิงปริมาณ8)
ความสำคัญทางคลินิกของ “Sponge Sign”:
การเพิ่มขึ้นของความหนาคอรอยด์ใต้รอยโรค I-CNV ที่ตรวจพบด้วย OCT (ซึ่งลดลงหลังการรักษา เรียกว่า “สปองจ์ไซน์”) กำลังได้รับความสนใจในฐานะตัวบ่งชี้เสริมใหม่สำหรับการติดตามกิจกรรมของ I-CNV นอกจากนี้ยังอาจนำไปใช้ในการวินิจฉัยแยกโรคระหว่าง CNV อักเสบและ CNV สายตาสั้นได้อีกด้วย1)
ผลลัพธ์ระยะยาวของการรักษาด้วย anti-VEGF:
มีข้อมูลระยะกลางถึงระยะยาวสะสมว่าหลังการรักษาด้วย anti-VEGF (1-5 ครั้ง) สำหรับ posterior uveitis จากหลายสาเหตุ ผู้ป่วยมีการมองเห็นดีขึ้นประมาณ 0.3 หน่วย logMAR4) ในผู้ป่วย PIC ที่ได้รับการรักษาด้วย anti-VEGF เพียงอย่างเดียว มีรายงานอัตราการกลับเป็นซ้ำ 50% ซึ่งการจัดการโรคพื้นฐานมีผลต่อการพยากรณ์โรคระยะยาว7)
แนวทางการรักษาแบบ Treat & Extend (T&E):
กำลังมีการศึกษาการประยุกต์ใช้ระบบการรักษาแบบ T&E (การค่อยๆ ขยายระยะเวลาการรักษา) ซึ่งได้รับการยอมรับใน AMD และ CNV จากสายตาสั้น มาใช้กับ I-CNV แม้จะมีศักยภาพในการลดภาระการรักษาและคงการมองเห็นไว้ได้ แต่ยังคงต้องรอการสะสมหลักฐานที่เฉพาะเจาะจงสำหรับ CNV อักเสบ
faricimab (ยาที่ยับยั้งทั้ง VEGF-A และ Ang-2):
faricimab ซึ่งยับยั้ง VEGF-A และแองจิโอพอยอิติน-2 (Ang-2) พร้อมกัน ได้รับการอนุมัติสำหรับ AMD และเบาหวานขึ้นจอประสาทตาบวมน้ำ และกำลังอยู่ในขั้นตอนการวิจัยเพื่อประยุกต์ใช้กับ CNV อักเสบ เนื่องจาก Ang-2 เกี่ยวข้องทั้งการสร้างเส้นเลือดใหม่และการอักเสบ จึงคาดว่าจะมีผลเฉพาะต่อ I-CNV
การกำหนดมาตรฐานของแนวทางแบบหลายรูปแบบ (Multimodal Approach):
สำหรับการวินิจฉัย I-CNV แนวทางแบบหลายมิติที่รวม FAF, OCTA และการถ่ายภาพด้วยแสงฟลูออเรสเซนต์อินฟราเรดใกล้มีแนวโน้มดี โดยเฉพาะอย่างยิ่ง FAF มีประโยชน์ในการตรวจจับและติดตาม I-CNV บริเวณรอบนอก1)
การควบคุมโรคม่านตาอักเสบพื้นฐานและการรักษาด้วยยา anti-VEGF ตั้งแต่เนิ่นๆ สามารถช่วยรักษาหรือปรับปรุงการมองเห็นได้ อย่างไรก็ตาม ใน PIC มีรายงานอัตราการกลับเป็นซ้ำ 50% หลังการรักษาด้วยยา anti-VEGF เพียงอย่างเดียว ดังนั้นการจัดการโรคพื้นฐานจึงมีผลต่อการพยากรณ์โรคในระยะยาว7) การติดตามด้วย OCT และ OCTA เป็นประจำมีประโยชน์ในการตรวจหาการกลับเป็นซ้ำได้ตั้งแต่เนิ่นๆ
8. เอกสารอ้างอิง
หัวข้อที่มีชื่อว่า “8. เอกสารอ้างอิง”- Karska-Basta I, Pociej-Marciak W, Zuber-Laskawiec K, et al. Diagnostic challenges in inflammatory choroidal neovascularization. Medicina. 2024;60(3):465.
- Cheung CMG, Arnold JJ, Holz FG, et al. Myopic choroidal neovascularization: review, guidance, and consensus statement on management. Ophthalmology. 2017;124(11):1690-1711.
- 日本眼科学会ぶどう膜炎診療ガイドライン作成委員会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635-696.
- D’Souza Y, Balasubramaniam S, Nair U. Anti-VEGF treatment for inflammatory choroidal neovascularization: a comprehensive review. Surv Ophthalmol. 2023;68(3):435-461.
- Baxter SL, Pistilli M, Pujari SS, et al. Risk of choroidal neovascularization among the uveitides. Am J Ophthalmol. 2013;156(3):468-477.e2.
- Rouvas A, Petrou P, Douvali M, et al. Intravitreal ranibizumab for the treatment of inflammatory choroidal neovascularization. Retina. 2011;31(5):871-879.
- Amer R, Lois N. Punctate inner choroidopathy. Surv Ophthalmol. 2011;56(1):36-53.
- Astroz P, Miere A, Mrejen S, et al. Optical coherence tomography angiography to distinguish choroidal neovascularization from macular inflammatory lesions in multifocal choroiditis. Retina. 2018;38(2):299-309.
- Neri P, Lettieri M, Fortuna C, et al. Inflammatory choroidal neovascularization. Middle East Afr J Ophthalmol. 2009;16(4):245-251.
