Penyakit dengan insiden I-CNV tinggi
Punctate inner choroidopathy (PIC): 17–40%
Multifokal koroiditis (MFC) : 32–50%
Koroiditis serpiginosa : 10–25%
Penyakit Harada (VKH) : 9–15%
Sindrom histoplasmosis okular : 5–17,4%
Korioretinitis Birdshot: 5%

Neovaskularisasi koroidal (choroidal neovascularization; CNV) adalah penyakit di mana neovaskularisasi yang berasal dari koroid sering terjadi di makula. Neovaskularisasi tumbuh di bawah epitel pigmen retina (RPE) (tipe 1/klasik) atau di atas RPE (tipe 2/okult). Pada kasus koroiditis atau idiopatik, peradangan berperan besar, dan CNV dianggap sebagai perubahan reaktif atau proses penyembuhan luka akibat kerusakan pada membran RPE-Bruch-koriokapilaris.
Neovaskularisasi koroid inflamasi (I-CNV) adalah komplikasi berat dari uveitis posterior yang disebabkan oleh inflamasi koroidoretina. Dapat terjadi pada uveitis infeksius maupun non-infeksius1). I-CNV merupakan penyebab CNV ketiga setelah AMD dan miopia patologis1).
Pada pasien uveitis posterior, CNV terjadi pada 2,7%, pada pasien panuveitis 0,8%, lebih sering dibandingkan uveitis anterior dan intermediet (0,1%)1). Pada uveitis idiopatik, CNV terjadi sebagai komplikasi pada 13–20% kasus3). Sebagian besar I-CNV muncul sebagai CNV tipe 2 (klasik), menembus membran Bruch dan terbentuk di bawah RPE (tipe 1) atau di atas RPE (tipe 2)1).
Penyakit dengan insiden I-CNV tinggi
Punctate inner choroidopathy (PIC): 17–40%
Multifokal koroiditis (MFC) : 32–50%
Koroiditis serpiginosa : 10–25%
Penyakit Harada (VKH) : 9–15%
Sindrom histoplasmosis okular : 5–17,4%
Korioretinitis Birdshot: 5%
I-CNV pada penyakit infeksi
Korioretinitis Toksoplasma: 0,3–19%
Histoplasmosis okular: 5–17,4%
Tuberkulosis okular: laporan kasus yang jarang
Korioretinitis kandida: jarang (prevalensi tidak diketahui)
Retinopati rubella: laporan kasus yang jarang
Toksokariasis: laporan kasus yang jarang
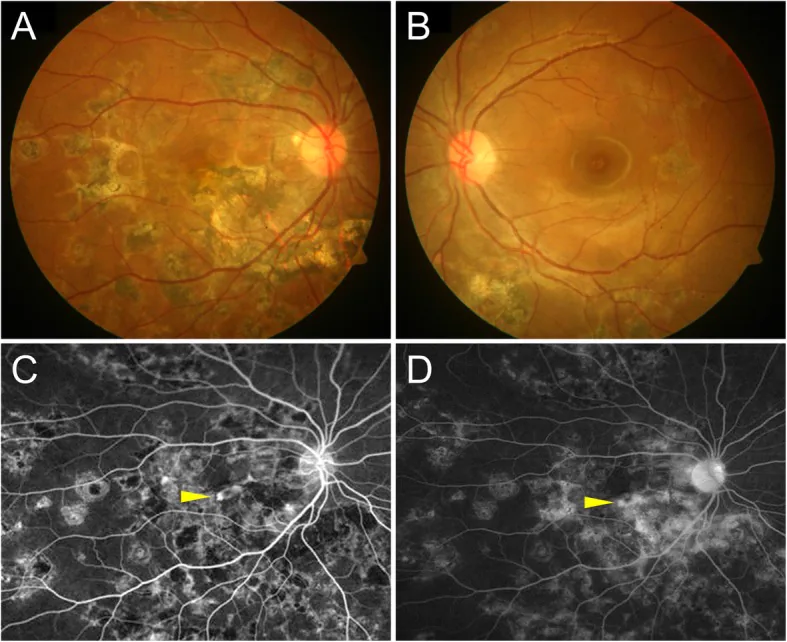
Gejala awal yang khas dari I-CNV adalah penurunan tajam penglihatan secara mendadak dan munculnya metamorphopsia1).
Lesi aktif yang terletak di luar fovea mungkin tidak bergejala dan dapat terlewatkan karena lesi inflamasi, jaringan parut, pigmentasi, atau akumulasi cairan intraretinal/subretinal 1).
Pada pemeriksaan fundus, ditemukan lesi subretinal berwarna putih kekuningan di sekitar makula.
Setelah CNV mengering, terbentuk lesi atrofi pada epitel pigmen retina dan membran koroid-kapiler. Pada CNV di atas epitel pigmen retina, jaringan fibrosa terbentuk di bawah retina, sehingga penurunan visus, skotoma sentral, dan metamorfopsia dapat menetap.
Patofisiologi: 2 mekanisme1)
Ketika sel inflamasi teraktivasi, mereka mengeluarkan enzim sitotoksik yang mendegradasi membran Bruch. Sitokin proangiogenik yang dilepaskan (IL-6, IL-8, TNF-α) meningkatkan ekspresi VEGF dan mendorong proliferasi CNV2). Pada uveitis, sitokin seperti TNF-α, IL-6, dan IL-1 merusak RPE, semakin memperkuat ekspresi VEGF, dan mendorong pembentukan I-CNV3).
Pedoman praktik klinis untuk uveitis (2019) menyatakan bahwa pada uveitis posterior seperti PIC, koroiditis multifokal, sarkoidosis, penyakit Harada, dan koroiditis serpiginosa, perlu diwaspadai komplikasi CNV, dan kombinasi pengendalian inflamasi dengan terapi anti-VEGF direkomendasikan3).
Faktor risiko5):
| Faktor risiko | Deskripsi |
|---|---|
| Adanya neovaskularisasi epitel retina | Risiko terjadinya I-CNV meningkat lebih dari 3 kali lipat |
| Peradangan aktif | Risiko CNV secara signifikan lebih tinggi dibandingkan fase non-aktif |
| Peradangan bilik mata depan grade 2+ | Hubungan signifikan dengan I-CNV |
| Riwayat CNV pada mata kontralateral | Risiko CNV beberapa kali lipat |
| Uveitis unilateral | Risiko CNV lebih tinggi dibandingkan bilateral |
Diagnosis I-CNV sulit dan multimodal imaging direkomendasikan 1).
Fluorescein Angiography (FA): Sebagian besar I-CNV tampak sebagai CNV tipe klasik (tipe 2). Lesi CNV menunjukkan isofluoresensi hingga hiperfluoresensi dini + kebocoran fluoresensi akhir. Namun, lesi inflamasi aktif juga menunjukkan temuan FA serupa, sehingga diagnosis dengan FA saja memiliki keterbatasan 1). Hiperfluoresensi batas tegas pada fase awal (tipe klasik) atau kebocoran difus pigmen pada fase akhir (tipe okult) merupakan karakteristik.
Indocyanine Green Angiography (ICGA): Menilai struktur pembuluh darah koroid lebih detail daripada FA. I-CNV menunjukkan hiperfluoresensi sejak awal, dan dapat dibedakan dari fokus inflamasi aktif (hipofluoresensi awal) 1). ICGA sangat penting untuk membedakan CNV sub-RPE, dan pada koroiditis multifokal berguna untuk menilai area non-perfusi dari lamina kapilaris koroid serta mengevaluasi risiko perkembangan CNV 1).
Optical Coherence Tomography (OCT): Dapat memeriksa penampang makula secara non-invasif dalam waktu singkat, serta mengevaluasi hubungan antara CNV dan fovea, apakah CNV berada di atas atau di bawah RPE, serta kondisi ablasi retina, ablasi RPE, dan edema makula kistik yang menyertainya.
OCT Angiografi (OCTA): Dapat memvisualisasikan struktur pembuluh darah CNV secara non-invasif. Memiliki akurasi lebih tinggi dalam membedakan CNV dan lesi inflamasi dibandingkan FA saja, dan sangat berguna untuk mengidentifikasi jaringan neovaskular tipe 18).
Fundus Autofluoresensi (FAF): Pada I-CNV aktif, menunjukkan fluoresensi normal atau hiperautofluoresensi. Area hipoautofluoresensi berkorelasi dengan hilangnya fotoreseptor dan RPE, berguna untuk mendeteksi I-CNV perifer1).
OCT sangat berguna untuk evaluasi I-CNV, namun seringkali sulit untuk menegakkan diagnosis pasti hanya dengan OCT. Temuan OCT yang khas untuk I-CNV seperti “tanda garpu rumput” memiliki nilai tambahan, namun diagnosis multimodal yang menggabungkan FA, ICGA, OCTA, dan FAF sangat penting untuk diagnosis akurat dan membedakan dari lesi inflamasi1).
Pengobatan cepat untuk I-CNV sangat penting untuk mencegah kehilangan penglihatan yang ireversibel. Pengobatan memerlukan kombinasi dari dua pendekatan.
Pertama, singkirkan penyakit infeksi (seperti toksoplasma, tuberkulosis, Bartonella henselae) dan berikan terapi anti-infeksi yang tepat. Setelah itu, penanganan uveitis dasar meliputi:
Terlepas dari penyakit penyebabnya, CNV foveal diberikan penghambat VEGF secara intravitreal. Karena VEGF terlibat erat dalam perkembangan CNV, obat yang menghambatnya berguna untuk regresi CNV dan pencegahan perdarahan serta eksudasi.
| Obat | Ikhtisar | Aplikasi pada CNV inflamasi |
|---|---|---|
| Aflibercept (Eylea) | Penghambat VEGF-A/VEGF-B/PlGF | Tidak tercakup asuransi (AMD dan maktulopati miopia tercakup) |
| Ranibizumab (Lucentis) | Fragmen antibodi monoklonal anti-VEGF-A | Tidak tercakup asuransi (AMD dan maktulopati miopia tercakup) |
| Bevacizumab (Avastin) | Antibodi monoklonal anti-VEGF-A full-length | Tidak tercakup asuransi (off-label), digunakan untuk CNV inflamasi |
Cakupan asuransi untuk aflibercept dan ranibizumab terbatas pada degenerasi makula terkait usia dan mopati miopia. Untuk CNV inflamasi, bevacizumab (1,25 mg/0,05 mL injeksi intravitreal) diberikan secara off-label3).
Kombinasi terapi anti-inflamasi dan anti-VEGF menghasilkan perbaikan pada 80% pasien dan stabil pada 15% pasien4). Pengobatan anti-VEGF saja pada pasien PIC melaporkan tingkat kekambuhan 50%, menunjukkan perlunya terapi sistemik untuk uveitis dasar7).
Perbandingan antara fase induksi (suntikan bulanan selama 3 bulan) dan pemberian sesuai kebutuhan (PRN) menunjukkan bahwa fase induksi tidak memberikan hasil yang lebih baik1). Uji coba acak terkendali mengonfirmasi bahwa anti-VEGF (ranibizumab 0,5 mg intravitreal) efektif dalam meningkatkan ketajaman visual dan regresi neovaskular pada I-CNV6).
Aflibercept (Eylea) dan ranibizumab (Lucentis) hanya memiliki persetujuan asuransi untuk degenerasi makula terkait usia dan miopia makulopati. Untuk CNV inflamasi, bevacizumab (Avastin, off-label) kadang digunakan di fasilitas oftalmologi. Pilihan pengobatan harus didiskusikan secara menyeluruh dengan dokter yang merawat.
Pada CNV ekstrafoveal, dilakukan fotokoagulasi dengan laser termal. Fotokoagulasi menutup CNV secara langsung, namun area yang diiradiasi akan mengalami kerusakan retina permanen, sehingga jarak dari fovea harus dievaluasi secara hati-hati untuk menentukan indikasi.
Patofisiologi I-CNV mirip dengan CNV pada AMD dan miopia patologis, namun ditandai dengan adanya faktor inflamasi1).
Inflamasi kronis, stres oksidatif, dan iskemia berperan, dan CNV terjadi sebagai perubahan reaktif atau proses penyembuhan luka terhadap kerusakan pada RPE-membran Bruch-lapisan kapiler koroid.
Mekanisme molekuler:
Pada uveitis, sitokin seperti TNF-α, IL-6, IL-1 disekresikan oleh sel inflamasi, merusak RPE, dan semakin meningkatkan ekspresi VEGF 3). Interaksi antara sitokin dan VEGF ini mendorong pembentukan I-CNV.
Perbedaan antara I-CNV dan CNV terkait AMD: Studi imunohistokimia melaporkan bahwa pola pewarnaan CXCR4 pada anyaman pembuluh darah I-CNV berbeda dengan CNV terkait AMD, menunjukkan bahwa kapiler mungkin memiliki peran berbeda dalam pembentukan membran 9).
Beberapa CNV “idiopatik” juga dapat muncul sebagai gejala awal uveitis posterior 1). Pembuluh darah baru sering tumbuh dari tepi fokus inflamasi (tepi bekas luka koroidoretinal atrofi pasca-inflamasi).
Peningkatan Akurasi Diagnostik dengan OCTA:
OCTA memainkan peran penting dalam diagnosis dan pemantauan I-CNV. Keunggulan OCTA dibandingkan FA dan ICGA saja semakin terakumulasi, dan telah ditunjukkan bahwa OCTA sangat penting untuk mengidentifikasi jaringan neovaskular tipe 1 bahkan ketika hasil FA dan ICGA tidak meyakinkan8). OCTA juga berguna sebagai indikator pemantauan CNV aktif, dan dapat mengevaluasi secara kuantitatif regresi neovaskular setelah pengobatan8).
Signifikansi Klinis dari “Tanda Spons”:
Peningkatan ketebalan koroid di bawah I-CNV yang terdeteksi oleh OCT (“tanda spons” yang menurun setelah terapi) sedang menjadi perhatian sebagai indikator tambahan baru untuk pemantauan aktivitas I-CNV. Hal ini juga berpotensi diterapkan dalam diagnosis banding antara CNV inflamasi dan CNV miopia 1).
Hasil jangka panjang terapi anti-VEGF:
Data jangka menengah hingga panjang menunjukkan bahwa terapi anti-VEGF (1-5 suntikan) untuk uveitis posterior berbagai penyebab menghasilkan perbaikan sekitar 0,3 unit pada logMAR visual acuity 4). Pada pasien PIC yang diterapi hanya dengan obat anti-VEGF, dilaporkan angka kekambuhan 50%, sehingga penanganan penyakit dasar sangat memengaruhi prognosis jangka panjang 7).
Regimen Treat & Extend (T&E):
Penerapan rejimen T&E (metode perpanjangan interval pengobatan secara bertahap) yang telah mapan untuk AMD dan CNV miopia pada I-CNV sedang dipertimbangkan. Meskipun berpotensi mempertahankan penglihatan sambil mengurangi beban pengobatan, diperlukan akumulasi bukti yang spesifik untuk CNV inflamasi.
faricimab (penghambat ganda anti-VEGF-A/Ang-2):
Faricimab, yang menghambat VEGF-A dan angiopoietin-2 (Ang-2) secara bersamaan, telah disetujui untuk AMD dan edema makula diabetik, dan penerapannya pada CNV inflamasi masih dalam tahap penelitian. Karena Ang-2 terlibat dalam angiogenesis dan inflamasi, diharapkan memiliki efek spesifik pada I-CNV.
Standarisasi pendekatan multimodal:
Pendekatan multi-aspek yang mencakup FAF, OCTA, dan pencitraan fluoresensi inframerah dekat menjanjikan untuk diagnosis I-CNV, terutama FAF berguna untuk deteksi dan pemantauan I-CNV perifer 1).
Kontrol uveitis dasar dan pengobatan dini dengan anti-VEGF dapat mempertahankan atau memperbaiki penglihatan. Namun, pada PIC, dilaporkan tingkat kekambuhan 50% dengan terapi anti-VEGF saja, sehingga manajemen penyakit dasar memengaruhi prognosis jangka panjang 7). Pemantauan OCT dan OCTA secara teratur berguna untuk deteksi dini kekambuhan.