بیماریهای با شیوع بالای I-CNV
کوریورتینوپاتی نقطهای داخلی (PIC): 17 تا 40%
کوریورتینیت چندکانونی (MFC): ۳۲ تا ۵۰٪
کوریورتینیت مارپیچی: ۱۰ تا ۲۵٪
بیماری هارادا (VKH): ۹ تا ۱۵٪
سندرم هیستوپلاسموز چشمی: ۵ تا ۱۷.۴٪
کوریورتینیت شات گان : ۵٪

نئوواسکولاریزاسیون مشیمیه (CNV) بیماری است که در آن رگهای خونی جدید از مشیمیه منشأ گرفته و اغلب در ناحیه ماکولا ایجاد میشوند. این رگهای جدید در زیر اپیتلیوم رنگدانه شبکیه (RPE) (نوع 1/کلاسیک) یا بالای RPE (نوع 2/اکالت) رشد میکنند. در موارد کوروئیدیت یا ایدیوپاتیک، التهاب نقش مهمی دارد و CNV به عنوان یک واکنش به آسیب غشای بروخ-مشیمیه-مویرگی یا فرآیند ترمیم زخم در نظر گرفته میشود.
نئوواسکولاریزاسیون مشیمیهای التهابی (I-CNV) یک عارضه جدی یووئیت خلفی است که در اثر التهاب مشیمیه-شبکیه ایجاد میشود. این عارضه میتواند در هر دو نوع یووئیت عفونی و غیرعفونی رخ دهد1). I-CNV به عنوان سومین علت CNV پس از AMD و نزدیکبینی پاتولوژیک در نظر گرفته میشود1).
در بیماران مبتلا به یووئیت خلفی، CNV در 2.7% موارد و در بیماران مبتلا به پانیووئیت در 0.8% موارد رخ میدهد که بیشتر از یووئیت قدامی و میانی (0.1%) است1). در یووئیت ایدیوپاتیک، CNV به عنوان عارضه در 13 تا 20% موارد ایجاد میشود3). اکثر I-CNV ها به صورت CNV نوع 2 (کلاسیک) ظاهر میشوند و با عبور از غشای بروخ، در زیر (نوع 1) یا بالای (نوع 2) اپیتلیوم رنگدانه شبکیه تشکیل میشوند1).
بیماریهای با شیوع بالای I-CNV
کوریورتینوپاتی نقطهای داخلی (PIC): 17 تا 40%
کوریورتینیت چندکانونی (MFC): ۳۲ تا ۵۰٪
کوریورتینیت مارپیچی: ۱۰ تا ۲۵٪
بیماری هارادا (VKH): ۹ تا ۱۵٪
سندرم هیستوپلاسموز چشمی: ۵ تا ۱۷.۴٪
کوریورتینیت شات گان : ۵٪
I-CNV در بیماریهای عفونی
کوریورتینیت توکسوپلاسمایی : ۰.۳ تا ۱۹٪
هیستوپلاسموز چشمی : ۵ تا ۱۷.۴٪
سل چشمی: گزارش نادر موردی
کاندیدا کوریورتینیت: نادر (شیوع نامشخص)
رتینوپاتی سرخجه: گزارش نادر موردی
توکسوکاریازیس: گزارش نادر موردی
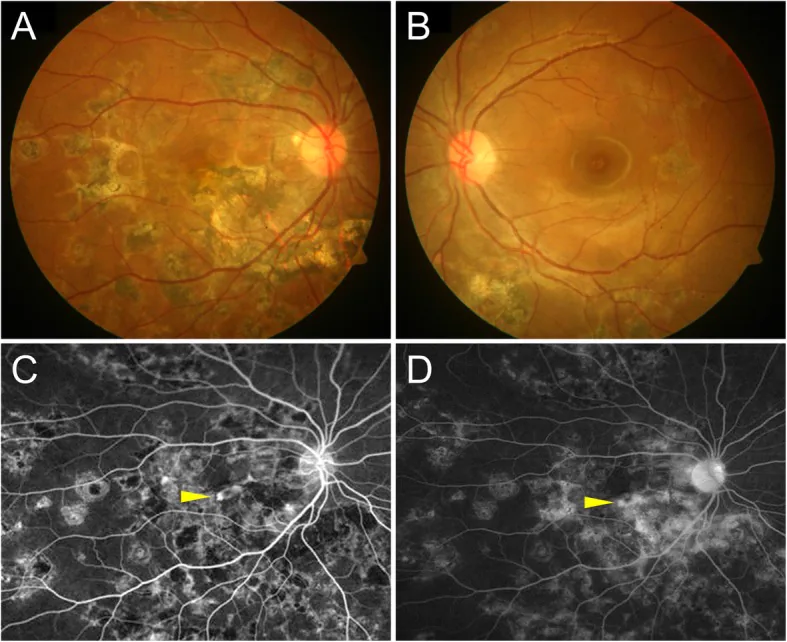
علائم اولیه معمول I-CNV شامل بدتر شدن ناگهانی بینایی و ظهور دگرنمایی (مترامورفوپسی) است1).
ضایعات فعال خارج از فووآ ممکن است بدون علامت باشند و به دلیل ضایعات التهابی، اسکار، رنگدانهگذاری یا تجمع مایع داخل و خارج شبکیه نادیده گرفته شوند1).
در معاینه فوندوس، ضایعات زیرشبکیهای زرد-سفید در اطراف ماکولا مشاهده میشود.
پس از خشک شدن CNV، آتروفی لایه اپیتلیوم رنگدانهای شبکیه و مویرگهای مشیمیه ایجاد میشود. در CNV روی اپیتلیوم رنگدانهای، بافت فیبروز در زیر شبکیه تشکیل میشود که ممکن است کاهش بینایی، اسکوتوم مرکزی و دگرگونیبینی دائمی ایجاد کند.
پاتوفیزیولوژی: دو مکانیسم1)
هنگامی که سلولهای التهابی فعال میشوند، آنزیمهای سیتوتوکسیک ترشح کرده و غشای بروخ را تجزیه میکنند. سایتوکاینهای پیشبرنده رگزایی آزاد شده (IL-6، IL-8، TNF-α) بیان VEGF را افزایش داده و تکثیر CNV را تحریک میکنند2). در یووئیت، سایتوکاینهایی مانند TNF-α، IL-6 و IL-1 به RPE آسیب زده و بیان VEGF را بیشتر تقویت کرده و تشکیل I-CNV را تسریع میکنند3).
طبق دستورالعمل بالینی یووئیت (2019)، در موارد یووئیت خلفی مانند PIC، کوریورتینیت چندکانونی، سارکوئیدوز، بیماری هارادا و کوریورتینیت مارپیچی، باید به همراهی CNV توجه کرد و ترکیب کنترل التهاب با درمان ضد VEGF توصیه میشود3).
عوامل خطر5):
| عوامل خطر | توضیحات |
|---|---|
| وجود نئوواسکولاریزاسیون اپیرتینال | افزایش خطر ابتلا به I-CNV به بیش از سه برابر |
| التهاب فعال | خطر CNV در مقایسه با فاز غیرفعال به طور قابل توجهی بالاتر است |
| التهاب اتاق قدامی درجه 2+ | ارتباط معنیدار با I-CNV |
| سابقه CNV در چشم مقابل | چندین برابر خطر ابتلا به CNV |
| یووئیت یکطرفه | خطر CNV بیشتر از نوع دوطرفه است |
تشخیص I-CNV دشوار است و تصویربرداری چندوجهی توصیه میشود1).
آنژیوگرافی فلورسین (FA): بیشتر I-CNVها به صورت نوع کلاسیک (نوع 2) ظاهر میشوند. ضایعه CNV در مراحل اولیه ایزوفلورسنت تا هایپرفلورسنت و در مراحل پایانی نشت فلورسین نشان میدهد. با این حال، ضایعات التهابی فعال نیز یافتههای مشابهی در FA دارند، بنابراین تشخیص تنها با FA محدودیت دارد1). در مراحل اولیه آنژیوگرافی، هایپرفلورسنس با مرز مشخص (نوع کلاسیک) یا در مراحل پایانی نشت منتشر رنگ (نوع مخفی) مشخصه است.
آنژیوگرافی با ایندوسیانین گرین (ICGA): ساختار عروق کوروئید را با جزئیات بیشتری نسبت به FA ارزیابی میکند. I-CNV از مراحل اولیه هایپرفلورسنت است و میتوان آن را از کانونهای التهابی فعال (هیپوفلورسنت اولیه) افتراق داد1). ICGA برای افتراق CNV زیر اپیتلیوم رنگدانه شبکیه ضروری است و در کوروئیدیت چندکانونی، برای ارزیابی ناحیه عدم پرفیوژن مویرگهای کوروئید و ارزیابی خطر بروز CNV مفید است1).
توموگرافی انسجام نوری (OCT): به صورت غیرتهاجمی و در مدت کوتاه میتوان مقطع ماکولا را بررسی کرد و موقعیت CNV نسبت به فووآ، قرارگیری CNV در بالا یا پایین RPE، و وضعیت جداشدگی شبکیه، جداشدگی RPE و ادم ماکولار کیستیک همراه را ارزیابی کرد.
آنژیوگرافی OCT (OCTA): میتواند ساختار عروقی CNV را به صورت غیرتهاجمی تجسم کند. دقت بالاتری نسبت به FA به تنهایی در افتراق CNV از ضایعات التهابی دارد و به ویژه برای شناسایی شبکه عروقی نوع 1 مفید است8).
عکسبرداری خودفلورسانس فوندوس (FAF): در I-CNV فعال، فلورسانس طبیعی یا بیشفلورسانس نشان میدهد. نواحی کمفلورسانس با از دست رفتن گیرندههای نوری و RPE مرتبط است و برای تشخیص I-CNV محیطی مفید میباشد1).
درمان سریع I-CNV از کاهش بینایی غیرقابل برگشت جلوگیری میکند. درمان نیاز به ترکیبی از دو رویکرد دارد.
ابتدا بیماریهای عفونی (مانند توکسوپلاسما، سل، بارتونلا هنزله) را رد کرده و درمان ضدعفونی مناسب انجام دهید. پس از رد، درمان یووئیت زمینهای:
صرف نظر از بیماری زمینهای، برای CNV زیرحفرهای، تزریق داخل زجاجیهای داروهای مهارکننده VEGF انجام میشود. از آنجا که VEGF در ایجاد و رشد CNV نقش مهمی دارد، داروهای مهارکننده آن برای پسرفت CNV و جلوگیری از خونریزی و ترشح مفید هستند.
| دارو | خلاصه | کاربرد در CNV التهابی |
|---|---|---|
| آفلیبرسپت (آیلیا) | مهار VEGF-A/VEGF-B/PlGF | غیرقابل استفاده در بیمه (AMD و ماکولوپاتی نزدیکبینی تحت پوشش بیمه هستند) |
| رانیبیزوماب (لوسنتیس) | قطعه آنتیبادی مونوکلونال ضد VEGF-A | غیرقابل استفاده در بیمه (AMD و ماکولوپاتی نزدیکبینی تحت پوشش بیمه هستند) |
| بوسیزیوماب (آواستین) | آنتیبادی مونوکلونال تمامطول علیه VEGF-A | بدون پوشش بیمه (آف-لیبل)، استفاده در CNV التهابی |
پوشش بیمهای آفلیبرسپت و رانیبیزوماب仅限于 دژنراسیون ماکولای وابسته به سن و ماکولوپاتی نزدیکبینی است. برای CNV التهابی، بوسیزیوماب (1.25 mg/0.05 mL تزریق داخل زجاجیهای) به صورت آف-لیبل تجویز میشود3).
ترکیب درمان ضدالتهابی و داروی ضد VEGF باعث بهبود 80% بیماران و تثبیت 15% از آنها شده است 4). درمان با داروی ضد VEGF به تنهایی در بیماران PIC نرخ عود 50% را گزارش کرده است که نیاز به درمان سیستمیک برای یووئیت زمینهای را نشان میدهد 7).
مقایسه فاز القایی (تزریق ماهانه به مدت 3 ماه) با درمان بر اساس نیاز (PRN) نشان داده است که فاز القایی منجر به پیامدهای برتر نمیشود 1). کارآزمایی تصادفیشده تأیید کرده است که داروی ضد VEGF (تزریق داخل زجاجیهای 0.5 میلیگرم رانیبیزوماب) در بهبود بینایی و پسرفت عروق جدید در I-CNV مؤثر است 6).
آفلیبرسپت (آیلیا) و رانیبیزوماب (لوسنتیس) فقط برای دژنراسیون ماکولا وابسته به سن و ماکولوپاتی نزدیکبینی تحت پوشش بیمه هستند. برای CNV التهابی، بواسیزوماب (آواستین، خارج از پوشش بیمه) ممکن است در مراکز چشمپزشکی استفاده شود. انتخاب درمان باید با مشورت کامل با پزشک معالج تعیین شود.
در CNV خارج از فووه آ، فتوکواگولاسیون با لیزر حرارتی انجام میشود. فتوکواگولاسیون مستقیماً CNV را مسدود میکند، اما ناحیه تابش باعث آسیب دائمی شبکیه میشود، بنابراین فاصله از فووه آ باید با دقت ارزیابی شده و اندیکاسیون تعیین شود.
پاتوفیزیولوژی I-CNV مشابه CNV در AMD و نزدیکبینی پاتولوژیک است، اما با این تفاوت که عوامل التهابی نیز در آن نقش دارند1).
التهاب مزمن، استرس اکسیداتیو و ایسکمی در ایجاد آن نقش دارند و CNV به عنوان یک واکنش به آسیب لایه RPE-غشای بروخ-مویرگهای مشیمیه یا فرآیند ترمیم زخم رخ میدهد.
مکانیسم مولکولی:
در یووئیت، سیتوکینهایی مانند TNF-α، IL-6 و IL-1 از سلولهای التهابی ترشح میشوند و به RPE آسیب میرسانند و بیان VEGF را بیشتر تقویت میکنند 3). تعامل این سیتوکینها با VEGF باعث تشکیل I-CNV میشود.
تفاوت بین I-CNV و CNV مرتبط با AMD: مطالعات ایمونوهیستوشیمی نشان دادهاند که الگوی رنگآمیزی CXCR4 در شبکه عروقی I-CNV با CNV مرتبط با AMD متفاوت است که نشان میدهد مویرگها ممکن است نقش متفاوتی در تشکیل غشا داشته باشند9).
برخی از CNVهای «ایدیوپاتیک» ممکن است به عنوان علامت اولیه یووئیت خلفی ظاهر شوند1). رگهای جدید اغلب از لبه کانون التهابی (لبه اسکار کوریورتینال آتروفیک پس از التهاب) رشد میکنند.
بهبود دقت تشخیصی با OCTA:
OCTA نقش مهمی در تشخیص و پیگیری I-CNV ایفا میکند. مزایای OCTA نسبت به FA و ICGA به تنهایی در حال افزایش است و نشان داده شده است که حتی در مواردی که نتایج FA و ICGA نامشخص هستند، برای شناسایی شبکه عروق جدید نوع 1 ضروری است8). OCTA همچنین به عنوان شاخصی برای پایش CNV فعال مفید است و میتواند پسرفت عروق جدید پس از درمان را به صورت کمی ارزیابی کند8).
اهمیت بالینی «علامت اسفنجی»:
افزایش ضخامت مشیمیه زیر I-CNV در OCT (که پس از درمان کاهش مییابد و “علامت اسفنجی” نامیده میشود) به عنوان یک شاخص کمکی جدید برای پایش فعالیت I-CNV مورد توجه قرار گرفته است. همچنین ممکن است در تشخیص افتراقی CNV التهابی و CNV نزدیکبینی کاربرد داشته باشد1).
نتایج بلندمدت درمان ضد VEGF:
دادههای میانمدت و بلندمدت نشان میدهد که درمان ضد VEGF (۱ تا ۵ تزریق) در یووئیت خلفی با علل مختلف، بهبود حدود ۰٫۳ واحد در logMAR را به همراه دارد4). در بیماران PIC، درمان تنها با داروی ضد VEGF با نرخ عود ۵۰٪ همراه بوده است و مدیریت بیماری زمینهای پیشآگهی بلندمدت را تعیین میکند7).
رژیم Treat & Extend (T&E):
کاربرد رژیم T&E (روش افزایش تدریجی فاصله درمان) که برای AMD و CNV نزدیکبینی تثبیت شده است، برای I-CNV در حال بررسی است. این روش ممکن است بتواند بار درمان را کاهش داده و بینایی را حفظ کند، اما نیاز به جمعآوری شواهد اختصاصی برای CNV التهابی وجود دارد.
فاریسیماب (مهارکننده دوگانه VEGF-A/Ang-2):
فاریسیماب که به طور همزمان VEGF-A و آنژیوپوئتین-2 (Ang-2) را مهار میکند، برای AMD و ادم ماکولای دیابتی تأیید شده است و کاربرد آن برای CNV التهابی در مرحله تحقیقاتی قرار دارد. از آنجایی که Ang-2 در هر دو فرآیند رگزایی و التهاب نقش دارد، انتظار میرود که اثر اختصاصی بر I-CNV داشته باشد.
استانداردسازی رویکرد چندوجهی:
برای تشخیص I-CNV، رویکرد چندجانبه شامل FAF، OCTA و تصویربرداری فلورسانس خودبخودی نزدیک به مادون قرمز امیدوارکننده است و FAF به ویژه برای تشخیص و پایش I-CNV محیطی مفید است 1).
با کنترل یووئیت زمینهای و درمان زودهنگام با داروهای ضد VEGF میتوان انتظار حفظ و بهبود بینایی را داشت. با این حال، در PIC میزان عود 50% با درمان تکدارویی ضد VEGF گزارش شده است و مدیریت بیماری زمینهای پیشآگهی طولانیمدت را تعیین میکند 7). پایش منظم با OCT و OCTA برای تشخیص زودهنگام عود مفید است.