โรคกระจกตารูปกรวย (Keratoconus)

โรคกระจกตาเสื่อมขอบ Pellucid
ประเด็นสำคัญโดยสังเขป
หัวข้อที่มีชื่อว่า “ประเด็นสำคัญโดยสังเขป”1. โรคกระจกตาเสื่อมขอบโปร่งแสง (Pellucid Marginal Corneal Degeneration) คืออะไร?
หัวข้อที่มีชื่อว่า “1. โรคกระจกตาเสื่อมขอบโปร่งแสง (Pellucid Marginal Corneal Degeneration) คืออะไร?”โรคกระจกตาเสื่อมขอบโปร่งแสง (PMD, PMCD) เป็นโรคกระจกตาโป่งพองที่ไม่มีการอักเสบและไม่ถ่ายทอดทางพันธุกรรม มีลักษณะเฉพาะคือกระจกตาส่วนปลายด้านล่างบางลงทั้งสองข้าง คำว่า “pellucid” แปลว่า “โปร่งใส” หมายถึงบริเวณที่บางยังคงโปร่งใส ไม่มีอาการอักเสบ เช่น หลอดเลือดงอกหรือความขุ่นในบริเวณที่บาง และถือเป็นโรคที่เกี่ยวข้องกับโรคกระจกตารูปกรวย
PMD เป็นโรคกระจกตาบางที่ไม่มีการอักเสบที่พบบ่อยเป็นอันดับสองรองจากโรคกระจกตารูปกรวย อย่างไรก็ตาม มักถูกวินิจฉัยผิดเป็นโรคกระจกตารูปกรวย ดังนั้นความชุกที่แท้จริงอาจถูกประเมินต่ำเกินไป 3) PMD มักเริ่มมีอาการในช่วงอายุ 30-50 ปี 2,4) ช้ากว่าโรคกระจกตารูปกรวยเล็กน้อย พบในเพศชายมากกว่า
เนื่องจาก PMD และโรคกระจกตารูปกรวยมีลักษณะทางคลินิกและเนื้อเยื่อวิทยาหลายอย่างร่วมกัน จึงมีมุมมองที่ถือว่าทั้งสองเป็นสเปกตรัมต่อเนื่อง 3) ประมาณ 10% ของผู้ป่วย PMD มีโรคกระจกตารูปกรวยร่วมด้วย และ 13% มีโรคกระจกตาทรงกลมร่วมด้วย 4) มีรายงานผู้ป่วยที่มี PMD และโรคกระจกตารูปกรวยร่วมกันในผู้ป่วยรายเดียวกัน ในการสำรวจระดับประเทศของญี่ปุ่น จากผู้ป่วย PMD ข้างเดียว 27 ราย พบว่า 17 รายมีโรคกระจกตารูปกรวยหรือสงสัยโรคกระจกตารูปกรวยในตาอีกข้าง 1)
เมื่อความผิดปกติของรูปทรงกระจกตาดำเนินไป จะเกิดสายตาเอียงไม่สม่ำเสมออย่างรุนแรง ทำให้การมองเห็นบกพร่อง มีแนวโน้มสายตาเอียงกลับทิศทางรุนแรง และการแก้ไขด้วยแว่นตาหรือคอนแทคเลนส์มักทำได้ยากกว่าโรคกระจกตารูปกรวย 4)
PMD มีระยะเวลาที่ไม่มีอาการนาน มักถูกมองข้ามในการตรวจสุขภาพช่วงอายุ 20 ปีหรือการตัดแว่น ผู้ป่วยจำนวนมากได้รับการวินิจฉัยครั้งแรกในช่วงอายุ 30-40 ปี เมื่อสายตาเอียงกลับทิศทางรุนแรงขึ้นและไม่สามารถมองเห็นได้ชัดเจนด้วยการแก้ไข ในขณะที่โรคกระจกตารูปกรวยถูกตรวจพบค่อนข้างเร็วเนื่องจากกระจกตาบวมน้ำเฉียบพลันหรือการโป่งตรงกลางชัดเจน PMD ดำเนินไปอย่างช้าๆ ในรูปแบบ “สายตาเอียงกลับทิศทางที่ไม่ดีขึ้น” และ “แว่นตาที่ค่อยๆ ใช้ไม่ได้” ข้อมูลทางระบาดวิทยามีจำกัด และยังไม่มีการศึกษาขนาดใหญ่ระดับประเทศเช่นโรคกระจกตารูปกรวย ดังนั้นความชุกที่แท้จริงจึงไม่เป็นที่ทราบ มีรายงานผู้ป่วยที่ตรวจพบโดยบังเอิญระหว่างการตรวจก่อนผ่าตัดแก้ไขสายตาผิดปกติ ซึ่งบ่งชี้ว่าจำนวนผู้ที่อาจเป็นโรคนี้ไม่น้อย
ใน PMD ส่วนปลายล่างของกระจกตาจะบางลง และส่วนที่นูนมากที่สุดจะอยู่เหนือบริเวณที่บาง (ไปทางศูนย์กลาง) ในขณะที่ในโรคกระจกตารูปกรวย (keratoconus) ส่วนกลางถึงกึ่งกลางของกระจกตาจะบางลง และบริเวณที่บางจะตรงกับส่วนที่นูน ใน PMD จะไม่พบวงแหวน Fleischer หรือเส้น Vogt และสายตาเอียงไม่สม่ำเสมอมีแนวโน้มรุนแรง นอกจากนี้ PMD มักเกิดหลังอายุ 30 ปี ในขณะที่ keratoconus เกิดในวัยรุ่น
2. อาการหลักและผลการตรวจทางคลินิก
หัวข้อที่มีชื่อว่า “2. อาการหลักและผลการตรวจทางคลินิก”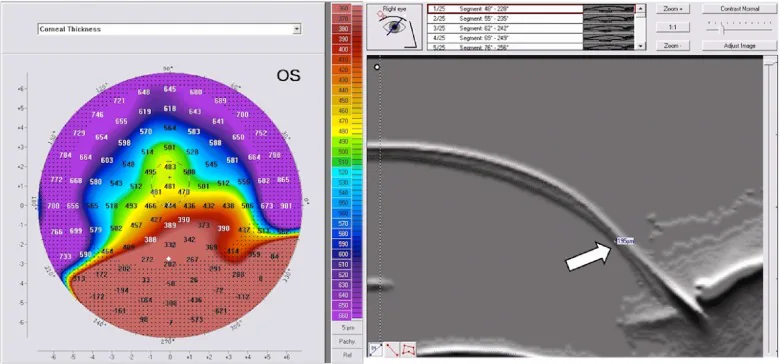
อาการที่ผู้ป่วยรับรู้
หัวข้อที่มีชื่อว่า “อาการที่ผู้ป่วยรับรู้”- การมองเห็นลดลงแบบค่อยเป็นค่อยไป: ไม่สามารถมองเห็นได้เพียงพอแม้จะแก้ไขด้วยแว่นตาเนื่องจากสายตาเอียงไม่สม่ำเสมออย่างรุนแรง
- ภาพบิดเบี้ยว: เนื่องจากรูปร่างกระจกตาผิดปกติ
- ปวดเฉียบพลันและการมองเห็นลดลง: เกิดขึ้นไม่บ่อยในภาวะกระจกตาบวมน้ำเฉียบพลัน
- ค่าสายตาไม่คงที่: การมองเห็นไม่คงที่แม้จะเปลี่ยนแว่นตาบ่อยครั้ง2)
ผลการตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด (Slit-lamp)
หัวข้อที่มีชื่อว่า “ผลการตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด (Slit-lamp)”| ผลการตรวจ | ลักษณะ |
|---|---|
| การบางเป็นแถบ | ตำแหน่ง 4 ถึง 8 นาฬิกา ห่างจากขอบตา 1-2 มม. กว้าง 1-2 มม. |
| การนูนไปข้างหน้า | อยู่เหนือบริเวณที่บาง (ไปทางศูนย์กลาง) ลักษณะคล้ายพุงเบียร์ (พุงกลม) |
| ความโปร่งใสของกระจกตา | บริเวณบางใส ไม่มีการบุกรุกของหลอดเลือดหรือความขุ่น |
| เยื่อบุผิว | คงสภาพอยู่เสมอ (ไม่มีไขมันสะสม) |
การบางเป็นแถบกว้าง 1-2 มม. อยู่เหนือลิมบัส 1-2 มม. ทอดยาวจากตำแหน่ง 4 นาฬิกาถึง 8 นาฬิกา การบางอาจถึง 20% ของความหนากระจกตาปกติ บริเวณที่นูนมากที่สุดอยู่เหนือบริเวณบาง และภาพตัดขวางของกระจกตาดูเหมือน “พุงเบียร์” (beer belly) 2) การนูนนี้ทำให้เกิดสายตาเอียงเฉียงสูงถึง 20 D ซึ่งทำให้การแก้ไขสายตาทำได้ยากมาก
ใน PMD จะไม่พบวงแหวน Fleischer กรวย (cone) หรือแผลเป็นที่ยอด กระจกตาระหว่างบริเวณบางและลิมบัสปกติ และบริเวณบางจะมีเยื่อบุผิวปกคลุมเสมอ แตกต่างจาก Terrien degeneration ตรงที่ไม่มีไขมันสะสม
ผลการวิเคราะห์รูปทรงกระจกตา
หัวข้อที่มีชื่อว่า “ผลการวิเคราะห์รูปทรงกระจกตา”แผนที่ภูมิประเทศกระจกตาแสดงรูปแบบลักษณะเฉพาะดังนี้:
- รูปแบบก้ามปู (crab claw): ลักษณะเฉพาะคือบริเวณรูปพระจันทร์เสี้ยวที่มีความโค้งชันในส่วนล่างบนแผนที่กำลังหักเหของกระจกตา
- รูปแบบผีเสื้อ (butterfly): รูปแบบผีเสื้อแนวตั้งสีเย็นในบริเวณกลาง
- รูปแบบนกพิราบจูบ / นกจูบ (kissing doves / kissing birds): ลักษณะที่เห็นในการถ่ายภาพ Scheimpflug 5)
- สายตาเอียงเฉียงและรัศมีความโค้งใหญ่: เครื่องวัดความโค้งกระจกตา (keratometer) แสดงสายตาเอียงเฉียงที่รุนแรง แต่ต่างจาก keratoconus ตรงที่รัศมีความโค้งของกระจกตากลับใหญ่ขึ้น
อย่างไรก็ตาม รูปแบบก้ามปูอาจพบได้ใน keratoconus ที่ลุกลามเช่นกัน จึงไม่จำเพาะต่อ PMD 3) บนแผนที่ความสูงของกระจกตา ทั้งผิวหน้าและผิวหลังแสดงการนูนออกในส่วนปลายด้านล่าง และบนแผนที่ความหนากระจกตา จุดที่บางที่สุดอยู่ต่ำกว่าบริเวณนูนเล็กน้อย
เครื่องวิเคราะห์รูปทรงกระจกตาแบบ Placido สามารถประเมินพื้นผิวกระจกตาได้เพียงประมาณ 60% จึงมีข้อจำกัดในการประเมิน PMD ซึ่งเป็นโรคบริเวณปลาย 2) การถ่ายภาพ Scheimpflug หรือการตรวจเอกซเรย์แบบกรีดสแกน (เช่น Pentacam, Orbscan) สามารถประเมินทั้งผิวหน้าและผิวหลังของกระจกตาและแผนที่ความหนาทั้งหมด มีประโยชน์ในการวินิจฉัย PMD และแยกจาก keratoconus 2,5) โดยเฉพาะการโป่งของผิวหลังไปทางส่วนปลายด้านล่างและตำแหน่งของจุดที่บางที่สุดที่อยู่ต่ำกว่าบริเวณนูนเป็นองค์ประกอบสำคัญที่ช่วยในการวินิจฉัย PMD การแยก PMD ออกจาก keratoconus มีความสำคัญทางคลินิก แต่เนื่องจากมีกรณีเปลี่ยนผ่านระหว่างทั้งสอง การยืนยันจากภาพเพียงอย่างเดียวอาจทำได้ยากในบางกรณี จึงจำเป็นต้องติดตามการดำเนินโรคตามเวลา
ในการประเมินความก้าวหน้าของภาวะกระจกตาโป่งพอง (ectasia) จะใช้การจำแนกประเภท ABCD ที่รวมอยู่ในเครื่อง Scheimpflug ซึ่งเป็นคะแนนรวมจากองค์ประกอบสี่ประการ ได้แก่ รัศมีความโค้งด้านหน้า (A) รัศมีความโค้งด้านหลัง (B) ความหนากระจกตาต่ำสุด (C) และความคมชัดของสายตาระยะไกลที่ดีที่สุดที่แก้ไขแล้ว (D) เพื่อติดตามการเปลี่ยนแปลงเมื่อเวลาผ่านไป 2)
3. สาเหตุและปัจจัยเสี่ยง
หัวข้อที่มีชื่อว่า “3. สาเหตุและปัจจัยเสี่ยง”สาเหตุของ PMD ยังไม่ชัดเจน แต่เชื่อว่าความอ่อนแอจากความผิดปกติของโครงสร้างคอลลาเจนในชั้นสโตรมาของกระจกตา ร่วมกับความเครียดเชิงกลจากความดันลูกตา ทำให้เกิดการบางลงและโป่งออก ทางจุลกายวิภาคศาสตร์พบคอลลาเจนแบบ fibrous long-spacing (FLS) ที่ผิดปกติ (คาบ 100-110 นาโนเมตร) ในสโตรมา คอลลาเจนปกติมีคาบ 60-64 นาโนเมตร และความผิดปกตินี้อาจมีส่วนทำให้กระจกตาอ่อนแอ 4)
ในช่วงไม่กี่ปีที่ผ่านมา มีการถกเถียงกันว่าควรถือว่า PMD และโรคกระจกตารูปกรวย (keratoconus) เป็นโรคในสเปกตรัมเดียวกันหรือไม่ Belin และคณะเสนอว่า “ภาวะกระจกตาเสื่อมขอบใส (pellucid marginal degeneration) ไม่ใช่โรคอิสระ แต่ควรถือเป็นฟีโนไทป์หนึ่งของ keratoconus ที่เบี่ยงลงด้านล่าง” 3) มุมมองนี้มีพื้นฐานจากรายงานจำนวนมากเกี่ยวกับการเกิดร่วมกันของ PMD และ keratoconus ในผู้ป่วยรายเดียวกัน ความคล้ายคลึงกันของลักษณะทางจุลกายวิภาคและความผิดปกติของคอลลาเจน รวมถึงความต่อเนื่องของภาพถ่าย ในทางกลับกัน ในทางปฏิบัติทางคลินิก PMD ยังคงถูกปฏิบัติเป็นฟีโนไทป์อิสระเนื่องจากความแตกต่างในตำแหน่งที่บาง ตำแหน่งที่โป่ง อายุที่เริ่มเป็น และความเร็วในการดำเนินโรค
ปัจจัยเสี่ยง
หัวข้อที่มีชื่อว่า “ปัจจัยเสี่ยง”- ภาวะภูมิแพ้: ภาวะภูมิแพ้ เช่น ผิวหนังอักเสบภูมิแพ้และหอบหืด พบร่วมประมาณ 30% ของกรณี ในการสำรวจระดับประเทศของญี่ปุ่น รายงานภาวะภูมิแพ้ใน 22.2% ของกรณี 1)
- การขยี้ตา: สันนิษฐานว่าเป็นปัจจัยที่ทำให้กระจกตาโป่งพองแย่ลง และแนะนำให้ควบคุมภูมิแพ้ด้วยยาควบคุมการหลั่งสารจากแมสต์เซลล์ 2)
- ภูมิแพ้และความเสี่ยงต่อการทะลุ: ภาวะภูมิแพ้ถือเป็นปัจจัยเสี่ยงต่อภาวะกระจกตาบวมน้ำเฉียบพลันและการทะลุของกระจกตา 1,2) Ueji และคณะรายงานว่า 6 ใน 18 รายของ PMD ที่เกิดการทะลุของกระจกตามีภาวะภูมิแพ้หรือนิสัยขยี้ตา 1)
- ภาวะหยุดหายใจขณะหลับจากการอุดกั้นและค่าดัชนีมวลกายสูง: มีรายงานความสัมพันธ์กับกระจกตาโป่งพองโดยทั่วไป 2)
- ปัจจัยทางพันธุกรรม: PMD เพียงอย่างเดียวถือว่าไม่ถ่ายทอดทางพันธุกรรม แต่ในช่วงไม่กี่ปีที่ผ่านมามีรายงานความสัมพันธ์กับยีนที่เกี่ยวข้องกับคอลลาเจนของกระจกตา เช่น การกลายพันธุ์ของยีน KERA
ภาวะแพ้ถือเป็นปัจจัยเสี่ยงของภาวะบวมน้ำเฉียบพลันและกระจกตาทะลุ เป็นที่ทราบกันว่าภาวะแพ้เป็นปัจจัยเสี่ยงของภาวะบวมน้ำเฉียบพลันในโรคกระจกตารูปกรวย และมีการเสนอว่ามีความสัมพันธ์ที่คล้ายคลึงกันใน PMD อาการคันตาจากการแพ้อาจกระตุ้นให้ขยี้ตา ซึ่งเพิ่มความเครียดเชิงกลต่อกระจกตา การรักษาด้วยยาต้านการแพ้ตั้งแต่เนิ่นๆ และการเพิ่มยารักษาเสถียรภาพของแมสต์เซลล์อาจมีประสิทธิภาพในการป้องกันการทะลุ
4. การวินิจฉัยและวิธีการตรวจ
หัวข้อที่มีชื่อว่า “4. การวินิจฉัยและวิธีการตรวจ”การวินิจฉัยทางคลินิก
หัวข้อที่มีชื่อว่า “การวินิจฉัยทางคลินิก”การวินิจฉัย PMD ขึ้นอยู่กับการตรวจด้วยกล้องจุลทรรศน์ชนิดกรีดและประวัติโรค โดยยืนยันด้วยการวิเคราะห์รูปทรงกระจกตา สงสัย PMD เมื่อพบการบางเป็นแถบในบริเวณรอบนอกส่วนล่างของกระจกตา (ใส ไม่มีการอักเสบ ไม่มีไขมันสะสม) และการนูนเหนือบริเวณที่บาง
ในการตรวจวัดค่าสายตา PMD มีลักษณะเฉพาะคือสายตาเอียงตรงชนิดรุนแรงและสายตาเอียงไม่สม่ำเสมอซึ่งแก้ไขได้ยากด้วยแว่นตาทั่วไป 4) การตรวจรีติโนสโคปีพบรีเฟล็กซ์แบบกรรไกร (scissors reflex) 2) ผู้ป่วยที่ไม่รุนแรงมักได้รับการวินิจฉัยผิดว่าเป็นสายตาเอียงตรงธรรมดา ดังนั้นการตรวจวิเคราะห์รูปทรงกระจกตาอย่างละเอียดจึงมีความสำคัญ
บทบาทของการตรวจ
หัวข้อที่มีชื่อว่า “บทบาทของการตรวจ”- เครื่องวัดความโค้งกระจกตา (Keratometer): ตรวจพบสายตาเอียงตรงชนิดรุนแรง แตกต่างจากโรคกระจกตารูปกรวยตรงที่รัศมีความโค้งของกระจกตามักจะใหญ่กว่า
- แผนที่ภูมิประเทศกระจกตา (ชนิด Placido): ตรวจพบรูปแบบก้ามปู (crab claw) แต่มีข้อจำกัดในการประเมินบริเวณรอบนอก 2)
- การถ่ายภาพตัดขวาง Scheimpflug: มีประโยชน์ในการวินิจฉัยและประเมินการดำเนินโรคของ PMD ผ่านแผนที่ความสูงของผิวหน้าด้านหน้าและด้านหลัง และแผนที่ความหนากระจกตาทั้งหมด 2,5)
- การถ่ายภาพตัดขวางแบบสลิตสแกน (Orbscan): ตรวจพบลักษณะเฉพาะ เช่น รูปแบบนกพิราบจูบกัน (kissing doves)
- OCT ส่วนหน้าดวงตา (AS-OCT): ประเมินแผนที่ความหนากระจกตาและแผนที่ความหนาของเยื่อบุผิวผ่านภาพตัดขวางความละเอียดสูง แสดงให้เห็นการบางของสโตรมาและการปรับโครงสร้างของเยื่อบุผิว 2)
- การวัดชีวกลศาสตร์ของกระจกตา: การลดลงของฮิสเทอรีซิสของกระจกตา (corneal hysteresis) และปัจจัยความต้านทานของกระจกตา (corneal resistance factor) คาดว่าจะมีประโยชน์ในการตรวจพบตั้งแต่เนิ่นๆ 2)
ตามฉันทามติระหว่างประเทศปี 2015 การดำเนินโรคถูกกำหนดให้มีการแย่ลงในสองข้อขึ้นไปจาก: «ความโค้งของกระจกตาด้านหน้าเพิ่มขึ้น», «ความโค้งของกระจกตาด้านหลังเพิ่มขึ้น», «การบางลง (หรืออัตราการเปลี่ยนแปลงความหนากระจกตาจากรอบนอกถึงจุดที่บางที่สุดเพิ่มขึ้น)» 2)
การวินิจฉัยแยกโรค
หัวข้อที่มีชื่อว่า “การวินิจฉัยแยกโรค”โรคกระจกตาเสื่อมขอบ Terrien
แผลที่กระจกตา Mooren
การอักเสบ: มีการอักเสบรุนแรงของส่วนหน้าของตาและมีแผลที่กระจกตา
ความเสียหายของเยื่อบุ: พบความเสียหายของเยื่อบุกระจกตา ใน PMD เยื่อบุยังคง完好
สายตาเอียงตรงแบบง่าย
ความหนากระจกตา: ไม่พบการบาง
ภูมิประเทศกระจกตา: รูปแบบผีเสื้อปกติ ไม่มีความชันด้านล่างแบบก้ามปู
ในการประเมินก่อนการผ่าตัดแก้ไขสายตา หาก PMD ระดับเล็กน้อยถูกวินิจฉัยผิดว่าเป็น “สายตาเอียงตามขวางอย่างง่าย” และทำการผ่าตัด อาจมีความเสี่ยงในการทำให้เกิดภาวะกระจกตาโป่งพอง (keratectasia) หลังผ่าตัด 2,4) สิ่งสำคัญที่สุดคือการแยก PMD ออกอย่างแน่ชัดในการคัดกรองก่อนผ่าตัด โดยเฉพาะในผู้ป่วยอายุน้อยที่มีสายตาเอียงตามขวางรุนแรง ค่าสายตาไม่คงที่ และมีข้อบ่งชี้ว่ากระจกตาส่วนล่างบาง (ความไม่สมมาตร I/S ส่วนล่าง, ค่าความสูงส่วนล่างเพิ่มขึ้น, ค่าความหนากระจกตาส่วนล่างลดลง) ควรแยกพวกเขาออกจากข้อบ่งชี้ของ LASIK, SMILE และ PRK
ควรวินิจฉัยโดยอาศัยผลการตรวจที่สอดคล้องกันจากหลายวิธี โดยผสมผสานการประเมินความหนากระจกตา รูปร่างกระจกตา และชีวกลศาสตร์ เนื่องจากการวินิจฉัยโดยอาศัยค่าผิดปกติชั่วคราวจากการตรวจเพียงครั้งเดียวอาจทำให้เกิดผลบวกลวง จึงแนะนำให้ตรวจสองครั้งขึ้นไปเพื่อติดตามการเปลี่ยนแปลงเมื่อเวลาผ่านไป
5. วิธีการรักษามาตรฐาน
หัวข้อที่มีชื่อว่า “5. วิธีการรักษามาตรฐาน”การแก้ไขการมองเห็นด้วยคอนแทคเลนส์
หัวข้อที่มีชื่อว่า “การแก้ไขการมองเห็นด้วยคอนแทคเลนส์”ผู้ป่วย PMD ส่วนใหญ่ได้รับการจัดการแบบไม่ผ่าตัด ตามรายงานพบว่าประมาณ 88% ได้รับการจัดการแบบไม่ผ่าตัด โดยในจำนวนนี้ 36% ใช้แว่นตา และ 52% ใช้คอนแทคเลนส์ 4) การแก้ไขด้วยแว่นตาจะถึงขีดจำกัดค่อนข้างเร็วเมื่อสายตาเอียงตามขวางเพิ่มขึ้น
| ประเภทเลนส์ | ลักษณะ |
|---|---|
| เลนส์แข็ง (RGP) | มีประสิทธิภาพมากที่สุดในการแก้ไขสายตาเอียงไม่สม่ำเสมอ แต่มักเลื่อนซ้ายขวาเนื่องจากเยื้องศูนย์ด้านล่าง ทำให้สั่งจ่ายยาก |
| เลนส์สเคลอรัล | ครอบคลุมกระจกตาโดยไม่สัมผัส ให้ความเสถียรดีเยี่ยม เป็นตัวเลือกแรกใน PMD ที่ลุกลาม 2) |
| เลนส์ไฮบริด | แกนกลาง RGP + ขอบนิ่ม ใส่สบาย 2) |
| Piggyback | RGP ซ้อนบนคอนแทคเลนส์นิ่ม ผสมผสานความสบายและกำลังแก้ไข 2) |
ใน PMD เนื่องจากส่วนที่นูนออกมาอยู่บริเวณรอบนอกของกระจกตา เลนส์ RGP ทั่วไปจึงมักเลื่อนไปทางซ้ายและขวาได้ง่าย และยากต่อการจ่ายยาเมื่อเทียบกับโรคกระจกตาโป่งพองรูปกรวย อาจมีการลองใช้เลนส์ RGP เส้นผ่านศูนย์กลางใหญ่หรือเลนส์ที่ใส่ใต้เปลือกตาบน แต่บางครั้งอาจทำให้เกิดการระคายเคืองหรือเลนส์หลุดได้ เลนส์สเคลอรัลไม่สัมผัสผิวกระจกตาเลย จึงมีประสิทธิภาพในกรณีที่ลุกลามหรือมีรูปร่างด้านหน้าไม่สม่ำเสมอ 2) เลนส์และชั้นน้ำตาด้านหลังทำหน้าที่ทางแสงเป็น “เลนส์ของเหลว” ซึ่งช่วยแก้ไขสายตาเอียงไม่สม่ำเสมอของกระจกตา ต้องใช้เวลาในการทำความคุ้นเคยกับการใส่ แต่สามารถบรรลุทั้งการมองเห็นที่แก้ไขแล้วที่ดีและความสบายในการใส่ได้ง่าย และในช่วงไม่กี่ปีที่ผ่านมาได้กลายเป็นตัวเลือกแรกสำหรับโรคกระจกตาโป่งพองโดยทั่วไป
การเชื่อมขวางคอลลาเจนกระจกตา (CXL)
หัวข้อที่มีชื่อว่า “การเชื่อมขวางคอลลาเจนกระจกตา (CXL)”การเชื่อมขวางคอลลาเจนกระจกตาเป็นการรักษาที่ยับยั้งการลุกลามของโรคกระจกตาโป่งพองโดยการสร้างพันธะเชื่อมขวางระหว่างเส้นใยคอลลาเจนในชั้นสโตรมาของกระจกตา เพิ่มความแข็งแรงทางชีวกลศาสตร์ของกระจกตา FDA ของสหรัฐอเมริกาอนุมัติให้ใช้ในโรคกระจกตาโป่งพองรูปกรวยที่ลุกลามและโรคกระจกตาโป่งพองหลังการผ่าตัดในอายุ 14-65 ปี 2) และยังใช้กับ PMD ด้วย
- โปรโตคอลมาตรฐาน (โปรโตคอลเดรสเดน): หลังจากลอกเยื่อบุผิวกระจกตาออก หยดริโบฟลาวิน 0.1% ทุก 2 นาทีเป็นเวลา 30 นาที จากนั้นฉายรังสี UV-A ความยาวคลื่น 370 นาโนเมตรที่ความเข้ม 3 mW/cm² เป็นเวลา 30 นาที (พลังงานรวม 5.4 J/cm²) 2,7)
- โปรโตคอลแบบเร่ง: ได้มีการพัฒนาวิธีการโดยเพิ่มความเข้ม UV-A เป็น 9-30 mW/cm² และลดระยะเวลาการฉายรังสี 2)
- ประสิทธิผล: มีรายงานการหยุดการลุกลามของโรคกระจกตาโป่งพองทั้งในกรณีระยะแรกและระยะลุกลาม รวมถึงการทำให้กระจกตาแบนลง 1.0-2.5 D 2,7,8) การติดตามระยะยาวแสดงให้เห็นความคงตัวหลัง CXL 10 ปี 7)
- ข้อห้ามใช้: กรณีที่มีความหนาของชั้นสโตรมากระจกตาน้อยกว่า 400 ไมโครเมตร ณ เวลาที่ฉายรังสี UV เป็นข้อห้ามเนื่องจากเสี่ยงต่อการทำลายเซลล์เยื่อบุผนังกระจกตา 2) อย่างไรก็ตาม มีรายงานโปรโตคอลเฉพาะสำหรับกระจกตาบางมาก (โปรโตคอล sub400) เช่นกัน 9)
- ภาวะแทรกซ้อน: กระจกตาอักเสบแบบจุดตื้น, รอยย่นของกระจกตา, กลัวแสง, ตาแห้ง, กระจกตาอักเสบติดเชื้อ, การแทรกซึมแบบปราศจากเชื้อ, ฝ้าที่กระจกตา, แผลเยื่อบุผิวหายช้า, กระจกตาบวมน้ำ ฯลฯ 2)
- Stojanovic และคณะ รายงานประโยชน์ของขั้นตอนเดียวของ PRK เฉพาะที่ (การลอกเยื่อบุผิวผ่านชั้นเยื่อบุผิวแบบนำทางด้วยภูมิประเทศ) และ CXL ใน PMD และโรคกระจกตาโป่งพองรูปกรวย 6)
ในเนเธอร์แลนด์ มีรายงานว่าหลังจากนำ CXL มาใช้ จำนวนการปลูกถ่ายกระจกตาสำหรับโรคกระจกตาโป่งพองรูปกรวยลดลงประมาณ 25% 10) การทบทวนของ Cochrane ก็สรุปว่า CXL มีประสิทธิภาพในการชะลอการลุกลามของภาวะกระจกตาโป่งพอง 12) ใน PMD ไม่มีการสะสมของการทดลองแบบสุ่มที่มีกลุ่มควบคุมขนาดใหญ่เท่ากับโรคกระจกตาโป่งพองรูปกรวย แต่ในระดับรายงานผู้ป่วย มีรายงานการคงรูปทรงของกระจกตาและการลดลงของค่า Keratometry สูงสุดในหลายกรณี และแนะนำให้นำ CXL มาใช้ตั้งแต่เนิ่นๆ ในผู้ป่วยอายุน้อยถึงวัยกลางคนที่มีการลุกลามที่ได้รับการยืนยัน
วงแหวนคั่นกลางชั้นกระจกตา (ICRS)
หัวข้อที่มีชื่อว่า “วงแหวนคั่นกลางชั้นกระจกตา (ICRS)”วงแหวนคั่นกลางชั้นกระจกตา (ICRS, ชื่อทางการค้า Intacs, Ferrara ฯลฯ) เป็นหัตถการที่ใส่วงแหวน PMMA ครึ่งวงกลมเข้าไปในชั้นเนื้อกระจกตาเพื่อทำให้รูปทรงกระจกตาแบนลงและลดสายตาเอียงที่ไม่สม่ำเสมอ
- ข้อบ่งชี้: กระจกตาโป่งพองที่มีศูนย์กลางใสและความหนากระจกตา ≥ 400 ไมโครเมตร 2)
- ผล: การมองเห็นดีขึ้นทั้งแบบไม่แก้ไขและแก้ไขแล้ว ลดความคลาดเคลื่อนลำดับสูง ทำให้การใส่คอนแทคเลนส์ง่ายขึ้น 2)
- เทคนิค: การสร้างช่องด้วยเลเซอร์เฟมโตวินาทีเป็นวิธีหลัก และให้ผลลัพธ์เทียบเท่ากับเทคนิคแบบใช้มือ 2)
- การใช้ร่วมกับ CXL: รายงานส่วนใหญ่เพิ่ม CXL หลังการใส่ ICRS เพื่อเสริมฤทธิ์ยับยั้งการลุกลาม
ในช่วงไม่กี่ปีที่ผ่านมา ได้มีการพัฒนา CAIRS (วงแหวนคั่นกลางชั้นกระจกตาจากผู้บริจาค) โดยใช้เนื้อเยื่อกระจกตาจากผู้บริจาค ในการศึกษานำร่องในตาโรคกระจกตาโป่งพองรูปกรวย 24 ตา ไม่พบภาวะแทรกซ้อนที่เกี่ยวข้องกับวงแหวนหลังการใช้ร่วมกับ CXL 11) ICRS เป็นเพียงวิธีการเปลี่ยนรูปทรงเพื่อปรับปรุงการมองเห็นเท่านั้น และฤทธิ์ยับยั้งการลุกลามมีจำกัด ดังนั้น ในกรณีที่มีการลุกลามที่ได้รับการยืนยัน จึงใช้แนวทางการใช้ตามลำดับร่วมกับ CXL เพื่อให้ได้ประโยชน์ทั้งสองอย่าง
การปลูกถ่ายกระจกตา
หัวข้อที่มีชื่อว่า “การปลูกถ่ายกระจกตา”การผ่าตัดจะพิจารณาเมื่อไม่สามารถใส่คอนแทคเลนส์ได้หรือการแก้ไขการมองเห็นไม่เพียงพอ ใน PMD เนื่องจากบริเวณที่นูนอยู่บริเวณรอบนอกของกระจกตา เทคนิคการผ่าตัดจึงซับซ้อนกว่าการปลูกถ่ายกระจกตาส่วนกลางทั่วไป
- การปลูกถ่ายกระจกตาชั้นนอกแบบเสี้ยววงเดือน: หัตถการที่ใส่ชิ้นปลูกถ่ายชั้นกระจกตารูปเสี้ยววงเดือนเข้าไปในบริเวณบาง ความเสี่ยงต่อการปฏิเสธค่อนข้างต่ำ และเป็นหนึ่งในวิธีที่นิยมมากที่สุดในปัจจุบัน หากการมองเห็นไม่เพียงพอ แนะนำให้ผ่าตัดสองขั้นตอนโดยเพิ่มการปลูกถ่ายกระจกตาทะลุส่วนกลางในภายหลัง
- การปลูกถ่ายกระจกตาชั้นลึก (DALK): หัตถการที่แทนที่เฉพาะชั้นเนื้อกระจกตาและคงไว้ซึ่งเยื่อบุผนังกระจกตาของผู้รับ ไม่มีความเสี่ยงต่อการปฏิเสธเยื่อบุผนังกระจกตา การลดลงของเซลล์เยื่อบุผนังกระจกตาหลังผ่าตัดช้ากว่าการปลูกถ่ายแบบทะลุ และความเสี่ยงต่อการแตกของลูกตาก็ต่ำกว่าเช่นกัน 2)
- การปลูกถ่ายกระจกตาแบบทะลุ (PKP): หัตถการแบบดั้งเดิม ใน PMD จำเป็นต้องเปลี่ยนด้วยชิ้นปลูกถ่ายขนาดใหญ่ (≥ 9.0 มม.) ที่เยื้องศูนย์ลงด้านล่าง ทำให้ความเสี่ยงต่อการสร้างเส้นเลือดใหม่และการปฏิเสธสูง
- การปลูกถ่ายกระจกตาชั้นผิวบางส่วน: ขั้นตอนการตัดส่วนที่บางออกเป็นรูปพระจันทร์เสี้ยวและแทนที่ด้วยแผ่นปลูกถ่ายแบบชั้น หากจำเป็นต้องปรับปรุงการมองเห็นเพิ่มเติม อาจใช้แนวทางสองขั้นตอนโดยเพิ่มการปลูกถ่ายกระจกตาทะลุส่วนกลางในภายหลัง
การจัดการภาวะกระจกตาบวมน้ำเฉียบพลันและการทะลุของกระจกตา
หัวข้อที่มีชื่อว่า “การจัดการภาวะกระจกตาบวมน้ำเฉียบพลันและการทะลุของกระจกตา”ภาวะกระจกตาบวมน้ำเฉียบพลัน เช่นเดียวกับในโรคกระจกตารูปกรวย จะรักษาแบบประคับประคองด้วยยาหยอดตาไฮเปอร์ออสโมติก การลดความดันลูกตา และการฉีดแก๊ส PMD มีความเสี่ยงต่อการทะลุเนื่องจากส่วนที่บางมาก ดังนั้นการจัดการกรณีที่มีการทะลุจึงมีความสำคัญทางคลินิก
Ueji และคณะรายงานกรณีกระจกตาทะลุใน PMD ที่ปิดได้ด้วยการรักษาแบบประคับประคองโดยใช้คอนแทคเลนส์ชนิดนิ่มเพื่อการรักษา (TCL) และการมองเห็นที่แก้ไขแล้วดีขึ้นเป็น 1.0 หลังจากหนึ่งปี การรักษาแบบประคับประคองยังช่วยลดสายตาเอียงลงประมาณครึ่งหนึ่ง 1) ในการทบทวนวรรณกรรมก่อนหน้านี้ มีการลองรักษาแบบประคับประคอง (กาวเนื้อเยื่อ/TCL) ใน 13 จาก 20 ตาที่มีกระจกตาทะลุจาก PMD และประสบความสำเร็จใน 4 ตา 1) ในกรณีที่มีรูทะลุขนาดค่อนข้างเล็ก การรักษาแบบประคับประคองก็คุ้มค่าที่จะลอง
การผ่าตัดแก้ไขสายตา เช่น LASIK มีข้อห้ามในผู้ป่วย PMD การกรอกระจกตาเมื่อมีเนื้อกระจกตาบางอยู่อาจทำให้เกิดภาวะกระจกตาโป่งพอง (keratectasia) กรณี PMD ที่ไม่รุนแรงมักถูกวินิจฉัยผิดว่าเป็นสายตาเอียงธรรมดา ดังนั้นจึงเป็นสิ่งสำคัญที่จะต้องแยก PMD ออกอย่างแน่ชัดในระหว่างการคัดกรองก่อนการผ่าตัดแก้ไขสายตา
ผู้ป่วย PMD ส่วนใหญ่สามารถจัดการได้ด้วยคอนแทคเลนส์ โดยประมาณ 88% ของกรณีได้รับการจัดการโดยไม่ต้องผ่าตัด อย่างไรก็ตาม เนื่องจากการโป่งออกด้านล่าง คอนแทคเลนส์ชนิดแข็งทั่วไปจึงหลุดง่าย และการสั่งจับยากกว่าในโรคกระจกตารูปกรวย ในกรณีที่ลุกลาม มักเลือกใช้คอนแทคเลนส์สเคลอรัลหรือคอนแทคเลนส์แบบผสม คอนแทคเลนส์ช่วยปรับปรุงการมองเห็นโดยการชดเชยสายตาเอียงที่ไม่สม่ำเสมอ แต่ไม่ได้ยับยั้งการดำเนินของโรค ดังนั้นหากตรวจพบการลุกลาม จะทำร่วมกับการเชื่อมขวางกระจกตา (CXL)
6. พยาธิสรีรวิทยาและกลไกการเกิดโรคโดยละเอียด
หัวข้อที่มีชื่อว่า “6. พยาธิสรีรวิทยาและกลไกการเกิดโรคโดยละเอียด”ลักษณะทางเนื้อเยื่อวิทยา
หัวข้อที่มีชื่อว่า “ลักษณะทางเนื้อเยื่อวิทยา”ผลการตรวจทางพยาธิวิทยาของ PMD คล้ายกับโรคกระจกตารูปกรวย มีการบางของเนื้อกระจกตา แต่เยื่อบุผิว เยื่อบุภายใน และเยื่อหุ้มเดสเซเม็ตเป็นปกติ มีความบกพร่องหรือการฉีกขาด (การทำลายเฉพาะที่) ของเยื่อหุ้มโบว์แมน และโดยปกติไม่มีการสะสมของไขมัน เมทริกซ์ของเนื้อกระจกตาอุดมไปด้วยมิวโคโพลีแซ็กคาไรด์
ในการตรวจด้วยกล้องจุลทรรศน์อิเล็กตรอนบริเวณที่บางลง พบคอลลาเจนชนิด fibrous long-spacing (FLS) ที่ผิดปกติ คาบของคอลลาเจน FLS คือ 100-110 นาโนเมตร ซึ่งยาวกว่าคอลลาเจนปกติ (60-64 นาโนเมตร) อย่างมีนัยสำคัญ คอลลาเจน FLS นี้ยังพบได้ในโรคกระจกตารูปกรวยระยะลุกลาม ซึ่งสนับสนุนความสัมพันธ์ระหว่างโรคทั้งสอง 4)
กลไกทางชีวเคมีของการบางลงของกระจกตา
หัวข้อที่มีชื่อว่า “กลไกทางชีวเคมีของการบางลงของกระจกตา”ในโรคกระจกตารูปกรวยและภาวะกระจกตาโป่งพองที่เกี่ยวข้อง มีรายงานการเพิ่มขึ้นของกิจกรรม matrix metalloproteinase (MMP) และการลดลงของสารยับยั้งภายใน (TIMP) ซึ่งบ่งชี้ว่าการสลายคอลลาเจนในชั้นสโตรมาที่เพิ่มขึ้นมีส่วนทำให้กระจกตาบางลง 2) นอกจากนี้ยังมีรายงานการเพิ่มขึ้นของสารสื่อการอักเสบ เช่น IL-6, TNF-α และ MMP-9 ในน้ำตา ซึ่งบ่งชี้ถึงความเป็นไปได้ขององค์ประกอบการอักเสบระดับต่ำใน PMD และโรคกระจกตารูปกรวย ซึ่งก่อนหน้านี้ถือว่า “ไม่มีการอักเสบ” 2) การค้นพบนี้สอดคล้องกับการสังเกตทางคลินิกที่ว่าการขยี้ตาและการกระตุ้นจากภูมิแพ้มีส่วนทำให้โรคแย่ลง การตายของเซลล์กระจกตาที่เกิดจากไซโตไคน์อักเสบที่เพิ่มขึ้นจะลดจำนวนเซลล์ในสโตรมา ขัดขวางการเผาผลาญและการสร้างเส้นใยคอลลาเจนใหม่ ซึ่งอาจนำไปสู่ความแข็งแรงเชิงกลของกระจกตาที่ลดลงและการบางลง
กลไกเชิงกลของการโป่งของกระจกตา
หัวข้อที่มีชื่อว่า “กลไกเชิงกลของการโป่งของกระจกตา”เนื่องจากความผิดปกติของโครงสร้างคอลลาเจนในชั้นสโตรมา กระจกตาจึงอ่อนแอและไม่สามารถทนต่อความดันลูกตาปกติ ทำให้เกิดการบางลงและโป่งออกในบริเวณรอบนอกด้านล่าง บริเวณที่โป่งมากที่สุดอยู่เหนือบริเวณที่บาง เนื่องจากบริเวณที่บางนั้นบางตามโครงสร้าง แต่ความเค้นจากความดันลูกตาจะสูงสุดใกล้ขอบระหว่างบริเวณที่บางกับกระจกตาปกติ ด้วยกลไกเชิงกลนี้ ภาพตัดขวางของกระจกตาจะแสดงการรวมกันของแถบบางและการโป่งขึ้นด้านบน ทำให้เกิดรูปร่างที่มีลักษณะเฉพาะซึ่งอธิบายว่า “พุงเบียร์” (beer belly) ความผิดปกติของรูปร่างนี้ทำให้เกิดสายตาเอียงไม่สม่ำเสมออย่างรุนแรง ซึ่งไม่สามารถแก้ไขได้อย่างเพียงพอด้วยแว่นตาทั่วไป และเป็นสาเหตุโดยตรงของความบกพร่องทางการมองเห็น
อาการบวมน้ำเฉียบพลันและการทะลุ
หัวข้อที่มีชื่อว่า “อาการบวมน้ำเฉียบพลันและการทะลุ”เมื่อกระจกตาบางลงอย่างมีนัยสำคัญ เยื่อหุ้มเดสเซเม็ตจะแตก และอารมณ์ขันในช่องหน้าม่านตาไหลเข้าสู่สโตรมา ทำให้เกิดอาการบวมน้ำเฉียบพลัน ตามรายงานของ Ueji และคณะ อายุเฉลี่ยของการทะลุของกระจกตาใน PMD คือ 50.1 ± 14.6 ปี ซึ่งช้ากว่าโรคกระจกตารูปกรวย (36.9 ± 16.3 ปี) 1) สิ่งนี้สะท้อนให้เห็นว่าการดำเนินโรคของ PMD ช้ากว่าโรคกระจกตารูปกรวย การทะลุเป็นภาวะแทรกซ้อนที่พบได้ค่อนข้างน้อย แต่เมื่อเกิดขึ้นแล้วจะทำให้การมองเห็นบกพร่องอย่างรุนแรง ดังนั้นการติดตามการดำเนินโรค การแนะนำให้หลีกเลี่ยงการขยี้ตา และการควบคุมภูมิแพ้จึงมีความสำคัญ ใน PMD แถบบางจะอยู่บริเวณรอบนอก ดังนั้นความเครียดเชิงกลเฉพาะที่ เช่น การบาดเจ็บ ความผันผวนของความดันลูกตา หรือการขยี้ตามากเกินไป อาจเป็นตัวกระตุ้นให้เกิดการทะลุได้ แนะนำให้ติดตามเป็นระยะด้วยกล้องกรีดและการวัดความหนาของกระจกตา และพิจารณาการผ่าตัดตั้งแต่เนิ่นๆ ในกรณีที่ความหนาของกระจกตาลดลงอย่างมีนัยสำคัญ เพื่อป้องกันการทะลุ
7. งานวิจัยล่าสุดและแนวโน้มในอนาคต
หัวข้อที่มีชื่อว่า “7. งานวิจัยล่าสุดและแนวโน้มในอนาคต”หัวข้อการวิจัยล่าสุดที่เกี่ยวข้องกับ PMD ได้แก่:
- การตรวจพบตั้งแต่ระยะแรกด้วยกลไกทางชีวภาพ: การตรวจหา PMD ในระยะก่อนแสดงอาการ (ระยะกลไกทางชีวภาพ) โดยใช้ Ocular Response Analyzer และ Corvis ST เพื่อวัดค่า corneal hysteresis, corneal resistance factor และการวิเคราะห์ Scheimpflug แบบไดนามิก 2)
- CXL เฉพาะบุคคล: โปรโตคอล sub400 โดย Hafezi และคณะเป็นเทคนิคที่ปรับระยะเวลาการฉายรังสีตามความหนาของกระจกตาสำหรับกระจกตาที่บางมาก (<400 µm) ซึ่งแสดงให้เห็นถึงความเป็นไปได้ในการประยุกต์ใช้กับกรณีที่ลุกลามซึ่งเดิมเป็นข้อห้ามสำหรับ CXL ทั่วไป 9)
- PRK นำทางด้วยภูมิประเทศร่วมกับ CXL พร้อมกัน: รายงานโดย Stojanovic และคณะประสบความสำเร็จในการปรับปรุงการมองเห็นและยับยั้งการลุกลามพร้อมกันทั้งใน PMD และ keratoconus 6)
- ICRS จากการปลูกถ่ายกระจกตาต่างบุคคล (CAIRS): มีรายงานการใช้ CAIRS (โดยใช้เนื้อเยื่อกระจกตาของมนุษย์) ร่วมกับ CXL และไม่พบภาวะแทรกซ้อนที่เกี่ยวข้องกับชิ้นส่วนในการศึกษานำร่องใน keratoconus 11)
- การตรวจทางพันธุกรรม: การตรวจทางพันธุกรรมที่คัดกรองยีน 75 ยีน (รวมถึงยีน TGFBI) และการกลายพันธุ์มากกว่า 2000 รายการได้ถูกนำมาใช้ในทางปฏิบัติเพื่อประเมินความเสี่ยงของภาวะกระจกตาโป่งพอง 2)
- การวิเคราะห์ด้วย AI และแผนที่ความหนาของเยื่อบุผิว: ความพยายามในการตรวจหาภาวะกระจกตาโป่งพองในระยะก่อนแสดงอาการโดยอัตโนมัติกำลังได้รับการพัฒนาโดยใช้แผนที่ความหนาของเยื่อบุผิวจาก AS-OCT และการวิเคราะห์ด้วย AI ของภาพส่วนหน้าของดวงตา 2) เนื่องจากเยื่อบุผิวชดเชยความผิดปกติของชั้นสโตรมาที่อยู่ข้างใต้โดยการเปลี่ยนความหนา รูปแบบความหนาของเยื่อบุผิวจึงถือเป็นเครื่องหมายเริ่มต้นของภาวะสโตรมาโป่งพอง
8. เอกสารอ้างอิง
หัวข้อที่มีชื่อว่า “8. เอกสารอ้างอิง”- Ueji N, Kato K, Yonekawa Y, et al. Case of unilateral pellucid marginal corneal degeneration progressing to corneal perforation with keratoconus in contralateral eye. Am J Ophthalmol Case Rep. 2022;25:101293.
- American Academy of Ophthalmology Cornea/External Disease Panel. Corneal Ectasia Preferred Practice Pattern. San Francisco, CA: American Academy of Ophthalmology; 2023.
- Belin MW, Asota IM, Ambrosio R Jr, Khachikian SS. What’s in a name: keratoconus, pellucid marginal degeneration, and related thinning disorders. Am J Ophthalmol. 2011;152(2):157-162.
- Jinabhai A, Radhakrishnan H, O’Donnell C. Pellucid corneal marginal degeneration: a review. Cont Lens Anterior Eye. 2011;34(2):56-63.
- Walker RN, Khachikian SS, Belin MW. Scheimpflug photographic diagnosis of pellucid marginal degeneration. Cornea. 2008;27(8):963-966.
- Stojanovic A, Zhang J, Chen X, et al. Topography-guided transepithelial surface ablation followed by corneal collagen cross-linking performed in a single combined procedure for the treatment of keratoconus and pellucid marginal degeneration. J Refract Surg. 2010;26(2):145-152.
- Raiskup-Wolf F, Hoyer A, Spoerl E, Pillunat LE. Collagen crosslinking with riboflavin and ultraviolet-A light in keratoconus: long-term results. J Cataract Refract Surg. 2008;34(5):796-801.
- Hersh PS, Stulting RD, Muller D, et al. United States multicenter clinical trial of corneal collagen crosslinking for keratoconus treatment. Ophthalmology. 2017;124(9):1259-1270.
- Hafezi F, Kling S, Gilardoni F, et al. Individualized corneal cross-linking with riboflavin and UV-A in ultrathin corneas: the sub400 protocol. Am J Ophthalmol. 2021;224:133-142.
- Godefrooij DA, Gans R, Imhof SM, Wisse RP. Nationwide reduction in the number of corneal transplantations for keratoconus following the implementation of cross-linking. Acta Ophthalmol. 2016;94(7):675-678.
- Jacob S, Patel SR, Agarwal A, et al. Corneal allogenic intrastromal ring segments (CAIRS) combined with corneal cross-linking for keratoconus. J Refract Surg. 2018;34(5):296-303.
- Sykakis E, Karim R, Evans JR, et al. Corneal collagen cross-linking for treating keratoconus. Cochrane Database Syst Rev. 2015;(3):CD010621.
