是一种非炎症性、非遗传性的角膜扩张症 ,特征为下方周边角膜 带状变薄和前凸。
角膜缘 上方1-2毫米处,从4点到8点方向存在带状变薄区域。被认为是圆锥角膜 的类缘疾病,10%合并圆锥角膜 ,13%合并球形角膜 。
角膜地形图 显示特征性的“蟹爪”和“蝴蝶结”图案。主要症状是由高度逆规散光 引起的不规则散光 ,通过硬性接触镜或巩膜 镜矫正。
角膜交联术 (CXL )和角膜内环 (ICRS )旨在阻止进展并改善视功能。LASIK 等屈光 矫正手术是禁忌的。
透明性角膜 边缘变性(pellucid marginal corneal degeneration: PMD, PMCD )是一种非炎症性、非遗传性角膜扩张症 ,以双眼下方周边角膜 变薄为特征。“pellucid”意为“透明的”,源于变薄区域保持透明。变薄区域无血管侵入或混浊等炎症表现,被认为是圆锥角膜 的类缘疾病。
PMD是仅次于圆锥角膜 的第二常见的非炎症性角膜 变薄疾病。然而,由于常被误诊为圆锥角膜 ,实际患病率可能被低估3) 。PMD通常在30-50岁发病2,4) ,比圆锥角膜 稍晚,男性更常见。
由于PMD与圆锥角膜 在临床和组织学上有很多共同点,一些观点认为圆锥角膜 和PMD是一个连续谱3) 。约10%的PMD病例合并圆锥角膜 ,约13%合并球形角膜 4) 。有报道同一患者同时存在PMD和圆锥角膜 ;日本全国调查发现,27例单眼PMD中,17例对侧眼有圆锥角膜 或疑似圆锥角膜 1) 。
角膜 形态异常的进展导致严重的不规则散光 和视力 障碍。有强烈的逆规散光 倾向,眼镜或接触镜矫正通常比圆锥角膜 更困难4) 。
PMD常有较长的无症状期;在20多岁的健康检查或配镜时经常被漏诊,直到30-40岁逆规散光 加重、矫正视力 不佳时才首次确诊。与圆锥角膜 因急性水肿或明显的角膜 中央突出而相对早期发现不同,PMD以“治不好的逆规散光 ”、“逐渐不合适的眼镜”形式缓慢进展。流行病学数据有限,没有像圆锥角膜 那样进行国家层面的大规模研究,因此真实患病率未知。也有在屈光 手术术前检查中偶然发现PMD的病例,推测潜在患者不在少数。
Q
与圆锥角膜的区别是什么?
A
PMD表现为角膜 下方周边部变薄,最大突出位于变薄区域的上方(中央侧)。而圆锥角膜 表现为角膜 中央至旁中央部变薄,变薄区域与突出部位一致。PMD无Fleischer环或Vogt条纹,倾向于高度逆规性散光 。此外,PMD多在30岁以后发病,而圆锥角膜 在青春期发病。
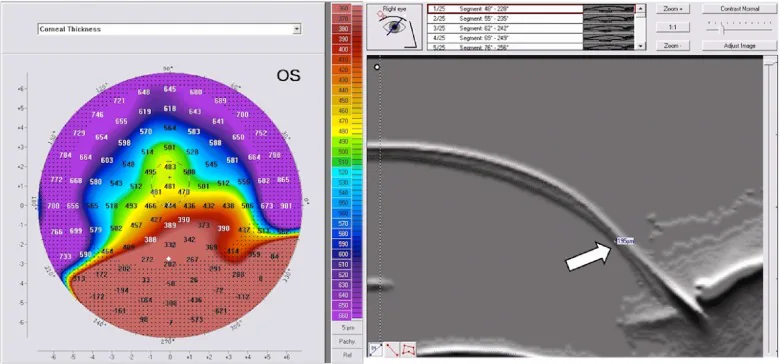
Pellucid角膜边缘变性的角膜厚度图和Scheimpflug断面图像,显示下方周边角膜变薄 Sinjab MM, et al. Pellucid-like keratoconus. F1000Res. 2012. Figure 2. PM
CI D: PMC3752625. License: CC BY.
PMD中角膜 厚度测量显示的下方角膜 变薄:A为厚度图上的Bell征,B为Scheimpflug图像上的变薄部位(白色箭头)。这与本文“2. 主要症状与临床所见”部分讨论的下方角膜 变薄相对应。
进行性视力 下降 :高度不规则散光 导致即使眼镜矫正也无法获得足够视力 图像扭曲 :由于角膜 形状异常急性疼痛和视力 下降 :罕见情况下发生急性角膜水肿 时出现屈光 不稳定视力 仍不稳定2)
所见 特征 带状变薄 4至8点钟方向,距角膜缘 1–2 mm,宽度1–2 mm 前方突出 位于变薄区域的上方(中央侧),呈啤酒肚样 角膜 透明度变薄区域透明,无血管侵入或混浊 上皮 始终保持完整(无脂质沉积)
变薄区域位于角膜缘 上方1–2毫米处,呈1–2毫米宽的带状,从4点方向延伸至8点方向。厚度可减少至正常角膜 厚度的20%。最大突出部位位于变薄区域的上方,角膜 横截面呈“啤酒肚”样外观2) 。这种突出导致高达20D的高度逆规性散光 ,使视力 矫正极为困难。
PMD中无Fleischer环、圆锥顶点或顶点瘢痕。变薄区域与角膜缘 之间的角膜 健康,变薄区域始终有上皮覆盖。与Terrien角膜边缘变性 不同,PMD无脂质沉积。
角膜地形图 显示以下特征性模式。
蟹爪(crab claw)模式 :角膜 屈光 力图上下方新月形陡峭化的特征性表现蝴蝶结(butterfly)模式 :中央区域垂直方向的冷色蝴蝶结样模式接吻鸽/接吻鸟(kissing doves / kissing birds)模式 :Scheimpflug成像中观察到的外观5) 逆规性散光 和大曲率半径 :角膜 曲率计显示强逆规性散光 ,但与圆锥角膜 不同,角膜 曲率半径反而增大
然而,蟹爪样表现也可见于进展期圆锥角膜 ,并非PMD特有3) 。角膜 高度图上,前表面和后表面均可见下方周边部隆起,角膜 厚度图上最薄点位于隆起部稍下方。
Placido盘式角膜地形图 仅能评估约60%的角膜 表面,对于周边部病变PMD的评估存在局限性2) 。Scheimpflug成像或裂隙扫描断层成像(Pentacam、Orbscan等)可评估角膜 前后表面及全角膜 厚度图,对PMD的诊断及其与圆锥角膜 的鉴别诊断具有价值2,5) 。特别是后表面高度图下方周边部的膨隆以及最薄点位于膨隆部下方的表现,是诊断PMD的重要依据。PMD与圆锥角膜 的鉴别在临床上很重要,但存在过渡病例,仅凭影像学表现难以确诊,需要纵向观察病情进展。
角膜扩张症 的进展评估采用集成于Scheimpflug成像设备的ABCD分类。该分类由四个要素组成:前表面曲率半径(A)、后表面曲率半径(B)、最小角膜 厚度(C)和最佳矫正远视 力(D),用于追踪随时间的变化2) 。
PMD的病因尚不明确,但认为是由角膜基质 胶原蛋白结构异常导致的脆弱化与眼压 引起的力学应力共同作用,导致角膜 变薄和突出。组织学上,基质胶原蛋白出现异常的纤维状长周期(FLS)胶原蛋白(周期100-110 nm),而正常胶原蛋白周期为60-64 nm。这种结构异常可能与角膜 脆弱化有关4) 。
近年来,有观点认为PMD和圆锥角膜 属于同一疾病谱。Belin等人提出“边缘性透明变性不是一种独立的疾病,而应被视为下方偏移的圆锥角膜 的一种表型”3) 。这一观点基于大量同一患者同时存在PMD和圆锥角膜 的病例报告、共同的组织学和胶原蛋白异常,以及影像学表现的连续性。另一方面,在临床实践中,由于变薄部位、突出部位、发病年龄和进展速度的差异,通常仍将PMD作为独立表型处理。
过敏体质 :约30%的患者合并特应性皮炎或哮喘等过敏性疾病。日本的一项全国调查显示22.2%的患者有过敏体质1) 。揉眼 :被认为是角膜扩张症 的加重因素,建议使用肥大细胞稳定剂控制过敏2) 。过敏与穿孔风险 :过敏体质被认为是急性水肿和角膜 穿孔的风险因素1,2) 。Ueji等人报告,在18例因PMD导致角膜 穿孔的病例中,6例有过敏体质或揉眼习惯1) 。阻塞性睡眠呼吸暂停综合征和高BMI :与角膜扩张症 总体相关2) 。遗传因素 :PMD单独被认为非遗传性,但近年来有报告称与角膜 胶原相关基因(如KERA基因突变)存在关联。
Q
过敏会使PMD恶化吗?
A
过敏体质被认为是急性水肿和角膜 穿孔的危险因素。圆锥角膜 中已知过敏体质是急性水肿的危险因素,PMD中也有类似的关联。过敏引起的眼痒可能诱发揉眼,增加角膜 的机械应力。早期抗过敏治疗和加用肥大细胞稳定剂可能有效预防穿孔。
PMD的诊断基于裂隙灯 检查和病史,并通过角膜地形图 确认。如果发现下方周边角膜 带状变薄(透明、非炎症性、无脂质沉积)且变薄区域上方突出,则怀疑PMD。
屈光 检查通常表现为高度逆规散光 和不规则散光 ,难以用常规眼镜矫正4) 。视网膜 检影可见剪刀样反射2) 。轻症病例易被误诊为单纯逆规散光 ,因此角膜地形图 详细检查很重要。
角膜 曲率计散光 。与圆锥角膜 不同,角膜 曲率半径往往较大。角膜地形图 (Placido盘型)2) 。Scheimpflug断层扫描 :通过前后表面高度图和全角膜 厚度图,有助于PMD的诊断和进展评估2,5) 。裂隙扫描断层扫描(Orbscan) :可检测接吻鸽图案等特征性表现。眼前节OCT (AS-OCT ) :通过高分辨率横断面图像评估角膜 厚度图和上皮厚度图,显示基质变薄和上皮重塑2) 。角膜生物力学 测量角膜 滞后量和角膜 阻力因子降低有望用于早期检测2) 。
根据2015年国际共识,进展定义为以下至少两项恶化:前表面角膜 曲率变陡、后表面角膜 曲率变陡、变薄(或从周边到最薄点的角膜 厚度变化率增加)2) 。
圆锥角膜
变薄部位 :角膜 中央至旁中央。PMD位于下方周边。
突出部位 :与变薄部位一致。PMD中位于变薄部位上方。
特征性表现 :可见Fleischer环、Vogt线。PMD中未见。
发病年龄 :青春期。PMD在30岁以后。
Terrien角膜边缘变性
炎症表现 :伴有脂质沉积、假性翼状胬肉 、表层血管侵入。PMD中未见。
变薄模式 :多见于上方,但可发生于任何方向。PMD位于下方。
边缘形态 :贝壳状扇形边缘。
Mooren角膜溃疡
炎症 :前眼部炎症严重,表现为角膜溃疡 。
上皮损伤 :可见角膜上皮 损伤。PMD中上皮保持完整。
单纯顺规性散光
角膜 厚度
角膜地形图
在屈光 手术的术前评估中,如果误将轻度PMD诊断为“单纯逆规散光 ”并进行手术,则有术后诱发角膜扩张症 (keratectasia)的风险2,4) 。术前筛查中可靠地排除PMD最为重要。特别是对于年轻、高度逆规散光 、屈光 度不稳定、或提示角膜 下方变薄的表现(下方I/S不对称、下方高度升高、下方角膜 厚度减少)的患者,应排除LASIK 、SMILE 和PRK的适应证。
建议结合角膜 厚度、角膜 形态和生物力学评估,基于多种检查手段的一致结果进行诊断。仅凭单一检查的暂时性异常值容易导致假阳性,因此推荐进行两次或以上检查以追踪随时间的变化。
大多数PMD病例通过非手术方式管理。据报道,约88%为非手术管理,其中36%通过眼镜矫正,52%通过隐形眼镜矫正4) 。随着逆规散光 的增加,眼镜矫正相对较早达到极限。
镜片类型 特点 硬性透气性角膜 接触镜(RGP ) 对中和不规则散光 最有效,但因下方偏心易左右移位,验配困难 巩膜 镜不接触角膜 ,覆盖角膜 ,稳定性极佳;进展期PMD的首选2) 混合镜片 RGP 中央+软性裙边。佩戴舒适度良好2) 背驮式 在软性CL上放置RGP ,兼顾舒适度和矫正力2)
在PMD中,由于突出部位位于角膜 周边部,普通RGP镜片 容易左右偏移,比圆锥角膜 更难验配。有时会尝试大直径RGP 或上眼睑支撑镜片,但可能导致刺激感或镜片脱落。巩膜 镜片完全不接触角膜 表面,因此对进展期或前表面形态不规则的病例有效2) 。镜片与镜片后方的泪液层在光学上起到“液体镜片”的作用,中和角膜 的不规则散光 。虽然需要时间适应佩戴,但容易同时获得良好的矫正视力 和佩戴舒适感,近年来正逐渐成为角膜扩张症 的首选方案。
角膜交联术 是一种通过在角膜基质 胶原纤维之间形成交联,增加角膜生物力学 刚度,从而抑制扩张症进展的治疗方法。美国FDA已批准用于14-65岁进展性圆锥角膜 和角膜扩张症 术后患者2) ,也应用于PMD。
标准方案(德累斯顿方案) :去除角膜上皮 后,每2分钟滴用0.1%核黄素滴眼液,持续30分钟,然后用波长370 nm的UV-A以3 mW/cm²的强度照射30分钟(总能量5.4 J/cm²)2,7) 加速方案 :已开发出将UV-A强度提高到9-30 mW/cm²并缩短照射时间的方法2) 效果 :早期和进展期病例均报告扩张症进展停止,并观察到1.0-2.5 D的角膜 平坦化2,7,8) 。长期随访确认CXL 后10年稳定性7) 禁忌症 :UV照射时角膜基质 厚度小于400 µm的病例因内皮损伤风险而禁忌2) 。但也有针对超薄角膜 的个体化方案(sub400方案)的报道9) 并发症 :点状角膜 炎、角膜 纹、畏光 、干眼、感染性角膜 炎、无菌性浸润、角膜 雾状混浊、上皮缺损 迁延、角膜水肿 等2) Stojanovic等人 报道了局部PRK(地形图引导经上皮消融)与CXL 一期联合手术对PMD和圆锥角膜 的有效性6)
据报道,在荷兰引入CXL 后,圆锥角膜 的角膜移植 数量减少了约25% 10) 。Cochrane综述也得出结论,CXL 能有效抑制角膜扩张 的进展 12) 。对于PMD,虽然不像圆锥角膜 那样有大规模RCT的积累,但多个病例报告显示角膜 形态稳定和最大角膜 曲率值变平。因此,对于确认进展的年轻至中年患者,建议早期引入CXL 。
角膜内环段 (ICRS ,商品名:Intacs 、Ferrara等)是一种将半圆形PMMA环插入角膜基质 以平坦角膜 形状并减少不规则散光 的手术方法。
适应症 :中央透明且角膜 厚度≥400 µm的扩张性角膜 2) 效果 :改善裸眼视力 和矫正视力 ,减少高阶像差,便于隐形眼镜佩戴 2) 技术 :飞秒激光 辅助制作通道是主流方法,效果与手工技术相当 2) 与CXL 联合 :许多报告在ICRS 植入后添加CXL 以增强抑制进展的效果
近年来,还开发了使用同种角膜 组织的CAIRS (角膜 同种异体角膜内环段 )。在一项针对24只圆锥角膜 眼的初步研究中,联合CAIRS 和CXL 后未观察到与环段相关的并发症 11) 。ICRS 主要是为了改善视功能而改变角膜 形状的手段,其抑制进展的效果有限。因此,对于确认进展的病例,采取与CXL 顺序联合的策略以获得两者的优势。
当无法佩戴隐形眼镜或视力 矫正不足时考虑手术。PMD中,突出部位位于角膜 周边部,因此手术比常规的中央角膜移植 更复杂。
周边新月形板层角膜移植术 :将新月形板层移植物插入变薄区域的手术。排斥反应风险相对较低,是近年来最受欢迎的方法之一。如果视力 不足,建议进行两步手术,随后进行中央穿透性角膜移植术 。深板层角膜移植术 (DALK )角膜基质 而保留宿主内皮的手术。没有内皮排斥反应的风险,术后内皮细胞丢失比穿透性移植慢,眼球破裂 风险也较低 2) 。穿透性角膜移植术 (PKP )新生血管 和排斥反应的风险。部分板层角膜移植术 :将菲薄区域半月形切除并用板层移植物置换的手术方式。若需进一步改善视功能,有时会采用两步法,后期再行中央穿透性角膜移植 。
急性水肿的处理与圆锥角膜 类似,采用高渗滴眼液、降眼压 、气体注入等保守治疗。PMD因菲薄区域较薄,有穿孔风险,穿孔病例的管理在临床上很重要。
Ueji等人报告了一例PMD导致角膜 穿孔的病例,通过治疗性软性接触镜(TCL)保守治疗后穿孔闭合,术后1年矫正视力 改善至1.0。保守治疗也使散光 减少约一半1) 。过去的文献综述中,PMD角膜 穿孔20眼中13眼尝试了保守治疗(组织粘合剂/TCL),其中4眼成功1) 。对于较小的穿孔,值得尝试保守治疗。
Q
我可以接受LASIK手术吗?
A
PMD患者禁忌进行LASIK 等屈光 矫正手术。在角膜基质 菲薄化的状态下切除角膜 会诱发角膜扩张症 (keratectasia)。PMD轻症病例有时会被误诊为常规逆规散光 ,因此在屈光 手术前筛查中可靠地排除PMD非常重要。
Q
我可以使用隐形眼镜吗?
A
许多PMD患者可通过隐形眼镜管理,约88%的病例采用非手术管理。但由于下方突出,普通硬性隐形眼镜容易移位,验配比圆锥角膜 更困难。进展病例常选择巩膜 镜或混合镜片。隐形眼镜通过中和不规则散光 改善视力 ,但不能抑制疾病进展,因此确认进展时应联合角膜 交联(CXL )。
PMD的组织病理学表现与圆锥角膜 相似。可见角膜基质 菲薄化,但上皮、内皮和Descemet膜正常。Bowman层 可见缺损 或断裂(局灶性破坏),通常无脂质沉积。基质富含粘多糖。
变薄区域的电子显微镜观察发现异常的长间距胶原纤维(fibrous long-spacing, FLS)。FLS胶原的周期为100-110 nm,明显长于正常胶原(60-64 nm)。这种FLS胶原也在晚期圆锥角膜 中观察到,支持两种疾病之间的关联4) 。
在圆锥角膜 及相关角膜扩张症 中,已报道基质金属蛋白酶(MMP)活性升高及其内源性抑制剂(TIMP)降低,表明基质胶原降解增强导致变薄2) 。此外,泪液中IL-6、TNF -α、MMP-9等炎症介质增加,提示传统上被认为是“非炎症性”的PMD和圆锥角膜 也可能存在低度炎症成分2) 。这些发现与揉眼和过敏刺激加重病情的临床观察一致。炎症细胞因子升高引起的角膜 细胞凋亡 降低了基质细胞密度,损害胶原纤维代谢和重塑,可能导致角膜 力学强度下降和变薄。
角膜基质 胶原结构异常导致角膜 脆弱,无法承受正常眼压 ,从而引起下方周边部变薄并突出。最大突出点位于最薄区域的上方,这是因为最薄区域本身结构薄弱,但眼压 应力在最薄区域与正常角膜 交界处最大。由于这种力学机制,角膜 横截面呈现“啤酒肚”样独特形态,结合了变薄带和向上膨隆。这种形态异常导致严重的逆规散光 ,是普通眼镜无法充分矫正的视功能障碍的直接原因。
当角膜 变薄严重进展时,Descemet膜破裂,房水 流入基质引起急性水肿。根据Ueji等人的报告,PMD角膜 穿孔的平均年龄为50.1±14.6岁,晚于圆锥角膜 的36.9±16.3岁1) 。这反映了PMD进展较圆锥角膜 缓慢。穿孔是相对罕见的并发症,但一旦发生会导致严重视功能障碍,因此监测进展、指导避免揉眼和控制过敏非常重要。在PMD中,由于变薄带位于周边部,外伤、眼压 波动或过度揉眼等局部机械应力可能诱发穿孔。建议定期进行裂隙灯 检查和角膜 厚度测量监测,对于角膜 厚度显著降低的病例考虑早期手术干预,以预防穿孔。
近年来与PMD相关的研究课题包括以下内容:
生物力学早期检测 :利用Ocular Response Analyzer和Corvis ST等设备,通过角膜 滞后量、角膜 阻力因子和动态Scheimpflug分析,在发病前阶段(生物力学阶段)检测PMD 2) 个性化CXL :Hafezi等人提出的sub400方案针对厚度小于400 µm的超薄角膜 ,根据角膜 厚度调整照射时间,显示出对传统CXL 禁忌的进展病例的适用性 9) 地形图引导PRK与CXL 同时联合 :Stojanovic等人的报告显示,对PMD和圆锥角膜 同时实现了视功能改善和进展抑制 6) 角膜 同种异体移植ICRS (CAIRS )角膜 组织片的CAIRS 与CXL 联合应用已有报道,在圆锥角膜 的初步研究中未发现与片段相关的并发症 11) 基因检测 :针对包括TGFBI在内的75个基因、2000多种突变进行筛查的基因检测,正逐步应用于角膜扩张症 风险评估 2) AI分析与上皮厚度图 :利用AS-OCT 的上皮厚度图及眼前段图像的AI分析,自动检测发病前阶段角膜扩张症 的尝试正在推进 2) 。由于上皮通过改变厚度来补偿下方基质的形态不规则,上皮厚度模式作为基质扩张症的早期标志物备受关注
Ueji N, Kato K, Yonekawa Y, et al. Case of unilateral pellucid marginal corneal degeneration progressing to corneal perforation with keratoconus in contralateral eye. Am J Ophthalmol Case Rep. 2022;25:101293.
American Academy of Ophthalmology Cornea/External Disease Panel. Corneal Ectasia Preferred Practice Pattern. San Francisco, CA: American Academy of Ophthalmology; 2023.
Belin MW, Asota IM, Ambrosio R Jr, Khachikian SS. What’s in a name: keratoconus, pellucid marginal degeneration, and related thinning disorders. Am J Ophthalmol. 2011;152(2):157-162.
Jinabhai A, Radhakrishnan H, O’Donnell C. Pellucid corneal marginal degeneration: a review. Cont Lens Anterior Eye. 2011;34(2):56-63.
Walker RN, Khachikian SS, Belin MW. Scheimpflug photographic diagnosis of pellucid marginal degeneration. Cornea. 2008;27(8):963-966.
Stojanovic A, Zhang J, Chen X, et al. Topography-guided transepithelial surface ablation followed by corneal collagen cross-linking performed in a single combined procedure for the treatment of keratoconus and pellucid marginal degeneration. J Refract Surg. 2010;26(2):145-152.
Raiskup-Wolf F, Hoyer A, Spoerl E, Pillunat LE. Collagen crosslinking with riboflavin and ultraviolet-A light in keratoconus: long-term results. J Cataract Refract Surg. 2008;34(5):796-801.
Hersh PS, Stulting RD, Muller D, et al. United States multicenter clinical trial of corneal collagen crosslinking for keratoconus treatment. Ophthalmology. 2017;124(9):1259-1270.
Hafezi F, Kling S, Gilardoni F, et al. Individualized corneal cross-linking with riboflavin and UV-A in ultrathin corneas: the sub400 protocol. Am J Ophthalmol. 2021;224:133-142.
Godefrooij DA, Gans R, Imhof SM, Wisse RP . Nationwide reduction in the number of corneal transplantations for keratoconus following the implementation of cross-linking. Acta Ophthalmol. 2016;94(7):675-678.
Jacob S, Patel SR, Agarwal A, et al. Corneal allogenic intrastromal ring segments (CAIRS ) combined with corneal cross-linking for keratoconus. J Refract Surg. 2018;34(5):296-303.
Sykakis E, Karim R, Evans JR, et al. Corneal collagen cross-linking for treating keratoconus. Cochrane Database Syst Rev. 2015;(3):CD010621.