قوز قرنیه

بیماری دژنراسیون حاشیهای پلوسید قرنیه
نکات کلیدی در یک نگاه
Section titled “نکات کلیدی در یک نگاه”1. دژنراسیون حاشیهای شفاف قرنیه چیست؟
Section titled “1. دژنراسیون حاشیهای شفاف قرنیه چیست؟”دژنراسیون حاشیهای شفاف قرنیه (PMD یا PMCD) یک اکتازی قرنیه غیرالتهابی و غیرارثی است که با نازک شدن دوطرفه قرنیه محیطی تحتانی مشخص میشود. واژه «pellucid» به معنای «شفاف» است و به شفاف ماندن ناحیه نازک شده اشاره دارد. ناحیه نازک شده فاقد علائم التهابی مانند نفوذ عروق یا کدورت است و این بیماری به عنوان یک بیماری مرتبط با قوز قرنیه در نظر گرفته میشود.
PMD دومین بیماری شایع نازکشونده غیرالتهابی قرنیه پس از قوز قرنیه است. با این حال، اغلب با قوز قرنیه اشتباه تشخیص داده میشود، بنابراین شیوع واقعی ممکن است کمتر از حد واقعی برآورد شود3). PMD معمولاً در دهه سوم تا پنجم زندگی ظاهر میشود2,4) که کمی دیرتر از قوز قرنیه است. از نظر جنسیت، مردان بیشتر مبتلا میشوند.
از آنجایی که PMD و قوز قرنیه اشتراکات زیادی در تصویر بالینی و بافتشناسی دارند، برخی محققان آنها را به عنوان یک طیف پیوسته در نظر میگیرند3). حدود ۱۰٪ از موارد PMD با قوز قرنیه و حدود ۱۳٪ با قرنیه کروی همراه است4). مواردی از共存 PMD و قوز قرنیه در یک بیمار گزارش شده است. در یک مطالعه ملی در ژاپن، از ۲۷ مورد PMD یکطرفه، ۱۷ مورد در چشم مقابل قوز قرنیه یا مشکوک به قوز قرنیه داشتند1).
با پیشرفت ناهنجاری شکل قرنیه، آستیگماتیسم نامنظم شدید ایجاد میشود و منجر به اختلال بینایی میگردد. تمایل به آستیگماتیسم خلاف قاعده قوی است و اصلاح با عینک یا لنزهای تماسی اغلب دشوارتر از قوز قرنیه است4).
PMD دوره طولانی بدون علامت دارد و اغلب در معاینات سلامت دهه سوم زندگی یا هنگام تجویز عینک نادیده گرفته میشود. معمولاً در دهه چهارم یا پنجم زندگی، زمانی که آستیگماتیسم خلاف قاعده تشدید میشود و دید اصلاحشده قابل قبول نیست، تشخیص داده میشود. در حالی که قوز قرنیه نسبتاً زود با هیدروپس حاد یا برجستگی مرکزی مشخص تشخیص داده میشود، PMD به صورت «آستیگماتیسم خلاف قاعده درمانناپذیر» و «عینکی که به تدریج نامناسب میشود» به آرامی پیشرفت میکند. دادههای اپیدمیولوژیک محدود است و مطالعات بزرگ ملی مانند قوز قرنیه انجام نشده است، بنابراین شیوع واقعی ناشناخته است. مواردی از تشخیص تصادفی در معاینات قبل از جراحی انکساری گزارش شده است که نشان میدهد تعداد قابل توجهی از افراد مبتلا تشخیص داده نشدهاند.
در PMD، قسمت پایینی محیطی قرنیه نازک میشود و حداکثر برآمدگی در بالای (سمت مرکزی) ناحیه نازک قرار دارد. در مقابل، در قوز قرنیه، قسمت مرکزی تا پارامرکزی قرنیه نازک میشود و ناحیه نازک و برآمدگی منطبق هستند. در PMD، حلقه Fleischer و خطوط Vogt دیده نمیشوند و آستیگماتیسم معکوس شدیدتر است. همچنین، PMD معمولاً بعد از ۳۰ سالگی بروز میکند، در حالی که قوز قرنیه در نوجوانی ظاهر میشود.
۲. علائم اصلی و یافتههای بالینی
Section titled “۲. علائم اصلی و یافتههای بالینی”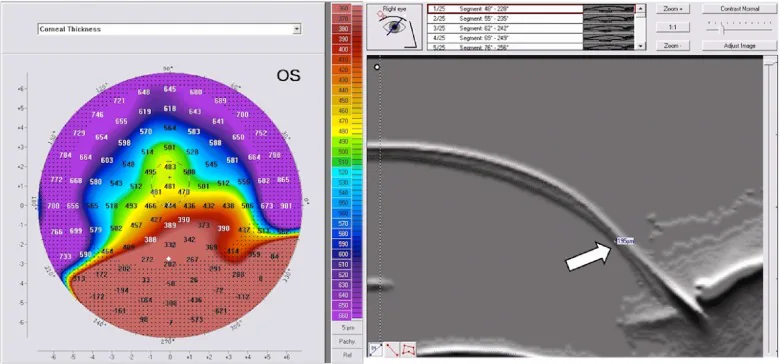
علائم ذهنی
Section titled “علائم ذهنی”- کاهش تدریجی بینایی: به دلیل آستیگماتیسم نامنظم شدید، حتی با عینک نیز دید کافی حاصل نمیشود
- اعوجاج تصویر: ناشی از ناهنجاری شکل قرنیه
- درد حاد و کاهش بینایی: به ندرت در صورت بروز ادم حاد قرنیه رخ میدهد
- ناپایداری انکساری: حتی با تغییر مکرر نسخه، بینایی پایدار نمیماند2)
یافتههای معاینه با لامپ شکافی
Section titled “یافتههای معاینه با لامپ شکافی”| یافته | ویژگی |
|---|---|
| نازک شدن نواری | در جهت ساعت ۴ تا ۸، با فاصله ۱-۲ میلیمتر از لیمبوس، عرض ۱-۲ میلیمتر |
| برآمدگی قدامی | در بالای ناحیه نازک (سمت مرکزی)، شبیه شکم آبجو (beer belly) |
| شفافیت قرنیه | ناحیه نازک شفاف است و عروقزایی یا کدورت ندارد |
| اپیتلیوم | همیشه حفظ میشود (بدون رسوب چربی) |
نازکشدگی به صورت نواری به عرض ۱-۲ میلیمتر در ۱-۲ میلیمتری بالای لیمبوس، در جهت ساعت ۴ تا ۸ وجود دارد. ممکن است تا ۲۰٪ ضخامت طبیعی قرنیه نازک شود. حداکثر برجستگی در بالای ناحیه نازک قرار دارد و مقطع قرنیه شبیه «شکم آبجو (beer belly)» است 2). این برجستگی باعث آستیگماتیسم معکوس شدید تا ۲۰ دیوپتر میشود که اصلاح بینایی را بسیار دشوار میکند.
در PMD، حلقه Fleischer، قوز (cone) و اسکار قوز دیده نمیشود. قرنیه بین ناحیه نازک و لیمبوس سالم است و ناحیه نازکشده همیشه اپیتلیالیزه است. با عدم وجود رسوب چربی از دژنراسیون Terrien متمایز میشود.
یافتههای آنالیز شکل قرنیه
Section titled “یافتههای آنالیز شکل قرنیه”توپوگرافی قرنیه الگوهای مشخصه زیر را نشان میدهد:
- الگوی پنجه خرچنگ (crab claw): یک یافته مشخصه در نقشه قدرت قرنیه که یک ناحیه هلالی شکل از شیبشدگی در پایین را نشان میدهد
- الگوی پروانه (butterfly): یک الگوی پروانهای شکل سرد در جهت عمودی در مرکز
- الگوی کبوترهای بوسهزن / پرندگان بوسهزن (kissing doves / kissing birds): ظاهری که در تصویربرداری Scheimpflug دیده میشود 5)
- آستیگماتیسم معکوس و شعاع انحنای بزرگ: کراتومتر آستیگماتیسم معکوس شدید را نشان میدهد، اما برخلاف قوز قرنیه، شعاع انحنای قرنیه بزرگتر میشود
با این حال، یافته شبه پنجه خرچنگ ممکن است در قوز قرنیه پیشرفته نیز دیده شود و اختصاصی PMD نیست 3). در نقشه ارتفاع قرنیه، برجستگی در قسمت پایینی محیطی در هر دو سطح قدامی و خلفی دیده میشود و در نقشه ضخامت قرنیه، نازکترین نقطه کمی پایینتر از برجستگی قرار دارد.
دستگاههای توپوگرافی قرنیه از نوع پلاسیدو (Placido) تنها حدود ۶۰٪ از سطح قرنیه را ارزیابی میکنند و برای ارزیابی PMD که یک بیماری محیطی است محدودیت دارند 2). تصویربرداری Scheimpflug و توموگرافی اسلیتاسکن (مانند Pentacam، Orbscan و غیره) میتوانند سطوح قدامی و خلفی قرنیه و نقشه پاکیمتری کامل را ارزیابی کنند و برای تشخیص PMD و افتراق آن از قوز قرنیه مفید هستند 2,5). به ویژه برجستگی ارتفاع خلفی به سمت پایین محیطی و قرار گرفتن نازکترین نقطه در پایین برجستگی، عناصر مهمی در تشخیص PMD هستند. تمایز بین PMD و قوز قرنیه از نظر بالینی مهم است، اما موارد انتقالی نیز وجود دارد، بنابراین تشخیص تنها بر اساس یافتههای تصویربرداری در برخی موارد دشوار است و پیگیری پیشرفت در طول زمان ضروری است.
برای ارزیابی پیشرفت اکتازی قرنیه، از طبقهبندی ABCD که در دستگاههای Scheimpflug یکپارچه شده است استفاده میشود. این یک نمره ترکیبی شامل چهار مؤلفه است: شعاع انحنای قدامی (A)، شعاع انحنای خلفی (B)، حداقل ضخامت قرنیه (C) و بهترین حدت بینایی اصلاحشده با عینک (D) که تغییرات در طول زمان را پیگیری میکند 2).
3. علل و عوامل خطر
Section titled “3. علل و عوامل خطر”سببشناسی
Section titled “سببشناسی”سببشناسی PMD مشخص نیست، اما تصور میشود که ترکیبی از ضعف ناشی از ناهنجاری ساختاری کلاژن استرومای قرنیه و تنش مکانیکی ناشی از فشار داخل چشم منجر به نازکشدن و برآمدگی میشود. از نظر بافتشناسی، کلاژن غیرطبیعی با دوره طولانی فیبری (FLS) با دوره 100-110 نانومتر در استروما مشاهده میشود. دوره طبیعی کلاژن 60-64 نانومتر است و این ناهنجاری ساختاری ممکن است در ضعف قرنیه نقش داشته باشد 4).
اخیراً بحثهایی وجود دارد که PMD و قوز قرنیه را به عنوان بیماریهایی در یک طیف در نظر میگیرند. بلین و همکاران پیشنهاد کردهاند که «دژنراسیون حاشیهای شفاف یک بیماری مستقل نیست، بلکه باید به عنوان یک فنوتیپ از قوز قرنیه با جابجایی به سمت پایین در نظر گرفته شود» 3). این دیدگاه بر اساس گزارشهای متعدد از هموجودی PMD و قوز قرنیه در یک بیمار، اشتراکات بافتشناسی و ناهنجاری کلاژن، و تداوم یافتههای تصویربرداری است. با این حال، در عمل بالینی، PMD معمولاً به عنوان یک فنوتیپ مستقل به دلیل تفاوت در محل نازکشدن، محل برآمدگی، سن شروع و سرعت پیشرفت در نظر گرفته میشود.
عوامل خطر
Section titled “عوامل خطر”- زمینه آلرژیک: حدود 30٪ از بیماران دارای زمینه آلرژیک مانند درماتیت آتوپیک یا آسم هستند. یک بررسی ملی در ژاپن، زمینه آلرژیک را در 22.2٪ گزارش کرده است 1)
- مالش چشم: به عنوان یک عامل تشدیدکننده اکتازی قرنیه مطرح شده است و کنترل آلرژی با تثبیتکنندههای ماست سل توصیه میشود 2)
- آلرژی و خطر سوراخشدگی: زمینه آلرژیک یک عامل خطر برای هیدروپس حاد و سوراخشدگی قرنیه در نظر گرفته میشود 1,2). اوجی و همکاران گزارش کردند که از 18 مورد سوراخشدگی قرنیه ناشی از PMD، 6 مورد زمینه آلرژیک یا عادت مالش چشم داشتند 1)
- آپنه انسدادی خواب و BMI بالا: ارتباط با اکتازی قرنیه به طور کلی گزارش شده است 2)
- عوامل ژنتیکی: PMD به تنهایی غیرارثی در نظر گرفته میشود، اما اخیراً ارتباط با ژنهای مرتبط با کلاژن قرنیه مانند جهش KERA گزارش شده است
استعداد آلرژیک یک عامل خطر برای ادم حاد و سوراخ شدن قرنیه در نظر گرفته میشود. استعداد آلرژیک به عنوان یک عامل خطر برای ادم حاد در قوز قرنیه شناخته شده است، اما در PMD نیز ارتباط مشابهی پیشنهاد شده است. خارش چشم ناشی از آلرژی ممکن است باعث مالش چشم شده و فشار مکانیکی بر قرنیه را افزایش دهد. درمان زودهنگام ضدآلرژی و افزودن تثبیتکنندههای ماست سل ممکن است در پیشگیری از سوراخ شدن مؤثر باشد.
4. تشخیص و روشهای آزمایش
Section titled “4. تشخیص و روشهای آزمایش”تشخیص بالینی
Section titled “تشخیص بالینی”تشخیص PMD بر اساس معاینه با لامپ شکاف و سابقه پزشکی انجام میشود و با آنالیز توپوگرافی قرنیه تأیید میگردد. وجود نوار نازکشدگی در قسمت پایینی محیط قرنیه (شفاف، غیرالتهابی، بدون رسوب چربی) و برآمدگی بالای ناحیه نازک شده، نشاندهنده PMD است.
در معاینه انکساری، آستیگماتیسم معکوس شدید و آستیگماتیسم نامنظم که با عینک معمولی قابل اصلاح نیست، مشخصه PMD است 4). در رتینوسکوپی، رفلکس قیچیای (scissors reflex) مشاهده میشود 2). موارد خفیف اغلب با آستیگماتیسم معکوس ساده اشتباه گرفته میشوند، بنابراین بررسی دقیق با توپوگرافی قرنیه اهمیت دارد.
نقش آزمایشها
Section titled “نقش آزمایشها”- کراتومتر: آستیگماتیسم معکوس شدید را تشخیص میدهد. برخلاف قوز قرنیه، شعاع انحنای قرنیه در PMD بزرگتر میشود.
- توپوگرافی قرنیه (پلاسیدو): الگوی پنجه خرچنگ (crab claw) را تشخیص میدهد، اما در ارزیابی نواحی محیطی محدودیت دارد 2).
- توموگرافی Scheimpflug: نقشههای ارتفاع سطح قدامی و خلفی و نقشه کامل پاکیمتری برای تشخیص و ارزیابی پیشرفت PMD مفید است 2,5).
- توموگرافی اسکن شکافی (Orbscan): یافتههای مشخص مانند الگوی کبوترهای بوسهزن (kissing doves) را تشخیص میدهد.
- OCT بخش قدامی (AS-OCT): تصاویر مقطعی با وضوح بالا برای ارزیابی نقشه پاکیمتری و نقشه ضخامت اپیتلیوم، نازکشدگی استروما و بازسازی اپیتلیوم را可视化 میکند 2).
- اندازهگیری بیومکانیک قرنیه: کاهش هیسترزیس قرنیه و فاکتور مقاومت قرنیه ممکن است برای تشخیص زودهنگام مفید باشد 2).
طبق اجماع بینالمللی 2015، پیشرفت بیماری به عنوان بدتر شدن حداقل دو مورد از موارد زیر تعریف میشود: «افزایش انحنای سطح قدامی قرنیه»، «افزایش انحنای سطح خلفی قرنیه»، «نازکشدگی (یا افزایش نرخ تغییر ضخامت قرنیه از محیط به نازکترین نقطه)» 2).
تشخیص افتراقی
Section titled “تشخیص افتراقی”دژنراسیون حاشیهای قرنیه ترین
زخم قرنیه مورن
التهاب: التهاب شدید بخش قدامی چشم و زخم قرنیه.
آسیب اپیتلیال: آسیب اپیتلیوم قرنیه دیده میشود. در PMD، اپیتلیوم سالم است.
آستیگماتیسم ساده معکوس
ضخامت قرنیه: نازکشدگی دیده نمیشود.
توپوگرافی: الگوی پروانهای طبیعی. هیچ گونه شیب تند به سمت پایین (crab claw) مشاهده نمیشود.
در ارزیابی قبل از جراحی انکساری، اگر PMD خفیف به اشتباه به عنوان «آستیگماتیسم معکوس ساده» تشخیص داده شود و جراحی انجام شود، خطر ایجاد اکتازی قرنیه (keratectasia) پس از عمل وجود دارد2,4). مهمترین نکته، حذف قطعی PMD در غربالگری قبل از عمل است. به ویژه در افراد جوان با آستیگماتیسم معکوس شدید، انکسار ناپایدار، و یافتههای حاکی از نازک شدن قرنیه در بخش تحتانی (عدم تقارن I/S تحتانی، افزایش ارتفاع تحتانی، کاهش پاکیمتری تحتانی)، باید از انجام LASIK، SMILE یا PRK خودداری کرد.
تشخیص باید بر اساس ترکیبی از ضخامت قرنیه، شکل قرنیه و ارزیابی بیومکانیکی و با استفاده از یافتههای همخوان از چندین روش انجام شود. از آنجایی که تشخیص تنها بر اساس یک مقدار غیرطبیعی گذرا از یک آزمایش منجر به نتایج مثبت کاذب میشود، توصیه میشود که حداقل دو بار آزمایش با پیگیری تغییرات در طول زمان انجام شود.
5. روشهای درمانی استاندارد
Section titled “5. روشهای درمانی استاندارد”اصلاح بینایی با لنزهای تماسی
Section titled “اصلاح بینایی با لنزهای تماسی”اکثر موارد PMD به صورت غیرجراحی مدیریت میشوند. بر اساس گزارشها، حدود 88% موارد به صورت غیرجراحی مدیریت میشوند که از این تعداد، 36% با عینک و 52% با لنزهای تماسی اصلاح میشوند4). اصلاح با عینک به دلیل افزایش آستیگماتیسم معکوس نسبتاً زود به محدودیت خود میرسد.
| نوع لنز | ویژگیها |
|---|---|
| لنز سخت (RGP) | موثرترین روش برای خنثیسازی آستیگماتیسم نامنظم، اما به دلیل انحراف به سمت پایین، مستعد جابجایی به چپ و راست و تجویز دشوار است. |
| لنز اسکلرال | به دلیل عدم تماس با قرنیه و پوشش آن، پایداری بالایی دارد و در PMD پیشرونده به عنوان گزینه اول انتخاب میشود2). |
| لنز هیبریدی | مرکز RGP + دامن نرم. احساس راحتی در هنگام استفاده2). |
| پیگیبک | قرار دادن RGP روی لنز نرم، ترکیب راحتی و قدرت اصلاحی2). |
در PMD، به دلیل قرارگیری ناحیه برجسته در بخش محیطی قرنیه، لنزهای معمولی RGP به راحتی به چپ و راست میلغزند و تجویز آنها دشوارتر از قوز قرنیه است. لنزهای RGP با قطر بزرگ و لنزهای زیر پلک فوقانی نیز ممکن است امتحان شوند، اما گاهی باعث تحریک یا افتادن لنز میشوند. لنزهای اسکلرال به دلیل عدم تماس کامل با سطح قرنیه، در موارد پیشرفته یا با شکل نامنظم سطح قدامی مؤثر هستند 2). لایه اشکی بین لنز و سطح پشتی آن از نظر نوری به عنوان «لنز مایع» عمل کرده و آستیگماتیسم نامنظم قرنیه را خنثی میکند. اگرچه عادت کردن به استفاده از آنها زمانبر است، اما دستیابی به حدت بینایی اصلاحشده خوب و راحتی استفاده آسانتر است و در سالهای اخیر به عنوان گزینه اول در تمامی اکتازیهای قرنیه مطرح شده است.
کراسلینکینگ قرنیه (CXL)
Section titled “کراسلینکینگ قرنیه (CXL)”کراسلینکینگ قرنیه درمانی است که با ایجاد پیوندهای عرضی بین فیبرهای کلاژن استرومای قرنیه، استحکام بیومکانیکی قرنیه را افزایش داده و پیشرفت اکتازی را مهار میکند. FDA ایالات متحده این روش را برای قوز قرنیه پیشرونده و موارد پس از جراحی اکتازی قرنیه در سنین ۱۴ تا ۶۵ سال تأیید کرده است 2) و در PMD نیز کاربرد دارد.
- پروتکل استاندارد (پروتکل درسدن): پس از برداشتن اپیتلیوم قرنیه، قطره چشمی ریبوفلاوین ۰٫۱٪ هر ۲ دقیقه به مدت ۳۰ دقیقه چکانده میشود، سپس اشعه UV-A با طول موج ۳۷۰ نانومتر و شدت ۳ میلیوات بر سانتیمتر مربع به مدت ۳۰ دقیقه تابانده میشود (انرژی کل ۵٫۴ ژول بر سانتیمتر مربع) 2,7)
- پروتکل تسریعشده: روشهایی با افزایش شدت UV-A به ۹ تا ۳۰ میلیوات بر سانتیمتر مربع و کاهش زمان تابش توسعه یافته است 2)
- اثربخشی: در موارد اولیه و پیشرونده، توقف پیشرفت اکتازی گزارش شده و علاوه بر آن، ۱٫۰ تا ۲٫۵ دیوپتر صافشدگی قرنیه مشاهده میشود 2,7,8). پیگیری طولانیمدت پایداری را تا ۱۰ سال پس از CXL تأیید کرده است 7)
- موارد منع مصرف: مواردی که ضخامت استرومای قرنیه در زمان تابش UV کمتر از ۴۰۰ میکرومتر است، به دلیل خطر آسیب اندوتلیال منع مصرف دارند 2). با این حال، پروتکلهای فردیسازیشده برای قرنیههای بسیار نازک (پروتکل sub400) نیز گزارش شده است 9)
- عوارض: کراتوپاتی اپیتلیال نقطهای، استریای قرنیه، فوتوفوبی، خشکی چشم، کراتیت عفونی، نفوذ استریل، هیز قرنیه، تأخیر در ترمیم نقص اپیتلیال، ادم قرنیه و غیره 2)
- استویانوویچ و همکاران usefulness ترکیب همزمان PRK موضعی (ابلیشن اپیتلیال توپوگرافی-گاید) و CXL را در یک مرحله برای PMD و قوز قرنیه گزارش کردند 6)
گزارش شده است که در هلند، پس از معرفی CXL، تعداد پیوند قرنیه برای قوز قرنیه حدود ۲۵٪ کاهش یافته است 10). مرور کاکرین نیز نتیجه گرفته است که CXL در مهار پیشرفت اکتازی قرنیه مؤثر است 12). در PMD، اگرچه کارآزماییهای تصادفی کنترل شده در مقیاس بزرگ به اندازه قوز قرنیه وجود ندارد، اما در سطح گزارش موارد، تثبیت شکل قرنیه و صاف شدن حداکثر مقدار کراتومتری در چندین گزارش ذکر شده است و در موارد جوان تا میانسال که پیشرفت تأیید شده است، معرفی زودهنگام CXL توصیه میشود.
بخشهای حلقه داخل استرومایی قرنیه (ICRS)
Section titled “بخشهای حلقه داخل استرومایی قرنیه (ICRS)”بخشهای حلقه داخل استرومایی قرنیه (intrastromal corneal ring segments: ICRS، با نامهای تجاری Intacs، Ferrara و غیره) روشی است که در آن حلقههای نیمدایرهای از جنس PMMA در استرومای قرنیه قرار داده میشود تا شکل قرنیه صاف شده و آستیگماتیسم نامنظم کاهش یابد.
- اندیکاسیون: قرنیه اکتاتیک با مرکز شفاف و ضخامت قرنیه ≥ ۴۰۰ میکرومتر 2)
- اثر: بهبود دید بدون اصلاح و دید اصلاح شده، کاهش انحرافات مرتبه بالا، و سهولت در تطابق لنز تماسی 2)
- روش: ایجاد کانال با لیزر فمتوثانیه رایج است و نتایج مشابه با روش دستی به دست میآید 2)
- ترکیب با CXL: گزارشهای متعددی از افزودن CXL پس از قرار دادن ICRS برای افزایش اثر مهار پیشرفت وجود دارد
در سالهای اخیر، CAIRS (بخشهای حلقه داخل استرومایی آلوژنیک قرنیه) با استفاده از بافت قرنیه همگونه نیز توسعه یافته است. در یک مطالعه مقدماتی روی ۲۴ چشم مبتلا به قوز قرنیه، پس از ترکیب CAIRS و CXL هیچ عارضهای ناشی از بخشها مشاهده نشد 11). ICRS صرفاً وسیلهای برای تغییر شکل به منظور بهبود عملکرد بینایی است و اثر مهار پیشرفت آن محدود است؛ بنابراین در مواردی که پیشرفت تأیید شده است، با ترکیب متوالی با CXL از مزایای هر دو بهره گرفته میشود.
پیوند قرنیه
Section titled “پیوند قرنیه”در صورت عدم امکان استفاده از لنز تماسی یا اصلاح ناکافی بینایی، جراحی مد نظر قرار میگیرد. در PMD، ناحیه برجسته در قسمت محیطی قرنیه قرار دارد، بنابراین روش پیوند نسبت به پیوند مرکزی معمول پیچیدهتر است.
- پیوند لایهای هلالی محیطی: روشی که در آن یک پیوند لایهای هلالی شکل در ناحیه نازک قرار داده میشود. خطر رد پیوند نسبتاً کم است و یکی از روشهای ترجیحی در سالهای اخیر است. در صورت ناکافی بودن بینایی، جراحی دو مرحلهای با افزودن بعدی پیوند نافذ تمام ضخامت مرکزی توصیه میشود
- پیوند عمقی لایهای قدامی قرنیه (DALK): روشی که در آن فقط استرومای قرنیه جایگزین شده و اندوتلیوم میزبان حفظ میشود. خطر رد اندوتلیال وجود ندارد، کاهش سلولهای اندوتلیال پس از عمل کندتر از پیوند نافذ است و خطر پارگی کره چشم نیز کمتر است 2)
- پیوند نافذ قرنیه (PKP): روش کلاسیک. در PMD، نیاز به جایگزینی با پیوند بزرگ (≥ ۹.۰ میلیمتر) به صورت غیرمرکز به سمت پایین است و خطر عروقی شدن و رد پیوند بالا است
- پیوند لایهای سطحی قرنیه: روشی که در آن ناحیه نازک شده به صورت هلالی برداشته شده و با پیوند لایهای جایگزین میشود. در صورت نیاز به بهبود بیشتر عملکرد بینایی، ممکن است رویکرد دو مرحلهای شامل افزودن پیوند نافذ مرکزی در روز بعد انجام شود.
مدیریت هیدروپس حاد و سوراخ شدگی قرنیه
Section titled “مدیریت هیدروپس حاد و سوراخ شدگی قرنیه”هیدروپس حاد مشابه قوز قرنیه با درمانهای محافظهکارانه مانند قطرههای چشمی هیپراسمولار، کاهش فشار چشم و تزریق گاز مدیریت میشود. در PMD به دلیل نازک بودن ناحیه، خطر سوراخ شدگی وجود دارد و مدیریت موارد سوراخ شدگی از نظر بالینی مهم است.
Ueji و همکاران گزارش کردند که در یک مورد سوراخ شدگی قرنیه ناشی از PMD، درمان محافظهکارانه با لنز تماسی نرم درمانی (TCL) منجر به بسته شدن سوراخ شدگی و بهبود دید اصلاح شده به 1.0 پس از یک سال شد. همچنین درمان محافظهکارانه آستیگماتیسم را تقریباً به نصف کاهش داد1). در مرور مقالات گذشته، از 20 چشم با سوراخ شدگی قرنیه ناشی از PMD، در 13 چشم درمان محافظهکارانه (چسب بافتی و TCL) امتحان شد که در 4 چشم موفق بود1). در سوراخ شدگیهای نسبتاً کوچک، ارزش امتحان درمان محافظهکارانه وجود دارد.
جراحیهای انکساری مانند LASIK در بیماران PMD منع مصرف دارند. برداشتن قرنیه در حضور نازک شدن استرومای قرنیه باعث ایجاد اکتازی قرنیه میشود. موارد خفیف PMD ممکن است با آستیگماتیسم معمولی اشتباه تشخیص داده شوند، بنابراین حذف قطعی PMD در غربالگری قبل از جراحی انکساری مهم است.
بسیاری از بیماران PMD با لنز تماسی قابل مدیریت هستند و حدود 88٪ موارد به صورت غیرجراحی مدیریت میشوند. با این حال، به دلیل برجستگی پایینی، لنزهای تماسی سخت معمولی به راحتی جابهجا میشوند و تجویز آنها دشوارتر از قوز قرنیه است. در موارد پیشرفته، اغلب لنزهای اسکلرال یا هیبریدی انتخاب میشوند. لنزهای تماسی آستیگماتیسم نامنظم را خنثی کرده و دید را بهبود میبخشند، اما تأثیری در جلوگیری از پیشرفت بیماری ندارند، بنابراین در صورت مشاهده پیشرفت، از کراس لینکینگ قرنیه (CXL) نیز استفاده میشود.
6. پاتوفیزیولوژی و مکانیسم دقیق بروز
Section titled “6. پاتوفیزیولوژی و مکانیسم دقیق بروز”ویژگیهای بافتشناسی
Section titled “ویژگیهای بافتشناسی”یافتههای پاتولوژیک بافتی PMD مشابه قوز قرنیه است. نازک شدن استرومای قرنیه مشاهده میشود، اما اپیتلیوم، اندوتلیوم و غشای دسمه طبیعی هستند. نقص یا پارگی (تخریب موضعی) غشای بومن مشاهده میشود و رسوب لیپید معمولاً دیده نمیشود. ماتریکس استروما حاوی مقادیر زیادی موکوپلی ساکارید است.
در بررسی میکروسکوپ الکترونی نواحی نازکشده، کلاژن فیبروز طویلفاصله (FLS) غیرطبیعی مشاهده میشود. فاصله دورهای کلاژن FLS حدود 100 تا 110 نانومتر است که به طور قابل توجهی بیشتر از کلاژن طبیعی (60 تا 64 نانومتر) میباشد. این کلاژن FLS در قوز قرنیه پیشرفته نیز مشاهده شده است و یافتهای است که ارتباط بین این دو بیماری را تأیید میکند 4).
مکانیسم بیوشیمیایی نازکشدن قرنیه
Section titled “مکانیسم بیوشیمیایی نازکشدن قرنیه”در قوز قرنیه و اکتازی قرنیه مرتبط، افزایش فعالیت ماتریکس متالوپروتئاز (MMP) و کاهش مهارکنندههای درونزاد آن (TIMP) گزارش شده است و تصور میشود که افزایش تجزیه کلاژن استروما در نازکشدن نقش دارد 2). همچنین افزایش واسطههای التهابی مانند IL-6، TNF-α و MMP-9 در اشک گزارش شده است و احتمال دخالت عناصر التهابی خفیف در PMD و قوز قرنیه که قبلاً «غیرالتهابی» تلقی میشدند، مطرح شده است 2). این یافتهها با مشاهدات بالینی که مالش چشم و تحریک آلرژیک به تشدید بیماری کمک میکنند، همخوانی دارد. آپوپتوز کراتوسیتها ناشی از افزایش سایتوکینهای التهابی، سلولی بودن استروما را کاهش میدهد و متابولیسم و بازسازی فیبرهای کلاژن را مختل میکند که در نتیجه منجر به کاهش استحکام مکانیکی و نازکشدن قرنیه میشود.
مکانیسم مکانیکی برجستگی قرنیه
Section titled “مکانیسم مکانیکی برجستگی قرنیه”به دلیل ناهنجاری ساختار کلاژن استرومای قرنیه، قرنیه ضعیف شده و قادر به تحمل فشار طبیعی داخل چشم نیست، در نتیجه ناحیه محیطی تحتانی نازک و برجسته میشود. اینکه حداکثر برجستگی در بالای ناحیه نازک قرار دارد، به این دلیل است که ناحیه نازک خود از نظر ساختاری نازک است، اما تنش ناشی از فشار داخل چشم در مرز بین ناحیه نازک و قرنیه طبیعی به حداکثر میرسد. با این مکانیسم مکانیکی، در مقطع قرنیه، ترکیبی از نوار نازکشده و برآمدگی رو به بالا، شکلی منحصر به فرد ایجاد میکند که به «شکم آبجو» (beer belly) تشبیه میشود. این ناهنجاری مورفولوژیک باعث آستیگماتیسم شدید معکوس میشود و علت مستقیم اختلال بینایی است که با عینک معمولی به خوبی اصلاح نمیشود.
ادم حاد و سوراخ شدن
Section titled “ادم حاد و سوراخ شدن”هنگامی که نازکشدن قرنیه به شدت پیشرفت کند، غشای دسمه پاره میشود و زلالیه وارد استروما شده و ادم حاد ایجاد میکند. بر اساس گزارش Ueji و همکاران، میانگین سن سوراخ شدن قرنیه در PMD 50.1 ± 14.6 سال است که دیرتر از قوز قرنیه با 36.9 ± 16.3 سال رخ میدهد 1). این نشاندهنده پیشرفت کندتر PMD نسبت به قوز قرنیه است. سوراخ شدن عارضه نسبتاً نادری است، اما هنگامی که رخ دهد، باعث اختلال شدید بینایی میشود؛ بنابراین پایش پیشرفت، توصیه به اجتناب از مالش چشم و کنترل آلرژی مهم است. در PMD، نوار نازک در ناحیه محیطی قرار دارد، بنابراین استرس مکانیکی موضعی مانند ضربه، نوسان فشار داخل چشم و مالش بیش از حد چشم میتواند باعث سوراخ شدن شود. پایش منظم با لامپ شکاف و اندازهگیری ضخامت قرنیه و بررسی مداخله جراحی زودهنگام در موارد کاهش شدید ضخامت قرنیه برای پیشگیری از سوراخ شدن توصیه میشود.
7. تحقیقات جدید و چشمانداز آینده
Section titled “7. تحقیقات جدید و چشمانداز آینده”موضوعات تحقیقاتی اخیر مرتبط با PMD شامل موارد زیر است:
- تشخیص زودهنگام بیومکانیکی: تشخیص PMD در مرحله قبل از بروز (مرحله بیومکانیکی) با استفاده از تحلیلهای corneal hysteresis، corneal resistance factor و dynamic Scheimpflug توسط دستگاههایی مانند Ocular Response Analyzer و Corvis ST 2)
- CXL شخصیسازیشده: پروتکل sub400 توسط Hafezi و همکاران، تکنیکی است که زمان تابش را بر اساس ضخامت قرنیه برای قرنیههای بسیار نازک با ضخامت کمتر از 400 میکرومتر تنظیم میکند و امکان استفاده از CXL را در موارد پیشرفته که قبلاً منع مصرف داشت، نشان میدهد 9)
- ترکیب همزمان PRK هدایتشده با توپوگرافی و CXL: گزارش Stojanovic و همکاران نشان میدهد که این روش برای PMD و قوز قرنیه به طور همزمان بهبود عملکرد بینایی و توقف پیشرفت را به همراه داشته است 6)
- ICRS آلوگرافت قرنیه (CAIRS): ترکیب CAIRS با استفاده از قطعات بافت قرنیه انسانی و CXL گزارش شده است و در یک مطالعه آزمایشی بر روی قوز قرنیه، عوارض ناشی از قطعات مشاهده نشد 11)
- آزمایش ژنتیکی: آزمایش ژنتیکی که 75 ژن از جمله ژن TGFBI و بیش از 2000 جهش را غربال میکند، برای ارزیابی خطر اکتازی قرنیه در حال عملیاتی شدن است 2)
- تحلیل هوش مصنوعی و نقشه ضخامت اپیتلیوم: تلاشهایی برای تشخیص خودکار اکتازی قرنیه در مرحله قبل از بروز با استفاده از نقشه ضخامت اپیتلیوم AS-OCT و تحلیل هوش مصنوعی تصاویر بخش قدامی چشم در حال انجام است 2). از آنجایی که اپیتلیوم با تغییر ضخامت خود، بینظمی استرومای زیرین را جبران میکند، الگوی ضخامت اپیتلیوم به عنوان نشانگر اولیه اکتازی استروما مورد توجه قرار گرفته است
8. منابع
Section titled “8. منابع”- Ueji N, Kato K, Yonekawa Y, et al. Case of unilateral pellucid marginal corneal degeneration progressing to corneal perforation with keratoconus in contralateral eye. Am J Ophthalmol Case Rep. 2022;25:101293.
- American Academy of Ophthalmology Cornea/External Disease Panel. Corneal Ectasia Preferred Practice Pattern. San Francisco, CA: American Academy of Ophthalmology; 2023.
- Belin MW, Asota IM, Ambrosio R Jr, Khachikian SS. What’s in a name: keratoconus, pellucid marginal degeneration, and related thinning disorders. Am J Ophthalmol. 2011;152(2):157-162.
- Jinabhai A, Radhakrishnan H, O’Donnell C. Pellucid corneal marginal degeneration: a review. Cont Lens Anterior Eye. 2011;34(2):56-63.
- Walker RN, Khachikian SS, Belin MW. Scheimpflug photographic diagnosis of pellucid marginal degeneration. Cornea. 2008;27(8):963-966.
- Stojanovic A, Zhang J, Chen X, et al. Topography-guided transepithelial surface ablation followed by corneal collagen cross-linking performed in a single combined procedure for the treatment of keratoconus and pellucid marginal degeneration. J Refract Surg. 2010;26(2):145-152.
- Raiskup-Wolf F, Hoyer A, Spoerl E, Pillunat LE. Collagen crosslinking with riboflavin and ultraviolet-A light in keratoconus: long-term results. J Cataract Refract Surg. 2008;34(5):796-801.
- Hersh PS, Stulting RD, Muller D, et al. United States multicenter clinical trial of corneal collagen crosslinking for keratoconus treatment. Ophthalmology. 2017;124(9):1259-1270.
- Hafezi F, Kling S, Gilardoni F, et al. Individualized corneal cross-linking with riboflavin and UV-A in ultrathin corneas: the sub400 protocol. Am J Ophthalmol. 2021;224:133-142.
- Godefrooij DA, Gans R, Imhof SM, Wisse RP. Nationwide reduction in the number of corneal transplantations for keratoconus following the implementation of cross-linking. Acta Ophthalmol. 2016;94(7):675-678.
- Jacob S, Patel SR, Agarwal A, et al. Corneal allogenic intrastromal ring segments (CAIRS) combined with corneal cross-linking for keratoconus. J Refract Surg. 2018;34(5):296-303.
- Sykakis E, Karim R, Evans JR, et al. Corneal collagen cross-linking for treating keratoconus. Cochrane Database Syst Rev. 2015;(3):CD010621.
