Keratoconus

Pellisid Korneal Marjinal Dejenerasyon
Bir Bakışta Önemli Noktalar
Section titled “Bir Bakışta Önemli Noktalar”1. Pellücid Marjinal Kornea Dejenerasyonu Nedir?
Section titled “1. Pellücid Marjinal Kornea Dejenerasyonu Nedir?”Pellücid marjinal kornea dejenerasyonu (PMD, PMCD), enflamatuvar olmayan ve kalıtsal olmayan bir kornea ektazisidir ve bilateral alt periferik kornea incelmesi ile karakterizedir. ‘Pellücid’ ‘saydam’ anlamına gelir ve incelmiş bölgenin saydam kalmasından kaynaklanır. İncelmiş bölgede damar invazyonu veya bulanıklık gibi enflamatuvar bulgular yoktur ve keratokonusun akraba bir hastalığı olduğu düşünülür.
PMD, keratokonustan sonra en sık görülen ikinci enflamatuvar olmayan kornea incelme hastalığıdır. Ancak sıklıkla keratokonus ile karıştırıldığı için gerçek prevalansı olduğundan düşük tahmin edilebilir3). PMD genellikle 30-50 yaşları arasında ortaya çıkar2,4) ve keratokonustan biraz daha geç başlar. Cinsiyet olarak erkeklerde daha sıktır.
PMD ve keratokonus klinik ve histolojik olarak birçok ortak özellik taşıdığından, bazı araştırmacılar bunları sürekli bir spektrum olarak görür3). PMD vakalarının yaklaşık %10’unda keratokonus, %13’ünde küresel kornea eşlik eder4). Aynı hastada PMD ve keratokonusun birlikte görüldüğü vakalar bildirilmiştir. Japonya’da yapılan ulusal bir çalışmada, 27 tek taraflı PMD vakasının 17’sinde karşı gözde keratokonus veya keratokonus şüphesi bulunmuştur1).
Kornea şekil bozukluğunun ilerlemesiyle birlikte yüksek derecede düzensiz astigmatizma oluşur ve görme bozukluğuna yol açar. Kuraldışı astigmatizma eğilimi güçlüdür ve gözlük veya kontakt lenslerle düzeltilmesi keratokonustan daha zordur4).
PMD uzun süre semptomsuz kalabilir ve 20’li yaşlardaki sağlık taramalarında veya gözlük reçetelerinde gözden kaçabilir. Genellikle 30-40’lı yaşlarda, kuraldışı astigmatizma şiddetlendiğinde ve düzeltilmiş görme keskinliği sağlanamadığında teşhis edilir. Keratokonus akut hidrops veya belirgin santral protrüzyon ile nispeten erken teşhis edilirken, PMD ‘tedavi edilemeyen kuraldışı astigmatizma’ ve ‘yavaş yavaş uymayan gözlük’ şeklinde yavaş ilerler. Epidemiyolojik veriler sınırlıdır ve keratokonus gibi ulusal düzeyde büyük ölçekli çalışmalar yapılmamıştır, bu nedenle gerçek prevalans bilinmemektedir. Refraktif cerrahi için başvuran hastaların preoperatif değerlendirmesinde tesadüfen teşhis edilen vakalar bildirilmiştir ve potansiyel olarak azımsanmayacak sayıda hasta olduğu düşünülmektedir.
PMD’de korneanın alt periferik kısmı incelir ve maksimum çıkıntı incelmiş bölgenin üstünde (merkezi tarafta) yer alır. Keratokonusta ise korneanın merkezi ve paramerkezi kısmı incelir ve incelmiş bölge ile çıkıntı çakışır. PMD’de Fleischer halkası ve Vogt çizgileri görülmez ve ters astigmatizma daha belirgindir. Ayrıca PMD genellikle 30’lu yaşlardan sonra ortaya çıkarken, keratokonus ergenlik döneminde başlar.
2. Ana belirtiler ve klinik bulgular
Section titled “2. Ana belirtiler ve klinik bulgular”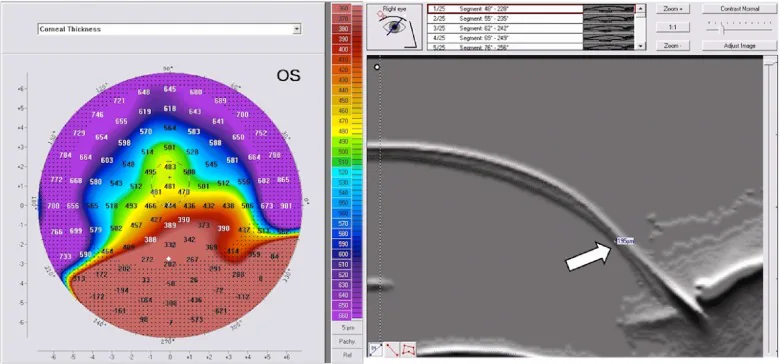
Subjektif belirtiler
Section titled “Subjektif belirtiler”- İlerleyici görme azalması: Şiddetli düzensiz astigmatizma nedeniyle gözlükle bile yeterli görme elde edilemez
- Görüntü bozulması: Kornea şekil bozukluğuna bağlı
- Akut ağrı ve görme azalması: Nadiren akut kornea ödemi oluştuğunda görülür
- Refraksiyon instabilitesi: Sık reçete değişikliklerine rağmen görme stabil değildir2)
Yarık lamba mikroskobu bulguları
Section titled “Yarık lamba mikroskobu bulguları”| Bulgular | Özellikler |
|---|---|
| Bant şeklinde incelme | Saat 4-8 yönünde, limbus’tan 1-2 mm uzaklıkta, genişlik 1-2 mm |
| Öne çıkıntı | İncelmiş bölgenin üstünde (merkezi tarafta), bira göbeği (beer belly) benzeri |
| Kornea şeffaflığı | İnceltilmiş alan şeffaftır, damar invazyonu veya bulanıklık yoktur |
| Epitel | Her zaman korunur (lipid birikimi yok) |
İnceltme, limbusun 1-2 mm üzerinde, saat 4 ile 8 yönleri arasında, 1-2 mm genişliğinde bir bant şeklinde bulunur. Normal kornea kalınlığının %20’sine kadar incelme olabilir. Maksimum çıkıntı, inceltilmiş alanın üzerinde yer alır ve kornea kesiti ‘bira göbeği (beer belly)’ gibi görünür 2). Bu çıkıntı, 20 diyoptriye kadar ulaşan yüksek derecede kuraldışı astigmatizmaya neden olur ve görme düzeltmesini belirgin şekilde zorlaştırır.
PMD’de Fleischer halkası, koni (apeks) ve apeks skarı görülmez. İnceltilmiş alan ile limbus arasındaki kornea sağlıklıdır ve inceltilmiş bölge her zaman epitelize olmuştur. Lipid birikiminin olmaması ile Terrien korneal dejenerasyondan ayrılır.
Kornea Topografisi Bulguları
Section titled “Kornea Topografisi Bulguları”Kornea topografisinde aşağıdaki karakteristik paternler görülür:
- Yengeç kıskacı (crab claw) paterni: Korneal güç haritasında alt kadranda hilal şeklinde dikleşme ile karakteristik bir bulgu
- Kelebek (butterfly) paterni: Merkezde dikey yönde soğuk renkli bir kelebek şeklinde patern
- Öpüşen güvercinler / öpüşen kuşlar (kissing doves / kissing birds) paterni: Scheimpflug görüntülemede görülen görünüm 5)
- Kuraldışı astigmatizma ve büyük eğrilik yarıçapı: Keratometrede güçlü kuraldışı astigmatizma gösterir, ancak keratokonusun aksine korneal eğrilik yarıçapı daha büyük olur
Bununla birlikte, yengeç kıskacı benzeri bulgu ilerlemiş keratokonusta da görülebilir ve PMD’ye özgü değildir 3). Kornea elevasyon haritasında hem ön hem de arka yüzeyde alt periferde çıkıntı görülür ve kornea kalınlık haritasında en ince nokta çıkıntının biraz altında yer alır.
Plasido tipi kornea topografi cihazları kornea yüzeyinin yalnızca yaklaşık %60’ını değerlendirebilir ve periferik bir hastalık olan PMD’nin değerlendirilmesinde sınırlıdır 2). Scheimpflug görüntüleme ve slit-scan tomografi (Pentacam, Orbscan vb.) korneanın ön ve arka yüzeylerini ve tüm pakimetri haritasını değerlendirebilir ve PMD tanısı ile keratokonustan ayırıcı tanısında faydalıdır 2,5). Özellikle arka yüzey elevasyonunun alt perifere doğru bombelenmesi ve en ince noktanın çıkıntının altında yer alması, PMD tanısına katkıda bulunan önemli unsurlardır. PMD ve keratokonus arasındaki ayrım klinik olarak önemlidir, ancak her iki durum arasında geçiş vakaları da mevcut olduğundan, yalnızca görüntüleme bulgularıyla kesin tanı koymak bazı vakalarda zordur ve zaman içinde ilerlemenin izlenmesi gerekir.
Korneal ektazinin ilerlemesini değerlendirmek için Scheimpflug cihazlarına entegre edilmiş ABCD sınıflandırması kullanılır. Ön eğrilik yarıçapı (A), arka eğrilik yarıçapı (B), minimum kornea kalınlığı (C) ve en iyi gözlükle düzeltilmiş uzak görme keskinliği (D) olmak üzere dört bileşenden oluşan bileşik bir skorla zaman içindeki değişim izlenir 2).
3. Nedenler ve Risk Faktörleri
Section titled “3. Nedenler ve Risk Faktörleri”Etyoloji
Section titled “Etyoloji”PMD’nin etyolojisi net değildir, ancak korneal stromal kollajenin yapısal anormalliğine bağlı zayıflama ile göz içi basıncının mekanik stresinin birleşiminin incelme ve çıkıntıya yol açtığı düşünülmektedir. Histolojik olarak, stromada normalden farklı, 100-110 nm periyotlu fibröz uzun aralıklı (FLS) kollajen görülür. Normal kollajen periyodu 60-64 nm’dir ve bu yapısal anormallik korneal zayıflamaya katkıda bulunabilir 4).
Son yıllarda PMD ve keratokonusun aynı spektrumdaki hastalıklar olarak ele alınması tartışılmaktadır. Belin ve arkadaşları, “pellucid marjinal dejenerasyonun bağımsız bir hastalık olmadığını, aşağıya doğru yer değiştirmiş keratokonusun bir fenotipi olarak düşünülmesi gerektiğini” öne sürmüştür 3). Bu görüş, aynı hastada PMD ve keratokonusun birlikte görüldüğü çok sayıda vaka raporuna, histoloji ve kollajen anormalliklerindeki ortaklıklara ve görüntüleme bulgularındaki sürekliliğe dayanmaktadır. Bununla birlikte, klinik pratikte incelme bölgesi, çıkıntı bölgesi, başlangıç yaşı ve ilerleme hızı gibi farklılıklar nedeniyle PMD genellikle bağımsız bir fenotip olarak ele alınır.
Risk Faktörleri
Section titled “Risk Faktörleri”- Alerjik yatkınlık: Hastaların yaklaşık %30’unda atopik dermatit veya astım gibi alerjik yatkınlık bulunur. Japonya’da yapılan ulusal bir çalışmada %22,2 oranında alerjik yatkınlık bildirilmiştir 1)
- Göz ovuşturma: Korneal ektaziyi kötüleştiren bir faktör olarak öne sürülmüştür ve mast hücre stabilizatörleri ile alerji kontrolü önerilir 2)
- Alerji ve perforasyon riski: Alerjik yatkınlık, akut hidrops ve kornea perforasyonu için bir risk faktörü olarak kabul edilir 1,2). Ueji ve arkadaşları, PMD’ye bağlı kornea perforasyonu gelişen 18 hastanın 6’sında alerjik yatkınlık veya göz ovuşturma alışkanlığı olduğunu bildirmiştir 1)
- Obstrüktif uyku apnesi ve yüksek BMI: Genel olarak korneal ektazi ile ilişkili olduğu bildirilmiştir 2)
- Genetik faktörler: PMD tek başına kalıtsal olmayan bir hastalık olarak kabul edilir, ancak son yıllarda KERA gen mutasyonu gibi korneal kollajen ile ilişkili genlerle bağlantı bildirilmektedir
Alerjik yatkınlık, akut hidrops ve kornea perforasyonu için bir risk faktörü olarak kabul edilir. Alerjik yatkınlık, keratokonusta akut hidrops için bir risk faktörü olarak bilinir, ancak PMD’de de benzer bir ilişki olduğu düşünülmektedir. Alerjiye bağlı göz kaşıntısı, göz ovuşturmayı tetikleyerek korneaya mekanik stresi artırabilir. Erken antialerjik tedavi ve mast hücre stabilizatörlerinin eklenmesi perforasyonu önlemede etkili olabilir.
4. Tanı ve Test Yöntemleri
Section titled “4. Tanı ve Test Yöntemleri”Klinik Tanı
Section titled “Klinik Tanı”PMD tanısı, yarık lamba muayenesi ve tıbbi öyküye dayanır ve kornea topografisi ile doğrulanır. Alt periferik korneada bant şeklinde incelme (saydam, inflamatuar olmayan, lipid birikimi olmayan) ve incelmiş bölgenin üzerinde bombeleşme varsa PMD’den şüphelenilir.
Refraksiyon muayenesinde, normal gözlük reçetesiyle düzeltilemeyen şiddetli kuraldışı astigmatizma ve düzensiz astigmatizma karakteristiktir 4). Retinoskopide makas refleksi (scissors reflex) görülür 2). Hafif vakalar sıklıkla basit kuraldışı astigmatizma ile karıştırıldığından, kornea topografisi ile detaylı inceleme önemlidir.
Testlerin Rolü
Section titled “Testlerin Rolü”- Kerotometre: Şiddetli kuraldışı astigmatizmayı tespit eder. Keratokonustan farklı olarak, kornea eğrilik yarıçapı daha büyük olma eğilimindedir.
- Kornea topografisi (Plasido): Yengeç pençesi (crab claw) paternini tespit eder, ancak periferik değerlendirmede sınırlıdır 2).
- Scheimpflug tomografisi: Ön ve arka yüzey elevasyon haritaları ve tüm pakimetri haritası ile PMD tanısı ve ilerleme değerlendirmesinde faydalıdır 2,5).
- Yarık taramalı tomografi (Orbscan): Öpüşen güvercinler (kissing doves) paterni gibi karakteristik bulguları tespit eder.
- Ön segment OCT (AS-OCT): Yüksek çözünürlüklü kesitsel görüntülerle pakimetri haritası ve epitel kalınlık haritasını değerlendirerek stromal incelme ve epitelyal yeniden şekillenmeyi görselleştirir 2).
- Kornea biyomekanik ölçümü: Korneal histerezis ve korneal direnç faktöründeki azalmanın erken tespitte faydalı olabileceği düşünülmektedir 2).
2015 uluslararası konsensusuna göre ilerleme, aşağıdakilerden en az ikisinin kötüleşmesi olarak tanımlanır: «ön kornea eğriliğinde dikleşme», «arka kornea eğriliğinde dikleşme», «incelme (veya periferden en ince noktaya kornea kalınlık değişim oranında artış)» 2).
Ayırıcı Tanı
Section titled “Ayırıcı Tanı”Terrien Marjinal Kornea Dejenerasyonu
Mooren Kornea Ülseri
Enflamasyon: Ön segmentte şiddetli enflamasyon ve kornea ülseri.
Epitel hasarı: Kornea epitelinde hasar görülür. PMD’de epitel sağlamdır.
Basit Ters Astigmatizma
Kornea kalınlığı: İncelme görülmez.
Topografi: Normal papyon deseni. Aşağıya doğru yengeç pençesi benzeri dikleşme yoktur.
Refraktif cerrahi öncesi değerlendirmede, hafif PMD yanlışlıkla “basit ters astigmatizma” olarak teşhis edilir ve cerrahi uygulanırsa, postoperatif keratektazi riski vardır2,4). Preoperatif taramada PMD’nin kesin olarak dışlanması en önemli noktadır. Özellikle genç yaşta şiddetli ters astigmatizma, stabil olmayan refraksiyon, kornea alt kısmında incelmeyi düşündüren bulgular (alt I/S asimetrisi, alt elevasyon artışı, alt pakimetri azalması) varsa, LASIK, SMILE veya PRK endikasyonu dışında bırakılmalıdır.
Kornea kalınlığı, kornea şekli ve biyomekanik değerlendirmenin birleşimiyle, birden fazla modalitede uyumlu bulgulara dayanarak tanı konulması tercih edilir. Tek bir testin geçici anormal değeriyle tanı koymak yalancı pozitifliğe yol açabileceğinden, zaman içindeki değişimi takip etmek için en az iki kez test yapılması önerilir.
5. Standart Tedavi Yöntemleri
Section titled “5. Standart Tedavi Yöntemleri”Kontakt Lens ile Görme Düzeltmesi
Section titled “Kontakt Lens ile Görme Düzeltmesi”PMD vakalarının çoğu cerrahi dışı yöntemlerle yönetilir. Raporlara göre yaklaşık %88’i cerrahi dışı yönetilir ve bunların %36’sı gözlük, %52’si kontakt lens ile düzeltilir4). Gözlük düzeltmesi, ters astigmatizmanın artmasıyla nispeten erken bir zamanda sınırına ulaşır.
| Lens Türü | Özellikler |
|---|---|
| Sert Lens (RGP) | Düzensiz astigmatizmayı nötralize etmede en etkili yöntemdir, ancak aşağıya doğru desantrasyon nedeniyle sağa sola kaymaya yatkındır ve reçetelendirmesi zordur. |
| Skleral Lens | Korneaya temas etmediği ve korneayı örttüğü için stabilitesi yüksektir ve ilerleyici PMD’de ilk seçenek haline gelir2). |
| Hibrit Lens | RGP merkez + yumuşak etek. Kullanım konforu iyidir2). |
| Piggyback | Yumuşak lens üzerine RGP yerleştirilir, kullanım konforu ve düzeltme gücü bir arada sağlanır2). |
PMD’de çıkıntı korneanın periferik kısmında olduğu için normal RGP lensler sağa sola kaymaya eğilimlidir ve reçetelendirilmesi keratokonustan daha zordur. Büyük çaplı RGP veya üst göz kapağı altına yerleştirilen lensler denenebilir ancak bunlar tahrişe veya lens düşmesine neden olabilir. Skleral lensler kornea yüzeyine hiç temas etmediği için ilerlemiş vakalarda veya düzensiz ön yüzey şekli olan hastalarda etkilidir 2). Lens ile lensin arka yüzeyi arasındaki gözyaşı tabakası optik olarak bir “sıvı lens” işlevi görür ve korneanın düzensiz astigmatizmasını nötralize eder. Kullanıma alışmak zaman alsa da iyi düzeltilmiş görme keskinliği ve konforu bir arada sağlamak daha kolaydır ve son yıllarda tüm kornea ektazilerinde birinci basamak seçenek haline gelmektedir.
Kornea Çapraz Bağlama (CXL)
Section titled “Kornea Çapraz Bağlama (CXL)”Kornea çapraz bağlama, kornea stromasındaki kolajen lifler arasında çapraz bağlar oluşturarak korneanın biyomekanik sertliğini artıran ve ektazinin ilerlemesini durduran bir tedavidir. ABD FDA tarafından 14-65 yaş arası ilerleyici keratokonus ve kornea ektazisi sonrası vakalar için onaylanmıştır 2) ve PMD’de de uygulanmaktadır.
- Standart protokol (Dresden protokolü): Kornea epiteli kaldırıldıktan sonra, %0.1 riboflavin göz damlası 2 dakikada bir 30 dakika süreyle damlatılır, ardından 370 nm dalga boyunda UV-A, 3 mW/cm² yoğunlukta 30 dakika süreyle uygulanır (toplam enerji 5.4 J/cm²) 2,7)
- Hızlandırılmış protokol: UV-A yoğunluğunun 9-30 mW/cm²’ye çıkarıldığı ve ışınlama süresinin kısaltıldığı yöntemler geliştirilmiştir 2)
- Etkinlik: Erken ve ilerlemiş vakalarda ektazi ilerlemesinin durduğu ve ek olarak 1.0-2.5 D kornea düzleşmesi gözlenmiştir 2,7,8). Uzun dönem takipte CXL’den 10 yıl sonra stabilite doğrulanmıştır 7)
- Kontrendikasyonlar: UV ışınlaması sırasında kornea stroma kalınlığı 400 µm’den az olan vakalar endotel hasarı riski nedeniyle kontrendikedir 2). Ancak çok ince kornealar için kişiselleştirilmiş protokoller (sub400 protokolü) de bildirilmiştir 9)
- Komplikasyonlar: Noktasal epitelyal keratopati, kornea striası, fotofobi, kuru göz, enfeksiyöz keratit, steril infiltrasyon, kornea halesi, epitel defektinde gecikme, kornea ödemi vb. 2)
- Stojanovic ve ark., PMD ve keratokonus için tek seansta topografi rehberliğinde epitelyal ablasyon ile lokal PRK ve CXL kombinasyonunun yararlılığını bildirmiştir 6)
Hollanda’da CXL’in uygulamaya girmesinden sonra keratokonus için kornea nakli sayısının yaklaşık %25 azaldığı bildirilmiştir 10). Cochrane incelemesi de CXL’in kornea ektazisinin ilerlemesini engellemede etkili olduğu sonucuna varmıştır 12). PMD’de keratokonus kadar büyük ölçekli randomize kontrollü çalışma birikimi olmamakla birlikte, vaka raporları düzeyinde kornea şeklinin stabilizasyonu ve maksimum keratometri değerinde düzleşme birden fazla kez bildirilmiş olup, ilerleme doğrulanmış genç-orta yaşlı olgularda erken CXL uygulaması önerilmektedir.
Kornea İçi Halka Segmentleri (ICRS)
Section titled “Kornea İçi Halka Segmentleri (ICRS)”Kornea içi halka segmentleri (intrastromal corneal ring segments: ICRS, ticari adları Intacs, Ferrara vb.), kornea stromasına yarım daire şeklinde PMMA halkalar yerleştirilerek kornea şeklini düzleştiren ve düzensiz astigmatizmayı azaltan bir cerrahi yöntemdir.
- Endikasyon: Merkezi saydam ve kornea kalınlığı ≥ 400 µm olan ektatik kornea 2)
- Etki: Çıplak görme ve düzeltilmiş görme keskinliğinde iyileşme, yüksek dereceli aberasyonlarda azalma, kontakt lens uyumunda kolaylık 2)
- Teknik: Femtosaniye lazer ile kanal oluşturma yaygındır ve manuel teknikle eşdeğer sonuçlar elde edilir 2)
- CXL ile kombinasyon: ICRS yerleştirilmesinin ardından CXL eklenerek ilerleme engelleyici etkinin artırıldığına dair çok sayıda rapor bulunmaktadır
Son yıllarda, aynı tür kornea dokusu kullanılarak CAIRS (kornea allojenik intrastromal halka segmentleri) de geliştirilmiştir. Keratokonuslu 24 göz üzerinde yapılan bir pilot çalışmada, CAIRS ve CXL kombinasyonu sonrası segment kaynaklı herhangi bir komplikasyon gözlenmemiştir 11). ICRS yalnızca görsel işlevi iyileştirmeye yönelik şekil değişikliği aracıdır ve ilerlemeyi engelleme etkisi sınırlıdır; bu nedenle ilerleme doğrulanmış olgularda, CXL ile sıralı kombinasyon yapılarak her iki yöntemin avantajlarından yararlanılması hedeflenir.
Kornea Nakli
Section titled “Kornea Nakli”Kontakt lens kullanımının mümkün olmadığı veya görme düzeltmesinin yetersiz olduğu durumlarda cerrahi düşünülür. PMD’de çıkıntı korneanın periferik kısmında yer aldığından, standart merkezi kornea nakline göre teknik daha karmaşıktır.
- Periferik hilal şeklinde lameller keratoplasti: İnce bölgeye hilal şeklinde lameller greft yerleştirilen yöntem. Red reaksiyonu riski nispeten düşüktür ve son yıllarda en çok tercih edilen yöntemlerden biridir. Görme yetersizse, daha sonra merkezi penetran keratoplasti eklenen iki aşamalı cerrahi önerilir
- Derin ön lameller keratoplasti (DALK): Sadece kornea stromasının değiştirilip konak endotelinin korunduğu yöntem. Endotel reddi riski yoktur, postoperatif endotel hücre kaybı penetran keratoplastiye göre daha yavaştır ve göz küresi rüptürü riski de daha düşüktür 2)
- Penetran keratoplasti (PKP): Klasik yöntem. PMD’de, büyük (≥ 9.0 mm) greftin aşağıya doğru eksantrik olarak yerleştirilmesi gerekir ve neovaskülarizasyon ile red reaksiyonu riski yüksektir
- Kısmi yüzeyel keratoplasti: İnceltilmiş bölgenin yarım ay şeklinde çıkarılıp lamellar greft ile değiştirildiği cerrahi yöntem. Görme fonksiyonunda ek iyileşme gerekiyorsa, daha sonra merkezi penetran keratoplasti eklenerek iki aşamalı bir yaklaşım uygulanabilir.
Akut hidrops ve kornea perforasyonu yönetimi
Section titled “Akut hidrops ve kornea perforasyonu yönetimi”Akut hidrops, keratokonus ile benzer şekilde hiperosmolar göz damlaları, göz içi basıncını düşürme ve gaz enjeksiyonu gibi konservatif tedavilerle yönetilir. PMD’de inceltilmiş bölge ince olduğu için perforasyon riski vardır ve perforasyon vakalarının yönetimi klinik olarak önemlidir.
Ueji ve ark., PMD’ye bağlı kornea perforasyonu olan bir vakada, terapötik yumuşak kontakt lens (TCL) ile konservatif tedavinin perforasyonu kapattığını ve bir yıl sonra düzeltilmiş görme keskinliğinin 1.0’a yükseldiğini bildirdi. Konservatif tedavi ile astigmatizmanın yaklaşık yarı yarıya azaldığı da gözlemlendi1). Geçmiş literatür taramasında, PMD’ye bağlı 20 kornea perforasyonunun 13’ünde konservatif tedavi (doku yapıştırıcısı ve TCL) denenmiş ve 4’ünde başarılı olunmuştur1). Nispeten küçük perforasyonlarda konservatif tedaviyi denemek değerlidir.
PMD hastalarında LASIK gibi refraktif cerrahiler kontrendikedir. Kornea stromasında incelme varken kornea dokusunun çıkarılması keratektaziye yol açar. PMD’nin hafif vakaları sıklıkla normal astigmatizma ile karıştırılabileceğinden, refraktif cerrahi öncesi taramada PMD’nin kesin olarak dışlanması önemlidir.
PMD hastalarının çoğu kontakt lens ile yönetilebilir ve vakaların yaklaşık %88’i cerrahi olmayan yöntemlerle yönetilir. Ancak alt kadrandaki çıkıntı nedeniyle normal sert kontakt lensler kolayca kayar ve reçetelendirilmesi keratokonustan daha zordur. İlerlemiş vakalarda sıklıkla skleral lensler veya hibrit lensler tercih edilir. Kontakt lensler düzensiz astigmatizmayı nötralize ederek görmeyi iyileştirir, ancak hastalığın ilerlemesini engellemez; bu nedenle ilerleme tespit edilirse kornea çapraz bağlama (CXL) ile birlikte kullanılır.
6. Patofizyoloji ve ayrıntılı oluşum mekanizması
Section titled “6. Patofizyoloji ve ayrıntılı oluşum mekanizması”Histolojik özellikler
Section titled “Histolojik özellikler”PMD’nin histopatolojik bulguları keratokonusa benzer. Kornea stromasında incelme görülür, ancak epitel, endotel ve Descemet membranı normaldir. Bowman membranında defekt veya yırtılma (lokalize yıkım) görülür ve lipid birikimi genellikle görülmez. Stromal matrikste bol miktarda mükopolisakkarit bulunur.
İncelmiş bölgelerin elektron mikroskobu incelemesinde, normalden farklı fibröz uzun aralıklı (fibrous long-spacing, FLS) kollajen gözlenir. FLS kollajeninin periyodu 100-110 nm olup, normal kollajenden (60-64 nm) belirgin şekilde daha uzundur. Bu FLS kollajeni ilerlemiş keratokonusta da gözlenmiştir ve bu iki hastalık arasındaki ilişkiyi destekleyen bir bulgudur 4).
Kornea incelmesinin biyokimyasal mekanizması
Section titled “Kornea incelmesinin biyokimyasal mekanizması”Keratokonus ve ilişkili kornea ektazilerinde, matriks metalloproteinaz (MMP) aktivitesinde artış ve endojen inhibitörlerinde (TIMP) azalma bildirilmiştir ve stromal kollajen yıkımının artmasının incelmeye katkıda bulunduğu düşünülmektedir 2). Ayrıca gözyaşında IL-6, TNF-α ve MMP-9 gibi inflamatuar mediatörlerin arttığı bildirilmiş olup, daha önce “noninflamatuar” olarak kabul edilen PMD ve keratokonusta hafif inflamatuar unsurların rol oynayabileceği belirtilmiştir 2). Bu bulgular, göz ovuşturma ve alerjik uyarının hastalığın kötüleşmesine katkıda bulunduğu klinik gözlemlerle de uyumludur. İnflamatuar sitokinlerin artışına bağlı keratosit apoptozu, stromanın hücreselliğini azaltır ve kollajen liflerinin metabolizmasını ve yeniden yapılanmasını bozarak korneanın mekanik dayanıklılığının azalmasına ve incelmesine yol açabilir.
Kornea çıkıntısının mekanik mekanizması
Section titled “Kornea çıkıntısının mekanik mekanizması”Kornea stromasındaki kollajen yapı anormalliği nedeniyle kornea zayıflar ve normal göz içi basıncına dayanamayarak alt periferik bölge incelir ve çıkıntı yapar. Maksimum çıkıntının incelmiş bölgenin üzerinde yer almasının nedeni, incelmiş bölgenin yapısal olarak ince olmasına karşın, göz içi basıncından kaynaklanan gerilimin incelmiş bölge ile normal kornea arasındaki sınırda maksimuma ulaşmasıdır. Bu mekanik mekanizma ile kornea kesitinde incelmiş bant ve yukarı doğru şişkinliğin birleşimi, “bira göbeği” (beer belly) olarak tanımlanan benzersiz bir morfoloji oluşturur. Bu morfolojik anormallik, güçlü bir kuraldışı astigmatizmaya neden olur ve normal gözlüklerle yeterli düzeltme sağlanamayan görme bozukluğunun doğrudan nedenidir.
Akut ödem ve perforasyon
Section titled “Akut ödem ve perforasyon”Kornea incelmesi ileri derecede ilerlediğinde Descemet membranı yırtılır ve ön kamara sıvısı stromaya sızarak akut ödem oluşturur. Ueji ve arkadaşlarının raporuna göre, PMD’de kornea perforasyonu için ortalama yaş 50.1±14.6 yıl olup, keratokonustaki 36.9±16.3 yıldan daha geçtir 1). Bu, PMD’nin ilerlemesinin keratokonustan daha yavaş olduğunu yansıtır. Perforasyon nispeten nadir bir komplikasyondur, ancak oluştuğunda ciddi görme bozukluğuna yol açar; bu nedenle ilerlemenin izlenmesi, göz ovuşturmaktan kaçınma önerisi ve alerji kontrolü önemlidir. PMD’de incelmiş bant periferde yer aldığından, travma, göz içi basınç dalgalanmaları ve aşırı göz ovuşturma gibi lokal mekanik stresler perforasyonu tetikleyebilir. Perforasyonu önlemek için düzenli yarık lamba muayenesi ve kornea kalınlığı ölçümü ile izleme ve kornea kalınlığı belirgin şekilde azalmış vakalarda erken cerrahi müdahalenin değerlendirilmesi önerilir.
7. Güncel araştırmalar ve gelecek perspektifleri
Section titled “7. Güncel araştırmalar ve gelecek perspektifleri”PMD ile ilgili son araştırma konuları şunları içerir:
- Biyomekanik erken tespit: Ocular Response Analyzer ve Corvis ST gibi cihazlarla corneal hysteresis, corneal resistance factor ve dinamik Scheimpflug analizi kullanılarak PMD’nin başlangıç öncesi evresinde (biyomekanik evre) tespiti 2)
- Kişiselleştirilmiş CXL: Hafezi ve ark. tarafından geliştirilen sub400 protokolü, 400 µm’den ince ultra ince kornealar için kornea kalınlığına göre ışınlama süresini ayarlayan bir tekniktir ve geleneksel CXL’de kontrendike olan ilerlemiş vakalarda uygulanabilirliğini göstermiştir 9)
- Topografi kılavuzlu PRK ve CXL’nin eşzamanlı kombinasyonu: Stojanovic ve ark. tarafından bildirilen çalışmada, PMD ve keratokonus için görsel işlev iyileştirmesi ve ilerlemenin durdurulması aynı anda sağlanmıştır 6)
- Korneal allogreft ICRS (CAIRS): İnsan kornea dokusu parçaları kullanılan CAIRS ve CXL kombinasyonu rapor edilmiş olup, keratokonus üzerine yapılan bir pilot çalışmada segment kaynaklı komplikasyon gözlenmemiştir 11)
- Genetik test: TGFBI geni dahil 75 gen ve 2000’den fazla mutasyonu tarayan genetik test, korneal ektazi risk değerlendirmesi için kullanıma sunulmaktadır 2)
- Yapay zeka analizi ve epitel kalınlık haritası: AS-OCT epitel kalınlık haritası ve ön segment görüntülerinin yapay zeka analizi ile başlangıç öncesi evrede korneal ektazinin otomatik tespiti için çalışmalar devam etmektedir 2). Epitel, alttaki stromal düzensizliği telafi etmek için kalınlığını değiştirdiğinden, epitel kalınlık paterni stromal ektazinin erken bir belirteci olarak dikkat çekmektedir
8. Kaynaklar
Section titled “8. Kaynaklar”- Ueji N, Kato K, Yonekawa Y, et al. Case of unilateral pellucid marginal corneal degeneration progressing to corneal perforation with keratoconus in contralateral eye. Am J Ophthalmol Case Rep. 2022;25:101293.
- American Academy of Ophthalmology Cornea/External Disease Panel. Corneal Ectasia Preferred Practice Pattern. San Francisco, CA: American Academy of Ophthalmology; 2023.
- Belin MW, Asota IM, Ambrosio R Jr, Khachikian SS. What’s in a name: keratoconus, pellucid marginal degeneration, and related thinning disorders. Am J Ophthalmol. 2011;152(2):157-162.
- Jinabhai A, Radhakrishnan H, O’Donnell C. Pellucid corneal marginal degeneration: a review. Cont Lens Anterior Eye. 2011;34(2):56-63.
- Walker RN, Khachikian SS, Belin MW. Scheimpflug photographic diagnosis of pellucid marginal degeneration. Cornea. 2008;27(8):963-966.
- Stojanovic A, Zhang J, Chen X, et al. Topography-guided transepithelial surface ablation followed by corneal collagen cross-linking performed in a single combined procedure for the treatment of keratoconus and pellucid marginal degeneration. J Refract Surg. 2010;26(2):145-152.
- Raiskup-Wolf F, Hoyer A, Spoerl E, Pillunat LE. Collagen crosslinking with riboflavin and ultraviolet-A light in keratoconus: long-term results. J Cataract Refract Surg. 2008;34(5):796-801.
- Hersh PS, Stulting RD, Muller D, et al. United States multicenter clinical trial of corneal collagen crosslinking for keratoconus treatment. Ophthalmology. 2017;124(9):1259-1270.
- Hafezi F, Kling S, Gilardoni F, et al. Individualized corneal cross-linking with riboflavin and UV-A in ultrathin corneas: the sub400 protocol. Am J Ophthalmol. 2021;224:133-142.
- Godefrooij DA, Gans R, Imhof SM, Wisse RP. Nationwide reduction in the number of corneal transplantations for keratoconus following the implementation of cross-linking. Acta Ophthalmol. 2016;94(7):675-678.
- Jacob S, Patel SR, Agarwal A, et al. Corneal allogenic intrastromal ring segments (CAIRS) combined with corneal cross-linking for keratoconus. J Refract Surg. 2018;34(5):296-303.
- Sykakis E, Karim R, Evans JR, et al. Corneal collagen cross-linking for treating keratoconus. Cochrane Database Syst Rev. 2015;(3):CD010621.
