是一種非炎症性、非遺傳性的角膜擴張症 ,特徵為下方周邊角膜 帶狀變薄和前凸。
角膜 輪部上方1-2毫米處,從4點到8點方向存在帶狀變薄區域。被認為是圓錐角膜 的類緣疾病,10%合併圓錐角膜 ,13%合併球形角膜 。
角膜地形圖 顯示特徵性的「蟹爪」和「蝴蝶結」圖案。主要症狀是由高度逆規散光 引起的不規則散光 ,透過硬式隱形眼鏡或鞏膜 鏡矯正。
角膜交聯術 (CXL )和角膜內環 (ICRS )旨在阻止進展並改善視功能。LASIK 等屈光 矯正手術是禁忌的。
透明性角膜 邊緣變性(pellucid marginal corneal degeneration: PMD, PMCD )是一種非發炎性、非遺傳性角膜擴張症 ,以雙眼下方周邊角膜 變薄為特徵。「pellucid」意為「透明的」,源於變薄區域保持透明。變薄區域無血管侵入或混濁等發炎表現,被認為是圓錐角膜 的類緣疾病。
PMD是僅次於圓錐角膜 的第二常見的非發炎性角膜 變薄疾病。然而,由於常被誤診為圓錐角膜 ,實際盛行率可能被低估3) 。PMD通常在30-50歲發病2,4) ,比圓錐角膜 稍晚,男性較常見。
由於PMD與圓錐角膜 在臨床和組織學上有很多共同點,一些觀點認為圓錐角膜 和PMD是一個連續譜3) 。約10%的PMD病例合併圓錐角膜 ,約13%合併球形角膜 4) 。有報告同一患者同時存在PMD和圓錐角膜 ;日本全國調查發現,27例單眼PMD中,17例對側眼有圓錐角膜 或疑似圓錐角膜 1) 。
角膜 形態異常的進展導致嚴重的不規則散光 和視力 障礙。有強烈的逆規散光 傾向,眼鏡或隱形眼鏡矯正通常比圓錐角膜 更困難4) 。
PMD常有較長的無症狀期;在20多歲的健康檢查或配鏡時經常被漏診,直到30-40歲逆規散光 加重、矯正視力 不佳時才首次確診。與圓錐角膜 因急性水腫或明顯的角膜 中央突出而相對早期發現不同,PMD以「治不好的逆規散光 」、「逐漸不合適的眼鏡」形式緩慢進展。流行病學數據有限,沒有像圓錐角膜 那樣進行國家層面的大規模研究,因此真實盛行率未知。也有在屈光 手術術前檢查中偶然發現PMD的病例,推測潛在患者不在少數。
Q
與圓錐角膜的區別是什麼?
A
PMD表現為角膜 下方周邊部變薄,最大突出位於變薄區域的上方(中央側)。而圓錐角膜 表現為角膜 中央至旁中央部變薄,變薄區域與突出部位一致。PMD無Fleischer環或Vogt條紋,傾向於高度逆規性散光 。此外,PMD多在30歲以後發病,而圓錐角膜 在青春期發病。
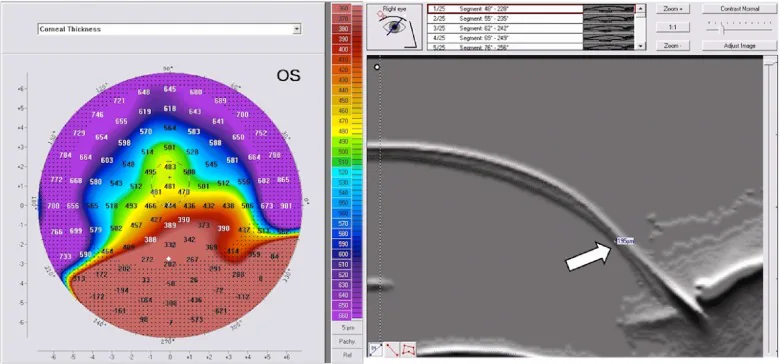
Pellucid角膜邊緣變性的角膜厚度圖和Scheimpflug斷面影像,顯示下方周邊角膜變薄 Sinjab MM, et al. Pellucid-like keratoconus. F1000Res. 2012. Figure 2. PM
CI D: PMC3752625. License: CC BY.
PMD中角膜 厚度測量顯示的下方角膜 變薄:A為厚度圖上的Bell徵,B為Scheimpflug影像上的變薄部位(白色箭頭)。這與本文「2. 主要症狀與臨床所見」部分討論的下方角膜 變薄相對應。
進行性視力 下降 :高度不規則散光 導致即使眼鏡矯正也無法獲得足夠視力 影像扭曲 :由於角膜 形狀異常急性疼痛和視力 下降 :罕見情況下發生急性角膜水腫 時出現屈光 不穩定視力 仍不穩定2)
所見 特徵 帶狀變薄 4至8點鐘方向,距角膜緣 1–2 mm,寬度1–2 mm 前方突出 位於變薄區域的上方(中央側),呈啤酒肚樣 角膜 透明度變薄區域透明,無血管侵入或混濁 上皮 始終保持完整(無脂質沉積)
變薄區域位於角膜緣 上方1–2毫米處,呈1–2毫米寬的帶狀,從4點方向延伸至8點方向。厚度可減少至正常角膜 厚度的20%。最大突出部位位於變薄區域的上方,角膜 橫截面呈「啤酒肚」樣外觀2) 。這種突出導致高達20D的高度逆規性散光 ,使視力 矯正極為困難。
PMD中無Fleischer環、圓錐頂點或頂點疤痕。變薄區域與角膜緣 之間的角膜 健康,變薄區域始終有上皮覆蓋。與Terrien角膜邊緣變性 不同,PMD無脂質沉積。
角膜地形圖 顯示以下特徵性模式。
蟹爪(crab claw)模式 :角膜 屈光 力圖上下方新月形陡峭化的特徵性表現蝴蝶結(butterfly)模式 :中央區域垂直方向的冷色蝴蝶結樣模式接吻鴿/接吻鳥(kissing doves / kissing birds)模式 :Scheimpflug成像中觀察到的外觀5) 逆規性散光 和大曲率半徑 :角膜 曲率計顯示強逆規性散光 ,但與圓錐角膜 不同,角膜 曲率半徑反而增大
然而,蟹爪樣表現也可見於進展期圓錐角膜 ,並非PMD特有3) 。角膜 高度圖上,前表面和後表面均可見下方周邊部隆起,角膜 厚度圖上最薄點位於隆起部稍下方。
Placido盤式角膜地形圖 僅能評估約60%的角膜 表面,對於周邊部病變PMD的評估存在局限性2) 。Scheimpflug成像或裂隙掃描斷層成像(Pentacam、Orbscan等)可評估角膜 前後表面及全角膜 厚度圖,對PMD的診斷及其與圓錐角膜 的鑑別診斷具有價值2,5) 。特別是後表面高度圖下方周邊部的膨隆以及最薄點位於膨隆部下方的表現,是診斷PMD的重要依據。PMD與圓錐角膜 的鑑別在臨床上很重要,但存在過渡病例,僅憑影像學表現難以確診,需要縱向觀察病情進展。
角膜擴張症 的進展評估採用整合於Scheimpflug成像設備的ABCD分類。該分類由四個要素組成:前表面曲率半徑(A)、後表面曲率半徑(B)、最小角膜 厚度(C)和最佳矯正遠視 力(D),用於追蹤隨時間的變化2) 。
PMD的病因尚不明確,但被認為是由角膜基質 膠原蛋白結構異常導致的脆弱化與眼壓 引起的力學應力共同作用,導致角膜 變薄和突出。組織學上,基質膠原蛋白出現異常的纖維狀長週期(FLS)膠原蛋白(週期100-110 nm),而正常膠原蛋白週期為60-64 nm。這種結構異常可能與角膜 脆弱化有關4) 。
近年來,有觀點認為PMD和圓錐角膜 屬於同一疾病譜。Belin等人提出「邊緣性透明變性不是一種獨立的疾病,而應被視為下方偏移的圓錐角膜 的一種表型」3) 。這一觀點基於大量同一患者同時存在PMD和圓錐角膜 的病例報告、共同的組織學和膠原蛋白異常,以及影像學表現的連續性。另一方面,在臨床實務中,由於變薄部位、突出部位、發病年齡和進展速度的差異,通常仍將PMD作為獨立表型處理。
過敏體質 :約30%的患者合併異位性皮膚炎或氣喘等過敏性疾病。日本的一項全國調查顯示22.2%的患者有過敏體質1) 。揉眼 :被認為是角膜擴張症 的加重因素,建議使用肥大細胞穩定劑控制過敏2) 。過敏與穿孔風險 :過敏體質被認為是急性水腫和角膜 穿孔的風險因素1,2) 。Ueji等人報告,在18例因PMD導致角膜 穿孔的病例中,6例有過敏體質或揉眼習慣1) 。阻塞性睡眠呼吸中止症候群和高BMI :與角膜擴張症 總體相關2) 。遺傳因素 :PMD單獨被認為非遺傳性,但近年來有報告稱與角膜 膠原相關基因(如KERA基因突變)存在關聯。
Q
過敏會使PMD惡化嗎?
A
過敏體質被認為是急性水腫和角膜 穿孔的危險因子。圓錐角膜 中已知過敏體質是急性水腫的危險因子,PMD中也有類似的關聯。過敏引起的眼睛癢可能誘發揉眼,增加角膜 的機械應力。早期抗過敏治療和加用肥大細胞穩定劑可能有效預防穿孔。
PMD的診斷基於裂隙燈 檢查和病史,並透過角膜地形圖 確認。如果發現下方周邊角膜 帶狀變薄(透明、非發炎性、無脂質沉積)且變薄區域上方突出,則懷疑PMD。
屈光 檢查通常表現為高度逆規散光 和不規則散光 ,難以用一般眼鏡矯正4) 。視網膜 檢影可見剪刀樣反射2) 。輕症病例易被誤診為單純逆規散光 ,因此角膜地形圖 詳細檢查很重要。
角膜 曲率計散光 。與圓錐角膜 不同,角膜 曲率半徑往往較大。角膜地形圖 (Placido盤型)2) 。Scheimpflug斷層掃描 :透過前後表面高度圖和全角膜 厚度圖,有助於PMD的診斷和進展評估2,5) 。裂隙掃描斷層掃描(Orbscan) :可檢測接吻鴿圖案等特徵性表現。眼前段OCT (AS-OCT ) :透過高解析度橫斷面影像評估角膜 厚度圖和上皮厚度圖,顯示基質變薄和上皮重塑2) 。角膜生物力學 測量角膜 滯後量和角膜 阻力因子降低有望用於早期檢測2) 。
根據2015年國際共識,進展定義為以下至少兩項惡化:前表面角膜 曲率變陡、後表面角膜 曲率變陡、變薄(或從周邊到最薄點的角膜 厚度變化率增加)2) 。
圓錐角膜
變薄部位 :角膜 中央至旁中央。PMD位於下方周邊。
突出部位 :與變薄部位一致。PMD中位於變薄部位上方。
特徵性發現 :可見Fleischer環、Vogt線條。PMD中未見。
發病年齡 :青春期。PMD在30歲以後。
Terrien角膜邊緣變性
炎症表現 :伴有脂質沉積、假性翼狀胬肉、表層血管侵入。PMD中未見。
變薄模式 :多見於上方,但可發生於任何方向。PMD位於下方。
邊緣形狀 :貝殼狀扇形邊緣。
Mooren角膜潰瘍
炎症 :前眼部炎症嚴重,呈現角膜潰瘍 。
上皮損傷 :可見角膜上皮 損傷。PMD中上皮保持完整。
單純順規性散光
角膜 厚度
角膜地形圖
在屈光 手術的術前評估中,若誤將輕度PMD診斷為「單純逆規散光 」並進行手術,則有術後誘發角膜擴張症 (keratectasia)的風險2,4) 。術前篩檢中可靠地排除PMD最為重要。特別是對於年輕、高度逆規散光 、處方不穩定、或提示角膜 下方變薄的表現(下方I/S不對稱、下方高度升高、下方角膜 厚度減少)的患者,應排除LASIK 、SMILE 和PRK的適應症。
建議結合角膜 厚度、角膜 形態和生物力學評估,基於多種檢查手段的一致結果進行診斷。僅憑單一檢查的暫時性異常值容易導致偽陽性,因此建議進行兩次或以上檢查以追蹤隨時間的變化。
大多數PMD病例通過非手術方式管理。據報導,約88%為非手術管理,其中36%通過眼鏡矯正,52%通過隱形眼鏡矯正4) 。隨著逆規散光 的增加,眼鏡矯正相對較早達到極限。
鏡片類型 特點 硬性透氣性角膜 接觸鏡(RGP ) 對中和不規則散光 最有效,但因下方偏心易左右移位,驗配困難 鞏膜 鏡不接觸角膜 ,覆蓋角膜 ,穩定性極佳;進展期PMD的首選2) 混合鏡片 RGP 中央+軟性裙邊。佩戴舒適度良好2) 背馱式 在軟性CL上放置RGP ,兼顧舒適度和矯正力2)
在PMD中,由於突出部位位於角膜 周邊部,一般RGP鏡片 容易左右偏移,比圓錐角膜 更難驗配。有時會嘗試大直徑RGP 或上眼瞼支撐鏡片,但可能導致刺激感或鏡片脫落。鞏膜 鏡片完全不接觸角膜 表面,因此對進展期或前表面形態不規則的病例有效2) 。鏡片與鏡片後方的淚液層在光學上起到「液體鏡片」的作用,中和角膜 的不規則散光 。雖然需要時間適應配戴,但容易同時獲得良好的矯正視力 和配戴舒適感,近年來正逐漸成為角膜擴張症 的首選方案。
角膜交聯術 是一種通過在角膜基質 膠原纖維之間形成交聯,增加角膜生物力學 剛度,從而抑制擴張症進展的治療方法。美國FDA已批准用於14-65歲進展性圓錐角膜 和角膜擴張症 術後患者2) ,也應用於PMD。
標準方案(德勒斯登方案) :去除角膜上皮 後,每2分鐘滴用0.1%核黃素滴眼液,持續30分鐘,然後用波長370 nm的UV-A以3 mW/cm²的強度照射30分鐘(總能量5.4 J/cm²)2,7) 加速方案 :已開發出將UV-A強度提高到9-30 mW/cm²並縮短照射時間的方法2) 效果 :早期和進展期病例均報告擴張症進展停止,並觀察到1.0-2.5 D的角膜 平坦化2,7,8) 。長期追蹤確認CXL 後10年穩定性7) 禁忌症 :UV照射時角膜基質 厚度小於400 µm的病例因內皮損傷風險而禁忌2) 。但也有針對超薄角膜 的個體化方案(sub400方案)的報導9) 併發症 :點狀角膜 炎、角膜 紋、畏光 、乾眼、感染性角膜 炎、無菌性浸潤、角膜 霧狀混濁、上皮缺損 遷延、角膜水腫 等2) Stojanovic等人 報導了局部PRK(地形圖引導經上皮消融)與CXL 一期聯合手術對PMD和圓錐角膜 的有效性6)
在荷蘭,導入CXL 後,圓錐角膜 的角膜移植 數量減少了約25% 10) 。Cochrane回顧也得出結論,CXL 能有效抑制角膜擴張 的進展 12) 。對於PMD,雖然不像圓錐角膜 那樣有大規模RCT的累積,但多個病例報告顯示角膜 形狀穩定和最大角膜 曲率值變平。因此,對於確認進展的年輕至中年患者,建議早期導入CXL 。
角膜內環節 (ICRS ,商品名:Intacs 、Ferrara等)是一種將半圓形PMMA環插入角膜基質 以平坦角膜 形狀並減少不規則散光 的手術方法。
適應症 :中央透明且角膜 厚度≥400 µm的擴張性角膜 2) 效果 :改善裸眼視力 和矯正視力 ,減少高階像差,便於隱形眼鏡佩戴 2) 技術 :飛秒雷射 輔助製作通道是主流方法,效果與手工技術相當 2) 與CXL 聯合 :許多報告在ICRS 植入後添加CXL 以增強抑制進展的效果
近年來,還開發了使用同種角膜 組織的CAIRS (角膜 同種異體角膜內環節 )。在一項針對24隻圓錐角膜 眼的初步研究中,聯合CAIRS 和CXL 後未觀察到與環節相關的併發症 11) 。ICRS 主要是為了改善視功能而改變角膜 形狀的手段,其抑制進展的效果有限。因此,對於確認進展的病例,採取與CXL 順序聯合的策略以獲得兩者的優勢。
當無法佩戴隱形眼鏡或視力 矯正不足時考慮手術。PMD中,突出部位位於角膜 周邊部,因此手術比常規的中央角膜移植 更複雜。
周邊新月形板層角膜移植術 :將新月形板層移植物插入變薄區域的手術。排斥反應風險相對較低,是近年來最受歡迎的方法之一。如果視力 不足,建議進行兩步手術,隨後進行中央穿透性角膜移植術 。深層前板層角膜移植術 (DALK ) :僅替換角膜基質 而保留宿主內皮的手術。沒有內皮排斥反應的風險,術後內皮細胞丟失比穿透性移植慢,眼球破裂 風險也較低 2) 。穿透性角膜移植術 (PKP )新生血管 和排斥反應的風險。部分板層角膜移植術 :將菲薄區域半月形切除並以板層移植片置換的手術方式。若需進一步改善視功能,有時會採用兩階段方法,後期再行中央穿透性角膜移植 。
急性水腫的處理與圓錐角膜 類似,採用高滲透壓眼藥水、降眼壓 、氣體注入等保守治療。PMD因菲薄區域較薄,有穿孔風險,穿孔病例的管理在臨床上很重要。
Ueji等人報告了一例PMD導致角膜 穿孔的病例,透過治療性軟式隱形眼鏡(TCL)保守治療後穿孔閉合,術後1年矯正視力 改善至1.0。保守治療也使散光 減少約一半1) 。過去的文獻回顧中,PMD角膜 穿孔20眼中13眼嘗試了保守治療(組織黏合劑/TCL),其中4眼成功1) 。對於較小的穿孔,值得嘗試保守治療。
Q
我可以接受LASIK手術嗎?
A
PMD患者禁忌進行LASIK 等屈光 矯正手術。在角膜基質 菲薄化的狀態下切除角膜 會誘發角膜擴張症 (keratectasia)。PMD輕症病例有時會被誤診為常規逆規散光 ,因此在屈光 手術前篩查中可靠地排除PMD非常重要。
Q
我可以使用隱形眼鏡嗎?
A
許多PMD患者可透過隱形眼鏡管理,約88%的病例採用非手術管理。但由於下方突出,普通硬式隱形眼鏡容易移位,驗配比圓錐角膜 更困難。進展病例常選擇鞏膜 鏡或混合鏡片。隱形眼鏡透過中和不規則散光 改善視力 ,但不能抑制疾病進展,因此確認進展時應聯合角膜 交聯(CXL )。
PMD的組織病理學表現與圓錐角膜 相似。可見角膜基質 菲薄化,但上皮、內皮和Descemet膜正常。Bowman層 可見缺損 或斷裂(局部破壞),通常無脂質沉積。基質富含黏多醣。
變薄區域的電子顯微鏡觀察發現異常的纖維狀長週期(fibrous long-spacing, FLS)膠原蛋白。FLS膠原的週期為100-110 nm,明顯長於正常膠原蛋白(60-64 nm)。這種FLS膠原也在晚期圓錐角膜 中觀察到,支持兩種疾病之間的關聯4) 。
在圓錐角膜 及相關角膜擴張症 中,已報導基質金屬蛋白酶(MMP)活性升高及其內源性抑制劑(TIMP)降低,表明基質膠原降解增強導致變薄2) 。此外,淚液中IL-6、TNF -α、MMP-9等發炎介質增加,提示傳統上被認為是「非發炎性」的PMD和圓錐角膜 也可能存在低度發炎成分2) 。這些發現與揉眼和過敏刺激加重病情的臨床觀察一致。發炎細胞因子升高引起的角膜 細胞凋亡 降低了基質細胞密度,損害膠原纖維代謝和重塑,可能導致角膜 力學強度下降和變薄。
角膜基質 膠原結構異常導致角膜 脆弱,無法承受正常眼壓 ,從而引起下方周邊部變薄並突出。最大突出點位於最薄區域的上方,這是因為最薄區域本身結構薄弱,但眼壓 應力在最薄區域與正常角膜 交界處最大。由於這種力學機制,角膜 橫截面呈現「啤酒肚」樣獨特形態,結合了變薄帶和向上膨隆。這種形態異常導致嚴重的逆規散光 ,是普通眼鏡無法充分矯正的視功能障礙的直接原因。
當角膜 變薄嚴重進展時,Descemet膜破裂,房水 流入基質引起急性水腫。根據Ueji等人的報告,PMD角膜 穿孔的平均年齡為50.1±14.6歲,晚於圓錐角膜 的36.9±16.3歲1) 。這反映了PMD進展較圓錐角膜 緩慢。穿孔是相對罕見的併發症,但一旦發生會導致嚴重視功能障礙,因此監測進展、指導避免揉眼和控制過敏非常重要。在PMD中,由於變薄帶位於周邊部,外傷、眼壓 波動或過度揉眼等局部機械應力可能誘發穿孔。建議定期進行裂隙燈 檢查和角膜 厚度測量監測,對於角膜 厚度顯著降低的病例考慮早期手術介入,以預防穿孔。
近年來與PMD相關的研究主題包括以下內容:
生物力學早期檢測 :利用Ocular Response Analyzer和Corvis ST等設備,透過角膜 滯後量、角膜 阻力因子和動態Scheimpflug分析,在發病前階段(生物力學階段)檢測PMD 2) 個人化CXL :Hafezi等人提出的sub400方案針對厚度小於400 µm的超薄角膜 ,根據角膜 厚度調整照射時間,顯示出對傳統CXL 禁忌的進展病例的適用性 9) 地形圖引導PRK與CXL 同時聯合 :Stojanovic等人的報告顯示,對PMD和圓錐角膜 同時實現了視功能改善和進展抑制 6) 角膜 同種異體移植ICRS (CAIRS )角膜 組織片的CAIRS 與CXL 聯合應用已有報導,在圓錐角膜 的初步研究中未發現與片段相關的併發症 11) 基因檢測 :針對包括TGFBI在內的75個基因、2000多種突變進行篩檢的基因檢測,正逐步應用於角膜擴張症 風險評估 2) AI分析與上皮厚度圖 :利用AS-OCT 的上皮厚度圖及眼前段影像的AI分析,自動檢測發病前階段角膜擴張症 的嘗試正在推進 2) 。由於上皮透過改變厚度來補償下方基質的形態不規則,上皮厚度模式作為基質擴張症的早期標誌物備受關注
Ueji N, Kato K, Yonekawa Y, et al. Case of unilateral pellucid marginal corneal degeneration progressing to corneal perforation with keratoconus in contralateral eye. Am J Ophthalmol Case Rep. 2022;25:101293.
American Academy of Ophthalmology Cornea/External Disease Panel. Corneal Ectasia Preferred Practice Pattern. San Francisco, CA: American Academy of Ophthalmology; 2023.
Belin MW, Asota IM, Ambrosio R Jr, Khachikian SS. What’s in a name: keratoconus, pellucid marginal degeneration, and related thinning disorders. Am J Ophthalmol. 2011;152(2):157-162.
Jinabhai A, Radhakrishnan H, O’Donnell C. Pellucid corneal marginal degeneration: a review. Cont Lens Anterior Eye. 2011;34(2):56-63.
Walker RN, Khachikian SS, Belin MW. Scheimpflug photographic diagnosis of pellucid marginal degeneration. Cornea. 2008;27(8):963-966.
Stojanovic A, Zhang J, Chen X, et al. Topography-guided transepithelial surface ablation followed by corneal collagen cross-linking performed in a single combined procedure for the treatment of keratoconus and pellucid marginal degeneration. J Refract Surg. 2010;26(2):145-152.
Raiskup-Wolf F, Hoyer A, Spoerl E, Pillunat LE. Collagen crosslinking with riboflavin and ultraviolet-A light in keratoconus: long-term results. J Cataract Refract Surg. 2008;34(5):796-801.
Hersh PS, Stulting RD, Muller D, et al. United States multicenter clinical trial of corneal collagen crosslinking for keratoconus treatment. Ophthalmology. 2017;124(9):1259-1270.
Hafezi F, Kling S, Gilardoni F, et al. Individualized corneal cross-linking with riboflavin and UV-A in ultrathin corneas: the sub400 protocol. Am J Ophthalmol. 2021;224:133-142.
Godefrooij DA, Gans R, Imhof SM, Wisse RP . Nationwide reduction in the number of corneal transplantations for keratoconus following the implementation of cross-linking. Acta Ophthalmol. 2016;94(7):675-678.
Jacob S, Patel SR, Agarwal A, et al. Corneal allogenic intrastromal ring segments (CAIRS ) combined with corneal cross-linking for keratoconus. J Refract Surg. 2018;34(5):296-303.
Sykakis E, Karim R, Evans JR, et al. Corneal collagen cross-linking for treating keratoconus. Cochrane Database Syst Rev. 2015;(3):CD010621.