คำจำกัดความ : เป็นโรคกระจกตา โป่งพองชนิดหนึ่งที่เนื้อกระจกตา ส่วนกลางบางลงแบบค่อยเป็นค่อยไปในขณะที่ยังคงใส และยื่นออกมาด้านหน้าเป็นรูปกรวย ทำให้เกิดสายตาเอียง ผิดปกติอย่างรุนแรงและการมองเห็น ลดลง
ระบาดวิทยา : เริ่มมีอาการในวัยรุ่น ดำเนินต่อเนื่องในช่วงอายุ 20–30 ปี และมักหยุดหรือช้าลงเมื่ออายุประมาณ 30 ปี1) มักเป็นทั้งสองตาแต่มักมีความแตกต่างระหว่างตาซ้ายและขวา
สาเหตุ : เป็นโรคที่มีหลายปัจจัยร่วมกัน โดยปัจจัยทางพันธุกรรมและปัจจัยสิ่งแวดล้อม (โดยเฉพาะการขยี้ตา) มีส่วนเกี่ยวข้อง1, 6)
การวินิจฉัย : การตรวจพบความชันและการบางลงของผิวกระจกตา ทั้งด้านหน้าและด้านหลังด้วยการตรวจภูมิประเทศของกระจกตา (corneal topography) และการตรวจภาพตัดขวางกระจกตา (corneal tomography) เป็นพื้นฐานสำคัญ1, 9)
การรักษา : ในกรณีที่ลุกลาม การทำ corneal cross-linking (CXL ) เป็นทางเลือกแรกในการยับยั้งการลุกลาม1, 2, 4) การแก้ไขสายตาใช้คอนแทคเลนส์ชนิดแข็งและคอนแทคเลนส์ชนิดสเคลอรัล
การพยากรณ์โรค : การตรวจพบตั้งแต่ระยะแรกและการทำ CXL ตั้งแต่เนิ่นๆ สามารถช่วยรักษาระดับการมองเห็น ที่มีประโยชน์ได้ตลอดชีวิต1, 2)
โรคกระจกตา ทรงกรวย (keratoconus) เป็นโรคกระจกตา โป่งพองที่พบได้บ่อยที่สุด ส่วนกลางหรือกึ่งกลางของกระจกตา จะบางลงและชันขึ้นอย่างต่อเนื่อง ทำให้กระจกตา ยื่นออกมาด้านหน้าเป็นรูปกรวย ความอ่อนแอของเนื้อกระจกตา ทำให้รูปทรงกระจกตา บิดเบี้ยว ส่งผลให้เกิดสายตาเอียง ผิดปกติระดับสูงและการมองเห็น บกพร่อง1)
การเริ่มเกิดโรคมักอยู่ในช่วงวัยรุ่น ดำเนินต่อเนื่องในช่วงอายุ 20–30 ปี และมักจะหยุดหรือช้าลงเมื่ออายุประมาณ 30 ปี1) การเกิดโรคก่อนอายุ 10 ปีพบได้น้อย อายุที่วินิจฉัยโดยทั่วไปคือ 15–30 ปี เพศชายมีแนวโน้มพบมากกว่าเล็กน้อย
ความชุกของโรคแตกต่างกันอย่างมากตามภูมิภาคและเชื้อชาติ ในเนเธอร์แลนด์พบ 1:375 (ประมาณ 265 ต่อ 100,000 คน) ในประชากรอายุ 20 ปีของออสเตรเลียพบ 1:84 และในบางกลุ่มชาติพันธุ์สูงถึง 1:452) การใช้เครื่องตรวจภูมิประเทศกระจกตา ที่แพร่หลายในช่วงไม่กี่ปีที่ผ่านมาช่วยให้ตรวจพบผู้ป่วยระยะเริ่มต้นได้มากขึ้น ส่งผลให้จำนวนผู้วินิจฉัยและความชุกเพิ่มขึ้น1) ประวัติครอบครัวพบใน 14% ของผู้เข้าร่วม 1,209 คนในการศึกษา CLEK และรายงานความชุกในญาติสายตรงระดับแรกอยู่ที่ 20.5%1)
โรคกระจกตา ทรงกรวยส่วนใหญ่เป็นทั้งสองตา แต่มักมีความรุนแรงแตกต่างกันระหว่างตาทั้งสองข้าง และบางกรณีอาจดูเหมือนมีอาการทางคลินิกเพียงข้างเดียว อย่างไรก็ตาม การตรวจภูมิประเทศกระจกตา อย่างละเอียดมักตรวจพบความผิดปกติเล็กน้อยในตาอีกข้างหนึ่ง มีรายงานกรณีที่ไม่สอดคล้องกันในฝาแฝดแท้ ซึ่งบ่งชี้ว่าปัจจัยด้านสิ่งแวดล้อมมีบทบาทสำคัญในการเกิดโรค นอกเหนือจากปัจจัยทางพันธุกรรม6) ส่วนใหญ่เป็นกรณีที่เกิดขึ้นโดยไม่มีการถ่ายทอดทางพันธุกรรม แต่ก็พบการเกิดในครอบครัวได้เช่นกัน1)
ผู้ป่วยส่วนใหญ่มักมีโรคร่วมเกี่ยวกับภูมิแพ้ (หอบหืด ไข้ละอองฟาง กลาก) เยื่อบุตาอักเสบจากภูมิแพ้ และนิสัยการขยี้ตา ซึ่งเชื่อว่าเกี่ยวข้องกับการอักเสบเรื้อรังและความเครียดเชิงกลซ้ำๆ นอกจากนี้ยังมีรายงานการเกิดร่วมกับโรคเนื้อเยื่อเกี่ยวพัน เช่น ดาวน์ซินโดรม เอลเลอร์ส-ดานลอสซินโดรม โรคกระดูกเปราะ มาร์ฟานซินโดรม รวมถึงโรคตาบอดกลางคืน แต่กำเนิดชนิด Leber และจอประสาทตา เสื่อม1)
ความชุกของโรคกระจกตา ทรงกรวยกำลังได้รับการปรับเพิ่มขึ้นตามการแพร่หลายของการตรวจภาพตัดขวางกระจกตา แต่ก่อนเคยเชื่อว่าพบได้ประมาณ 5 คนต่อประชากร 10,000 คน แต่ปัจจุบันรับรู้ว่าเป็นโรคที่พบบ่อยขึ้น1) ซึ่งตีความว่าเป็นผลจากการพัฒนาความไวในการตรวจจับผู้ป่วยที่ไม่สมบูรณ์แบบหรือระยะเริ่มแรก มากกว่าอัตราการเกิดโรคที่เพิ่มขึ้นจริง หลังจากปี 2000 เป็นต้นมา เมื่อความต้องการคัดกรองการผ่าตัดแก้ไขสายตากระจกตา เพิ่มขึ้น เครื่อง Scheimpflug และ OCT segment หน้าได้นำการวิเคราะห์กระจกตา แบบสามมิติมาใช้ในการปฏิบัติงานทางคลินิกประจำวัน ทำให้สามารถตรวจพบผู้ป่วยระยะเริ่มต้นที่ไม่มีอาการหรือมีอาการเล็กน้อยได้ แทนที่จะวินิจฉัยได้เฉพาะผู้ป่วยระดับปานกลางขึ้นไปที่มีอาการปรากฏแล้ว
ในขณะที่โรคกระจกตา ทรงกรวยปกติมีการโป่งพองของผิวหน้าของกระจกตา เป็นหลัก โรคกระจกตา ทรงกรวยด้านหลัง (posterior keratoconus) เป็นโรคกระจกตา โป่งพองที่พบได้ยาก ไม่ดำเนินไป มีลักษณะเด่นคือความโค้งของผิวหลังกระจกตา เพิ่มขึ้น ส่วนใหญ่เป็นมาแต่กำเนิด เกิดในตาข้างเดียว เกิดขึ้นแบบประปราย และมักดำเนินไปโดยไม่มีอาการ ไม่ทำให้การมองเห็น ลดลง ทางคลินิก การแยกโรคจากกระจกตา ทรงกรวยปกติเป็นสิ่งสำคัญ การติดตามและการแก้ไขสายตาเมื่อจำเป็นเป็นหัวใจหลัก
Q
โรคกระจกตาทรงกรวยเกิดขึ้นทั้งสองตาหรือไม่؟
A
โรคกระจกตา ทรงกรวยส่วนใหญ่เกิดในทั้งสองตา แต่มักมีความแตกต่างระหว่างตาทั้งสองข้าง แม้ในกรณีที่ดูเหมือนเกิดเพียงตาเดียว เมื่อตรวจด้วยเครื่องวัดภูมิประเทศกระจกตา หรือภาพตัดขวางกระจกตา ที่แม่นยำ มักตรวจพบความผิดปกติเล็กน้อยในตาอีกข้างได้เช่นกัน มีรายงานผู้ป่วยฝาแฝดแท้ที่เกิดโรคเพียงคนเดียว แสดงให้เห็นว่านอกจากปัจจัยทางพันธุกรรมแล้ว ปัจจัยแวดล้อมเช่นการขยี้ตามีบทบาทสำคัญในการเกิดโรค
ระยะเริ่มแรกมีลักษณะเด่นคือการเปลี่ยนค่าแว่นตาบ่อยครั้งในช่วงเวลาสั้นๆ และไม่สามารถรับสายตาที่แก้ไขแล้วได้อย่างเพียงพอ1) เมื่อดำเนินโรคมากขึ้น สายตาสั้น และสายตาเอียง ไม่สม่ำเสมอจะเพิ่มขึ้น ทำให้ต้องเปลี่ยนวิธีการแก้ไขจากคอนแทคเลนส์ชนิดนิ่มเป็นเลนส์ทอริกและคอนแทคเลนส์ชนิดแข็ง การเพิ่มขึ้นอย่างชัดเจนของความคลาดเคลื่อนลำดับสูงของกระจกตา โดยเฉพาะความคลาดเคลื่อนแบบดาวหางแนวตั้ง ทำให้ผู้ป่วยบางรายมองเห็นแหล่งกำเนิดแสงจุดหรือเป้าสายตาเป็นเส้นหางยาวลงมาด้านล่างเหมือนดาวหาง
ความบกพร่องทางการมองเห็น ในหลายกรณีเป็นอาการแสดงระยะท้ายที่ปรากฏช้ากว่าการเปลี่ยนแปลงทางสัณฐานวิทยา1) เมื่อเกิดภาวะกระจกตาบวมน้ำเฉียบพลัน จะมีอาการตามองเห็นลดลงอย่างฉับพลัน กลัวแสง ปวด และตาแดง
เมื่อตรวจด้วยกล้องจุลทรรศน์ชีวภาพชนิดร่องกราด (slit-lamp microscope) จะพบว่ากระจกตา ส่วนกลางบางลงและโป่งนูนไปข้างหน้า มีเทคนิคปฏิบัติที่สะดวกโดยการหมุนระบบสังเกตไปทางด้านหูของผู้ป่วยเกือบ 90 องศา ซึ่งจะช่วยให้เห็นการโป่งรูปกรวยของกระจกตา ในมุมด้านข้างได้ชัดเจนยิ่งขึ้น ในระยะแรก แม้กระทั่งตาข้างตรงข้ามที่ดูปกติ การตรวจด้วยเครื่องวัดภูมิประเทศของกระจกตา (corneal topography) อาจตรวจพบรูปแบบความโค้งชันเฉพาะจุดโดยทั่วไปได้
อาการระยะเริ่มแรก
สายตาเอียง ไม่สม่ำเสมอ (Irregular astigmatism)สายตาเอียง ระดับสูงที่แสดงลักษณะไม่เป็นมุมฉาก กล่าวคือ ผลรวมของแนวแกนหลักไม่เท่ากับ 180 องศา
ภาพสะท้อนแบบกรรไกร (Scissor reflex) : ในการตรวจหาค่าสายตาด้วยแสงสะท้อน (retinoscopy) ภาพสะท้อนสีแดงจะเคลื่อนที่ในลักษณะคล้ายกรรไกร
กระจกตา บางลง (Corneal thinning)1)
วงแหวน Fleischer (Fleischer ring) : การสะสมของเม็ดสีเหล็กเป็นวงกลมใต้เยื่อบุผิวที่ฐานของกรวย สามารถสังเกตเห็นได้ชัดเจนผ่านฟิลเตอร์สีน้ำเงินโคบอลต์1)
เส้น Vogt (Vogt striae) : เส้นเล็กๆ ในแนวตั้งที่พบในชั้นกลางถึงลึกของเนื้อกระจกตา มีลักษณะเฉพาะคือหายไปชั่วคราวเมื่อกดลูกตาเบาๆ และกลับมาปรากฏอีกครั้งเมื่อปล่อยแรงกด1)
อาการระยะหลัง
สัญญาณ Munson (Munson sign) : ลักษณะที่ไม่จำเพาะเจาะจง โดยเปลือกตาล่างจะโป่งนูนไปข้างหน้าเป็นรูปกรวยเมื่อผู้ป่วยมองลงล่าง1)
สัญญาณ Rizzuti (Rizzuti sign) : การส่องแสงร่องกราดจากด้านหาง ทำให้เกิดภาพจุดรวมแสงที่ขอบตาด้านจมูกผ่านยอดของกรวย
กระจกตา ขุ่น (Corneal opacification)กระจกตา ชั้นกลางถึงลึก
กระจกตาบวมน้ำ เฉียบพลัน (Acute corneal hydrops)กระจกตา ส่งผลให้กระจกตา บวมและขุ่นอย่างรุนแรง
เส้นประสาทกระจกตา เด่นชัดขึ้น (Prominent corneal nerves) : เมื่อเนื้อกระจกตา บางลง เส้นประสาทกระจกตา จะสามารถสังเกตเห็นได้เด่นชัดกว่าปกติ1)
ในเด็กและวัยรุ่น โรคดำเนินเร็วกว่าผู้ใหญ่ และมีสัดส่วนที่อยู่ในระยะลุกลาม ณ เวลาที่วินิจฉัยสูงกว่า Meyer และคณะติดตามเด็กและวัยรุ่น 148 ตาเป็นเวลาเฉลี่ย 2.9 ปี และพบการดำเนินโรคทางโทโมกราฟีใน 77.0%3) แม้แต่ในกลุ่มย่อยที่อายุต่ำกว่า 16 ปี 77.6% แสดงการดำเนินโรค3) นอกจากนี้ ในเด็กมักมีแนวโน้มที่กรวยจะก่อตัวใกล้ศูนย์กลางกระจกตา มากขึ้น รูปแบบการดำเนินโรคทั้งสองตาก็เป็นลักษณะเด่นเช่นกัน เมื่ออย่างน้อยหนึ่งตาเป็นกรณีรุนแรง (Amsler-Krumeich Stage III หรือ IV) อัตราการดำเนินโรคทั้งสองตาสูงถึง 73.9% ซึ่งสูงกว่าอย่างมีนัยสำคัญเมื่อเทียบกับ 36.8% ในกรณีที่ทั้งสองตาเป็นเล็กน้อย3) กรณีที่ตาข้างหนึ่งรุนแรงควรได้รับการเฝ้าระวังในฐานะเครื่องบ่งชี้การดำเนินโรคที่อาจแฝงอยู่ในตาอีกข้าง
ในรายที่ลุกลาม หาก Kmax ณ เวลาที่ตรวจครั้งแรก ≥55 D อัตราการลุกลามจะสูงกว่ากลุ่ม <55 D อย่างมีนัยสำคัญ (82% เทียบกับ 62%, p=0.02)3) กล่าวคือ ความรุนแรงของโรค ณ เวลาที่ตรวจครั้งแรกสามารถทำนายความเสี่ยงของการลุกลามในอนาคตได้ ในทางกลับกัน การวิเคราะห์พหุตัวแปรพบว่าอายุ เพศ โรคภูมิแพ้ และประวัติการขยี้ตาไม่ใช่ปัจจัยทำนายการลุกลามที่เป็นอิสระ3) ในการทบทวนวรรณกรรมอย่างเป็นระบบและการวิเคราะห์อภิมานขนาดใหญ่โดย Ferdi และคณะ ได้รวบรวมข้อมูลการดำเนินโรคตามธรรมชาติของดวงตา 11,529 ดวง ทำให้เข้าใจรูปแบบการลุกลามเมื่อไม่ได้รับการรักษาได้ลึกซึ้งยิ่งขึ้น13)
สาเหตุของโรคกระจกตา ทรงกรวยเป็นโรคที่มีหลายปัจจัยเกี่ยวข้องร่วมกัน ทั้งปัจจัยทางพันธุกรรม ปัจจัยทางชีวเคมี และปัจจัยทางชีวกลศาสตร์1) รูปแบบการถ่ายทอดทางพันธุกรรมที่เหมาะสมที่สุดคือแบบออโตโซมัลดอมมิแนนต์ที่มีการแสดงออกของลักษณะลดลง
ในด้านภูมิหลังทางพันธุกรรม มีรายงานความหลากหลายของยีนหลายชนิด ได้แก่ LOX (lysyl oxidase), CAST, VSX1, DOCK9, TGFBI และอื่นๆ1) ปัจจุบันมีการตรวจทางพันธุกรรมที่ได้รับการรับรองจาก FDA ซึ่งประเมินยีน 75 ชนิดและความแปรผันทางพันธุกรรมมากกว่า 2,000 รูปแบบ1)
การขยี้ตาและปัจจัยสิ่งแวดล้อม
การสะสมของการบาดเจ็บระดับจุลภาค : การกระตุ้นเชิงกลจากการขยี้ตาทำให้เกิดการบาดเจ็บระดับจุลภาคต่อเยื่อบุผิวและเนื้อกระจกตา เพิ่มกิจกรรมของโปรตีเอส และเร่งการสลายคอลลาเจน
บทบาทของโรคภูมิแพ้ : อาการคันตาจากโรคไข้ละอองฟาง ผิวหนังอักเสบภูมิแพ้ หอบหืด เยื่อบุตาอักเสบจากภูมิแพ้ ตามฤดูกาล และโรคอื่นๆ เป็นปัจจัยกระตุ้นให้ขยี้ตา1)
ท่าทางการนอน : การนอนตะแคงโดยให้ใบหน้าคว่ำลงบนหมอนอาจส่งผลให้เกิดแรงกดเชิงกลอย่างต่อเนื่อง6)
ปัจจัยทางพันธุกรรม
ประวัติครอบครัว : การศึกษา CLEK พบประวัติครอบครัวร้อยละ 141) ความชุกของโรคในญาติสายตรงสูงกว่าประชากรทั่วไปอย่างชัดเจน
ยีนที่เกี่ยวข้อง : ความหลากหลายของ LOX, CAST, VSX1, TGFBI และยีนอื่นๆ1)
รูปแบบการถ่ายทอด : แบบออโตโซมัลดอมมิแนนต์ที่มีการแสดงออกของลักษณะลดลงเป็นรูปแบบที่เหมาะสมที่สุด1)
โรคทางระบบที่เกี่ยวข้อง
ความผิดปกติของโครโมโซม : กลุ่มอาการดาวน์ เป็นโรคที่มีความสัมพันธ์มากที่สุด1)
โรคเนื้อเยื่อเกี่ยวพัน : กลุ่มอาการเอลเลอร์ส-ดานลอส กลุ่มอาการมาร์แฟน โรคกระดูกเปราะ1)
อื่นๆ : โรคตามัวแต่กำเนิดของ Leber, จอประสาทตา เสื่อม, กลุ่มอาการ Apert, กลุ่มอาการ Crouzon1)
เกี่ยวข้องกับพฤติกรรมการใช้ชีวิต : ภาวะหยุดหายใจขณะหลับจากการอุดกั้น, ค่า BMI สูง1)
การขยี้ตาเป็นปัจจัยแวดล้อมที่สำคัญที่สุดที่สามารถปรับเปลี่ยนได้1, 6) ในกรณีรายงานฝาแฝดไข่ใบเดียวกันที่มีความแตกต่างกันโดย Bitton และคณะ พบว่าฝาแฝดที่เกิดโรคมีนิสัยขยี้ตาอย่างแรงและมีท่านอนตะแคงซ้ายเป็นประจำเนื่องจากทำงานกะกลางคืน ในขณะที่ฝาแฝดที่ไม่เกิดโรคขยี้ตาเพียงเล็กน้อยและนอนหงาย6) กรณีนี้ซึ่งมีความแตกต่างของการเกิดโรคแม้จะมีพื้นฐานทางพันธุกรรมเดียวกัน แสดงให้เห็นถึงอิทธิพลชี้ขาดของปัจจัยแวดล้อม6)
สิ่งที่สำคัญที่สุดในการป้องกันการลุกลามของโรคตาเป็นรูปกรวยคือการไม่ขยี้ตา หากมีเยื่อบุตาอักเสบจากภูมิแพ้ หรือแพ้เกสรดอกไม้ ควรใช้ยาต้านภูมิแพ้เพื่อระงับอาการคันตาอย่างเพียงพอและลดการขยี้ตา ควรหลีกเลี่ยงท่านอนที่กดใบหน้าลงบนหมอนหรือแขนด้วย ผู้ที่มีประวัติครอบครัวเป็นโรคตาเป็นรูปกรวย หรือเด็กวัยรุ่นที่มีค่าสายตาเปลี่ยนแปลงในช่วงเวลาสั้นๆ ควรได้รับการตรวจคัดกรองด้วยเครื่องวัดภูมิประเทศกระจกตา แต่เนิ่นๆ
Q
การขยี้ตาทำให้เกิดโรคตาเป็นรูปกรวยหรือไม่?
A
การขยี้ตาเป็นปัจจัยแวดล้อมที่สำคัญอย่างยิ่งในการเกิดและการลุกลามของโรคตาเป็นรูปกรวย อย่างไรก็ตาม ปัจจัยทางพันธุกรรมก็เกี่ยวข้องด้วย และไม่ใช่ทุกคนที่ขยี้ตาจะเป็นโรคตาเป็นรูปกรวย การศึกษาในฝาแฝดไข่ใบเดียวกันพบว่าในฝาแฝดที่มียีนเดียวกันแต่นิสัยการขยี้ตาต่างกัน เฉพาะฝาแฝดที่ขยี้ตาอย่างแรงเท่านั้นที่เกิดโรค เมื่อได้รับการวินิจฉัยแล้ว คำแนะนำทั่วไปคือให้หยุดขยี้ตาโดยสิ้นเชิง
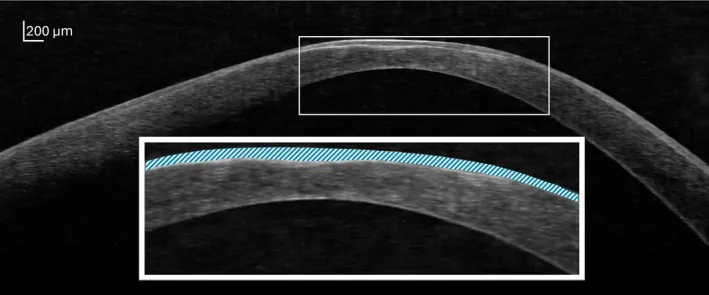
ภาพโรคตาเป็นรูปกรวย Gavin Swartz, Khyber Alam, Alex Gentle, Laura E Downie Impact of contact lens correction on wavefront aberrations and vision quality in keratoconus 2025 Oct 29 Ophthalmic Physiol Opt. 2025 Nov 29; 45(7):1811-1828 Figure 1. PM
CI D: PMC12682100. License: CC BY.
ภาพ OCT B-scan แสดงความแปรปรวนของความหนาชั้นเยื่อบุกระจกตา ในโรคตาเป็นรูปกรวย ในภาพขยายบริเวณที่อยู่ในกรอบสีขาว ชั้นเยื่อบุกระจกตา ถูกเน้นด้วยเส้นทแยงสีฟ้าอ่อน ในบริเวณนี้ ชั้นเยื่อบุจะหนาตัวขึ้นบนชั้นเนื้อกระจกตา ที่บางลง ทำให้รูปทรงของผิวหน้ากระจกตา เรียบขึ้น ในทางตรงกันข้าม ความโค้งของผิวหลังกระจกตา จะสังเกตเห็นว่าชันมาก
การวินิจฉัยโรคกระจกตา รูปกรวยอาศัยประวัติการเจ็บป่วยที่มีลักษณะเฉพาะ ผลการตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด และผลการตรวจด้วยวิธี corneal topography/tomography1) ตามอุดมคติแล้วควรวินิจฉัยให้ได้ตั้งแต่ระยะเริ่มแรกก่อนที่อาการจะปรากฏ แต่ยังไม่มีการตรวจคัดกรองที่ง่ายและคุ้มค่าที่เป็นมาตรฐาน1)
วิธีการตรวจ รายการประเมิน ผลการตรวจที่สำคัญ Corneal topography (Placido disc) ความโค้งด้านหน้า・SimK・SAI・SRI ความชันเฉพาะที่ด้านล่าง, การเพิ่มขึ้นของอัตราส่วน I/S Corneal tomography (Scheimpflug) ความสูงของผิวหน้าด้านหน้าและด้านหลัง・ความหนากระจกตา การโป่งเฉพาะจุดของผิวหน้าด้านหน้าและด้านหลัง, การบางแบบเยื้องศูนย์ OCT ส่วนหน้าดวงตาการทำแผนที่ความหนาของเยื่อบุผิว・ความหนากระจกตา เยื่อบุผิวบางในบริเวณที่บาง, หนาตัวเป็นรูปโดนัทรอบๆ การวิเคราะห์ความคลาดเคลื่อนของคลื่นแสง ความคลาดเคลื่อนลำดับสูง การเพิ่มขึ้นอย่างชัดเจนของความคลาดเคลื่อนแบบโคมาในแนวตั้ง การประเมินคุณสมบัติทางชีวกลศาสตร์ของกระจกตา CH・CRF・CBI・TBI ความแข็งแกร่งทางชีวกลศาสตร์ลดลง
การตรวจภูมิประเทศและวัดค่าความโค้งของกระจกตา : การประเมินทั้งผิวหน้าด้านหน้าและด้านหลังอย่างครอบคลุมมีความสำคัญต่อการวินิจฉัย1) อัตราส่วนความโค้งด้านล่าง/ด้านบน (I/S ratio) ตั้งแต่ 1.2 ขึ้นไป และการเบี่ยงเบนของแนวรัศมีตั้งแต่ 21 องศาขึ้นไปเป็นลักษณะทั่วไปของโรคกระจกตา โป่งพอง (keratoconus)1) การทำแผนที่ความสูงของผิวด้านหลังมีความไวและความจำเพาะค่อนข้างสูง แต่มีข้อจำกัดในการตรวจหา forme fruste1) วิธี Klyce/Maeda และวิธี Smolek/Klyce ถูกใช้อย่างแพร่หลายในฐานะอัลกอริทึมการคัดกรองโรคกระจกตา โป่งพอง
OCT ช่องหน้าตากระจกตา ที่มีความละเอียดสูง1) การทำแผนที่ความหนาของเยื่อบุกระจกตา แสดงรูปแบบโดนัท (donut) โดยที่เยื่อบุจะบางลงบริเวณที่เนื้อกระจกตา บางลง และมีขอบเยื่อบุที่หนาขึ้นล้อมรอบ1) เนื่องจากการปรับโครงสร้างของเยื่อบุผิวช่วยปิดบังความผิดปกติของผิวหน้าบางส่วน การวิเคราะห์ผิวด้านหลังจึงเป็นกุญแจสำคัญในการวินิจฉัยตั้งแต่ระยะแรก
การประเมินสมบัติทางชีวกลศาสตร์ของกระจกตา : ใช้ค่าความหน่วงของกระจกตา (CH), ปัจจัยความต้านทานของกระจกตา (CRF) และการวิเคราะห์การเปลี่ยนรูปแบบพลวัตด้วย Corvis ST8) ดัชนีทางชีวกลศาสตร์ร่วมกับการตรวจภูมิประเทศของกระจกตา (TBI) และดัชนีทางชีวกลศาสตร์ของกระจกตา (CBI) ได้รับการแนะนำให้เป็นดัชนีคัดกรองที่ครอบคลุม8) การเปลี่ยนแปลงทางชีวกลศาสตร์เชื่อว่าเกิดขึ้นก่อนการเปลี่ยนแปลงทางสัณฐานวิทยา จึงคาดหวังว่าจะนำไปประยุกต์ใช้ในการตรวจพบตั้งแต่ระยะแรกได้1)
ข้อควรระวังในการวัดความดันลูกตา : เนื่องจากกระจกตา บางลงและอ่อนแรงทางชีวกลศาสตร์ เครื่องวัดความดันลูกตาแบบ Goldmann จะประเมินความดันลูกตาต่ำ กว่าความเป็นจริง1) แนะนำให้ใช้เครื่องวัดความดันลูกตา แบบลมหรือเครื่องวัดความดันลูกตา แบบ Dynamic Contour (DCT)1)
ตามฉันทามติระหว่างประเทศว่าด้วยคำจำกัดความของการดำเนินโรค (ปี 2015) การดำเนินโรคถูกกำหนดเมื่อมีการเปลี่ยนแปลงอย่างน้อย 2 ใน 3 รายการต่อไปนี้เกินช่วงความแปรผันของระบบการวัด9)
ความชันของผิวหน้าด้านหน้าเพิ่มขึ้น
ความชันของผิวหน้าด้านหลังเพิ่มขึ้น
ความหนาของกระจกตา ลดลง หรืออัตราการเปลี่ยนแปลงความหนาของกระจกตา จากบริเวณรอบนอกไปยังจุดที่บางที่สุดเพิ่มขึ้น
Meyer vàคณะได้คำนวณเกณฑ์ความแปรปรวนจากการทดสอบซ้ำของ Orbscan tomograph ในกลุ่มเด็กและเยาวชน และกำหนดให้ Flat K +1.30 D, Steep K +1.88 D, Kmax +1.20 D, central K +0.87 D, ความสูงผิวหน้า +11.7 µm, ความสูงผิวหลัง +24.3 µm, central pachymetry −28.1 µm, thinnest pachymetry −30.5 µm เป็นเกณฑ์การวินิจฉัยการดำเนินโรค3) การกระจายตามความรุนแรงตามการจำแนก Amsler-Krumeich พบว่า Stage I 37.8%, Stage II 39.9%, Stage III 9.5%, Stage IV 12.8%3)
การจำแนก Amsler-Krumeich เป็นการจำแนกระดับความรุนแรงแบบดั้งเดิม 4 ระดับ โดยประเมินจากค่า K ค่าการหักเหของแสง pachymetry และการมีหรือไม่มีภาวะตาขาว ขุ่นมัวร่วมกัน การจำแนก ABCD ที่ใหม่กว่า (พ.ศ. 2559) ประเมิน 4 ปัจจัยอย่างอิสระ ได้แก่ A: รัศมีความโค้งผิวหน้า, B: รัศมีความโค้งผิวหลัง, C: pachymetry จุดบางที่สุด, D: การมองเห็น ที่ดีที่สุดที่แก้ไขแล้ว (BCVA)1) การจำแนกระดับเล็กน้อย/ปานกลาง/รุนแรงตามการศึกษา CLEK ก็ใช้ในการปฏิบัติงานประจำวันเช่นกัน
ผู้ป่วยที่มีแนวโน้มดำเนินโรคเร็วจำเป็นต้องติดตามผลอย่างใกล้ชิด แนะนำให้ติดตามด้วยช่วงเวลาที่สั้นลงสำหรับผู้ป่วยอายุต่ำกว่า 17 ปี และกรณีที่มี Kmax เกิน 55 D1) ในทางปฏิบัติทั่วไป ช่วงเวลาการติดตามที่แนะนำคือ 1–3 เดือนในเด็ก และ 6–12 เดือนในผู้ใหญ่
โรคกระจกตา เสื่อมแบบ Pellucid (PMD ) : มีลักษณะเฉพาะคือกระจกตา บางเป็นแนวบริเวณล่างส่วนปลาย โดยส่วนบางอยู่ห่างจากจุดศูนย์กลางมากกว่า keratoconus อายุที่เริ่มป่วยมักช้ากว่า คือประมาณ 30–50 ปีKeratoglobus : เป็นโรคแต่กำเนิดที่ทำให้กระจกตา ทั้งสองข้างบางลงทั้งหมดตั้งแต่แรกเกิด ไม่พบ Fleischer ring หรือ Vogt striaeภาวะกระจกตา ป่องหลังการผ่าตัดแก้ไขสายตา (post-LASIK ectasia) : อาจเกิดในผู้ป่วยที่มีปัจจัยเสี่ยงของ keratoconus ที่ดำเนินโรคหลังผ่าตัด หรือเกิดจากกระจกตา บางลงเนื่องจากการฉายรังสีมากเกินไปKeratoconus ทุติยภูมิ : เป็นภาวะที่กระจกตา บางลงจากกระบวนการเกิดแผลเป็นจากโรคหลัก เช่น เริมที่กระจกตา ร่วมกับการมีหลอดเลือดงอกและแผลเป็นการบิดเบี้ยวของกระจกตา จากคอนแทคเลนส์กระจกตา และสามารถกลับคืนสู่ปกติได้
การประเมินคุณสมบัติทางชีวกลศาสตร์ของกระจกตา มีบทบาทสำคัญในการตรวจพบโรคกระจกตา ทรงกรวยในระยะเริ่มต้นและในกรณีที่ไม่แน่ชัด เพื่อหลีกเลี่ยงผลลบเท็จและเพิ่มความแม่นยำในการวินิจฉัย แนะนำให้ตรวจคัดกรองก่อนผ่าตัดแบบครอบคลุมที่รวมการตรวจภูมิประเทศกระจกตา และการประเมินทางชีวกลศาสตร์ร่วมกัน 8)
เสาหลักสองประการของการรักษาคือ การแก้ไขการมองเห็น เพื่อรักษาการทำงานของสายตา และ การชะลอการดำเนินโรค เพื่อหยุดการลุกลาม1) ภาวะสายตาเอียง ไม่สม่ำเสมอระดับเล็กน้อยสามารถแก้ไขได้ด้วยแว่นตาหรือคอนแทคเลนส์ชนิดนิ่ม toric แต่เมื่อสายตาเอียง ไม่สม่ำเสมอมากขึ้น จำเป็นต้องใช้ฮาร์ดคอนแทคเลนส์ และหากลุกลามมากขึ้น อาจพิจารณาการแทรกแซงเช่น CXL , ICRS หรือการปลูกถ่ายกระจกตา
แว่นตาและคอนแทคเลนส์เป็นหลักสำคัญของการรักษาสำหรับผู้ป่วยจำนวนมาก1) ในกรณีเล็กน้อยสามารถแก้ไขได้ด้วยแว่นตาหรือคอนแทคเลนส์ชนิดนิ่ม toric แต่เมื่อสายตาเอียง ไม่สม่ำเสมอมากขึ้น ฮาร์ดคอนแทคเลนส์ (RGP ) เป็นตัวเลือกอันดับแรก ผู้ป่วยจำนวนมากได้รับการมองเห็น ที่ดีขึ้นอย่างมากด้วย RGP
การประกอบฮาร์ดคอนแทคเลนส์มีความท้าทายทางเทคนิคมากกว่าตาสั้นปกติ10) การกำหนด base curve จากรัศมีความโค้งของกระจกตา ที่วัดได้มักทำให้เลนส์กระชับเกินไป หลักการปฏิบัติคือไม่ยึดติดกับรัศมีความโค้งของกระจกตา แต่มุ่งเน้นการจัดตำแหน่งศูนย์กลางและการเคลื่อนที่ที่ดีของเลนส์ ในกรณีที่เลนส์ทรงกลมไม่เหมาะสม อาจพิจารณาใช้เลนส์หลายโค้ง
ในกรณีที่ไม่สามารถใส่ฮาร์ดคอนแทคเลนส์ได้ จะเลือกใช้เลนส์พิเศษ เช่น เลนส์สเคลอรัล (scleral lens) เลนส์ไฮบริด หรือวิธี piggyback (เลนส์แข็งทับบนเลนส์อ่อน)1) เลนส์สเคลอรัลใส่บนตาขาว ด้านนอกลิมบัส จึงกระตุ้นกลไกต่อกระจกตา น้อยกว่า สามารถปรับตัวกับความผิดปกติของรูปทรงกระจกตา ระดับรุนแรงได้ และมีรายงานว่าความนิยมที่เพิ่มขึ้นในปัจจุบันมีส่วนทำให้อัตราการปลูกถ่ายกระจกตา ลดลง1) ผู้ป่วยมากกว่า 90% สามารถคงการมองเห็น ที่ใช้งานได้ด้วยคอนแทคเลนส์บางประเภท
การทำ corneal cross-linking สำหรับโรคตาโปน (keratoconus) ที่มีการดำเนินโรค เป็นการสร้างพันธะเชื่อมขวางระหว่างเส้นใยคอลลาเจนของกระจกตา เพื่อเพิ่มความแข็งแรงทางชีวกลศาสตร์ ซึ่งปัจจุบันเป็นการรักษาทางเลือกแรกในการยับยั้งการดำเนินโรค1, 2, 4) CXL ช่วยหยุดหรือชะลอการดำเนินของโรค และลดความจำเป็นในการปลูกถ่ายกระจกตา ในอนาคต1) นอกจากการทำให้กระจกตา มั่นคงแล้ว CXL ยังอาจทำให้กระจกตาแบน ลง 1.0–2.5 D และช่วยให้การมองเห็น ดีขึ้น1) ข้อมูลระดับประเทศของเนเธอร์แลนด์รายงานว่าจำนวนการปลูกถ่ายกระจกตา สำหรับโรคตาโปนลดลงอย่างมีนัยสำคัญหลังจากการนำ CXL มาใช้12)
โปรโตคอลเดรสเดินมาตรฐาน (epi-off CXL ) 5) :
ลอกเยื่อบุผิวกระจกตา ขนาดเส้นผ่านศูนย์กลาง 8–9 มม.
หยอดตาด้วยสารละลายไรโบฟลาวิน 0.1% (เติมเดกซ์แทรน 20%) ทุก 2 นาที เป็นเวลา 30 นาที
ฉายรังสี UV-A (ความยาวคลื่น 365 nm) ต่อเนื่องที่ 3 mW/cm² เป็นเวลา 30 นาที
ปริมาณพลังงานรวม 5.4 J/cm²
หลังทำหัตถการ ใส่คอนแทคเลนส์รักษาเพื่อปกป้องกระจกตา จนกว่าเยื่อบุผิวจะสร้างใหม่เสร็จสมบูรณ์
ดูแลหลังผ่าตัดด้วยการหยอดยาปฏิชีวนะและสเตียรอยด์
CXL แบบเร่ง5) อย่างไรก็ตาม เงื่อนไขฟลูเอนซ์สูงเช่น 30 mW/cm²×3 นาที มีประสิทธิภาพด้อยกว่าเนื่องจากการพร่องออกซิเจนในเนื้อเยื่อ และได้มีการพัฒนาวิธีการฉายแบบพัลส์เพื่อเติมออกซิเจน5)
CXL ผ่านเยื่อบุผิว (epi-on)CXL ที่รักษาเยื่อบุผิวกระจกตา ไว้ มีข้อดีคือลดอาการปวดหลังผ่าตัดและลดความเสี่ยงในการติดเชื้อ อย่างไรก็ตาม เนื่องจากการซึมผ่านของไรโบฟลาวินลดลง การทดลองแบบสุ่มที่มีกลุ่มควบคุมพบว่ามีประสิทธิภาพด้อยกว่าวิธี epi-off มาตรฐาน และการศึกษาบางชิ้นรายงานว่าค่า Kmax แย่ลง5)
การทดลอง KERALINK เป็นการศึกษาแบบสุ่มและมีกลุ่มควบคุมแบบปิดบังผู้ประเมิน ซึ่งเปรียบเทียบ CXL กับการรักษามาตรฐาน (แว่นตา, คอนแทคเลนส์) ในผู้ป่วยเด็กอายุ 10–16 ปีที่มีภาวะเคอราโทโคนัส ลุกลามจำนวน 60 ราย2) ผู้ป่วยที่มีค่า K2 หรือ Kmax เพิ่มขึ้น ≥1.5 D ในระยะเวลาอย่างน้อย 3 เดือนถือว่ามีการลุกลามและถูกคัดเข้า โดยมีความหนากระจกตา บริเวณยอด ≥400 µm และ K2 ≤62 D2) การรักษาดำเนินการโดยใช้เครื่อง Avedro KXL ฉายรังสี 10 mW/cm² × 9 นาที (ปริมาณรวม 5.4 J/cm²) ร่วมกับหยดไรโบฟลาวิน2)
ตัวชี้วัด (ที่ 18 เดือน) กลุ่ม CXL (n=30) กลุ่มรักษามาตรฐาน (n=28) ค่า K2 เฉลี่ย 49.7 ± 3.8 D 53.4 ± 5.8 D ตาที่มีการลุกลาม 2 ตา (7%) 12 ตา (43%) Kmax พื้นฐาน 56.0 ± 4.8 D 57.2 ± 5.7 D ความหนากระจกตา บริเวณยอด 512 ± 47.9 µm 507 ± 41.2 µm
ที่ 18 เดือน ค่าเฉลี่ยปรับแล้วของ K2 ในกลุ่ม CXL ต่ำกว่าอย่างมีนัยสำคัญที่ −3.0 D (95% CI −4.93 ถึง −1.08 D, p=0.002)2) และค่าสายตาไม่ได้แก้ไขและสายตาแก้ไขแล้ว (logMAR) ก็ดีกว่าอย่างมีนัยสำคัญในกลุ่ม CXL (ทั้งสองค่า p=0.002)2) โอกาสเกิดการลุกลามในกลุ่ม CXL ต่ำกว่า 90% (OR 0.1, 95% CI 0.02–0.48, p=0.004) และแบบจำลอง Cox proportional hazards แสดงให้เห็นว่าความเสี่ยงต่อการลุกลามเมื่อพิจารณาตามเวลาลดลง 87% ในกลุ่ม CXL 2) ไม่พบเหตุการณ์ไม่พึงประสงค์ร้ายแรง2) CXL ไม่มีปฏิสัมพันธ์กับประวัติภูมิแพ้หรือเชื้อชาติ และมีประสิทธิภาพในผู้ป่วยเด็กจากภูมิหลังที่หลากหลาย2) การทดลอง CXL แบบหลายศูนย์ในสหรัฐอเมริกาก็ยืนยันประสิทธิภาพในผู้ใหญ่4) จากผลลัพธ์เหล่านี้ CXL ได้รับการแนะนำเป็นการรักษาทางเลือกแรกในผู้ป่วยเด็กที่มีการลุกลาม2) ผลการศึกษาของ KERALINK สนับสนุนอย่างยิ่งต่อการตัดสินใจทางคลินิกในปัจจุบันที่ควรพิจารณา CXL โดยเร็วหลังยืนยันการลุกลาม
พิจารณาการผ่าตัดเมื่อคอนแทคเลนส์ไม่สามารถให้สายตาที่เพียงพอ หรือผู้ป่วยไม่สามารถใส่คอนแทคเลนส์ได้1)
การรักษาภายในชั้นสโตรมาของกระจกตา
วงแหวนภายในกระจกตา (ICRS ) : ชิ้นส่วนสังเคราะห์รูปครึ่งวงกลม เช่น Intacs , Ferrara, Keraring ถูกสอดเข้าในอุโมงค์ภายในชั้นเนื้อกระจกตา ที่สร้างด้วยเลเซอร์เฟมโตวินาที เหมาะสำหรับผู้ป่วยระดับเล็กน้อยถึงปานกลางที่กระจกตา ส่วนกลางใสและความหนาของกระจกตา บริเวณที่สอด ≥ 400 µm1) ทำให้กระจกตาแบน ลง ลดสายตาเอียง ที่ไม่สม่ำเสมอ และช่วยให้ใส่คอนแทคเลนส์ได้ง่ายขึ้น
CAIRS (วงแหวนเนื้อเยื่อกระจกตา จากผู้บริจาค)กระจกตา ของผู้บริจาค ซึ่งรายงานว่าเป็นทางเลือกใหม่แทนวงแหวนสังเคราะห์ การใช้ร่วมกับ CXL รายงานว่าปลอดภัยและมีประสิทธิภาพ
การแก้ไขสายตาผิดปกติ
เลนส์แก้วตาเทียม ชนิด保留เลนส์เดิม (ICL )เลนส์แก้วตาเทียม ชนิดทอริก ICL หรือชนิดยึดม่านตา (Artiflex) ได้รับการรายงานว่าเป็นวิธีการแก้ไขสายตาผิดปกติหลังการทรงตัวของกระจกตา จาก CXL 5) การผ่าตัดแก้ไขสายตาผิดปกติที่กระจกตา เช่น LASIK มีข้อห้าม ดังนั้นการแก้ไขโดยใช้เลนส์แก้วตาเทียม จึงเป็นทางเลือก
การรักษาแบบผสมผสาน : โปรโตคอล Athens (PRK นำทางด้วยภูมิประเทศร่วมกับ CXL ), โปรโตคอล Cretan (PTK ผ่านเยื่อบุผิวร่วมกับ CXL ), และการจี้ DISC (decentered individualized sphero-cylindrical ablation) ร่วมกับ CXL ก็ได้มีการรายงานเช่นกัน11)
การปลูกถ่ายกระจกตา
การปลูกถ่ายกระจกตา ชั้นหน้าส่วนลึก (DALK )กระจกตา ส่วนหน้าในขณะที่รักษาชั้นเซลล์บุผนังกระจกตา ของผู้ป่วยไว้ โดยหลักการแล้วไม่มีความเสี่ยงต่อการปฏิเสธชั้นเซลล์บุผนังกระจกตา และความเสี่ยงต่อการแตกจากบาดแผลก็ต่ำกว่า PK ในกรณีที่ไม่มีอาการบวมน้ำเฉียบพลันของกระจกตา ปัจจุบัน DALK มักถูกเลือกเป็นทางเลือกแรกในระยะหลังนี้1)
การปลูกถ่ายกระจกตา ทั้งชั้น (PK)การปลูกถ่ายกระจกตา มีความเสี่ยงต่อการติดเชื้อ การปฏิเสธ การแตกจากบาดแผล และบางครั้งม่านตา ขยายแบบถาวรหลังผ่าตัดเป็นปัญหา หลังผ่าตัดมักยังจำเป็นต้องใช้คอนแทคเลนส์เพื่อแก้ไขสายตาผิดปกติ
การรักษาภาวะกระจกตาบวมน้ำเฉียบพลัน : สำหรับภาวะกระจกตาบวมน้ำเฉียบพลัน จากการฉีกขาดของเยื่อเดสเซเมต ให้ใส่ผ้าปิดตากดทับประมาณ 1 เดือน และรับประทานอะเซตาโซลาไมด์ (ไดอะม็อกซ์ ®) ตามความจำเป็น การใช้ยาหยอดตาน้ำเกลือความเข้มข้นสูง (NaCl 5%) หรือยาหยอดตาสเตียรอยด์ อาจช่วยลดอาการบวมได้ เมื่อเกิดแผลเป็นตามธรรมชาติ ให้ใส่คอนแทคเลนส์อีกครั้ง ในระยะหลัง มีรายงานการฉีดอากาศเข้าช่องหน้าม่านตา และการปลูกถ่ายเยื่อหุ้มรกเป็นทางเลือกในการรักษาเช่นกัน แผลเป็นหลังภาวะบวมน้ำอาจกระจายไปยังศูนย์กลางกระจกตา หรือในบางกรณีที่น่าประหลาดใจ แผลเป็นอาจช่วยลดความชันของกระจกตา ได้ตามธรรมชาติ จึงต้องประเมินสภาพการหักเหของแสง หลังจากแผลเป็นสงบก่อนตัดสินใจวางแผนการรักษาต่อไป
พื้นฐานของการป้องกันการดำเนินโรคคือ การหยุดขยี้ตาโดยเด็ดขาด 1, 6) หากเยื่อบุตาอักเสบจากภูมิแพ้ หรือโรคเยื่อบุตา จากภูมิแพ้เป็นสาเหตุของอาการคันตา ควรควบคุมอาการให้เพียงพอด้วยยาหยอดตาแก้แพ้หรือยาต้านฮีสตามีนเพื่อลดโอกาสในการขยี้ตา หากอาการคันตารุนแรง นอกเหนือจากยาหยอดตาแล้ว ควรพิจารณาจัดการภาวะภูมิแพ้ทั้งระบบ เช่น การกำจัดสารก่อภูมิแพ้และการปรับแต่งการดูแลผิวหนัง ควรใส่ใจท่านอนด้วย แนะนำให้ผู้ป่วยหลีกเลี่ยงการนอนตะแคงที่กดใบหน้าลงบนหมอนหรือแขน6) ไม่เพียงแต่ผู้ป่วยเท่านั้น แต่ควรอธิบายสภาพโรคและความสำคัญของการป้องกันให้ครอบครัวและผู้ดูแลเข้าใจด้วย การปรับเปลี่ยนพฤติกรรมที่กระตุ้นให้เกิดการขยี้ตาทั้งในสภาพแวดล้อมของครอบครัวมีประสิทธิภาพ
เมื่อผู้ป่วยโรคกระจกตา รูปกรวยมีต้อกระจก ร่วมด้วย ความไม่เสถียรของความโค้งกระจกตา และสายตาเอียง ไม่สม่ำเสมอระดับสูงทำให้การคำนวณกำลังของเลนส์แก้วตาเทียม และขั้นตอนการผ่าตัดทั้งสองอย่างมีความยากลำบาก แนะนำให้ทำ CXL หรือ ICRS เพื่อทำให้กระจกตา มีเสถียรภาพก่อนผ่าตัด กำหนดระยะเวลาหยุดใส่คอนแทคเลนส์ (อย่างน้อย 2 สัปดาห์สำหรับเลนส์อ่อน และ 5 สัปดาห์ขึ้นไปสำหรับเลนส์แข็ง) และยืนยันความเสถียรของการตรวจวัดทางชีวภาพก่อนผ่าตัด7) ในการคำนวณกำลังเลนส์แก้วตาเทียม สูตรมาตรฐานมีแนวโน้มทำให้เกิดสายตายาว หลังผ่าตัด (hyperopic surprise) ดังนั้นจึงแนะนำให้ใช้สูตรเฉพาะสำหรับโรคกระจกตา รูปกรวย เช่น Barrett True-K หรือ Kane keratoconus formula และตั้งเป้าหมายสายตาสั้น เล็กน้อย7) ไม่แนะนำให้ใช้เลนส์แก้วตาเทียม แบบหลายระยะเนื่องจากเพิ่มความคลาดเคลื่อนลำดับสูง7)
ในทางเทคนิคการผ่าตัด การกรีดกระจกตา ใสบนกระจกตา ที่บางลงมีความเสี่ยงต่อการรั่วของแผล ดังนั้นจึงแนะนำให้กรีดอุโมงค์แผลบริเวณตาขาว -กระจกตา 7) หากความขุ่นของกระจกตา ลดการมองเห็น ในการเปิดถุงหุ้มเลนส์ด้านหน้า การย้อมสีถุงหุ้มเลนส์ด้านหน้าด้วย trypan blue และการทาสารหนืดชนิดกระจายตัวบนผิวกระจกตา มีประโยชน์ ในกรณีรุนแรงที่จำเป็นต้องปลูกถ่ายกระจกตา การผ่าตัดสามอย่างพร้อมกัน (triple surgery) คือ การผ่าตัดต้อกระจก การใส่เลนส์แก้วตาเทียม และการปลูกถ่ายกระจกตา ในคราวเดียวกันก็เป็นทางเลือกหนึ่ง
Q
การทำ corneal cross-linking เจ็บหรือไม่?
A
ในวิธี epi-off มาตรฐาน เนื่องจากมีการลอกเยื่อบุผิวกระจกตา ออก มักมีอาการปวด รู้สึกมีสิ่งแปลกปลอม และน้ำตาไหลเป็นเวลาหลายวันหลังการผ่าตัด อาการปวดถูกจัดการด้วยการใส่คอนแทคเลนส์รักษา การประคบเย็น และยาแก้ปวด เยื่อบุผิวมักสร้างใหม่เสร็จภายใน 3-5 วัน หลังจากนั้นอาการปวดจะลดลง ในวิธี epi-on เนื่องจากไม่มีการลอกเยื่อบุผิว ความเจ็บปวดหลังผ่าตัดจึงน้อยกว่า แต่อาจมีประสิทธิภาพด้อยกว่าวิธี epi-off
Q
ผู้ป่วยโรคกระจกตาทรงกรวยสามารถใส่คอนแทคเลนส์ได้หรือไม่?
A
คอนแทคเลนส์มีบทบาทสำคัญในการแก้ไขสายตาสำหรับโรคกระจกตา ทรงกรวย คอนแทคเลนส์แข็ง (RGP ) ที่ช่วยหักล้างสายตาเอียง ไม่ปกติเป็นที่นิยมใช้มากที่สุด และมักให้การปรับปรุงการมองเห็น อย่างเห็นได้ชัด หากใส่คอนแทคเลนส์แข็งได้ยาก ก็สามารถเลือกใช้เลนส์พิเศษ เช่น เลนส์ตาขาว (scleral lens), เลนส์ไฮบริด, หรือวิธีพิกกี้แบ็ก (piggyback: วางเลนส์แข็งทับบนเลนส์อ่อน) ได้ มากกว่า 90% ของกรณีสามารถแก้ไขสายตาด้วยคอนแทคเลนส์บางรูปแบบได้
Q
โรคกระจกตาทรงกรวยในเด็กแตกต่างจากผู้ใหญ่อย่างไร?
A
โรคกระจกตาทรงกรวยในเด็ก และวัยรุ่นมีการดำเนินโรคที่เร็วกว่าในผู้ใหญ่ เนื่องจากความแข็งแรงทางชีวกลศาสตร์ของกระจกตา เพิ่มขึ้นตามอายุ กระจกตา ในเด็กจึงไวต่อการสลายคอลลาเจนมากกว่า การศึกษาที่ติดตามตา 148 ข้างของเด็กและวัยรุ่นเป็นเวลาเฉลี่ย 2.9 ปี พบว่ามีการดำเนินโรคใน 77.0% และสัดส่วนที่อยู่ในระยะลุกลามตั้งแต่แรกวินิจฉัยก็สูงเช่นกัน ในขณะที่ผู้ใหญ่แนะนำให้ติดตามทุก 6–12 เดือน เด็กควรได้รับการติดตามอย่างใกล้ชิดทุก 1–3 เดือน เมื่อยืนยันว่ามีการดำเนินโรค การทำ cross-linking กระจกตา อย่างทันท่วงทีเป็นการแทรกแซงเพียงอย่างเดียวที่ลดความเสี่ยงของการปลูกถ่ายกระจกตา
ในโรคกระจกตา ทรงกรวย การสลายคอลลาเจนของกระจกตา เป็นพื้นฐานของการบางลงของกระจกตา 1) ในเนื้อกระจกตา ที่แข็งแรง มัดเส้นใยคอลลาเจนซึ่งส่วนใหญ่เป็นคอลลาเจนชนิดที่ 1 จะเรียงตัวซ้อนกันเป็นสามมิติ รักษาความแข็งแรงและรูปร่างของกระจกตา ในชั้นตื้นที่ติดกับเยื่อโบว์แมน มัดเส้นใยคอลลาเจนจะค่อนข้างบาง มีมุมชันและมีหลายทิศทาง ในขณะที่ชั้นลึก มัดเส้นใยจะกว้างขึ้นและแบนราบขึ้นเกิดเป็นความลาดชันเชิงโครงสร้าง โครงสร้างมัดใยที่ชันและแน่นหนาในชั้นตื้นนี้มีส่วนสำคัญในการรักษารูปร่างด้านหน้าของกระจกตา แต่ในโรคกระจกตา ทรงกรวย โครงสร้างเหล่านี้เป็นที่ทราบกันว่าเปลี่ยนแปลงไป
ในระดับโมเลกุล การเพิ่มขึ้นของเมทริกซ์เมทัลโลโปรตีเนส (MMP) และการลดลงของเนื้อเยื่อยับยั้งเมทัลโลโปรตีเนส (TIMP) เกี่ยวข้องกับการสลายคอลลาเจนของเนื้อกระจกตา 1) ในน้ำตาของผู้ป่วยโรคกระจกตา ทรงกรวยพบความเข้มข้นของสื่อกลางการอักเสบ เช่น IL-6, TNF -α และ MMP-9 สูงขึ้น1) สื่อกลางการอักเสบเหล่านี้เหนี่ยวนำให้เกิดอะพอพโทซิส ของเซลล์เนื้อกระจกตา (เคอราโทไซต์) ส่งผลให้ความหนาแน่นของเซลล์ลดลง1)
แม้ว่าโรคกระจกตา ทรงกรวย (เคอราโตโคนัส) เดิมถูกจัดเป็นโรคกระจกตา บางลงแบบ “ไม่อักเสบ” แต่งานวิจัยล่าสุดพบว่ามีองค์ประกอบของการอักเสบที่เกี่ยวข้องทั้งทางตรงและทางอ้อมกับการเกิดและการดำเนินของโรค1)
ทางจุลพยาธิวิทยาพบการแตกหรือหายไปของชั้นโบว์แมน การเรียงตัวที่ผิดปกติของเส้นใยคอลลาเจน การเกิดแผลเป็น และการบางลงของเนื้อกระจกตา ในกรณีที่ลุกลามอาจเกิดรอยย่นหรือการแตกของเยื่อเดสเซเม็ท
จากมุมมองทางชีวกลศาสตร์ของกระจกตา การลดลงของโมดูลัสยืดหยุ่นเฉพาะที่สัมพันธ์กับการสลายและเสื่อมสภาพของเส้นใยคอลลาเจน8) เมื่อความแข็งเฉพาะที่ลดลง ภายใต้แรงกดดันคงที่จากความดันลูกตา ความเครียดจะรวมตัวและกระจายซ้ำที่บริเวณที่อ่อนแอ ทำให้เกิด “วงจรวิบัติทางชีวกลศาสตร์” ซึ่งกระจกตา จะค่อยๆ โค้งงอมากขึ้นและบางลง8)
นอกจากปัจจัยทางพันธุกรรมแล้ว การขยี้ตาซ้ำๆ ซึ่งเป็นความเครียดเชิงกลซ้ำๆ เชื่อว่าเป็นตัวกระตุ้นให้เกิดการวิบัติทางชีวกลศาสตร์นี้1, 6) กระจกตา ของคนหนุ่มสาวมีความหนาแน่นของ cross-link คอลลาเจนต่ำ และความแข็งจะเพิ่มขึ้นตามอายุ ดังนั้นกระจกตา ในเด็กและวัยรุ่นจึงไวต่อการถูกย่อยสลายทางกลและทางเอนไซม์มากกว่า1) นี่คือพื้นฐานทางชีววิทยาที่อธิบายว่าทำไมโรคจึงดำเนินไปเร็วขึ้นในผู้ป่วยเด็ก ความผิดปกติของกลไกป้องกันต่อภาวะเครียดออกซิเดชัน โดยเฉพาะการลดลงของกิจกรรม superoxide dismutase และความผิดปกติของการเผาผลาญ glutathione ก็อาจมีส่วนเกี่ยวข้องกับพยาธิสภาพของโรคเช่นกัน เส้นทางโมเลกุลเหล่านี้อาจก่อให้เกิดวงจรอุบาทว์ที่ขยายการผลิตสารสื่อกลางการอักเสบและการกระตุ้นเอนไซม์ย่อยสลายคอลลาเจน
การตายแบบอะพอพโทซิส ของเคอราโทไซต์ (keratocyte) เป็นกลไกระดับเซลล์โดยตรงที่ทำให้ความหนาแน่นของเซลล์เนื้อกระจกตา ลดลงและเนื้อกระจกตา บางลงในโรคเคอราโทโคนัส 1) ชั้น Bowman ปกติเป็นชั้นเมทริกซ์นอกเซลล์หนาประมาณ 10 µm แต่ในโรคเคอราโคนัส พบการฉีกขาดและการหายไปตั้งแต่ระยะแรก ซึ่งทำให้กลไกการรักษารูปร่างผิวหน้าของกระจกตา ล้มเหลว ชั้น Descemet เป็นเยื่อฐานที่ภายใต้กล้องจุลทรรศน์อิเล็กตรอนแบ่งออกเป็นชั้นแถบด้านหน้า (anterior banded layer) และชั้นไร้แถบด้านหลัง (posterior non-banded layer) เมื่อเกิดภาวะกระจกตาบวมน้ำเฉียบพลัน เยื่อนี้จะฉีกขาด ทำให้น้ำในช่องหน้าม่านตา ไหลเข้าสู่เนื้อกระจกตา ส่งผลให้การมองเห็น ลดลงอย่างรุนแรงชั่วคราว
CXL ในเด็กและวัยรุ่นตอนต้นNK แสดงให้เห็นประสิทธิภาพของ CXL ในกลุ่มอายุ 10–16 ปีด้วยหลักฐานระดับสูง2) อัตราการดำเนินโรคที่สูงถึง 77% ในเด็กและวัยรุ่นที่รายงานโดย Meyer และคณะ เป็นเหตุผลสนับสนุนการแทรกแซงตั้งแต่เนิ่นๆ ก่อนที่จะยืนยันการดำเนินโรค3) หากผลการคงตัวในระยะยาวของการไขว้เส้นใยคอลลาเจนกระจกตา ยังคงอยู่ อาจหลีกเลี่ยงความจำเป็นในการใส่คอนแทคเลนส์เป็นประจำหรือการปลูกถ่ายกระจกตา ในอนาคตได้2) ในการทบทวนวรรณกรรมอย่างเป็นระบบและการวิเคราะห์อภิมานโดย Ferdi และคณะ ได้รวบรวมข้อมูลจาก 11,529 ตาที่มีข้อมูลการดำเนินโรคตามธรรมชาติ แต่ข้อมูลในเด็กยังมีจำกัด และจำเป็นต้องมีการติดตามระยะยาวเพิ่มเติม13)
การตรวจพบตั้งแต่เนิ่นๆ ด้วยชีวกลศาสตร์ : ความก้าวหน้าในการประเมินชีวกลศาสตร์ของกระจกตา ทำให้สามารถตรวจพบได้ตั้งแต่ระยะ “ชีวกลศาสตร์” ก่อนที่จะมีการเปลี่ยนแปลงทางสัณฐานวิทยาแบบดั้งเดิม (ภูมิประเทศกระจกตา ภาพตัดขวางกระจกตา )1, 8) การสร้างกระบวนการคัดกรองที่ครอบคลุมโดยผสมผสานภาพตัดขวางกระจกตา และการประเมินชีวกลศาสตร์เข้าด้วยกันคือความท้าทายในอนาคต8)
การคัดกรองทางพันธุกรรม : การตรวจทางพันธุกรรมที่ได้รับการอนุมัติจาก FDA ซึ่งประเมินยีน 75 ยีนและความแปรผันมากกว่า 2,000 รายการได้พร้อมใช้งานแล้ว1) แนวทางการวินิจฉัยตั้งแต่เนิ่นๆ ที่บูรณาการปัจจัยสิ่งแวดล้อมและคะแนนความเสี่ยงทางพันธุกรรมอยู่ในขั้นตอนการวิจัย และจำเป็นต้องมีการตรวจสอบเพิ่มเติมเกี่ยวกับประโยชน์ทางคลินิก1)
การปรับปรุงโปรโตคอล CXL : การปรับปรุงโปรโตคอลแบบเร่งรัด การปรับปรุงการส่งออกซิเจนด้วยการฉายรังสีแบบพัลส์ และการปรับปรุงการซึมผ่านของวิธี epi-on กำลังอยู่ระหว่างการศึกษาอย่างแข็งขัน5) ภายใต้สภาวะฟลูเอนซ์สูง ออกซิเจนภายในเนื้อเยื่อจะหมดลงทำให้ประสิทธิภาพของปฏิกิริยาการเชื่อมขวางลดลง และได้มีการศึกษาวิธีการเติมออกซิเจนโดยการหยุดฉายรังสีเป็นช่วงๆ (CXL แบบพัลส์)5) มีรายงานวิธีการรักษาแบบผสมผสาน เช่น โปรโตคอล Athens (PRK นำทางด้วยภูมิประเทศร่วมกับ CXL ), โปรโตคอล Cretan (PTK ผ่านเยื่อบุผิวร่วมกับ CXL ), และโปรโตคอล DISC (การตัดกระจกตา แบบทรงกลม-ทรงกระบอกเฉพาะบุคคลแบบเยื้องศูนย์ร่วมกับ CXL ) เพื่อให้บรรลุทั้งการยับยั้งการดำเนินโรคและการปรับปรุงการมองเห็น 11) วิธีการรักษาแบบผสมผสานเหล่านี้จำเป็นต้องตัดเนื้อเยื่อกระจกตา เพิ่มเติม ดังนั้นจึงจำกัดเฉพาะกรณีที่มีความหนากระจกตา ที่เหลืออยู่เพียงพอ
การยืนยันความคงตัวในระยะยาว : ข้อมูลจากการศึกษาติดตามผลนานกว่า 10 ปีเกี่ยวกับประสิทธิภาพในการคงตัวของ CXL กำลังสะสมมากขึ้น มีรายงานถึงความยั่งยืนของผลการรักษา อย่างไรก็ตาม ในบางกรณีพบว่ามีการดำเนินโรคที่กลับมาลุกลามอีกเมื่อเวลาผ่านไป5) ประเด็นการศึกษาวิจัยในอนาคต ได้แก่ ข้อควรพิจารณาในการทำ CXL ซ้ำเมื่อเกิดการลุกลามอีก ปัจจัยทำนายการลุกลามซ้ำ และการพัฒนาโปรโตคอลที่มีความทนทานมากขึ้น นอกจากนี้ การแพร่หลายของเทคโนโลยีเลนส์สเคลอรัลคาดว่าจะช่วยลดจำนวนผู้ป่วยที่ต้องได้รับการปลูกถ่ายกระจกตา ลงอีก1)
AAO Corneal Ectasia PPP Panel. Corneal Ectasia Preferred Practice Pattern. Ophthalmology. 2024.
Larkin DFP, Chowdhury K, Burr JM, Raynor M, Edwards M, Tuft SJ, et al. Effect of Corneal Cross-linking versus Standard Care on Keratoconus Progression in Young Patients: The KERALINK Randomized Controlled Trial. Ophthalmology. 2021;128(11):1516-1526.
Meyer JJ, Gokul A, Vellara HR, McGhee CNJ. Progression of keratoconus in children and adolescents. Br J Ophthalmol. 2023;107:176-180.
Hersh PS, Stulting RD, Muller D, Durrie DS, Rajpal RK; United States Crosslinking Study Group. United States Multicenter Clinical Trial of Corneal Collagen Crosslinking for Keratoconus Treatment. Ophthalmology. 2017;124(9):1259-1270.
Lim L, Lim EWL. A Review of Corneal Collagen Cross-Linking: Current Trends in Practice Applications. Open Ophthalmol J. 2018;12:181-190.
Bitton K, Dubois M, Moran S, Gatinel D. Discordant Keratoconus in Monozygotic Twins. Case Rep Ophthalmol. 2022;13:313-317.
Findl O, Buehl W, Bauer P, et al. ESCRS Clinical Guidelines for Prevention and Treatment of Cataract. Vienna: European Society of Cataract & Refractive Surgeons; 2024.
AAO Refractive Management/Intervention PPP Panel. Evidence-Based Guidelines for Keratorefractive and Lens-Based Surgery. Ophthalmology. 2024.
Gomes JAP, Tan D, Rapuano CJ, Belin MW, Ambrosio R Jr, Guell JL, et al. Global consensus on keratoconus and ectatic diseases. Cornea. 2015;34(4):359-369.
Usgaonkar U, Chodankar S, Shetty A. Online survey about keratoconus management by optometrists. Indian J Ophthalmol. 2023;71:86-90.
Knezović I, Đurić S. Decentered individualized sphero-cylindrical (DISC) ablation and corneal crosslinking in patient with progressive keratoconus. Case Rep Ophthalmol Med. 2022;2022:1839848.
Godefrooij DA, Gans R, Imhof SM, Wisse RP L. Nationwide reduction in the number of corneal transplantations for keratoconus following the implementation of cross-linking. Acta Ophthalmol. 2016;94(7):675-678.
Ferdi AC, Nguyen V, Gore DM, Allan BD, Rozema JJ, Watson SL. Keratoconus Natural Progression: A Systematic Review and Meta-analysis of 11,529 Eyes. Ophthalmology. 2019;126(7):935-945.